HPLC-MS/MS法同时测定玄参中8个成分的含量△
2017-09-21周佳齐红艺
周佳,齐红艺
(1.四川省食品药品检验检测院,四川 成都 611731;2.西南大学,重庆 400715)
·基础研究·
HPLC-MS/MS法同时测定玄参中8个成分的含量△
周佳1*,齐红艺2
(1.四川省食品药品检验检测院,四川 成都 611731;2.西南大学,重庆 400715)
目的:建立HPLC-MS/MS法同时测定玄参中梓醇、哈巴苷、栀子苷、类叶升麻苷、安格洛苷C、肉桂酸、哈巴俄苷、5-羟甲基糠醛8个成分的含量。方法:采用Agilent ZORBAX Eclipse XDB-C18色谱柱(150 mm × 4.6 mm,5 μm),柱温为30 ℃,以甲醇-0.05%甲酸水为流动相,梯度洗脱,流速为0.6 mL·min-1,进样量2 μL,ESI源,正离子-MRM模式下检测;结果:梓醇、哈巴苷、栀子苷、类叶升麻苷、安格洛苷C、肉桂酸、哈巴俄苷、5-羟甲基糠醛质量浓度分别在0.194 0~7.76(r=0.999 0)、0.173 8~32.85(r=0.999 8)、0.394~23.64(r=0.996 4)、0.279 5~16.77(r=0.997 4)、0.3095~12.38(r=0.999 4)、0.087~5.220(r=0.999 1)、0.264 5~31.74(r=0.999 8)、0.034 3~1.370 0 μg·mL-1(r=0.999 2)线性关系良好,检出限(LOD)为5~50 ng·mL-1,平均回收率为91.33%~99.78%。样品测定结果显示,玄参中哈巴俄苷、哈巴苷及安格洛苷C含量较高,分别为1.517~9.735、0.289~5.997、0.898~3.568 mg·g-1。不同来源的样品中,8个成分的含量及各个成分之间比例存在较大差异。结论:本实验建立了在22 min内同时测定玄参中8个成分含量的方法,灵敏度高,准确度好,实验结果可为玄参质量提供参考。
玄参;梓醇;哈巴苷;栀子苷;类叶升麻苷;安格洛苷C;肉桂酸;哈巴俄苷;5-羟甲基糠醛;HPLC-MS/MS
传统中药玄参(Radix Scrophulariae)是玄参科植物浙玄参ScrophularianingpoensisHemsl.的干燥根[1],性微寒,味甘、苦、咸,归肺、胃、肾经;具有凉血滋阴、泻火解毒的功效[2]。玄参中主要含有环烯醚萜苷和苯丙素苷等[3-4],具有镇痛、消炎、抗菌、保肝、抗氧化、免疫调节、降血压、神经保护等作用[5-7]。玄参中测定哈巴苷、哈巴俄苷、肉桂酸、安格洛苷C的HPLC法已有报道[8],但用HPLC-MS/MS法同时测定玄参中梓醇、哈巴苷、栀子苷、类叶升麻苷、安格洛苷C、肉桂酸、哈巴俄苷、5-羟甲基糠醛8个成分的含量未见报道。本实验建立具有高灵敏度、高选择性的HPLC-MS/MS法对玄参中这8个成分进测定,并测定了不同产地玄参药材的8个成分的含量,为全面控制玄参质量奠定基础。
1 仪器与试剂
1.1材料
9批次玄参(产自重庆秀山,河北,四川北川、雅安、巫山、宝兴,贵州、河南、湖南)经四川省食品药品检验检测院黎跃成主任药师鉴定为玄参正品。
1.2仪器
高效液相色谱仪-三重四级杆质谱联用仪(Agilent1290-6460,MussHunter工作站);SartoriusCPA225D型电子天平;Milli-Q超纯水仪;超声仪(上海冠特超声仪器公司)。
1.3试剂与对照品
1.3.1试剂 甲醇、超纯水。
1.3.2对照品 梓醇(批号:110808-200508,99.5%)购自中国食品药品检定研究院,哈巴苷(批号:Must-12121902,≥95%)、栀子苷(批号:Must-13041809,≥95%)、类叶升麻苷(批号:Must-13051002,≥95%)、安格洛苷C(批号:Must-13051502,≥95%)、肉桂酸(批号:Must-12123102,≥95%)、哈巴俄苷(批号:Must-12071801,≥95%)、5-羟甲基糠醛(5-HMF)(批号:Must-12110805,≥95%)购自成都曼斯特生物科技有限公司。
2 方法与结果
2.1混合对照品溶液的制备
精密称定梓醇、哈巴苷、栀子苷、类叶升麻苷、安格洛苷C、肉桂酸、哈巴俄苷、5-羟甲基糠醛(5-HMF)对照品适量,分别置棕色量瓶中,用50%甲醇水溶解并定容至各量瓶中,得单一对照品储备液。精密量取上述各储备液适量,用50%甲醇水配制成混合对照品中间液,质量浓度为梓醇38.8μg·mL-1、哈巴苷54.75μg·mL-1、栀子苷78.8μg·mL-1、类叶升麻苷55.9μg·mL-1、安格洛苷C61.9μg·mL-1、肉桂酸17.4μg·mL-1、哈巴俄苷52.9μg·mL-1、5-羟甲基糠醛6.85μg·mL-1,备用。
2.2供试品溶液的制备
取各玄参,粉碎(过三号筛),称取粉末,精密称定,置具塞三角瓶中,精密加入50%甲醇水溶液50mL,称重,放置30min,超声处理45min(功率300W,频率45kHz),放冷,再称重,用50%甲醇水溶液补足减失的重量,过滤,取续滤液,过0.22μm微孔滤膜,即得。
2.3色谱条件
色谱柱:AgilentZORBAXEclipseXDB-C18(150mm×4.6mm,5μm);流动相:0.05%甲酸水溶液(A)-甲醇(B),梯度洗脱(0~5min,60%~60%A;5~8min,60%~40%A;8~19min,40%~20%A;19~19.1min,20%~60%A;19.1~22min,60%~60%A);流速:0.6mL·min-1;柱温:35℃;进样量:2μL。
2.4质谱条件
离子源:电喷雾离子源(ESI);扫描方式:正离子模式;检测方式:多反应监测(MRM)方式,干燥气流速:7.0L·min-1,干燥气温度:300℃;毛细管电压:3500V,四级杆温度:100℃,检测化合物离子参数见表1,对照品及玄参样品的MRM总离子流图见图1,各化合物的提取色谱图见图2。
2.5线性关系及检测下限考察
取2.1项下混合对照品中间液适量,用50%甲醇水溶液稀释成系列混合对照品溶液(每个化合物至少测定5个浓度水平),照上述方法进行测定,记录峰面积,以对照品浓度(μg·mL-1)为横坐标,以相应的峰面积为纵坐标,进行线性回归,计算回归方程。同时以信噪比(S/N)3∶1及10∶1为基准分别测定各化合物的检出限及定量限,结果见表2;结果表明各化合物在下列质量浓度(见表2)范围内线性关系良好,检出限在5~50 ng·mL-1,定量限在17~167 ng·mL-1。
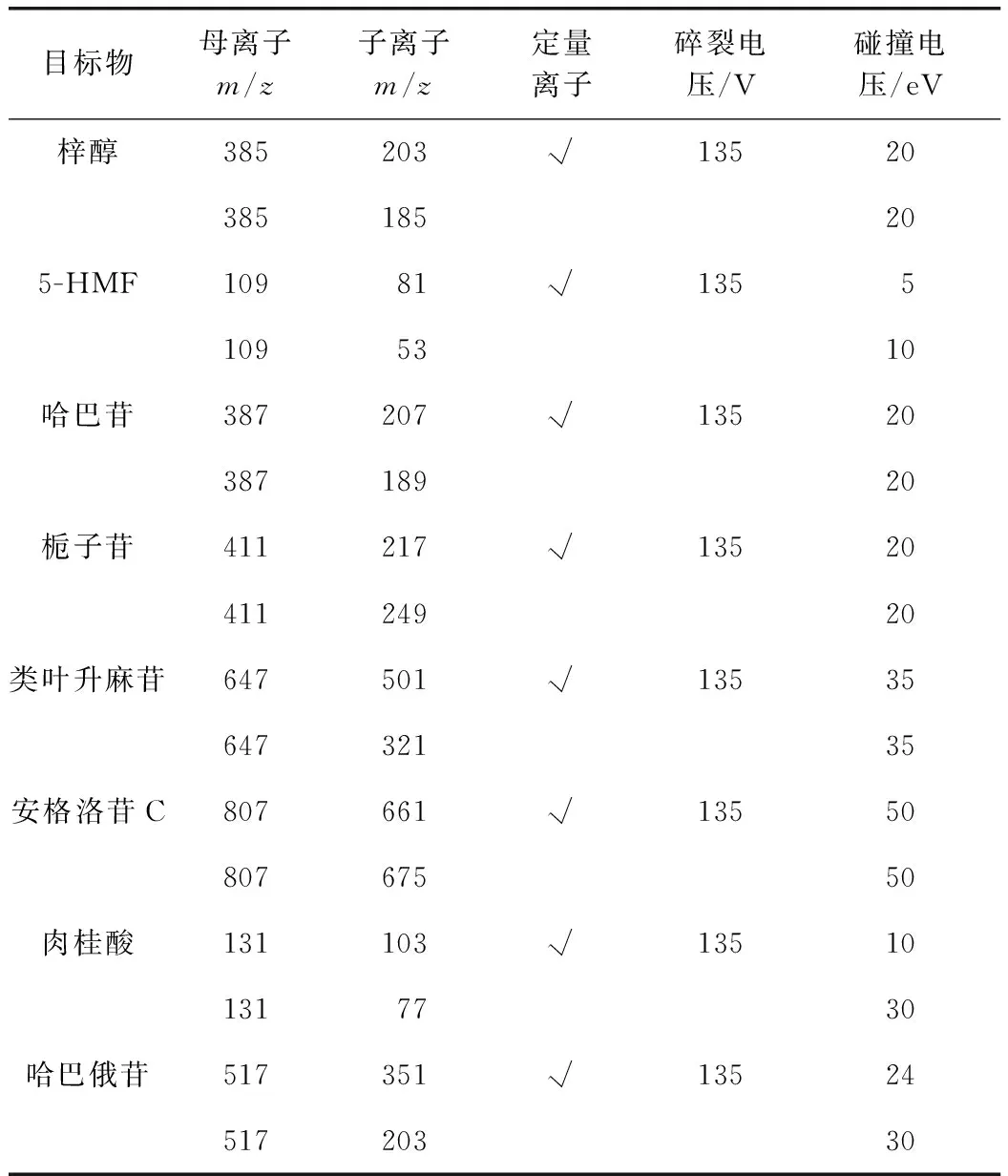
表1 检测化合物离子参数
2.6稳定性试验
取2.2项下制备的供试品溶液,室温放置,分别在0、2、4、8、12、48 h进样测定,记录其峰面积。结果各时间段梓醇、哈巴苷、栀子苷、类叶升麻苷、安格洛苷C、肉桂酸、哈巴俄苷、5-羟甲基糠醛峰面积的RSD分别为2.11%、1.95%、2.22%、3.91%、2.15%、1.44%、1.64%、4.01%,表明供试品在48 h内稳定。
2.7加样回收试验
精密称取已测定含量的玄参样品(样品编号1)粉末约0.1g,共9份,分别精密加入低、中、高3个水平的单一对照品溶液,每个浓度3份,按2.2项下制备加样回收率测定样品溶液,进样测定,记录峰面积,计算各化合物的平均回收率,结果见表3。回收率在91.33%~99.78%,RSD%小于5.3%,表明准确度良好。
2.8样品含量测定
取各个玄参样品约0.2g,精密称定,按2.2项下供试品溶液方法制备,进样测定,计算含量,结果见表4。

图2 玄参中8个化合物的提取色谱图

成分回归方程r线性范围/μg·mL-1检出限/ng·mL-1定量限/ng·mL-1类叶升麻苷Y=359.7X+77.80.99740.2795~16.7750167哈巴俄苷Y=1804.8X-259.10.99980.2645~31.7410335-HMFY=70989.4X+1671.70.99920.0343~1.3700517哈巴苷Y=12871.1X-1856.30.99980.2738~32.851033肉桂酸Y=58021.8X+964.60.9991 0.087~5.220827栀子苷Y=4142.0X+828.90.9964 0.394~23.6440133安格洛苷CY=825.6X-148.20.99940.3095~12.3830100梓醇Y=1125.9X-91.30.99900.1940~7.76 2067

表3 玄参中8种化合物的加样回收试验结果(n=3)

表3(续)

表4 不同来源玄参中8个成分含量 /mg·g-1
3 讨论
3.1 HPLC-MS/MS法同时测定玄参中8个成分较HPLC法的优势
玄参药材中含有多种成分,杂质较多,用HPLC法测定8个成分[9],色谱分离难度较大,如果强行分离,分析时间会长达50 min以上,并且选择性较HPLC-MS/MS法差;如果加上过多净化步骤,操作繁琐,费时,容易造成损失,回收率下降,用HPLC-MS/MS法可以同时分析玄参中8个成分,提取离子流图几乎看不到任何其他物质的干扰,分析时间短(22 min内),回收率高,适用于上述成分的同时测定。
3.2质谱条件的选择
化合物在质谱中以[M+Na]+或[M+NH4]+存在,在甲酸作用下,供试液呈酸性,正模式下,有助样品离子化。对甲酸浓度(0.05%、0.1%、0.2%)进行考察,发现灵敏度差距不大,最终选择甲醇-0.05%甲酸水溶液作为流动相。
3.3提取条件的优化
考察不同提取溶剂(甲醇、70%甲醇水、50%甲醇水、30%甲醇水、水)、不同提取方式(加热回流、超声)及提取时间(10、20、30、45、60min)和提取次数(1、2、3次),最终确定称取药材粉末0.2g、用50%甲醇水溶液提取45min、50mL分两次提取为最佳提取条件。
[1] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015:117.
[2] 肖培根.新编中药志[M].北京:化学工业出版社,2002:336.
[3] 胡瑛瑛,黄真.玄参的化学成分及药理作用研究进展[J].浙江中医药大学学报,2008,32(2):268.
[4] 邹臣亭,杨秀伟.玄参中一个新的环烯醚萜糖甙化合物[J].中草药,2000,31(4):241-243.
[5] 李静,陈长勋,高阳,等.玄参提取物抗炎与抗动脉硬化作用的探索[J].时珍国医国药,2010,21(3):532.
[6]GuWL,ChenCX,WuQ,etal.EffectsofChineseherbmedicineRadixScrophulariaeonventricularremodeling[J].Pharmazie,2010,65(10):770-775.
[7]SunX,XiongZ,ZhangY,etal.HarpagosideattenuatesMPTP/MPP+induceddopaminergicneurodegenerationandmovementdisorderviaelevating glial cell line-derived neurotrophic factor[J].J Neurochem,2012,120(6):1072.
[8] 张雪梅,王瑞,安睿,等.HPLC同时测定玄参中5种成分的含量[J].中国中药杂志,2011,36(6):709-711.
[9] Cao G,Cong X D,Cai H,et al.Simultaneous quantitation of eight active components in crude and processed Radix Scrophulariae extracts by high performance liquid chromatography with diode array detector[J].Chin J Nat Med,2012,10(3):213-217.
SimultaneousDeterminationofEightComponentsinRadixScrophulariaebyHPLC-MS/MS
ZHOU Jia1*,QI Hongyi2
(1.SichuanInstituteforFoodandDrugControl,Chengdu611731,China; 2.SouthwestUniversity,Chongqing400715,China)
Objective:To establish a method for simultaneous determination of eight components in Radix Scrophulariae including catalpol,harpagoside,geniposide,acteoside,angoroside C,cinnamic acid,harpagide,5-HMF.Methods:Chromatographic separation was performed on an Agilent ZORBAX Eclipse XDB-C18 column (150 mm × 4.6 mm,5 μm) at 30 ℃ of column temperature.0.05% aqueous formic acid (A) and methanol (B) were adopted as mobile phase with a gradient elution.The flow rate was set at 0.6 mL·min-1.The injection volume was 2 μL.Detection was carried out on a triple quadrupole mass spectrometer in the positive ion mode using an electrospray source.Multiple reaction monitoring(MRM) mode was employed.Results:The developed method showed good linearity in the range of 0.194 0-7.76 μg·mL-1(r=0.999 0) for catalpol,0.173 8-32.85 μg·mL-1(r=0.999 8) for harpagoside,0.394-23.64 μg·mL-1(r=0.996 4) for geniposide,0.279 5-16.77 μg·mL-1(r=0.9974) for acteoside,0.309 5-12.38 μg·mL-1(r=0.999 4) for angoroside C,0.087-5.220 μg·mL-1(r=0.9991) for cinnamic acid,0.264 5-31.74 μg·mL-1(r=0.999 8) for harpagide,0.034 3-1.370 0 μg·mL-1(r=0.999 2) for 5-HMF,respectively.The limit of detection was 5-50 ng·mL-1.The recoveries varied between 91.33%-99.78%.Harpagide,harpagoside and angoroside C were found to be the most abundant components in Radix Scrophulariae.There were significant differences in distribution of these components among the samples from different origins.Conclusion:The established method of determination of 8 kinds of component content in Radix Scrophulariae within 22 min is proved to be accurate and sensitive.The experimental results can provide reference for the quality of Radix Scrophulariae.
Radix Scrophulariae;catalpol;harpagoside;geniposide;acteoside;angoroside C;cinnamic acid;harpagide;5-HMF;HPLC-MS/MS
重庆市科技人才培养(创新青年科技人才培养)项目(cstc2013kjrc-qnrc10002)
] 周佳,主管药师,硕士,研究方向:食品药品检验;E-mail:275946785@qq.com
10.13313/j.issn.1673-4890.2017.5.015
2016-12-30)
*[
