适宜无机盐及浓度抑制麦胚脂肪酶存在时油水界面张力
2017-09-15陈中伟王力坤吴其飞
陈中伟,孙 俊,王力坤,吴其飞,徐 斌※
适宜无机盐及浓度抑制麦胚脂肪酶存在时油水界面张力
陈中伟1,2,孙 俊1,王力坤1,吴其飞2,徐 斌1※
(1. 江苏大学食品与生物工程学院,镇江 212013;2. 江苏大学农产品加工工程研究院,镇江 212013)
为了探明无机盐稳定化脂肪酶的潜在机理,该文以小麦胚芽脂肪酶为研究对象,基于界面酶学的分析方法,研究添加浓度介于1.0×10-9~1.0×10-2mol/L的Na+、K+、Ca2+、Mg2+的氯化物对小麦胚芽脂肪酶存在的油-水界面特性的影响。结果表明,当小麦胚芽脂肪酶体系浓度为1.7×10-6mol/L时,一价金属中Na+更有利于抑制油-水界面的表面张力(P<0.05),对麦胚脂肪酶存在时的油水界面特性影响也较大;二价金属离子Ca2+对界面张力的影响趋势与一价离子不同,在高浓度时反而增加界面张力;当油水界面上存在脂肪酶的催化底物(三油酸甘油酯)和产物(油酸)时,添加浓度分别为10-6、10-6、10-4和10-9mol/L的Na+、K+、Ca2+、Mg2+均可一定程度上降低油水界面张力,从而降低麦胚脂肪酶的作用效果,三油酸甘油酯存在时Mg2+的作用效果最明显(P<0.05),油酸存在时Na+的作用效果最明显(P<0.05)。综上,无机盐金属离子主要通过影响麦胚脂肪酶在油水界面的聚集行为及底物结构状态起到钝化麦胚脂肪酶的作用,该结果可为麦胚脂肪酶存在时界面的活性调控及麦胚的稳定化处理提供参考。
氯化物;脂肪酶;界面能;无机盐;小麦胚芽
陈中伟,孙 俊,王力坤,吴其飞,徐 斌. 适宜无机盐及浓度抑制麦胚脂肪酶存在时油水界面张力[J]. 农业工程学报,2017,33(15):308-314. doi:10.11975/j.issn.1002-6819.2017.15.039 http://www.tcsae.org
Chen Zhongwei, Sun Jun, Wang Likun, Wu Qifei, Xu Bin. Suitable inorganic salt and its content inhibiting tension of oil-water interface with wheat germ lipase[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2017, 33(15): 308-314. (in Chinese with English abstract) doi:10.11975/j.issn.1002-6819.2017.15.039 http://www.tcsae.org
0 引 言
小麦胚芽是小麦加工的主要副产物之一,约占整个小麦籽粒的2.5%~3.0%[1]。小麦胚芽营养丰富,被誉为“人类营养的天然宝库”[2-3]。全球每年5.5亿t小麦产量中,大约可产出100万t功能性油脂和300万t蛋白质,但目前有效利用率却不足10%[4],主要是因为小麦胚芽中含有丰富的脂肪酶,在其作用下脂肪极易水解,导致小麦胚芽的酸败变质[5-6],为此,小麦胚芽稳定化是当前备受关注的课题[7]。
小麦胚芽脂肪酶(LA,lipase A)是一种两亲性且具有界面活性的蛋白分子,只能作用于油水界面[8],该界面不仅是LA催化反应的关键场所,也是调控LA催化活性的合适位点[9]。多年来,学界关于油水界面的理解一直局限于所谓“界面性质”的模糊认识,并推测脂肪酶与底物之间的相互作用可能包括静电吸引,底物的取向性和水合作用等。直到最近,Reis应用生物物理学理论,才首次揭开了界面微环境与脂肪酶催化活性的内在关联[10]。事实上,脂类酶促水解是典型的多相催化反应,其反应速率和方向取决于界面微环境的所有组成成分[9]。界面组成所呈现出的特征及其与酶催化效率的关联性,不仅为今后研究脂肪酶界面催化反应提供了新方法,也为研究麦胚脂肪酶的钝化方法开辟了新的途径。
研究表明,全麦粉中添加一定量Na+,可抑制76.7%脂肪酶活力[11];Na+对膜结合脂肪酶活力抑制率达55%[12],由此可见,加入金属离子抑制剂可作为钝化LA的辅助手段[13]。此外,LA本身并不能决定酶促反应的平衡常数,其催化水解效率依赖于LA的界面活性以及底物、产物以及抑制剂在界面的扩散速率与动态分布[14]。Torcello-Gómez等[15]研究发现,金属离子可与离子化脂肪酸特异性形成某种复合物,改变脂肪酸溶解性和油水界面的某些性质,进而影响脂肪酶催化活性。因此,在无机盐作用下,LA所处微环境发生改变,势必影响界面层(水相)对LA的吸附[16]和底物在界面层(油相)的定位[15]。此外,各种界面活性分子也会在界面层产生竞争[15],如甘油三酯水解产生具有界面活性的二酰甘油、单酰甘油等会占据界面层与LA分子发生竞争,或者通过分子间相互作用使LA构象发生变化。上述两种作用机制都可能对LA的催化效果产生影响[17-18]。因此,对油水界面特性的深入研究与充分认识,将有助于发现新的LA活力调控方式。
目前,有关金属离子对LA影响作用的研究中,一般涉及无机盐对LA活性、结构等影响方面的研究[19-20],而金属离子是否会对麦胚LA存在时油水界面特性产生影响,进而影响LA的催化活性尚停留在推断阶段。基于上述现状,本研究基于界面酶学分析方法,研究不同浓度的NaCl、KCl、CaCl2、MgCl2对麦胚LA、麦胚LA+三油酸甘油酯和麦胚LA+油酸3种不同油水界面模型的影响,以期从界面特性角度分析Na+、K+、Ca2+、Mg2+4种金属离子对麦胚LA催化功能的影响机制,为小麦胚芽稳定化方法的建立提供理论研究依据。
1 材料与方法
1.1 材料与仪器
麦胚LA(产品编号L3001)、单油酸甘油酯,购自美国Sigma有限公司;癸烷,纯度99%,购自英国Alfa Aesar A Johnson Matthey公司;油酸、三油酸甘油酯、NaCl、KCl、CaCl2、MgCl2均为分析纯,购自上海国药化学试剂有限公司。
DCAT11界面张力仪,德国Dataphysics公司;AR-G2旋转流变仪,美国TA Instruments公司;ED-F12标准型加热水浴槽循环器,德国Julabo公司。
1.2 试验方法
1.2.1 界面张力测定
采用吊片法测定麦胚LA油水界面的张力[21]。界面张力结果为3次测量的平均值,试验温度为25.0±0.1 ℃。计算公式如下:
F=mg+2γ(L+d)cosθ (1)
式中F为铂片所受拉力,N,m为铂片质量,kg;g为重力加速度,m/s2;L为铂片长度,m;d为铂片厚度,m;γ为表面张力,N/m;θ为接触角,(°)。由于d<<L,所以F=mg+2γLcosθ。
1.2.2 界面流变性质的测定
利用配有Du Nouy环系统的AR-G2旋转流变仪进行测定,具体操作如下:1)将20 mL磷酸盐缓冲溶液加入样品杯;2)把盘放置在珀尔贴平板上的定位环内;3)降下机头直至环定位与液体上表面的平面;4)将约5 mL癸烷均匀地加入到水样表面,至完全浸没Du Nouy环;5)在振荡模式下,选择“Strain sweep step”,测试频率为1Hz时,油水界面的流变性质,选择G'(储能模量)和G''(损耗模量)呈线性变化区间内的应变(strain)值,进行后续测定。选择“Frequency sweep step”,测试25 ℃、特定Strain下、频率0.1~3 Hz区间内16个点的界面流变性质;6)程序设定完成后,测定界面剪切弹性模量和界面剪切黏度等。
1.2.3 不同浓度麦胚LA存在的界面模型构建
以癸烷为油相、0.1 mol/L的磷酸盐缓冲溶液(pH值=7.0)为水相,建立油水界面模型,同时分别添加1.70×10-8~1.70×10-6mol/L的麦胚LA到水相,研究不同浓度的麦胚LA对油水界面张力和界面流变特性的影响。
1.2.4 不同种类与浓度的无机盐对麦胚LA界面特性的影响
以NaCl、KCl、CaCl2、MgCl24种无机盐的形式向油水界面模型水相中分别添加4种金属离子,研究浓度介于1.0×10-9~1.0×10-2mol/L间的NaCl、KCl、CaCl2、MgCl2对麦胚LA界面张力和界面流变特性的影响。
1.2.5 不同浓度三油酸甘油酯对界面组成与结构的影响
根据1.2.3的试验结果,固定磷酸盐缓冲溶液中麦胚LA浓度,设定油水界面模型油相中三油酸甘油酯的浓度分别为1×10-7、1×10-6、1×10-5、1×10-4、1×10-3和1×10-2mol/L,分别按照1.2.1、1.2.2中的方法测定界面张力、界面流变参数。分析不同浓度三油酸甘油酯对油水界面组成与结构的影响。
1.2.6 不同浓度水解产物(油酸)对界面组成与结构的影响
根据1.2.3的试验结果,固定磷酸盐缓冲溶液中麦胚LA浓度,设定油水界面模型油相中油酸的浓度为5×10-6、5×10-5、5×10-4、5×10-3、5×10-2和5×10-1mol/L,分别按照1.2.1、1.2.2中的方法测定界面张力、界面流变参数。分析不同浓度水解产物对油水界面组成与结构的影响。
1.2.7 底物或产物存在时,无机盐对麦胚LA界面特性的影响
参考1.2.3的试验结果,在每种无机盐的不同研究浓度范围内,选取对麦胚LA界面张力和界面流变性质影响较大的某一浓度,同时按照1.2.5、1.2.6的试验结果,选取对界面特性影响最大时的三油酸甘油酯和油酸的浓度,研究有底物或产物存在时,NaCl、KCl、CaCl2、MgCl24种无机盐对麦胚LA界面张力和界面流变特性的影响。
1.3 统计方法
试验结果为3次重复测定结果的平均值。采用Minitab进行数据分析,数据间差异性以95%置信区间(P<0.05)来说明。
2 结果与分析
2.1 不同浓度麦胚LA对油水界面组成与结构的影响
麦胚LA浓度对油水界面特性的影响见图1。如图1a所示,随着麦胚LA浓度的增加,油水界面张力下降趋势明显[22],当麦胚LA浓度超过1.70×10-6mol/L时,油水界面处分子分布不稳定,无法测得稳定数据。
图1b是不同浓度麦胚LA对油水界面损耗因子(tanδ)即损耗角正切值的影响。tanδ越大,耗散能量的能力越强;由图可见,tanδ随麦胚LA浓度的增加而增加,当麦胚LA浓度为1.70×10-6mol/L,tanδ值达到最大。该变化趋势与界面张力变化趋势有一定的相似性,原因可能是,麦胚LA浓度具有两性特性,易富集在油水界面上。随着其浓度的增加,导致界面黏度增加,进而影响了因界面形变而耗散的能量[8]。综上,为了能够观察到明显而准确的试验结果,在后续研究中选取麦胚LA的浓度为1.70×10-6mol/L。
2.2 一价金属离子对油水界面组成与结构的影响
已有研究结果表明,电解质的加入能使溶液内部粒子之间的相互作用强于纯水[23]。因此,在一定浓度范围内,电解质的加入会使油/水溶液界面张力增大。本研究就Na+、K+离子对油水界面组成与结构的影响进行了验证研究。如图2所示,Na+、K+对界面张力的影响相似,对麦胚LA界面张力的影响随其浓度的增加呈现先增加后降低的趋势[24-25],但高浓度时K+对油水界面张力的影响不及Na+显著(P<0.05)。当离子浓度在1.0×10-9~1.0×10-6mol/L时,Na+、K+均可明显提高界面张力。当K+浓度高于1.0×10-5mol/L,麦胚LA的油水界面张力开始明显降低。原因可能是高浓度无机盐离子将影响麦胚LA在溶液界面上的聚集数量和稳定性。由于麦胚LA具有类似于分子表面活性剂的性质,可以紧密吸附界面上,从而降低界面张力[26]。
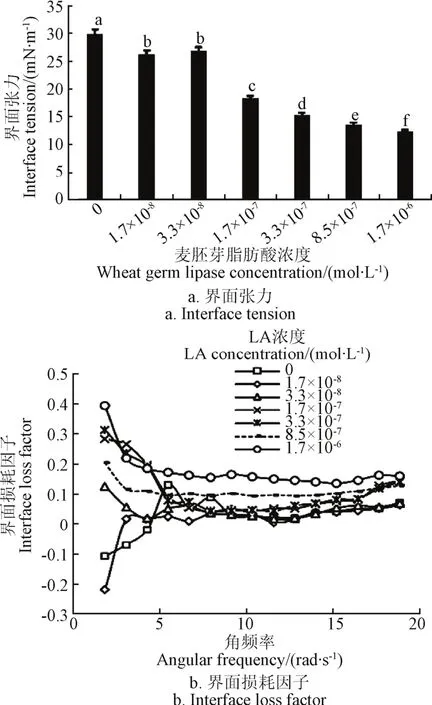
图1 麦胚LA浓度对油水界面特性的影响Fig.1 Effect of wheat germ lipase concentration on oil/water interfacial properties

图2 NaCl及KCl对麦胚LA浓度为1.7×10-6mol/L的油水界面张力的影响Fig.2 Effect of NaCl and KCl on tension of oil/water interface with LA concentration of 1.7×10-6mol/L
此外,Na+、K+对麦胚LA界面流变性质的影响的结果(见图3)表明:在所研究的无机盐浓度范围内,Na+、K+对界面流变参数的影响规律较差,不稳定,原因在于NaCl和KCl作为中性无机盐可通过“盐溶”和“盐析”作用对溶液中的表面活性剂的界面溶解度产生影响[21]。同时,Na+、K+表现出的界面惰性物质会阻止表面活性物质等在水中的溶解性,并且Na+、K+与水溶性酸离子结合后生成的酸式盐可占据界面,降低有效界面的面积[27]。

图3 NaCl、KCl浓度对油水界面流变特性的影响Fig.3 Effect of NaCl and KCl concentration on oil/water interfacial rheological properties
2.3 二价金属离子对油水界面组成与结构的影响
二价金属子Ca2+、Mg2+对油水界面张力的影响见图4。由图可知,低浓度时,Ca2+对油水界面张力的影响较小;当Ca2+浓度达到1.00×10-4mol/L时,界面张力骤然增至18.3 mN/m;而Mg2+对界面张力的影响与Ca2+有相反的趋势,呈现低浓度促进,高浓度抑制的现象,该结果与于立军等的研究结果一致[28]。原因在于在所试验温度的油水界面上,Ca2+和Mg2+形成不溶物的浓度明显不同,对油水界面张力产生影响的浓度范围也不同。
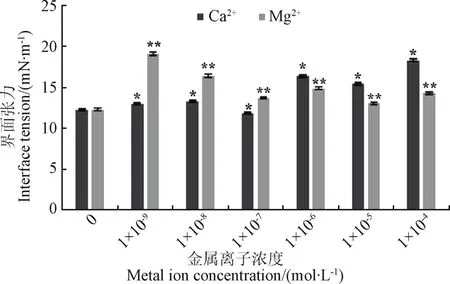
图4 CaCl2及MgCl2浓度对油水界面张力的影响Fig.4 Effect of CaCl2and MgCl2concentration on oil/waterinterface tension
Ca2+、Mg2+对界面流变参数的影响见图5。由图5可知,Ca2+、Mg2+对界面流变参数的影响规律性较差,可能是由于同为二价阳离子的Ca2+、Mg2+易与磷酸盐缓冲溶液中磷酸根结合形成微溶于水的沉淀,造成界面流变参数变化不稳定[29]。
与一价金属离子相比,较高浓度的二价金属离子反而会一定程度上增加油水界面的张力,这可能与二价金属离子在油水界面上的溶解特性有直接关系。本文中选取的二价金属离子为Ca2+、Mg2+,在水溶液中容易与体系中的磷酸根离子结合,进而破坏原有油水界面的离子状态。使得界面的黏度不降反升。该问题会在后续的研究中进一步验证。
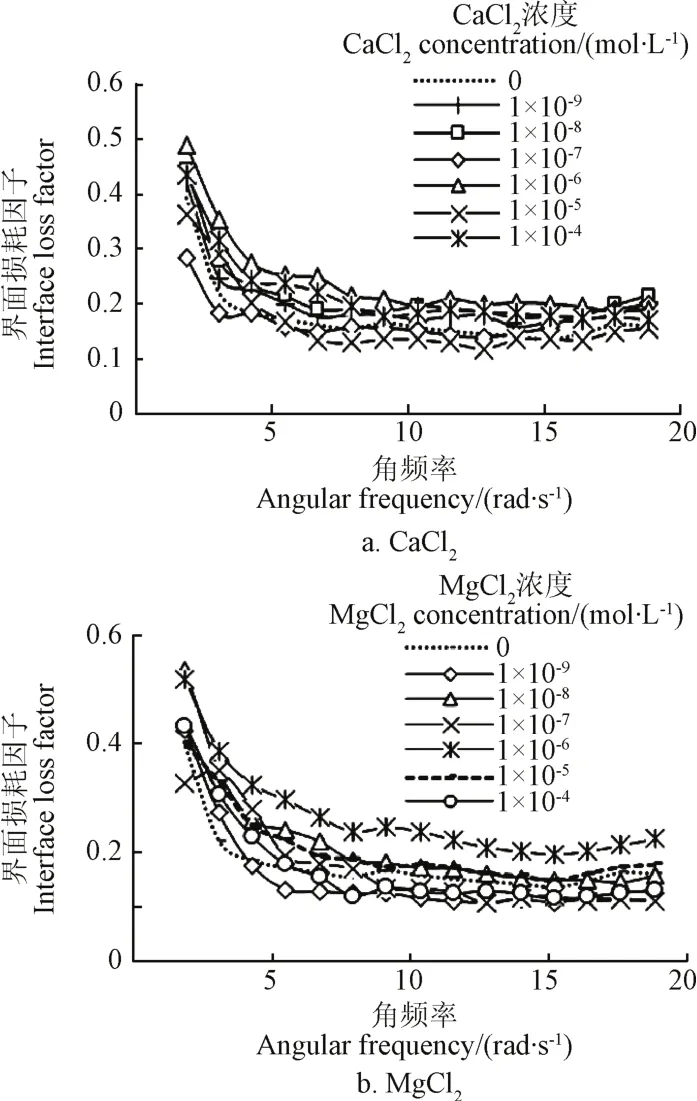
图5 CaCl2及MgCl2浓度对油水界面流变特性的影响Fig.5 Effect of CaCl2and MgCl2concentration on oil/water interfacial rheological properties
2.4 不同浓度三油酸甘油酯底物对油水界面组成与结构的影响
三油酸甘油酯浓度对油水界面特性的影响见图6。由图6可见,当麦胚LA浓度为1.70×10-6mol/L时,油水界面张力随癸烷中三油酸甘油酯浓度的增加呈现先增加后减小的变化规律;当三油酸甘油酯浓度介于10-5~10-3mol/L时,相同角频率时界面损耗因子随着浓度增加无明显变化规律。此外,在试验过程中,界面张力随时间延长呈现一定下降趋势,这说明麦胚LA与三油酸甘油酯的水解过程也会对界面张力产生一定影响。原因在于,在界面体系中,三油酸甘油酯可被麦胚LA水解,产生小分子的油酸等,三油酸甘油酯与麦胚LA组成的界面发生变化,进而影响界面特性。
2.5 水解产物对油水界面组成与结构的影响
油酸浓度对油水界面特性的影响见图7,由图可知:随着油酸浓度的增加,界面张力呈现先增加后减小的变化趋势,界面流变学参数的变化规律与其对界面张力的作用规律相似。油酸作为麦胚LA的小分子水解产物,更容易分布于油水界面处[30],与麦胚LA竞争有限的界面面积,显然油酸与麦胚LA对界面特性的影响不同。当油酸浓度处于5.0×10-6~5.0×10-5mol/L之间时,界面张力与tanδ均处于最大值范围,即该浓度范围内界面处油酸与麦胚LA的竞争关系最明显,可以理解为该浓度范围油酸的加入,对麦胚LA的抑制效果最好。

图6 三油酸甘油酯浓度对油水界面特性的影响Fig.6 Effect of glycerol trioleate concentration on oil/water interfacial properties
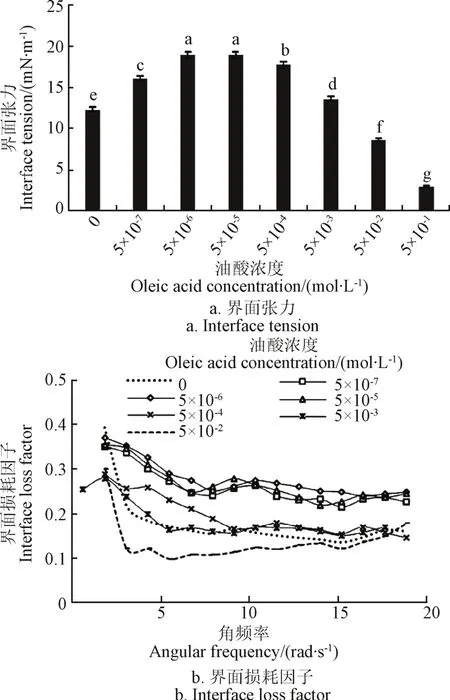
图7 油酸浓度对油水界面特性的影响Fig.7 Effect of oleic acid concentration on oil/water interfacial properties
2.6 底物或产物存在时无机盐对麦胚LA界面特性的影响
如图8a所示,当癸烷中分别添加1×10-5mol/L三油酸甘油酯(底物)或5×10-6mol/L油酸(产物)时,CaCl2浓度为1.0×10-4mol/L时,油酸存在时界面张力从17.6 mN/m增大至18.2 mN/m(P<0.05)。此外,不同种类及浓度无机盐的加入均降低了三油酸甘油酯或油酸存在时的油水界面张力(P<0.05)。其中,三油酸甘油酯存在时,Mg2+的作用效果最明显;油酸存在时,Na+的作用效果最明显,界面张力从17.8 mN/m降低至16.2 mN/m,差异显著(P<0.05)。
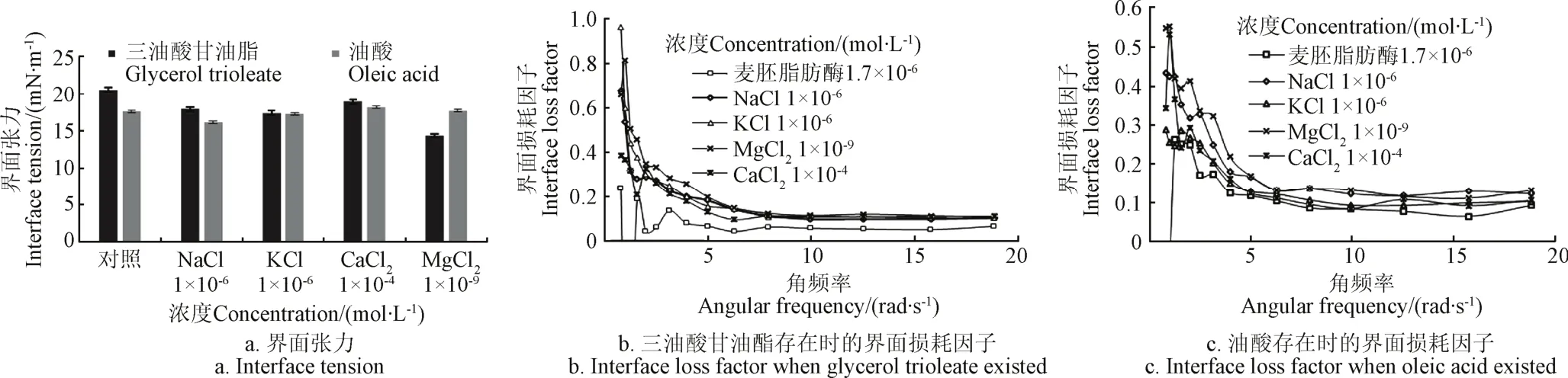
图8 底物(三油酸甘油酯1×10-5mol·L-1)和产物(油酸5×10-6mol·L-1)存在条件下无机盐对界面特性的影响Fig.8 Effect of inorganic salts on interfacial properties with the exist of substrate (1×10-5mol·L-1glycerol trioleate) or product (5×10-6mol·L-1oleic acid)
从图8b和图8c可以看出,三油酸甘油酯或油酸存在时,无机盐对tanδ的影响规律性较差,出现上述情况的原因可能是因为无机盐离子降低了麦胚LA在油水界面的溶解度,从而为三油酸甘油酯或油酸保留了更多的界面面积,有利于更多的三油酸甘油酯或油酸占据有效界面,以至于降低了底物或产物存在时的油水界面张力[16]。
3 结 论
1)当无机盐浓度在10-6~10-9mol/L范围内时,界面张力变化具有明显规律,而界面流变参数变化规律性较差。界面处仅有小麦胚芽脂肪酶存在时,一价金属中Na+更有利于抑制油-水界面的表面张力,对麦胚脂肪酶存在时的油水界面特性影响也较大;二价金属离子Ca2+对界面张力的影响趋势与一价离子不同,在高浓度时反而增加界面张力,可能是受到试验体系中磷酸根离子的影响;
2)在麦胚脂肪酶的作用底物,即三油酸甘油酯(10-5mol/L)存在时,添加浓度分别为10-6、10-6、10-4和10-9mol/L的Na+、K+、Ca2+、Mg2+均可一定程度上降低油水界面张力的加入降低了三油酸甘油酯存在时的油水界面张力,其中,Mg2+的作用效果最明显(P<0.05)。当麦胚脂肪酶的作用产物油酸(5×10-4mol/L)存在时,添加NaCl和KCl可降低油水界面张力。添加CaCl2和MgCl2可升高油水界面张力,其中Na+的作用效果最显著(P<0.05)。
[1] 何伟忠,于明,何爽.小麦麦胚的营养保健价值及加工利用途径[J]. 新疆农业科学,2010,47(2):388-391.
He Weizhong, Yu Ming, He Shuang. The nutrient functional value and the application path of wheat germ[J]. Xinjiang Agricultural Sciences, 2010, 47(2): 388-391. (in Chinese with English abstract)
[2] Shurpalekara S R, Haridas R P. Wheat germ[J]. Advances in Food Research, 1977, 23: 187-304.
[3] 赵福利,钟葵,佟立涛,等. 不同产地小麦胚芽营养成分的比较分析[J]. 现代食品科技,2014,30(3):182-188.
Zhao Fuli, Zhong Kui, Tong Litao, et al. Analysis of nutritional components of wheat germ from different producing areas[J]. Modern Food Science and Technology, 2014, 30(3): 182-188. (In Chinese with English abstract)
[4] De Vasconcelos M, Bennett R, Castro C, et al. Study of composition, stabilization and processing of wheat germ and maize industrial by-products[J]. Industrial Crops and Products, 2013, 42: 292-298.
[5] Rao H P, Kumar G V, Ranga R G. Studies on stabilization of wheat germ[J]. Food Science and Technology, 1980, 13: 302-307.
[6] 徐斌,李波,苗文娟,等. 小麦胚芽贮藏过程中的酸败变质机理[J]. 中国粮油学报,2011,26(9):123-128.
Xu Bin, Li Bo, Miao Wenjuan, et al. Mechanism of acidification and deterioration of wheat germ during storage[J]. Journal of the Chinese Cereals and Oils Association, 2011, 26(9): 123-128. (in Chinese with English abstract)
[7] Doblado-Maldonado A F, Pike O A, Sweley J C, et al. Key issues and challenges in whole wheat flour milling and storage[J]. Journal of Cereal Science, 2012, 56(2): 119-126.
[8] Carrasco-López C, Godoy C, de Las Rivas B, et al. Activation of bacterial thermoalkalophilic lipases isspurred by dramatic structural rearrangements[J]. Journal of Biological Chemistry, 2009, 284(7): 4365-4372.
[9] Reis P, Holmberg K, Watzke H, et al. Lipases at interfaces: a review[J]. Advances in Colloid and Interface Science, 2009, 147: 237-250.
[10] Reis P, Watzke H, Leser, M, et al. Interfacial mechanism of lipolysis as self-regulated process[J]. Biophysical Chemistry, 2010, 147(3): 93-103.
[11] Doblado-Maldonado A F. New Technologies for Whole Wheat Processing: Addressing Milling and Storage Issues[D]. Lincoln Nebraska: 2012, University of Nebraska-Lincoln.
[12] O'Connor J, Harwood J L. Solubilization and purification of membrane-bound lipases from wheat flour[J]. Journal of Cereal Science, 1992, 16(2): 141-152.
[13] 王明莹,郭晓娜,朱科学. 真空碱溶液润麦处理对全麦粉稳定性和品质特性的影响[J]. 食品与机械,2017,33(2):6-10.
Wang Mingying, Guo Xiaona, Zhu Kexue. Effects on stability and qualities of whole wheat flour by treatment of vacuum tempering with alkaline solutions[J]. Food and Machinery, 2017, 33(2): 6-10. (in Chinese with English abstract)
[14] Wilde P J, Chu B S. Interfacial & colloidal aspects of lipid digestion[J]. Advances in Colloid and Interface Science, 2011, 165(1): 14-22.
[15] Torcello-Gómez A, Jódar-Reyes A B, Maldonado-Valderrama J, et al. Effect of emulsifier type against the action of bile salts at oil-water interfaces[J]. Food Research International, 2012, 48(1): 140-147.
[16] Pradines V, Fainerman V B, Aksenenko E V, et al. Adsorption of protein-surfactant complexes at the water/oil interface[J]. Langmuir, 2011, 27(3): 965-971.
[17] Reis P, Holmberg K, Miller R, et al. Competition between lipases and monoglycerides at interfaces[J]. Langmuir, 2008, 24(14): 7400-7407.
[18] Delorme V, Dhouib R, Canaan S, et al. Effects of surfactants on lipase structure, activity, and inhibition[J]. Pharmaceutical Research, 2011, 28(8): 1831-1842.
[19] 刘艳霞. 微波协同无机盐对小麦胚芽稳定化作用研究[D].镇江:江苏大学,2015.
Liu Yanxia. Research on the Mechanism of Wheat Germ Stabilization by Microwave and Inorganic Salt[D]. Zhenjiang: Jiangsu University, 2015. (in Chinese with English abstract)
[20] Kermasha S, Bisakowski B, Ramaswamy H, et al. Comparison of microwave, conventional and combination heat treatments on wheat germ lipase activity[J]. International Journal of Food Science and Technology, 1993, 28(6): 617-623.
[21] 童海英. 表面活性物质的界(表)面扩张流变粘弹性研究[D].上海:华东师范大学,2007.
Tong Haiying. Studies on Dilatational Rheologieal Viscoelasticity of Interface (surficial) of Surface active Substance[D]. Shanghai: East China Normal University, 2007. (in Chinese with English abstract)
[22] 李果,周从直,方振东,等. 无机盐对表面活性剂淋洗疏水性有机污染物的影响机理[J]. 环境科学导刊,2010, 29(5):6-10.
Li Guo, Zhou Congzhi, Fang Zhendong, et al. Influence mechanism of inorganic salt on surfactant flushing for the removal of HOCS in soil[J]. Environmental Science Survey, 2010, 29(5): 6-10. (in Chinese with English abstract)
[23] 颜肖慈,罗明道. 界面化学[M]. 北京:化学工业出版社,2005.
[24] Gao Y Q. Simple theoretical model for ion cooperativity in aqueous solutions of simple inorganic salts and its effect on water surface tension[J]. The Journal of Physical Chemistry B, 2011, 115(43): 12466-12472.
[25] 于燕梅,李以圭. 单一电解质水溶液汽液界面张力的测定[J].实验技术与管理,2004,21(5):20-25.
[26] 蔡帮鑫,张琪琪,刚洪泽,等. 餐厨废油制备的生物基两性表面活性剂的油水界面性能[J]. 应用化学,2016,33(7):798-803.
Cai Bangxin, Zhang Qiqi, Gang Hongze, et al. Bio-based zwitterionic surfactants derived from Waste cooking oil and their interfacial performance[J]. Chinese Journal of Applied Chemistry, 2016, 33(7): 798-803. (in Chinese with English abstract)
[27] 申德勇,王殿生,王玉斗,等. 离子种类和质量浓度对不同温度稠油油水界面张力影响的实验研究[J]. 西安石油大学学报:自然科学版,2012,27(2):63-66.
Shen Deyong, Wang Diansheng, Wang Yudou, et al. Experimental study on the effects of the composition and mass concentration of ions and temperature on the interfacial tension between heavy oil and brine water[J]. Journal of Xi'an Shiyou University: Natural Science Edition, 2012, 27(2): 63-66. (in Chinese with English abstract)
[28] 于立军. 阴离子表面活性剂在油水界面吸附行为的实验和理论研究[D]. 北京:中国石油大学,2011.
Yu Lijun. Theoretical and Experimental Study of Anionic Surfactant Adsorbed Behavior at Water/Oil Interface[D]. Beijing: China University of Petroleum, 2011. (in Chinese with English abstract)
[29] 王吉中,冯昕,王丽娟. 不同金属离子对米糠解脂酶活性影响的研究[J]. 现代食品科技,2007,23(2):28-30.
Wang Jizhong, Feng Xin, Wang Lijuan. Influence of metal ions on activity of rice bran lipase[J]. Modern Food Science and Technology, 2007, 23(2): 28-30. (in Chinese with English abstract)
[30] 孙燕,庞新晶,张树永. 油/水界面张力的影响因素及无机盐对油水铺展的影响[J]. 大学化学,2015,30(2):74-77.
Sun Yan, Pang Xinjing, Zhang Shuyong. The interfacial tension of oil /water interface and the effect of salt on spreading of oil over water surface[J]. University Chemistry, 2015, 30(2): 74-77. (in Chinese with English abstract)
Suitable inorganic salt and its content inhibiting tension of oil-water interface with wheat germ lipase
Chen Zhongwei1,2, Sun Jun1, Wang Likun1, Wu Qifei2, Xu Bin1※
(1. School of Food and Biological Engineering, Jiangsu University, Zhenjiang 212013, China; 2. College of Food Process Engineering, Jiangsu University, Zhenjiang 212013, China)
The stabilization of lipase is an important means to control the rancidity of highly oil-containing agricultural products, such as wheat germ. In this paper, the effects of different concentrations of Na+, K+, Ca2+and Mg2+on the oil-water interface characteristics of wheat germ lipase A (LA) were examined, based on the interfacial enzymatic analysis methods using interfacial tension meter and rotary rheometer. Firstly, the influence of the different concentrations of wheat germ LA on the interfacial tension of oil-water was studied to determine the concentration of LA system for the subsequent investigation about the effects of inorganic salts on the oil-water interface. Then, the interface tension and rheological properties of the oil-water after adding monovalent and divalent metal salt were studied to explore the effects of species and concentration on the oil-water interface. Next, the effects of different kinds of inorganic salts on the surface tension and rheological properties of oil-water interface, where there were lipase-acting substrate and product, namely, glycerol trioleate and oleic acid, were studied. Finally, the potential mechanism of inhibiting the catalytic activity of metal ions of inorganic salt in inhibiting wheat germ LA activity was discussed. The results showed that, when the concentration of LA was 1.70×10-6mol/L, the monovalent metal ions Na+and K+were more favorable to decrease the interfacial activity of oil-water and the interfacial activity of wheat germ LA, than other divalent metal ions, i.e. Mg2+and Ca2+. And the effect of Na+was higher than that of K+. In the divalent metal ions, Ca2+could decrease the interfacial tension at a low concentration and increase interfacial tension at a high concentration, while Mg2+was opposite to Ca2+. At the same time, the decrease effect of Ca2+on the interfacial tension was more obvious than Mg2+. Besides, the effects of glycerol trioleate and oleic acid on the interfacial properties of wheat germ LA were studied; the effect extent was glycerol trioleate > oleic acid, and the concentration of these 2 compounds was 1.0×10-5and 5.0×10-6mol/L, respectively. Under the 2 concentrations of glycerol trioleate and oleic acid, adding Na+(10-6mol/L), K+(10-6mol/L), Ca2+(10-4mol/L), and Mg2+(10-9mol/L)to the oil-water system, could reduce the interfacial tension of oil and water, and then reduce the effect of wheat germ lipase. In summary, inorganic salts play an important role in the inhibition of interfacial activity of wheat germ LA mainly by reducing the catalytic effect through affecting the aggregation behavior of wheat germ LA in oil-water interface and the structure of substrate, and play a role of passivating wheat germ LA. The results of this paper can provide theoretical support for the regulation of lipase activity and wheat germ stabilization in wheat germ industry.
chloride minerals; lipase; interfacial energy; inorganic salt; wheat germ
10.11975/j.issn.1002-6819.2017.15.039
TS21
A
1002-6819(2017)-15-0308-07
2017-04-14
2017-07-25
国家自然科学基金面上项目(31371877),江苏大学高级人才引进(15JDG168)
陈中伟,男(汉),河北邯郸人,助理研究员,博士,主要从事粮油精深加工技术研究。镇江 江苏大学食品与生物工程学院,212013。Email:zwchen@ujs.edu.cn.
※通信作者:徐 斌,男(汉),江苏高邮人,博士,博士生导师,2013年赴美国堪萨斯州立大学研修,主要从事粮食加工过中品质变化规律与调控策略。镇江 江苏大学食品与生物工程学院,212013。Email:xubin@ujs.edu.cn.
