CgRGS7调控胶抱炭疽菌分生抱子产量、附着胞形成及致病性
2017-09-15吴曼莉柯智健柳志强李晓宇
吴曼莉,胡 坚,张 楠,柯智健,柳志强,李晓宇
CgRGS7调控胶抱炭疽菌分生抱子产量、附着胞形成及致病性
吴曼莉,胡 坚,张 楠,柯智健,柳志强*,李晓宇
(海南大学热带农林学院,海南海口 570228)
【目的】G蛋白信号调控因子(regulators of G-protein signaling,RGS)是G蛋白信号转导通路中的负调控因子,参与多个G蛋白信号通路介导的细胞内过程,目前对于胶抱炭疽菌相关RGS蛋白的生物学功能研究较少。【方法】本研究通过同源重组获得CgRGS7基因的敲除突变体,并对其生物学功能进行初步分析。【结果】CgRGS7基因编码620个氨基酸,具有7个跨膜结构域和1个RGS功能域。CgRGS7敲除突变体与野生型菌株相比,表现为分生抱子产量降低且抱子呈多端萌发,附着胞形成率下降以及致病性减弱。【结论】CgRGS7参与调控胶抱炭疽菌分生抱子产量,同时影响芽管的形态发育、附着胞形成及致病性。
胶抱炭疽菌;G蛋白信号调控因子;分生抱子;致病性
【研究意义】胶孢炭疽菌(Colletotrichum gloeosporioides)是丝状病原真菌,能够侵染多种木本植物,包括橡胶、香蕉、芒果等多种热带作物[1]。其中芒果炭疽病是由该病菌引起的侵染性病害,在芒果种植区常有发生,尤其在贮运期易引起果实腐烂,影响芒果外观质量和品质[2-3]。胶孢炭疽菌不但寄主范围广泛,而且侵染方式多样,目前对于该病菌分子致病机制的研究还不够深入,从而也限制了相关防治技术的发展[1,4]。因此,深入解析胶孢炭疽菌致病基因,对于该病菌的防治具有的意义。
植物病原菌在侵染过程中,信号的识别及传导起着重要的作用,其中G蛋白信号途径是其感应外界信号并传导到细胞内部的重要机制之一[5],当感受到胞外信号或是受到外界刺激时,G蛋白偶联感受器被激活,促使Gα亚基空间构象做出改变,导致Gα与Gβγ分离,而游离的Gα和Gβγ能够激活下游的靶蛋白,从而引起细胞内的多种生理活动。综上,G蛋白在生物信号转导网络中有着重要的作用,其中的某个信号传递环节发生改变都可能影响到整个生物信号系统,进而引起相关生物学特性的改变。RGS蛋白负调控G蛋白信号转导通路,其GAP作用能够引起Gα-GTP的水解,导致G蛋白失去活性[6-7]。【前人研究进展】相关研究已证明,G蛋白信号途径参与调控真菌的生长发育、生殖、致病等过程[8-9],但是目前开展胶孢炭疽菌相关RGS蛋白功能研究还较少。【本研究切入点】在前期研究中,本实验室从胶孢炭疽菌中鉴定了10个含RGS结构域的蛋白。本研究选取了其中一个RGS基因进行克隆鉴定,比对结果显示该基因与Magnaporthe oryzae中的MoRGS7基因同源,因此,将基因命名为CgRGS7。利用基因敲除的方法获得该基因的敲除转化子,通过一系列表型分析鉴定其所具有的生物学功能。【拟解决的关键问题】本研究旨在明确RGS蛋白在胶孢炭疽菌生长和侵染过程中的作用,为深入解析胶孢炭疽菌致病的分子机理奠定基础。
1 材料与方法
1.1 供试材料
1.1.1 菌株及试剂 胶孢炭疽菌野生型(WT)保存于海南大学热带农林学院。MiniBEST Agarose Gel DNA Extraction Kit、MiniBEST Plasmid Purification Kit、限制性内切酶(Kpn I,Eco R I,Bam H I)及PCR相关试剂等均购自TaKaRa公司;其他试剂均为国产分析纯。
1.1.2 培养基 PDA培养基:马铃薯200 g/L、葡萄糖20 g/L,琼脂粉18 g/L。LB培养基:胰蛋白胨10 g、酵母粉5 g、NaCl 10 g,琼脂粉18 g/L。CM培养基:胰化蛋白胨6 g、酵母提取物6 g、蔗糖10 g,琼脂粉18 g/L。CZAPEK培养基:蔗糖30 g、NaNO33 g、MgSO40.5 g、K2HPO41 g、FeSO40.01 g、KCl0.5 g,琼脂粉18 g/L。MM培养基:K2HPO47 g、KH2PO43 g、(NH4)2SO41 g、MgSO40.1 g、柠檬酸钠0.5 g、葡萄糖5 g,琼脂粉18 g/L。
1.2 试验方法
1.2.1 CgRGS7基因的克隆及序列分析 胶孢炭疽菌总RNA提取采用TaKaRa MiniBEST Plant RNA Extraction Kit(TaKaRa,中国),利用PrimeScriptTMII 1st Strand cDNA Synthesis Kit(TaKaRa,中国)合成
cDNA。以胶孢炭疽菌野生型菌株的cDNA为模板,CgRGS7F和CgRGS7R(表1)为引物扩增目的基因,PCR产物连接pMD18-T载体转化后提取质粒送公司进行测序。利用SMART(http://smart.embl-heidelberg.de/)工具对CgRGS7进行蛋白结构域分析,通过NCBI中BLASTp工具对CgRGS7进行蛋白同源性分析,用Clustal X(1.83)软件进行多序列比对,利用MEGA5.0软件以邻近相接法(Neighborjoining,NJ)构建系统进化树。
1.2.2 CgRGS7基因的敲除与验证 以图1的原理进行CgRGS7基因的敲除。胶孢炭疽菌基因组DNA提取方法参照文献[10],以提取的基因组作为模板,通过CgRGS7上下游片断引物[CgRGS7upF/ CgRGS7upR、CgRGS7downF/CgRGS7downR(表1)]分别进行CgRGS7基因的上下游序列扩增。利用试剂盒对扩增产物进行回收纯化,再分次连接到质粒pCB1532(含氯嘧磺隆抗性基因Sur)上,通过电泳验证无误后即获得敲除载体。将敲除载体经Eco R I酶切成线性化后转入到胶孢炭疽菌野生型原生质体中,参照文献的方法步骤进行原生质体制备及转化[11]。敲除转化子利用含有氯嘧磺隆的培养基进行筛选,随后提取抗性转化子的基因组DNA,分别根据基因上游片段的前段序列和下游片段的后段序列设计验证引物CgRGS7UU和CgRGS7DD,并根据pCB1532的内部序列设计引物PI和PI1,利用3对引物(CgRGS7F+CgRGS7R、CgRGS7UU+PI、CgRGS7DD+PI1)(表1)对转化子进行PCR鉴定,结果显示,若利用引物CgRGS7F+CgRGS7R扩增结果无条带,但引物CgRGS7UU+PI、CgRGS7DD+PI1能扩增出目的片段的转化子即为目的基因敲除转化子。
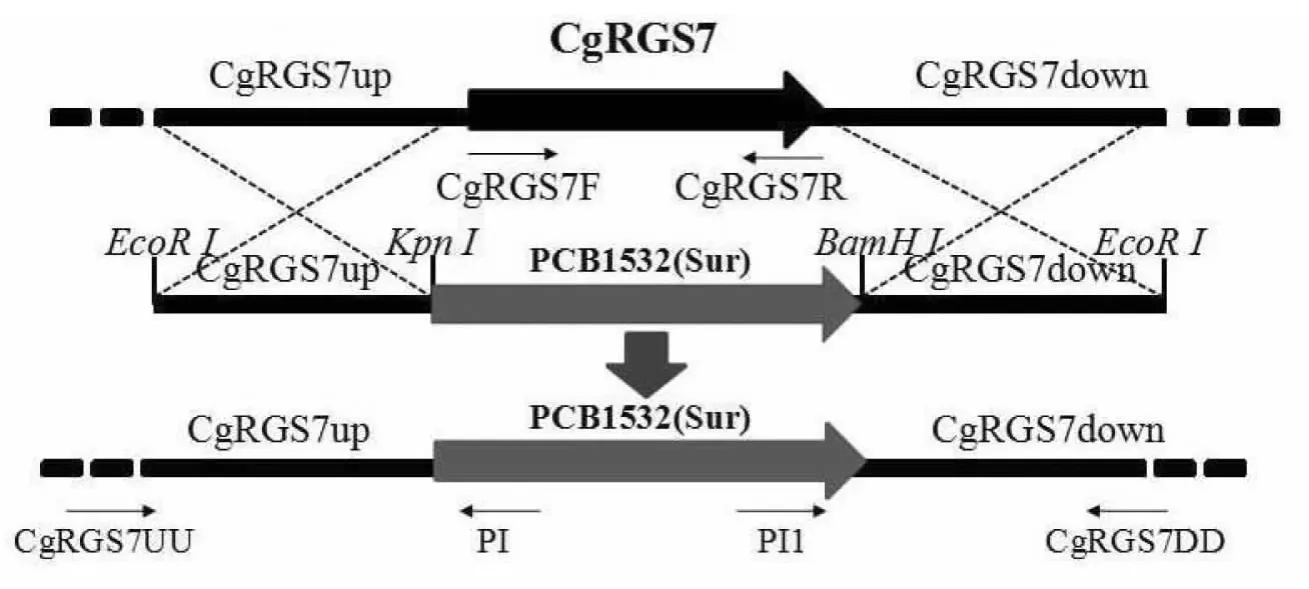
图1 CgRGS7基因敲除原理Fig.1 Gene knockout principle of CgRGS7
1.2.3 敲除转化子表型分析 ①营养生长及胁迫因子敏感性分析。无菌环境下,分别于PDA平板上接种胶孢炭疽菌野生型和敲除转化子,7 d后用打孔器打取菌落边缘、菌饼分别接种于PDA、CM、CZAPEK和MM培养基中。同时为了探究CgRGS7基因对胶孢炭疽菌渗透压及氧化应激反应的影响,打取5 mm的菌饼分别接种于含有NaCl(浓度分别为0、0.5、0.8和1.0 mol/L)、H2O2(浓度分别为0、5、10和20 mmol/L)及0.01%SDS的MM平板上,28℃培养7 d后,观察菌丝生长情况并测量菌落直径,每组设3个重复。②分生孢子产量及萌发。野生型和敲除转化子在PDA平板上28℃培养约9 d,用灭过菌的涂布棒轻扫菌落表面气生菌丝后28℃光照培养3 d诱导产孢,取含有0.4%吐温80的无菌水涂布平板,菌液经过滤制得孢子悬浮液,并用血球计数板进行孢子浓度计数,每处理设3个重复。取孢子悬浮液滴加于载玻片上,28℃保湿培养,于8 h后观察孢子萌发情况,18 h后观察附着胞形成情况。③致病性分析。选取无创伤且无病斑的芒果,用灭菌的大头针在芒果表面形成小创口,无菌条件下于活化好的PDA平板上打取菌饼,分别接种在芒果的无伤口及有伤口的位置,每处理3个重复,28℃保鲜盒内保湿培养,5 d后观察致病情况并记录。

表1 引物名称及序列Table 1 Primers and sequences
2 结果与分析
2.1 基因的克隆及序列分析
PCR扩增与pMD18-T载体连接,转化后提取质粒送公司测序,结果表明CgRGS7基因开放阅读框全长1860 bp,编码620个氨基酸,在N末端含有7次跨膜结构域,C末端第397~508位氨基酸含有1个RGS功能域(图2-A)。将CgRGS7在NCBI中进行BLASTp比对,通过MEGA5.0与不同真菌的RGS蛋白序列一起构建系统发育树(图2-B)。CgRGS7与C.gloeosporioides Nara gc5的RGS蛋白(XP-007278705)相似度达到95%,此外CgRGS7与C. salicis和C.sublineola同源蛋白相似性较高,分别为76%和69%。
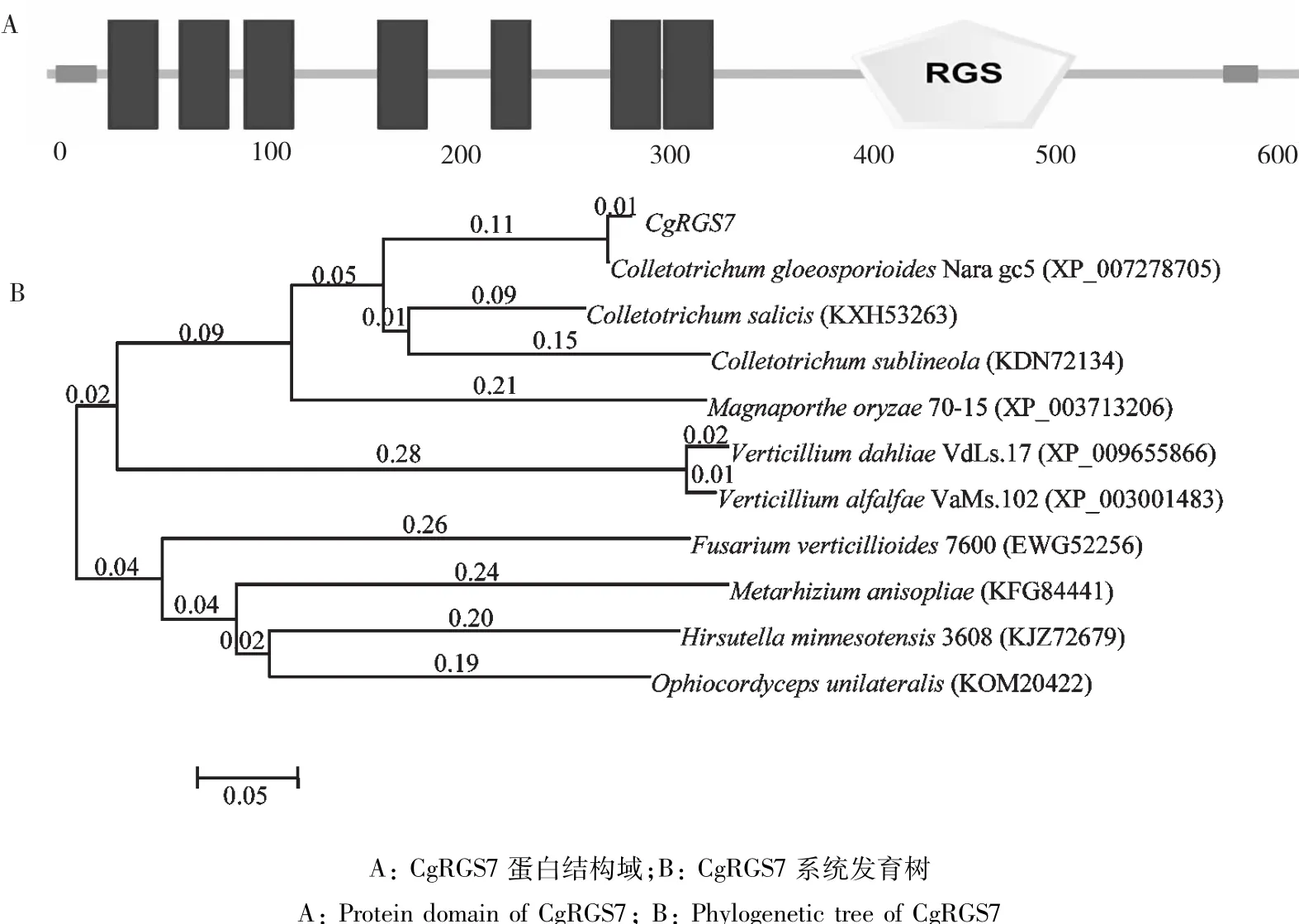
图2 CgRGS7蛋白结构域和系统发育树Fig.2 Protein domain and phylogenetic tree of CgRGS7

图3 CgRGS7敲除突变体的验证Fig.3 Verification of CgRGS7 gene knockoutmutant
2.2 CgRGS7基因的敲除与验证
将CgRGS7基因的敲除载体经限制性内切酶Eco R I酶切线性化后转入胶孢炭疽菌野生型原生质体中,共获得156个转化子,利用3对引物CgRGS7F+CgRGS7R、CgRGS7UU+PI、PI1+ CgRGS7DD(表1)进行筛选,其中第44号转化子利用CgRGS7F+CgRGS7R引物不能扩增目的条带,而通过CgRGS7UU+PI、PI1+CgRGS7DD引物能够分别扩增出目的条带(图3),即确定第44号转化子为阳性转化子,将其命名为ΔCgRGS7-44。
2.3 突变体表型分析
2.3.1 营养生长及胁迫因子敏感性分析 为了探究CgRGS7基因对胶孢炭疽菌营养生长的影响,将野生型和ΔCgRGS7-44分别接种于PDA、CM、CZAPEK和MM培养基中,28℃培养7 d,在前3种培养基中,ΔCgRGS7-44与野生型在菌落形态和生长速率方面无明显不同,但在MM培养基上敲除转化子较野生型生长速率稍显缓慢(图4)。在胁迫因子敏感性试验中,经抑制率计算分析,ΔCgRGS7-44在含不同浓度NaCl、H2O2和SDS的MM培养基上,生长形
态及速率与野生型相比均无显著性差异。由此可见,CgRGS7基因的敲除对胶孢炭疽菌的营养生长及相关胁迫因子敏感性的影响不大。
2.3.2 分生抱子产量及萌发情况 经过血球计数板计数,在产孢量方面ΔCgRGS7-44与野生型相比有明显对比,野生型分生孢子浓度平均为(8.16± 0.2×106)个/mL,敲除转化子ΔCgRGS7-44分生孢子浓度为(5.17±1.04×104)个/mL,两者之间差异显著。此外,在分生孢子形态方面,野生型孢子单端萌发及少部分双端萌发,ΔCgRGS7-44则是多端萌发(图5),进而统计了两者的孢子萌发率及附着胞形成率(表2),ΔCgRGS7-44孢子萌发率(8 h)约为85 %±4.3%,显著大于野生型孢子萌发率。但是敲除转化子的附着胞形成率较野生型有所延迟,18 h附着胞形成率为32.54%±3.75%,而野生型则达到68.07%±8.1%。由此可见,CgRGS7基因参与调控分生孢子的产量、芽管形态及附着胞的形成。
2.3.3 CgRGS7参与调控致病性 为了探究CgRGS7基因与胶孢炭疽菌致病力的关系,将野生型和ΔCgRGS7-44接种芒果果实,观察其致病结果。如图6所示,ΔCgRGS7-44在无伤口方式接种下几乎无病斑形成;而以伤口方式接种时,与野生型相比,ΔCgRGS7-44所形成的病斑明显减小,致病力减弱。由此说明,CgRGS7对胶胞炭疽菌的致病力有影响。

图4 不同培养基对菌株生长的影响Fig.4 Effects of differentmedia on growth of strains
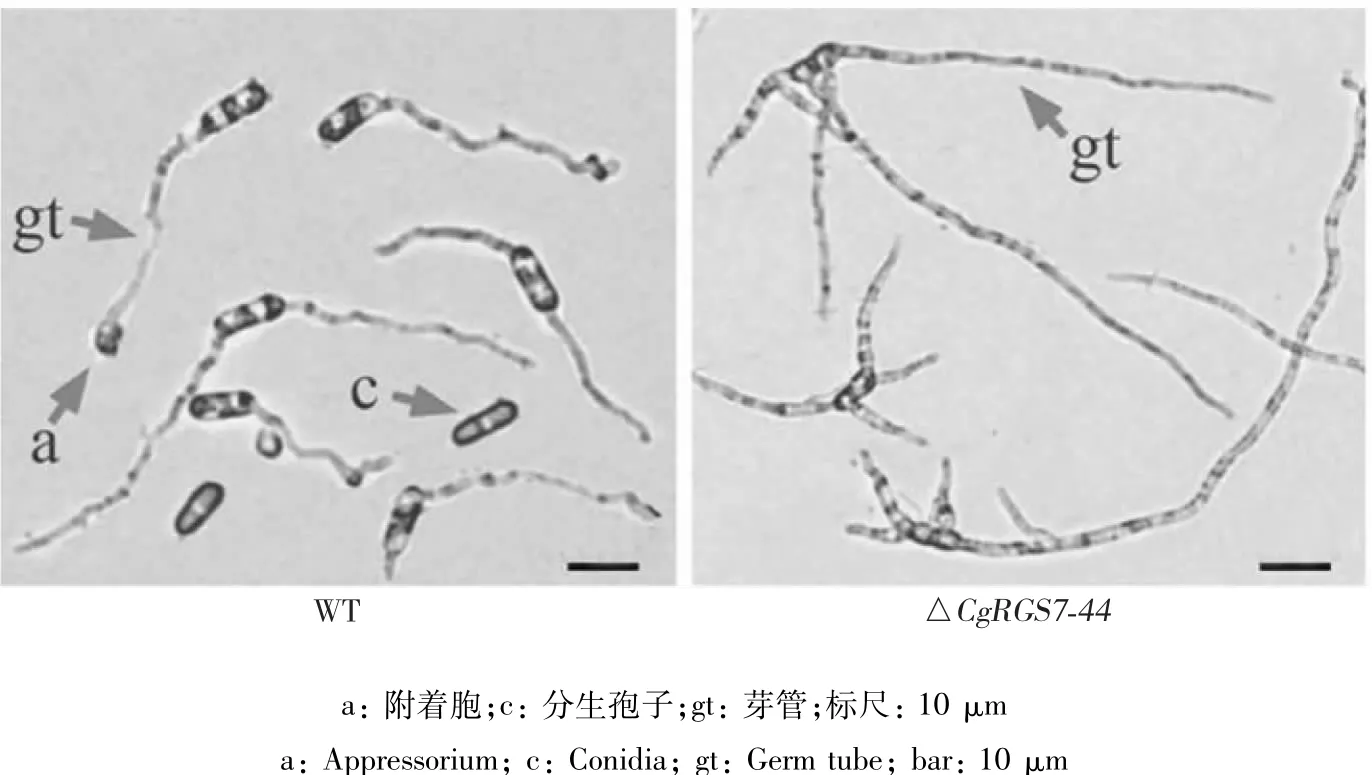
图5 野生型与CgRGS7敲除突变体分生抱子萌发形态Fig.5 Conidium germination of wild type and CgRGS7 deletion mutant

表2 产抱量、萌发率和附着胞形成率Table 2 Conidium production,germination rate and appressorium formation rate
3 讨 论
RGS蛋白是G蛋白信号转导的负调节子,相关研究表明其在众多生理生化过程中发挥着重要作用。本试验利用同源重组的方法获得了CgRGS7敲除转化子,并对其在营养生长、渗透压胁迫、氧化应激反应、分生孢子产生及萌发、及致病力等方面做了表型分析。结果表明,CgRGS7敲除转化子在营养生长及NaCl、H2O2、SDS的压力胁迫下,与野生型相比无显著变化;但在分生孢子的产量、芽管生长、附着胞形成率以及致病力方面两者存在显著差异,敲除转化子在产孢量及附着胞形成率方面均低于野生型菌株,致病力也减弱,这些结果与已报道的稻瘟病菌MoRGS7的功能有相似之处,张海峰等在M. oryzae中鉴定到8个RGS蛋白(MoRGS1~MoRGS8),结果分析显示这些基因参与调控该病菌的营养生长、细胞壁完整性、附着胞分化和侵入等生理过程[12-13],其中MoRGS7不仅参与芽管的生长,影响附着胞形成率,还参与稻瘟病菌的侵染过程,造成ΔMoRGS7致病力减弱,进一步试验显示ΔMoRGS7致病性下降是因为附着胞侵入率下降和侵染菌丝不能扩展造成的。CgRGS7与稻瘟病菌的MoRGS7相似,均在N端含有7个跨膜结构域,在C端含有一个RGS功能域,推测CgRGS7敲除转化子的分生孢子产量下降及附着胞形成率降低可能是造成其致病力减弱的主要原因,关于CgRGS7是否影响附着胞的侵入及侵染菌丝的扩展,还有待于进一步的试验验证。

图6 野生型与ΔCgRGS7-44致病力试验Fig.6 Pathogenicity tests of wild type andΔCgRGS7-44
目前,在胶孢炭疽菌信号传导途径中鉴定的与致病相关的基因还较少,已报道的包括MAPK途径中CgMEK1基因参与细胞分裂的极化及芽管的分化,其敲除突变体无附着胞形成,致病力丧失[14]; Cgl-slt2基因对营养菌丝生长和附着胞的形成有影响,其中敲除突变体的附着胞形成率明显降低[1]。cAMP-PKA途径中CgPKAC基因的敲除突变体附着胞形成缓慢及致病力减弱[15]。在以前的研究中,还发现G蛋白信号途径中CgRGS2蛋白参与了胶孢炭疽菌的营养生长,分生孢子产量及萌发,氧化应激反应及细胞壁完整性,其敲除突变体致病力减弱[16],CgRGS4蛋白则影响该菌的营养生长,参与渗透压响应及氧化应激反应,同时对黑色素产量有影响[17]。
4 结 论
本研究从胶孢炭疽菌中鉴定了一个RGS基因CgRGS7,表型分析发现其参与调控胶孢炭疽菌的分生孢子产生、附着胞形成及致病力,是该病菌一个新的致病因子。总的来说,目前关于胶孢炭疽菌致病机制研究尚处于起步阶段,本研究为该病菌分子致病机理的研究奠定了一定的基础。
[1]Yong H Y,Bakar FD A,Illias RM,etal.Cgl-SLT2 is required for appressorium formation,sporulation and pathogenicity in Colletotrichum gloeosporioides[J].Brazilian Journal of Microbiology,2013,44(4):1241-1250.
[2]毕方铖,戴宏芬,孟祥春.农杆菌介导的芒果胶孢炭疽菌遗传转化及致病性缺陷突变体的筛选[J].热带农业科学,2014,34 (8):47-51.
[3]贾 静,蒲金基,张 贺,等.芒果炭疽病菌环境pH信号调控基因PalF的克隆与分析[J].热带作物学报,2014,35(4):753-757.
[4]Cai Z Y,LiGH,Lin CH,et al.Identifying pathogenicity genes in the rubber tree anthracnose fungus Colletotrichum gloeosporioides through random insertional mutagenesis[J].Microbiological Research,2013,168:340-350.
[5]Li L,Shen G,Zhang ZG,etal.Canonical heterotrimeric G proteins regulatingmating and virulence of Cryptococcus neoformans[J].Molecular Biology of the Cell,2007,18(11):4201-4209.
[6]Siderovski D P,Willard FS.The GAPs,GEFs and GDIs of heterotrimeric G-Protein alpha subunits[J].International Journal of Biological Sciences,2005,1(2):51-66.
[7]Park A R,Cho A R,Seo JA,et al.Functional analyses of regulators of G protein signaling in Gibberella zeae[J].Fungal Genetics and Biology,2012,49(7):511-520.
[8]Yu JH.Heterotrimeric G protein signaling and RGSs in Aspergillus nidulans[J].Journal of Microbiology,2006,44(2):145-154.
[9]Wang Y,Geng Z,Jiang D,et al.Characterizations and functions of regulator of G protein signaling(RGS)in fungi[J].Applied Microbiology and Biotechnology,2013,97(18):7977-7987.
[10]Fang W G,Scully L R,Zhang L,et al.Implication of a regulator of G protein signalling(Bb RGS1)in conidiation and conidial thermotolerance of the insect pathogenic fungus Beauveria bassiana[J]. FEMSMicrobiology Letters,2008,279(2):146-156.
[11]Vries D L,Farquhar M G.RGS protein:more than just GAPs for heterotrimeric G protein[J].Trends in Cell Biology,1999,9(4): 138-144.
[12]Liu H,Suresh A,Willard F S,et al.Rgs1 regulatesmultiple Gα subunits in Magnaporthe,pathogenesis,asexual growth and thigmotropism[J].Embo Journal,2007,26(3):690-700.
[13]Zhang H,TangW,Liu K,et al.Eight RGSand RGS-like proteins orchestrate growth,differentiation,and pathogenicity of Magnaporthe oryzae[J].PLoSPathogens,2011,7(12):446-459.
[14]Kim Y K,Kawano T,Li D X,et al.A mitogen-activated protein kinase kinase required for induction of cytokinesis and appressorium formation by host signals in the conidia of Colletotrichum gloeosporioides[J].The Plant Cell,2000,12:1331-1343.
[15]Priyatno T P,Bakar F D A,Kamaruddin N,et al.Inactivation of the catalytic subunit of cAMP-dependent protein kinase A causes delayed appressorium formation and reduced pathogenicity of Colletotrichum gloeosporioides[J].The Scientific World Journal,2012,2012 (2):545784-545784.
[16]吴曼莉,李晓宇,张 楠,等.胶孢炭疽菌CgRGS2基因的克隆及生物学功能[J].微生物学报,2017(1):66-76.
[17]徐 爽,吴曼莉,柯智健,等.胶孢炭疽菌CgRGS4调控营养生长、渗透压响应、氧化应激反应和致病性[J].浙江农业学报,2017(2):277-285.
(责任编辑 陈 虹)
CgRGS7 Regulation of Conidium Production,Appressorium Formation and Pathogenicity in Colletotrichum gloeosporioides
WU Man-li,HU Jian,ZHANG Nan,KE Zhi-jian,LIU Zhi-qiang*,LIXiao-yu
(Institute of Tropical Agriculture and Forestry,Hainan University,Hainan Haikou 570228,China)
【Objective】Regulators of G-protein signaling(RGS)were a kind of negative regulatory factor of G protein,which were involved in various G protein-mediated signaling pathways.At present,therewas little research on the biological functions of RGS in Colletotrichum gloeosporioides.【Method】In the present study,the gene-knockoutmutantof CgRGS7 wasobtained by homologous recombination,and itsbiological functionswere analyzed.【Result】The gene CgRGS7 encoded a 620-amino acids protein,containing seven membrane spaning domains and a RGS function domain.Comparing to thewild type,the knockoutmutantof CgRGS7 reduced conidium production withmulti-end germination and appressorium formation rate and pathogenicity.【Conclusion】CgRGS7 is involved in regulation of conidium production,germ tubemorphogenesis,appressorium formation rate and pathogenicity of C.gloeosporioides.
Colletotrichum gloeosporioides;Regulators of G-protein signaling;Conidium;Pathogenicity
S432.44
A
1001-4829(2017)8-1802-06
10.16213/j.cnki.scjas.2017.8.018
2016-09-10
国家自然科学基金(31560045);海南省重点研发计划(ZDYF2016155)
吴曼莉(1992-),女,海南万宁人,硕士研究生,主要研究方向为植物病原真菌学,E-mail:wumanli0331@163.com,*为通讯作者,E-mail:liuzhiqiang80@126.com。
