间/对-二乙炔基苯的合成工艺研究
2017-09-11李昆明程晨
*李昆明 程晨
(浙江医药股份有限公司昌海生物分公司 浙江 312000)
间/对-二乙炔基苯的合成工艺研究
*李昆明 程晨
(浙江医药股份有限公司昌海生物分公司 浙江 312000)
以间/对二乙烯基苯为原料,经溴化加成反应得到二(α,β-二溴乙基)苯,再将分离后的二(α,β-二溴乙基)苯在甲醇钠/甲醇介质中脱去溴化氢,通过加水萃取和水蒸气蒸馏,得到纯度较高的间/对二乙炔基苯。
间/对二乙炔基苯;加成-消除反应;水蒸气蒸馏
1.引言
二乙炔基芳烃,例如二乙炔基苯(DEB),是重要的有机合成中间体。目前芳基乙炔的合成方法主要有芳基乙烯卤化-脱卤化氢法、芳烃酰化法、三甲基硅乙炔法、偶合法、膦叶立德法、二卤烯脱卤法和杂环裂解法、Vilsmeier法。但由于芳烃酰化法、三甲基硅乙炔法、偶合法所用试剂昂贵,操作复杂,目前仅限于实验室制备。而膦叶立德法、二卤烯脱卤法和杂环裂解法、Vilsmeier法产率普遍不高,后处理烦琐,不利于工业应用。芳基乙烯卤化-脱卤化氢法脱的卤化氢效率不高,且试剂价格高且操作危险。
本文以二乙烯基苯为原料,进行加成-消除反应,使用甲醇钾/氢氧化钠溶液进行脱溴化氢法制备二乙炔基苯,获得了较高的脱溴化氢效率。
2.实验部分
(1)原料及仪器。二乙烯基苯(AR,天津凯力达化工贸易有限公司);溴素(AR,国药集团);甲醇(AR,天津博迪化工股份有限公司);氢氧化钠(AR,天津博迪化工股份有限公司);四氯化碳(AR,天津博迪化工股份有限公司);去离子水(自制)
电子天平(上海精密科学仪器有限公司);磁力搅拌器(上海精密科学仪器有限公司);SHB-A循环式真空泵(上海鹏奕仪器有限公司)
(2)合成。①间/对-二(α,β-二溴乙基)苯的合成。在250ml的三口烧瓶中,加入75ml的四氯化碳,50ml(0.3587mol)混合二乙烯基苯,冷却到10-15℃,搅拌下逐滴加入溴素40ml(0.7806mol),保持体系温度在10-15℃,加完后,继续搅拌2h,静置过夜,过滤,得滤饼,干燥后,得产品间/对-二(α,β-二溴乙基)苯(54.3278g)。②间/对混合二乙炔基苯的合成。向100ml的三口烧瓶中加入间/对-二(α,β-二溴乙基)苯17.6112g(0.0395mol)溶入40ml甲醇,搅拌后,再加入KOH固体30g(0.5357mol),加热至回流,温度92-97℃,反应2.5h,反应结束,冷至室温,加入蒸馏水,使析出的KBr溶解在体系中,静置分层,萃取,上层油状液体即为间/对混合二乙炔基苯粗产品。③提纯方法。将上层油状液体加入到烧瓶中,采用水蒸气蒸馏的方法,将间/对混合二乙炔基苯蒸出,蒸出的混合液加入漏斗中,静置分层,上层黄色液体即为纯化后的间/对混合二乙炔基苯。低温下放置3~5天,有晶体析出。其中间二乙炔基苯为淡黄色油状液体,对二乙炔基苯为白色晶体。
3.结果与讨论
(1)二乙炔基苯的合成。二乙烯基苯加成-消除反应是制备二乙炔基苯的经典方法:第一步,利用二乙烯基苯与溴素的加成反应生成二(α,β-二溴乙基)苯,由于溴易与苯环氢发生取代反应,因而反应在低温下进行,在本实验中温度控制在10-15℃;第二步,二(α,β-二溴乙基)苯脱去四分子溴化氢生成二乙炔基苯,当消去第一分子溴化氢后生成了较稳定的-CH=CHBr共轭结构,要继续消去溴化氢生成-C≡C-的反应需要较高的能量来破坏-CH=CHBr共轭结构,因此必须强化消去条件。在强碱、高温等条件下获得的二乙炔基苯产率较高。反应方程式如下:

①碱对间二乙炔基苯产率的影响。本实验中,碱液的溶度对所得产物的产率影响比较大。当碱液浓度较低时,会稀释反应体系,使得反应温度只能达到醇的沸点,而这使得反应中的消除反应不完全。而使用过量的碱可以促进反应,且使用过量适当的碱可使温度保持稳定,加快反应。②反应温度对间二乙炔基苯产率的影响。在碱性介质中脱溴化氢的反应分两步。温度对第一步溴加成反应产率影响较大,温度高溴化反应一般在发生苯环上,使得间/对-二乙炔基苯的生成率降低。第一步是放热反应,反应很容易,温度控制在10-15℃,当反应不再放热,反应结束;第二步是吸热反应,二(α,β-二溴乙基)苯脱去四分子的溴化氢可得到二乙炔基苯,但是温度高于100℃时容易发生聚合,温度低于90℃,会导致脱HBr不完全,对二乙炔基苯的产率和精制都造成影响,所以反应温度不能过高,90-100℃是比较适宜的反应温度,产率也较高。③反应时间对间二乙炔基苯产率的影响。通过薄层监测反应发现,当反应进行2小时,仍有大量原料剩余,此时,已参与反应的原料生成了四种产物,仍有大量的溴化物未完全把溴脱去。因此,若使反应产率大大增加,需延长反应时间,将溴化物完全脱溴,生成所需要的产物。
(2)二乙炔基苯的红外分析。对合成的间/对-二乙烯基苯利用KBr压片法进行红外表征,得出如下结果:
①炔基的特征峰,3278cm-1处的炔基C-H伸缩振动峰,2100cm-1处的炔键伸缩振动峰;②苯环的间位取代特征:1480cm-1为苯核的C=C伸缩振动峰,695cm-1、795cm-1为间位取代苯的C-H面外弯曲振动峰,在2000-1667cm-1间出现间位取代苯的倍频峰形;③苯环的对位取代特征:1480cm-1为苯核的C=C伸缩振动峰,830cm-1为对位取代苯的C-H面外弯曲振动峰,在2000~1667cm-1间出现对位取代苯的倍频峰形。
(3)反应副产物分析。第一步,反应温度控制10-15℃。反应是放热反应,在滴加液溴的过程中,若溴滴加稍快,会导致体系温度升高,当温度升高至50℃时,苯环上的氢也会被溴取代,导致最终产物间/对-二乙炔基苯的产率降低。第二步,由于反应时间不够长,导致脱溴化氢的反应不完全。间/对-二乙炔基苯在100℃以上会发生聚合。所以温度稍高,会发生聚合反应,使得产物产率降低。可能的副反应如下:
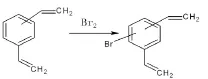
①苯环上的氢被溴取代:
②未完全脱溴化氢:由于-CH=CHBr较稳定,因此可能的副产物如下:

③温度过高引起二乙炔基苯的聚合反应:

4.结论
(1)二乙炔基苯是重要的有机合成中间体,因此尽可能选择试剂易得、产率高、分离效果好的合成方法和试剂。(2)本实验在合成间/对二乙炔基苯的过程中,注意温度的影响。实验必须严格控制反应温度,温度严重影响产物的产率,造成副产物的生成。(3)结果表明,本方法简单易行,产率较一般方法高,间/对二乙炔基苯纯度高。
(责任编辑 宋小蒙)
The synthesis process of a/p-diethyl benzene
Li Kunming Cheng Chen
(zhejiang pharmaceutical co., LTD. Changhai biological branch ,zhejiang,312000)
to room/divinyl benzene as raw material, through bromination addition reaction under two (alpha, beta 2 bromomethyl) benzene, then after separation of 2 (alpha, beta 2 bromomethyl) benzene in sodium methoxide/methanol medium remove hydrogen bromide and through water extraction and vapor distillation, get high purity/between the two ethinyl benzene.
inter/diethylbenzene;Addition-elimination reaction; Steam distillation
T
A
李昆明(1983~),男,浙江医药股份有限公司昌海生物分公司;研究方向:医药化工中间体的研发和生产管理。
