SrMoO4∶Sm3+,Na+红色荧光粉的形貌调控和发光性能
2017-09-06吴锦绣李梅崔松松柳召刚胡艳宏王觅堂
吴锦绣 李梅 崔松松 柳召刚,3 胡艳宏,3 王觅堂,3
(1北京科技大学冶金与生态工程学院,北京100083)(2内蒙古科技大学材料与冶金学院,包头014010)(3内蒙古自治区高校稀土现代冶金新技术与应用重点实验室,包头014010)
SrMoO4∶Sm3+,Na+红色荧光粉的形貌调控和发光性能
吴锦绣*,1,2,3李梅*,1,2,3崔松松2柳召刚2,3胡艳宏2,3王觅堂2,3
(1北京科技大学冶金与生态工程学院,北京100083)
(2内蒙古科技大学材料与冶金学院,包头014010)
(3内蒙古自治区高校稀土现代冶金新技术与应用重点实验室,包头014010)
以Sm3+为激活剂,Na+为电荷补偿剂,柠檬酸为配位剂,乙二醇作为辅助配位剂,采用溶胶-凝胶法合成前驱体,然后在800℃下焙烧,成功制备了一系列SrMoO4∶Sm3+,Na+红色荧光粉。用X射线衍射仪、扫描电镜、荧光光谱和傅里叶变换红外光谱等手段对样品的物相、形貌、组成、发光性能和量子效率等进行测试和表征。分析结果表明:制备的SrMoO4∶Sm3+,Na+荧光粉均为四方晶系结构,掺杂离子的加入对基质晶体结构影响不大。在403 nm近紫外光激发下,产物有4个发射峰,分别位于563、600、647和707 nm处,归属于5G5/2→6HJ(J=5/2,7/2,9/2,11/2)的电子跃迁,其中位于647 nm处的主发射峰的相对发光强度最大。当Sm3+的掺杂物质的量分数为1%~3%时,发光强度最好,当浓度超过1%~3%时,会发生荧光猝灭。对实验数据进行分析,确定荧光猝灭机理是由于钐离子间交换作用引起的,并计算了能量传递的临界距离为1.77~2.56 nm。此外,还详细研究了乙二醇对SrMoO4∶Sm3+,Na+荧光粉形貌的影响,研究结果表明:乙二醇加入量为5 mL时,产物形貌均匀,呈球形或椭球形;且分散性较好;荧光强度最大。
钼酸锶;Sm3+;溶胶-凝胶法;荧光粉
目前,白色发光二极管(LED)备受关注,因为其能耗低、结构紧凑、光输出量高、寿命长、环保等优点远超过传统的荧光灯和白炽灯[1-5];但是白光LED所用红色荧光粉的商业化仍局限于Eu3+掺杂Y2O2S和Eu2+激活的碱土二硫化物。其硫化物基红色荧光粉有发光效率低、寿命短、化学不稳定性等弊端。因此,寻找一种在近紫外光波段具有高吸收和稳定性好的红色荧光粉是一个具有吸引力和挑战性的研究课题[6-8]。
钼酸盐和钨酸盐由于特有的物理和化学性质作为无机发光材料的基质,在荧光灯、固体激光器、闪烁器、白色发光二极管(LED)等领域有着广泛应用[9-11]。在众多稀土离子中,研究比较多的是三价Eu3+[12-14],而具有发红光特性的Sm3+研究的较少。Lin等[15]采用高温固相法制备出了NaSrMoO4∶Sm3+荧光粉。研究发现钐离子的最佳掺杂浓度为2%,超过2%会发生荧光猝灭。Du等[16]用静电纺丝法制备SrMoO4∶Sm3+纳米纤维。目前,绝大多数的发光材料都用传统高温固相法制备,一般需要较高的温度和磨削[17]。磨削过程中的荧光粉表面易损伤,导致发光强度的降低。此外,聚集和不规则形状也在所难免,这会抑制激发能量的吸收从而降低发光强度。
高质量的荧光粉应具备高纯度、组成可控、成分均匀、具有所需物相、颗粒尺寸分布范围窄、无硬团聚体等特性。溶胶凝胶法与传统固相法相比有易于计量控制,均匀性好,煅烧温度低等优点,更重要的是所制备的样品具有尺寸小和粒径分布窄和良好的发光特性,可克服高温固相法的缺陷。目前还没有用溶胶-凝胶法合成SrMoO4∶Sm3+,Na+荧光粉的研究报告。本文通过溶胶-凝胶法制备了不同Sm3+掺杂浓度的SrMoO4∶Sm3+,Na+荧光粉,在溶胶过程中加入乙二醇,改善凝胶稳定性,可以制得均匀透明的凝胶,并在一定程度上减少了产物的硬团聚,系统的研究乙二醇的加入量对该类荧光粉的形貌和光致发光性能的影响。
1 实验部分
1.1 主要试剂和原料
Sr(NO3)2、NaNO3、柠檬酸、乙二醇和(NH4)6Mo7O24·4H2O(AR,天津市北联精细化学品开发有限公司),Sm2O3(纯度>99.99%,包头稀土研究院),无水乙醇、浓硝酸和浓盐酸(AR,国药集团化学试剂有限公司),实验用水全为纯净水(自制)。
1.2 样品的制备
采用溶胶-凝胶法制备Sr1-2xMoO4:x(Sm3+,Na+)(x= 0,0.005,0.01,0.15,0.02,0.03,0.05,0.08)荧光粉前驱体。首先按化学计量比称取一定量的Sr(NO3)2、NaNO3和Sm(NO3)3溶液混合均匀倒入烧杯中,然后加入一定量的柠檬酸作为配位剂(n柠檬酸/n阳离子=3),随后加入一定量的乙二醇做为辅助配位剂,最后称取钼酸铵倒入烧杯溶解,将上述溶液充分搅拌均匀。用氨水调节pH值为1~2,再放入80℃的恒温水浴锅搅拌4 h并保温数小时直到形成凝胶为止;然后放入120℃的恒温干燥箱中干燥48 h形成黑褐色干胶,取出后在玛瑙研钵中充分研磨,把粉末放入刚玉坩埚中,在800℃的箱式高温烧结炉中焙烧4 h,升温速率为3℃·min,随炉冷却到室温,得到粉末样品。1.3样品的表征
样品的晶体结构采用德国ADVANCE公司的Brukor D8 X-射线粉末衍射仪测定,Cu Kα,λ= 0.154 06 nm,电压为40 kV,电流为40 mA,扫描范围10°~70°;用H-800透射显微镜观测样品的晶体尺寸和形貌并确定产物的粒径大小和分布(20 kV),并测定能谱;用日立的F-4600荧光分光光度计测定样品的激发和发射光谱;傅里叶变换红外光谱仪是用美国BROKER的ALPHAA仪测定;产物的量子效率和色坐标用英国的HORIBA Fluoromax-4设备测试;所有样品都在室温下测试。
2 结果与讨论
2.1 乙二醇对Sr0.98MoO4∶0.01(Sm3+,Na+)荧光粉的影响
在溶胶-凝胶体系中,形成胶体的过程中加入乙二醇,不仅改善凝胶稳定性,从而制得均匀透明的凝胶;并在一定程度上减少了产物的硬团聚,得到颗粒尺寸分布范围窄、无硬团聚体的产物。本文经过大量的实验研究发现,用溶胶-凝胶法制备的SrMoO4∶Sm3+,Na+前驱体在溶胶形成凝胶的过程中,作为辅助配位剂乙二醇的加入量不同,产物的形貌和荧光性能有差异,因此系统的研究乙二醇的加入量对产物性能的影响。
2.1.1 物相分析
如图1所示给出了加入不同量的乙二醇的Sr0.98MoO4∶0.01(Sm3+,Na+)荧光粉的X射线衍射图,测量结果表明产物的衍射图均一致。为了对比方便,图1同时给出了JCPDS No.08-0482的XRD图。从图1中可以看出,所得样品的衍射峰位置都与SrMoO4标准卡片(No.08-0482)的主衍射峰位置相对应,没有其它杂峰出现,说明所制备的荧光粉为纯相的四方晶系的结构。从图1中可以看出乙二醇的加入量没有改变产物的晶体结构,这是由于在制备过程中乙二醇只参与前驱体的溶胶-凝胶的形成过程,最终形成稳定的、均匀透明的凝胶;然后在焙烧的过程中将全部以气体的形式放出,从而减少了最终产物的硬团聚。所以乙二醇的加入量不会改变产物的晶体结构。
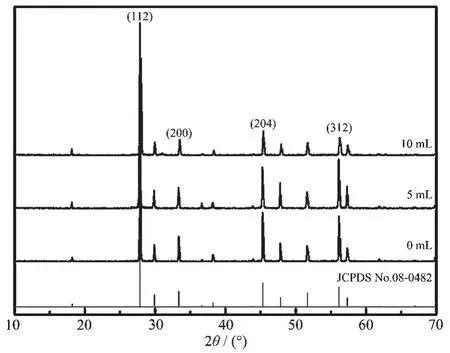
图1 不同量乙二醇所制备的产物Sr0.98MoO4∶0.01(Sm3+, Na+)的XRD图Fig.1XRD patterns of Sr0.98MoO4∶0.01(Sm3+,Na+)with different amounts of ethylene glycol
2.1.2 SEM图分析
如图2所示,可以明显的看到当不加乙二醇时,产物为不规则颗粒,团聚现象特别严重,颗粒间界面模糊,可能为硬团聚;当加入乙二醇后,产物为明显的圆形或椭球形,也出现团聚现象,但颗粒界面清晰,可见为软团聚。这与文献[18]相吻合。当乙二醇的加入量为1 mL和3 mL时,产物都为圆形或椭球形,直径分散范围也为1~8 μm,团聚现象都比较严重,但乙二醇的加入量为3 mL时产物的团聚现象有所减轻,颗粒界面更加清晰;当乙二醇的加入量为5 mL时,产物为类球形颗粒,直径约为3~8 μm,分散性较好;当乙二醇的加入量为8 mL时,产物也为类球形颗粒,直径约为1~8 μm,分散性也较好;当乙二醇加入量增加到10 mL时,产物的大小变化不大,直径约为1~8 μm,但容易连接成一片,分散性不好,界面比较清晰。可见乙二醇的不同加入量对产物的微观形貌有很大影响。在本实验中乙二醇的最佳加入量为5 mL时,类球形产物比较均匀;分散性也较好。

图2 不同量乙二醇所制备的产物Sr0.98MoO4∶0.01(Sm3+, Na+)荧光粉的SEM图Fig.2SEM patterns of Sr0.98MoO4∶0.01(Sm3+,Na+)with different amounts of ethylene glycol
2.1.3 红外光谱(IR)和EDS图谱分析
如图3所示,从上往下分别表示乙二醇加入量分别为10、5和0 mL的产物的红外光谱图。从图中可知在820 cm-1处有宽而强的吸收峰,该处的吸收峰是由于孤立的钼氧四面体[MoO42-]伸缩振动,及γ1、γ3振动的结果[19]。在1 700 cm-1左右处有一微弱小的吸收峰和3 500 cm-1弱的宽带吸收峰都是属于水中O-H弯曲和伸缩振动吸收峰[20],也可能是在测定时吸收空气中的水蒸气而形成的。除此之外,没有其它峰出现,说明最终产物不含有乙二醇,这与XRD分析的结果相吻合。为了进一步确定产物的元素组成,对样品进行能谱分析,结果如图4的EDS所示,所制备的荧光粉由元素O、Mo、Sr、Sm和Na组成。
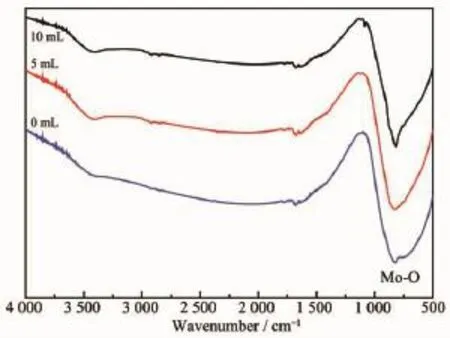
图3 不同量的乙二醇所制备的Sr0.98MoO4∶0.01(Sm3+, Na+)的傅立叶变换红外光谱图Fig.3FT-IR patterns of Sr0.98MoO4∶0.01(Sm3+,Na+)with different amounts of ethylene glycol
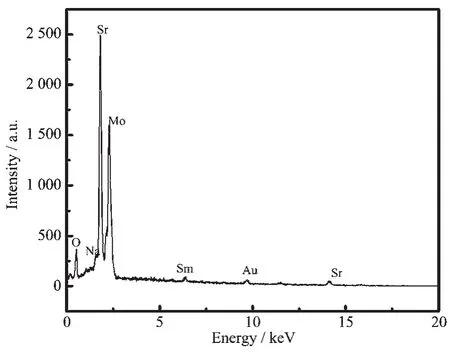
图4 加入5 mL乙二醇制备的Sr0.98MoO4∶0.01(Sm3+, Na+)的能谱图Fig.4EDS patterns of Sr0.98MoO4∶0.01(Sm3+,Na+)with 5 mL ethylene glycol
2.1.4 发光性能
如图5所示为Sr0.98MoO4∶0.01(Sm3+,Na+)荧光粉的激发和发射光谱图,监测波长为λex=403 nm和λem=647 nm,从图中可以看出,虽然乙二醇的含量不同,但是Sr0.98MoO4∶0.01(Sm3+,Na+)荧光粉的激发和发射光谱的峰形,峰位基本相同,主发射峰位于647 nm处,属于5G5/2→6H9/2电子跃迁;主激发峰位于403 nm处,属于6H5/2→4F7/2电子跃迁。表面活性剂的量对发光强度的影响规律为5 mL>10 mL>0 mL。可见乙二醇的加入量为5 mL时,产物的形貌较均匀,且分散性较好,荧光强度最大。
2.2 SrMoO4∶Sm3+,Na+荧光粉Sm3+最佳掺杂浓度的研究
2.2.1 物相分析
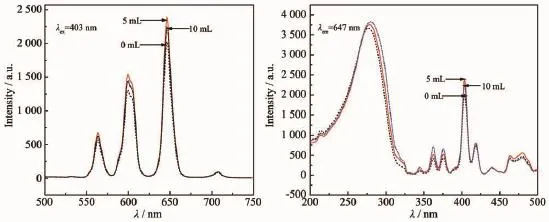
图5 不同乙二醇加入量产物Sr0.98MoO4∶0.01(Sm3+,Na+)荧光粉的发射和激发光谱图Fig.5Emission and Excitation spectrum of Sr0.98MoO4∶0.01(Sm3+,Na+)with different amounts of ethylene glycol
如图6所示给出了不同Sm3+含量的SrMoO4∶Sm3+,Na+荧光粉的XRD图,从上到下,Sm3+的百分含量分别为5%、1%和0%。从图中可以看出,所得样品的衍射图的主衍射峰位置与SrMoO4标准卡片(No. 08-0482)的主衍射峰位置相对应,没有其它杂峰出现,说明所制备的SrMoO4∶Sm3+,Na+和SrMoO4同为四方晶系的结构,没有杂相。分析得知晶体的晶格参数为:a=b=0.539 4 nm,c=1.202 nm,Z=4,空间群为I41/a。四方晶系的SrMoO4中的Sr2+是八配位,所以半径为0.126 nm。从图6中可以看出Na+和Sm3+的掺入没有改变产物的主晶体结构,这是由于Na+和Sm3+的物质的量比较少,且八配位的Sm3+离子半径(0.108 nm)与Sr2+的离子半径相近,所以Sm3+容易占据Sr2+的格位进入SrMoO4基质中,故对SrMoO4的晶体结构几乎没有影响。在产物晶格中如果1个Sm3+取代1个Sr2+将产生电荷不平衡,所以在反应体系中加入与Sm3+等物质的量的Na+作为电荷补偿剂,由1个Sm3+和1个Na+取代2个Sr2+使产物晶格电荷平衡。
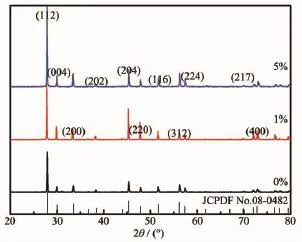
图6 不同Sm3+含量的SrMoO4∶Sm3+,Na+的XRD图Fig.6XRD patterns of SrMoO4∶Sm3+,Na+doped with different amounts of Sm3+
2.2.2 形貌和成分分析
如图7所示为前躯体加入乙二醇的量为5 mL时不同Sm3+含量的SrMoO4∶Sm3+,Na+荧光粉的SEM图谱,可以看出样品都为块状的不规则颗粒,分散性都较好。当没有稀土钐离子掺杂时,产物为不规则多边形的大颗粒;当Sm3+的物质的量分数为1%,颗粒接近于球形或类球形,直径尺寸约为3~8 μm;当浓度达到3%时,产物的颗粒接近于球形或类球形并分散均匀,类球型的直径尺寸约为1~3 μm;当浓度达到8%时,产物为不规则多面体和球形或类球形相结合,颗粒分散不均匀。可见随着Sm3+和Na+离子的掺入,产物的类球型颗粒尺寸明显变小且向畸形发展。为了进一步明确产物的元素组成,进行EDS分析。如图8为Sm3+含量占8%的EDS能谱,从图谱中可以看到产物的组成元素为O、Na、Sr、Sm和Mo。EDS能谱中有Au峰,是由于制样时喷金的缘故。

图7 不同Sm3+含量的SrMoO4∶Sm3+,Na+的SEM图Fig.7SEM patterns of SrMoO4∶Sm3+,Na+doped with different amounts of Sm3+
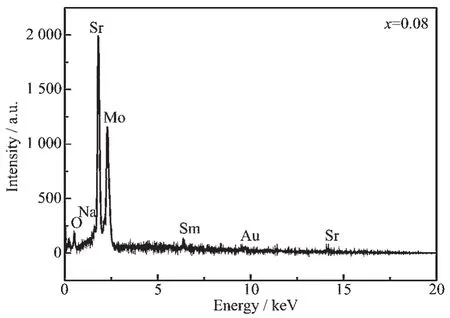
图8 Sm3+含量8%的SrMoO4∶Sm3+,Na+的EDS图谱Fig.8EDS spectrum of SrMoO4∶Sm3+,Na+doped with 8% of Sm3+
2.2.3 样品的荧光性能
图9为不同Sm3+掺杂物质的量分数(分别为0.5%、1%、1.5%、2%、3%、5%、8%)钼酸盐的发射和激发光谱图。根据图9可以看出,稀土Sm3+掺杂的钼酸盐发光材料在403 nm波长下激发的发射光谱图有4个主要的荧光发射峰分别位于563、600、646和707 nm处,是Sm3+离子4f轨道电子的特征发射峰,归属于5G5/2→6HJ(J=5/2,7/2,9/2,11/2)的电子跃迁[21-24],对应的发射强度分别为632、1451、2261、94,其中位于647 nm处的发射峰最强。所以激发光谱的监测波长为λem=647 nm。由图9可见,不同Sm3+掺杂SrMoO4∶Sm3+,Na+的荧光粉在200~300 nm存在一个很宽的电荷跃迁吸收带,最大值在280 nm,归属于O2-→Mo6+的电荷迁移。在300~500 nm处有一组较强的锐线吸收带,属于Sm3+的4f内层电子间的f-f跃迁吸收。以Sm3+含量1%为例,在362 nm(6H5/2→4D3/2)、376 nm(6H5/2→6P7/2)、403 nm(6H5/2→4F7/2)、418 nm (6H5/2→6P5/2)、440 nm(6H5/2→4I13/2)、464 nm(6H5/2→4I11/2)、480 nm(6H5/2→4D3/2)处,分别对应的激发强度为198、716、658、2 263、771、182、400、438。其中最强激发峰位于403 nm处。对于基质来说激发峰强度最大在280 nm,对应的掺钐浓度为3%的激发峰最强,说明该浓度O2-→Mo6+的电荷迁移吸收的能量较多;对于激活剂Sm3+来说激发强度最大在403 nm处对应的掺钐浓度为1%的激发峰最强,说明浓度为1%的Sm3+的4f内层电子间的f-f跃迁吸收的能量较大。
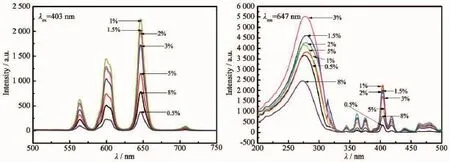
图9 不同Sm3+掺杂浓度SrMoO4∶Sm3+,Na+的发射和激发光谱图Fig.9Emission spectrum and Excitation spectrum of SrMoO4∶Sm3+,Na+doped with different amounts of Sm3+
如图10所示为不同Sm3+含量的SrMoO4∶Sm3+,Na+在监测波长为280 nm的发射光谱图。从图10中可以看出在400~550 nm之间有一个很宽的发射峰,即O2-→Mo6+的电荷迁移,且发射峰值都不高,这说明在MoO42-与Sm3+之间存在很强的能量传递作用。在550~750 nm之间是Sm3+的4f-4f跃迁特征发射峰,与图9的发射峰位完全一样,但荧光强度远远大于图9的荧光发射强度,其掺钐浓度为3%的产物发射峰最强。可见该产物的最佳激发波长为紫外区280 nm和近紫外区403 nm。当激发波长为280 nm时,稀土钐含量为3%的产物的发射光谱最强,这是由于MoO42-将吸收的能量传递给Sm3+;当激发波长为403 nm时,稀土钐含量为1%的产物的发射光谱最强,这是由于Sm3+的4f内层电子间的f-f跃迁吸收和跃迁而产生的。可见本研究所制备的产物中Sm3+最佳含量为1%~3%。
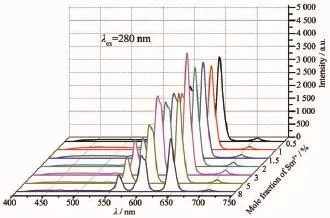
图10 不同Sm3+含量的SrMoO4∶Sm3+,Na+的发射光谱图(λex=280 nm)Fig.10Emission spectrum of SrMoO4∶Sm3+,Na+doped with different amounts of Sm3+
2.2.4 浓度猝灭机理和能量传递的临界距离的探讨
因为稀土离子有丰富的能级,尤其是在晶体中,由于晶体场的作用能级发生了劈裂,能级匹配的机会也随之增多,就会出现稀土离子间的能量传递和浓度猝灭等现象。根据Dexter理论[19,22],发光强度I与激活剂浓度x之间遵循如下关系:
I/x∝(βxs/3)-1或lg(I/x)=C-(s/3)lgx
β是常数,s为电多级相互作用的指数。以lgx为横坐标,lg(I/x)为纵坐标做图,得到一条直线,斜率为-s/3。当s=6时,分别代表电偶极-电偶极;s=8为电偶极-电四极;s=10为电四极-电四极相互作用。本研究以Sm3+的特征激发波长403 nm波长下激发的发射光谱来研究钐离子的浓度猝灭机理。
图11为Sm3+掺杂浓度大于最佳浓度(x=1.0%)时lg(I/x)与lgx的关系图,I为发射峰(563,600和646 nm)强度。利用Origin7.5软件对图9中的发射光谱图的实验点进行线性拟合,几乎得出3条平行线,3个发射峰的lg(I/x)与lgx基本都呈线性关系(相关系数分别为-0.986 16,-0.996 79,-0.989 97),斜率分别为-1.355 14、-1.327 1、-1.280 37,基本都接近1,由此斜率可求出s值为3,因此在SrMoO4基质中Sm3+中心的浓度猝灭主要是钐离子间交换作用引起的。
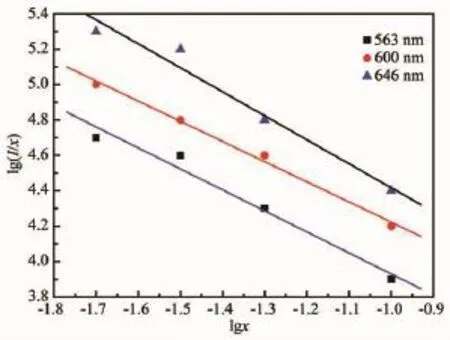
图11 产物的SrMoO4∶Sm3+,Na+的lg(I/x)与lgx的关系Fig.11Relationship between lg(I/x)and lgx of SrMoO4∶Sm3+,Na+
能量传递是有距离的,这个临界距离是指发光离子间发生浓度猝灭时的距离。浓度猝灭发生时发光中心之间的平均距离。稀土离子能量传递的临界距离可以表示为[19,22]。
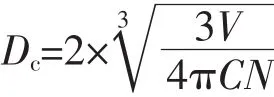
上式中V代表一个晶胞的体积,N是一个晶胞中阳离子个数,C代表临界猝灭浓度。对于四方相SrMoO4∶Sm3+,Na+晶体,N=4,V=0.349 8 nm3,Sm3+的猝灭浓度C=0.01~0.03 mol·L-1。代入公式中可以得出Dc=1.77~2.56 nm,可见能量传递的临界距离为1.77~2.56 nm。
2.2.5 量子效率和色坐标的研究
发光材料辐射出的量子数与吸收的激发量子数之比称为量子效率。一种好的荧光粉应具备充分吸收激发态能量且尽可能高效转化为发射光的特点。换而言之,荧光粉的量子效率应最大化。本文最佳产物的量子效率和色坐标见表1。由表1可知,最佳产物的量子效率随着Sm3+含量的增大而增大,即Sr1-0.06MoO4∶0.03(Sm3+,Na+)的量子效率最大,达到33.10%;而颜色却随着Sm3+含量的增加由红色向橙红色转变。
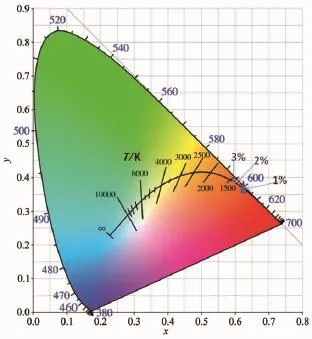
图12 最佳产物SrMoO4∶Sm3+,Na+的CIE图Fig.12CIE diagrams of the best samples SrMoO4∶Sm3+,Na+
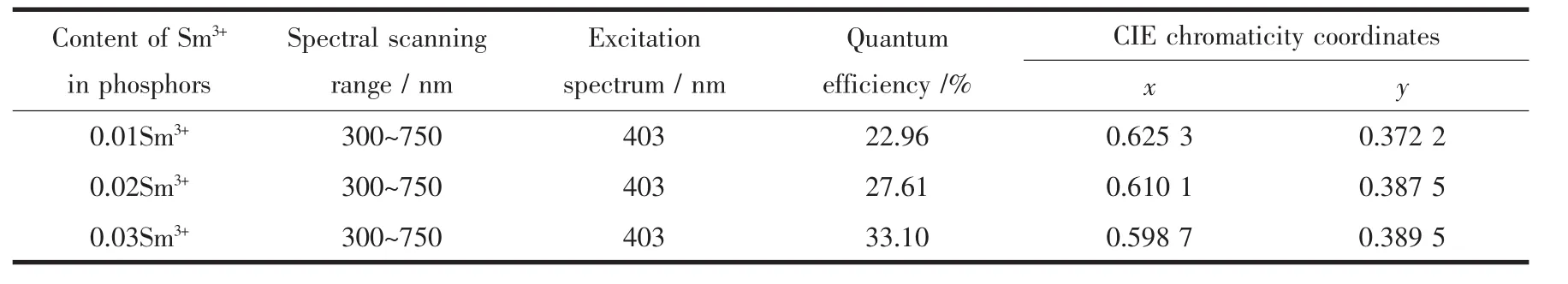
表1 最佳产物SrMoO4∶Sm3+,Na+的量子效率和色坐标Table 1Quantum efficiency and CIE chromaticity coordinates of the best product SrMoO4∶Sm3+,Na+
3 结论
本文通过溶胶凝胶法合成了前驱体,然后在800℃下焙烧成功制备四方晶系结构的SrMoO4∶ Sm3+,Na+系列荧光粉。在280和403 nm的紫外和近紫外光激发下,样品的发射光谱都有4个峰组成,其中位于647 nm处的主发射峰的相对发光强度最大。Sm3+的浓度猝灭机理是钐离子间交换作用引起的,能量传递的临界距离1.77~2.56 nm。本研究可知Sm3+的最佳含量为1%~3%;加入乙二醇得到无硬团聚的产物,当乙二醇的加入量为5 mL时制备的荧光粉的形貌较均匀,且分散性较好,发光强度最大,量子效率达到33.1%。由激发和发射光谱可以看出,该产物可以作为荧光灯、紫外芯片和蓝光芯片LED用荧光粉的备用材料。
[1]Mu J S,Zhang L,Zhao M,et al.ACS Appl.Mater.Interfaces, 2014,6:7090-7098
[2]CHEN Ai-Min(陈爱民),WANG Jing(汪晶),BO Ying-Ying (博盈盈),et al.Chinese J.Inorg.Chem.(无机化学学报), 2015,31(8):1548-1554
[3]Zhang J J,Li R Q,Liu L,et al.Ultrason.Sonochem.,2014, 21(5):1736-1744
[4]GENG Xiu-Juan(耿秀娟),CHEN Yong-Jie(陈永杰),XIAO Lin-Jiu(肖林久),et al.Chinese J.Ceram.Soc.(硅酸盐学报),2015,43(7):957-962
[5]WU Jin-Xiu(吴锦绣),LI Mei(李梅),LIU Zhao-Gang(柳召刚),et al.Chinese J.Inorg.Chem.(无机化学学报),2016,32 (1):34-42
[6]Wang Y Z,Lin C X,Zheng H,et al.J.Alloys Compd.,2013, 559:123-128
[7]LIU Yong(刘永),CHENG Ping(程萍),YANG Zhi-Yu(杨至雨),et al.Chinese J.Lumin.(发光学报),2015,36(4):424-428
[8]Shivakumara C,Rohit S.Opt.Mater.,2015,42:178-186
[9]GENG Xiu-Juan(耿秀娟),TIAN Yan-Wen(田彦文),CHEN Yong-Jie(陈永杰),et al.J.Mater.Rev.A(材料导报:综述篇),2010,24(7):54-57
[10]Lei F,Yan B.J.Solid State Chem.,2008,181:855-862
[11]Ju Z H,Wei R P,Gao X P,et al.Opt.Mater.,2011,33(6): 909-913
[12]MENG Qin-Yu(孟庆裕),ZHANG Qi(张庆),LI Ming(李明), et al.Acta Phys.Sin.(物理学报),2012,61(10):107804 (8pages)
[13]GAO Yang(高杨),LÜ Qiang(吕强),WANG Yang(汪洋), et al.Acta Phys.Sin.(物理学报),2012,61(7):077802 (9pages)
[14]Zhou Y,Yan B.CrystEngComm,2013,15:5694-5702
[15]Lin X,Qiao X S,Fan X P.Solid State Sci.,2011,13:579-583
[16]Du P F,Song L X,Xiong J,et al.J.Alloys Compd.,2012, 540:179-183
[17]Li X,Guan L,Sun M S,et al.J.Lumin,2011,131:1022-1025
[18]YIN Bang-Yue(尹邦跃),WANG Ling-Sen(王零森),FAN Yi (樊毅),et al.Chinese J.Ceram.Soc.(硅酸盐学报),1999,27 (3):337-341
[19]Titipun T,Sukjit K,Budsabong K,et al.J.Alloys Compd., 2010,506(1):475-481
[20]ZHONG Cheng(忠诚),WU Yun(吴云),LI Tao(李涛),et al. Chinese J.Lumin.(发光学报),2013,35(6):666-671
[21]REN Yan-Dong(任艳东),DONG Yun-Feng(董云峰),LIU Yong-Hao(刘永浩).Chinese J.Daqing Nor.Univ.(大庆师范学院学报),2013,33(3):51-53
[22]WU Jin-Xiu(吴锦绣),LI Mei(李梅),LIU Zhao-Gang(柳召刚),et al.Chinese J.Inorg.Chem.(无机化学学报),2015,31 (3):452-458
[23]Maheshwary B P,Singh R A.New J.Chem.,2015,39:4494-4507
[24]Yang Z P,Dong H Y,Liu P F,et al.J.Rare Earths,2014, 32(5):404-408
Controllable Morphology and Luminescence Properties of SrMoO4∶Sm3+,Na+Red Emitting Phosphors
WU Jin-Xiu*,1,2,3LI Mei*,1,2,3CUI Shong-Shong2LIU Zhao-Gang2,3
HU Yan-Hong2,3WANG Mi-Tang2,3
(1Metallurgical and Ecological Engineering School,University of Science and Technology Beijing,Beijing 100083,China)
(2College of Materials and Metallurgy,Inner Mongolia University of Science and Technology,Baotou,Inner Mongolia 014010,China)
(3Key Laboratory of Inner Mongolia Autonomous University on New Technologies of
Modern Metallurgy and Application of Rare Earth,Baotou,Inner Mongolia 014010,China)
With Sm3+as activator,Na+as doping charge compensatory,citric acid as complexing agent,ethylene glycol as auxiliary complexing agent by sol-gel method red phosphors precursor was synthesized,then a series of SrMoO4∶Sm3+,Na+red phosphor samples were sintered at 800℃.The crystalline phase,morphology and luminescence properties and quantum efficiency of the samples were characterized by X-ray diffraction,scanning electron microscopy,fluorescence spectrophotometry and fourier transform infrared spectroscopy,respectively. The results show that the synthesized NaSrMoO4∶Sm3+crystallines are a tetragonal structure.The doped ions have little impact on the matrix crystal structure.The emission spectra of the samples are composed of four peaks, 563,600,647 and 707 nm belonging to the5G5/2→6HJ(J=5/2,7/2,9/2,11/2)under the near UV excitation of 403nm,the relative luminous intensity at 647 nm main emission peak is maximum.When the doping molar fraction of Sm3+is 1%~3%,the emission intensity is the maximum,luminescence concentration quenching could be observed when the doping molar fraction of Sm3+ions was more than 1%~3%.The energy transfer type between Sm3+ions was determined to be the exchange interaction and the critical energy transfer distance(Dc)was calculated to be 1.77~2.56 nm.In addition,Influences of ethylene glycol on the performance of SrMoO4∶Sm3+,Na+phosphors were investigated in detail.The research result shows that when ethylene glycol addition amount was 5 mL,the sample grains show spherical or elliptical and the structure is uniform and loose and the fluorescence intensity is optimal.
strontium molybdate;Sm3+;sol-gel method;phosphor
O482.31
A
1001-4861(2017)02-0219-08
10.11862/CJIC.2017.036
2016-07-16。收修改稿日期:2016-11-22。
国家杰出青年基金(No.51045216);内蒙古高校基金(No.NJZY13134)和内蒙古科技大学材料与冶金学院青年孵化平台资助项目。*
。E-mail:wujinxiu888@126.com,limei@163.com
