溶胶-凝胶法低温制备Ce0.8Sm0.2O2-α及其复合电解质的中温燃料电池性能
2017-09-06管清梅王洪涛
管清梅,王洪涛
(阜阳师范学院化学与材料工程学院,安徽环境污染物降解与监测省级重点实验室,安徽 阜阳 236037)
溶胶-凝胶法低温制备Ce0.8Sm0.2O2-α及其复合电解质的中温燃料电池性能
管清梅,王洪涛
(阜阳师范学院化学与材料工程学院,安徽环境污染物降解与监测省级重点实验室,安徽 阜阳 236037)
以三氧化二钐、浓硝酸、硝酸铈铵、柠檬酸为原料,采用溶胶-凝胶法低温(900℃)制备Ce0.8Sm0.2O2–α(SDC),低于通常高温烧结温度(1400℃),并与(Li/K)2CO3共熔体进行复合。采用DSC-TGA确定制备Ce0.8Sm0.2O2–α的烧结温度。XRD结果表明,(Li/K)2CO3与Ce0.8Sm0.2O2–α复合后没有发生化学反应。SEM图像表明,SDC粒径均匀一致,(Li/K)2CO3作为SDC颗粒黏结剂均匀覆盖SDC颗粒表面。采用电化学工作站研究了复合电解质在400~600℃下干燥氮气气氛中的电导率。结果表明,温度为600℃时,复合电解质在干燥氮气气氛中的电导率达到最大值3.3×10-2S/cm,高于单一二氧化铈材料在相同条件下的电导率。氧分压与电导率关系曲线表明,复合电解质具有良好的氧离子导电性。H2/O2燃料电池性能测试表明复合电解质Ce0.8Sm0.2O2–α-(Li/K)2CO3(SDC-SG-LK)在600℃开路条件下的电解质阻抗、极化阻抗分别为3.13Ω·cm2、0.81Ω·cm2,最大输出功率密度为130mW/cm2。
二氧化铈;复合材料;电解质;氢;燃料电池;电导率
氧化钇稳定的氧化锆(YSZ)是固体氧化物燃料电池(SOFC)最为广泛使用的固体电解质。然而,YSZ这种材料在高温(约1000℃)下才具有较高的离子电导率。在如此高的温度下各种材料的成本很高,所以降低SOFC工作温度是必要的[1-6]。掺杂氧化铈在中温400~800℃范围内具有足够的氧离子电导率,逐渐成为中温SOFC电解质材料[7-8]。
到目前为止,对于掺杂氧化铈的研究重点集中在合成及其电化学性能、热膨胀系数、力学性能等[9-10]。在合成方面,液相合成在分子水平上将原料混合反应,克服了固相法混合不均匀及烧结温度过高的缺点[11-14]。PRASAD等[12]通过新型溶胶-凝胶热分解法制备了纳米晶Ce1–xGdxO2–x/2(GDC)粉末,经400℃和600℃煅烧后,合成的GDC粉末均呈立方萤石结构,具有良好的结晶度。TADOKORO等[13]以硝酸铈、氧化钇、氧化镝为起始原料,用氨水作为沉淀剂,通过铈、钇、镝氢氧化物共沉淀,从而制备了Ce1-x(Y0.5Dy0.5)xO2-δ(0≤x≤0.15)固溶体。
近年来,二氧化铈与碳酸盐复合电解质成为最有前途的中温SOFC电解质材料[15-17]。对二氧化铈-碳酸盐复合材料,众多研究学者从制备方法、离子导电性、材料的相互作用、SOFC性能等方面进行了相关研究[18-20]。
本文以溶胶-凝胶法低温制备Ce0.8Sm0.2O2–α(SDC)并与(Li/K)2CO3共熔体进行复合。通过XRD对复合电解质材料的结构进行分析,通过SEM对复合电解质材料的形貌进行观察,并以交流阻抗技术对复合电解质中温电性能进行深入的研究,最后以复合电解质为隔膜构筑H2/O2燃料电池,探索其燃料电池性能。
1 实验部分
1.1 样品制备
首先采用溶胶-凝胶法制备Ce0.8Sm0.2O2–α(SDC-SG),按所需摩尔比称量Sm2O3溶于浓硝酸,再称取所需量的硝酸铈铵溶解,加入柠檬酸的量为总金属离子摩尔数的3倍。以适量的氨水调节pH至8~9,充分搅拌,加热,至形成透明溶胶。放置于烘箱中,在一定温度下恒温一定时间形成凝胶。将凝胶进行灰化处理,在900℃下烧结5h,得到Ce0.8Sm0.2O2–α。
碳酸锂、碳酸钾按照1∶1摩尔比例称量,研磨,混合均匀,置于箱式电阻炉中加热,温度设置为550℃,加热30min左右,冷却至室温后取出,研碎至细粉末状。将共熔体按上述操作重复一次,条件相同。冷却至室温后取出,研碎至细粉末状并用200目标准筛过筛后放入密封袋中并贴上标签备用。
取2.4g Ce0.8Sm0.2O2–α和0.6g碳酸锂、碳酸钾共熔体,混合于研钵中,并充分研磨均匀,在200 MPa压强下用压片机迅速压制成片,置于电炉中580℃下灼烧1h得到复合电解质Ce0.8Sm0.2O2–α-(Li/K)2CO3(SDC-SG-LK)。
1.2 样品的表征
采用DSC-TGA热分析仪(Universal V 3.7A)分析以确定Ce0.8Sm0.2O2–α的烧结温度,以XRD仪器测试复合电解质Ce0.8Sm0.2O2–α-(Li/K)2CO3的相结构,以SEM(日立S-4700)观察复合电解质断面及表面的形貌。
1.3 电性能测试
以国产CHI660E系电化学工作站测量复合电解质在400~600℃下干燥氮气气氛中的EIS,测试600℃下干燥气氛中不同氧分压下的EIS。其中干燥气体是采用P2O5干燥,氧分压用在线氧传感器测定。将复合电解质组装燃料电池,研究其中温燃料电池性能。
2 结果与讨论
2.1 DSC-TGA、XRD、SEM分析
将采用溶胶-凝胶法制备得到的凝胶进行热重分析(以空气为介质,升温速率为20℃/min),研究Ce0.8Sm0.2O2–α的物理、化学变化情况。图1是DSC-TGA(differential scanning calorimetry and thermogravimetric analysis)曲线。由图1可见,Ce0.8Sm0.2O2–α的质量在室温~160℃没有显著变化,这是仅有凝胶中水的蒸发所致。随后,提高温度至300℃,有两个较大的失重峰,对应于有机物热解及热解产物的挥发和分解过程。温度继续升高到760℃以上,几乎没有失重,表明开始逐渐形成二氧化铈立方相结构。

图1 差示扫描量热法热重分析曲线
采用X射线衍射仪分析了复合电解质的相分布和组分之间可能的反应。图2是复合电解质SDC-SG-LK的X射线衍射谱图。从图2中可看出,在2θ=30°附近出现最强的衍射峰,峰型较尖锐,半峰宽比较窄,表明样品具有很高的结晶度。SDC-SG-LK与标准衍射图谱JCPDS(00-046-0507)对比可看出,所有的衍射峰均与SDC晶面指数,即(110)、(200)、(220)、(311)、(222)、(400)、(331)和(420)强度与位置一致,还可以看出样品无衍射峰属于结晶碳酸盐衍射峰,说明(Li/K)2CO3以无定形态存在于复合电解质中,与Ce0.8Sm0.2O2–α复合后没有发生任何化学反应[21]。

图2 SDC-SG-LK的X射线衍射图(CuKα)
图3是SDC-SG-LK复合电解质的表面及断面的形貌照片。从图3可以看出,采用熔融(Li/K)2CO3与SDC在580℃下热处理1h,得到的复合电解质无孔洞。断面的SEM图像表明,SDC粒径均匀一致,(Li/K)2CO3作为SDC颗粒黏结剂均匀覆盖SDC颗粒表面,在微观结构中,SDC和(Li/K)2CO3在三维维度之间相互连接[22]。
2.2 电导率分析

图3 SDC-SG-LK表面和断面的SEM图
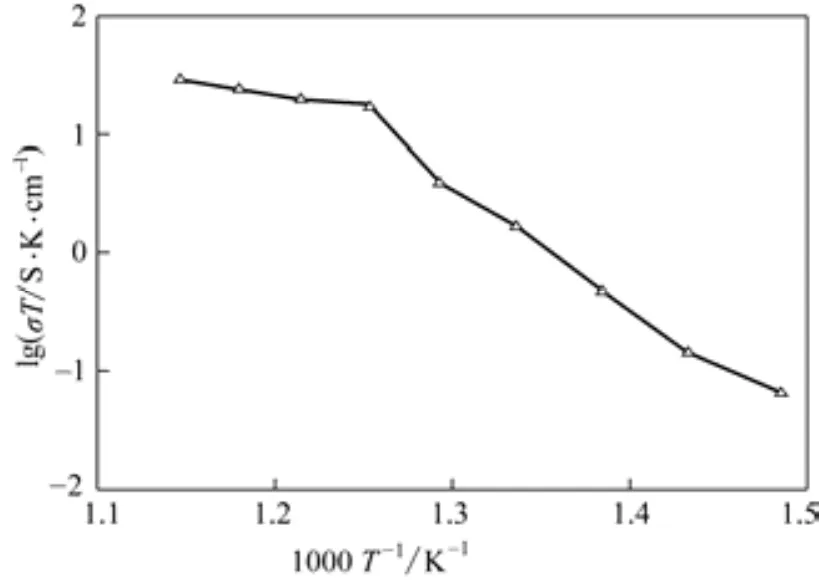
图4 SDC-SG-LK干燥氮气气氛下400~600℃的电导率
图4是复合电解质SDC-SG-LK在400~600℃下干燥氮气气氛中的电导率。由图4可见,随着温度逐渐升高,电导率逐渐增大,说明复合电解质具有较好的氧离子导电性。当温度为600℃时,复合电解质在干燥氮气气氛中的电导率达到最大值3.3×10–2S.cm–1,高于单一Nd3+、Y3+掺杂二氧化铈电解质[23]在相同温度下的电导率1.28×10–2S/cm。由文献可知,(Li/K)2CO3共熔温度为503℃[24],在400~500℃共熔温度以下SDC-SG-LK具有较大的斜率,对应较大的活化能。随着温度增加到(Li/K)2CO3共熔温度,再继续增大温度,斜率减小。这表明(Li/K)2CO3共熔体与Ce0.8Sm0.2O2–α复合在两个组成相之间的界面区域中形成了类似“高速公路”的传输通道,极大地降低了氧离子迁移必须克服的迁移活化能,有利于氧离子的传导[15-16]。
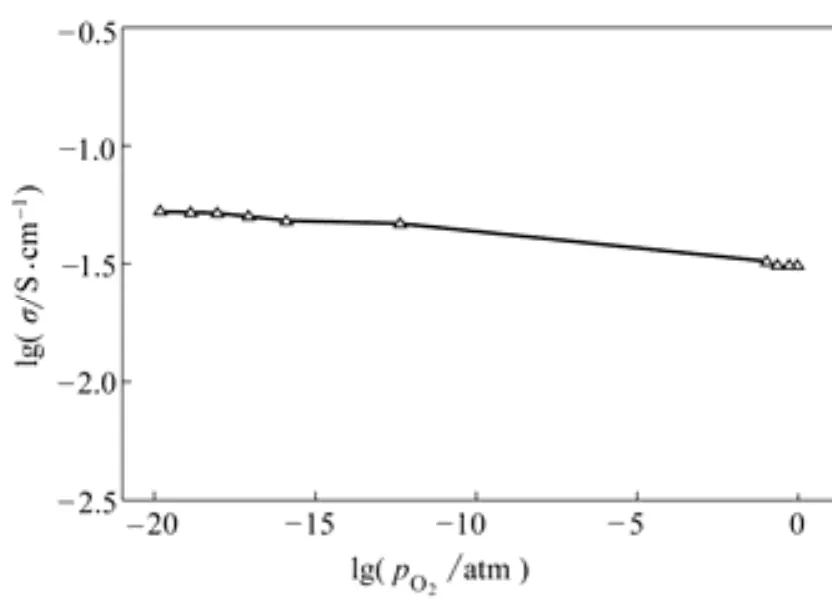
图5 SDC-SG-LK在干燥气氛中600℃下的电导率与氧分压关系曲线(1atm=101.325kPa)
图5为复合电解质SDC-SG-LK在干燥气氛中600℃下的氧分压与电导率关系曲线。对于氧分压与电导率关系曲线,当lgσ- lgpO2呈水平直线,表明电解质表现为离子导电性;当lgσ- lgpO2为非水平直线,表明电解质除了离子导电,还含有电子(或空穴)导电[25]。由图5可知,在pO2=100~10–5atm范围,SDC-SG-LK电导率几乎不随氧分压变化,表明复合电解质是良好氧离子导体;在pO2=10–5~10–20atm范围,电导率随着氧分压的减小而略有增加,表明样品除了氧离子导电,还存在少量电子导电。
2.3 燃料电池性能
SDC-SG-LK在开路电压下的EIS谱图表示在图6中。如图6所示,SDC-SG-LK的阻抗谱图由高频(HF)的半圆和低频(LF)的弧线组成,分别对应晶粒、晶界和电解质与电极界面间的电导过程。由图6可看出,复合电解质SDC-SG-LK在600℃开路条件下具有很小的电解质阻抗、极化阻抗,这说明复合中由于(Li/K)2CO3共熔体的存在,拓宽了氧离子的传导途径,有利于氧离子克服能垒而传导[15-16]。SDC-SG-LK在600℃开路条件下的电解质阻抗、极化阻抗分别为3.13Ω·cm2、0.81Ω·cm2。
分别以氢气为燃料气,氧气为氧化剂,以SDC-SG-LK为隔膜组装成H2/O2燃料电池,并测试I-V-P关系,结果如图7所示。在600℃下,SDC-SG-LK的开路电压为1.03V,接近于理论值,说明合成的复合电解质很致密,这是由于复合电解质中的 (Li/K)2CO3在共熔温度以上。对于单一二氧化铈电解质,由于部分Ce4+在还原性气氛中转变为Ce3+而产生电子传导,燃料电池的开路电压在这样的温度下很难超过0.90V,因此复合电解质中一定量无机碳酸盐的加入能有效抑制SDC的电子传导。开路电压逐渐降低,电流密度逐渐增大,功率密度逐渐增大,600℃下,最大输出功率密度为130mW/cm2。通过进一步降低复合电解质的厚度可以进一步提高最大输出功率密度。

图6 SDC-SG-LK在开路条件下的阻抗谱
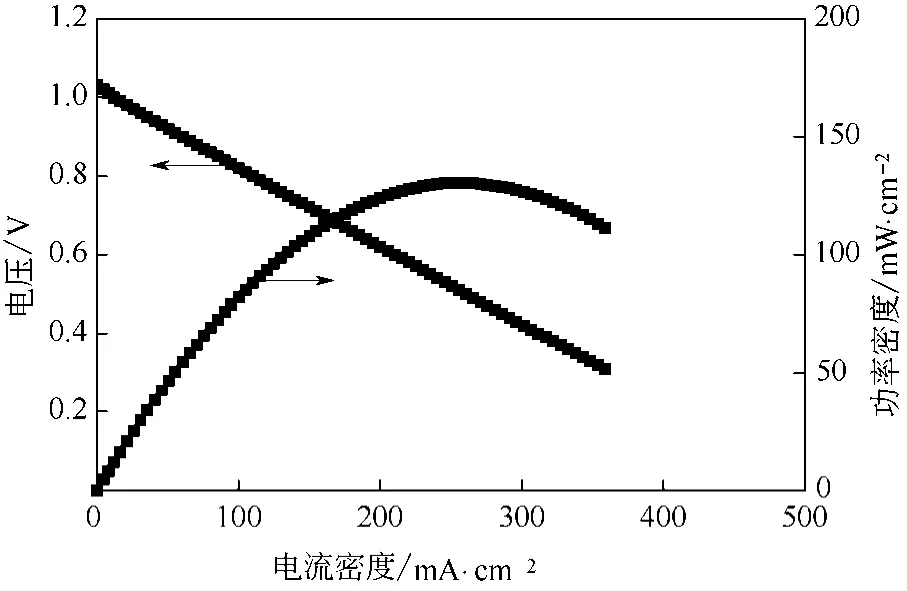
图7 SDC-SG-LK在600℃下的燃料电池I-V-P曲线
3 结论
以溶胶-凝胶法低温(900℃)制备Ce0.8Sm0.2O2–α,低于通常高温烧结温度(1400℃),并与 (Li/K)2CO3共熔体进行复合。XRD结果表明,(Li/K)2CO3与Ce0.8Sm0.2O2–α复合后没有发生化学反应。由于(Li/K)2CO3与Ce0.8Sm0.2O2–α复合极大地扩展了氧离子的传输途径,复合电解质在600℃干燥氮气气氛中电导率达到最大值3.3×10–2S/cm。600℃开路电压条件下的EIS谱图表明,复合电解质SDC-SG-LK具有很小的电解质阻抗3.13Ω·cm2和极化阻抗0.81Ω·cm2,最大输出功率密度为130mW/cm2。
[1] CHEN Y,ORLOVSKAYA N,PAYZANT E A,et al. A search for temperature induced time-dependent structural transitions in 10mol%Sc2O3-1mol% CeO2-ZrO2and 8mol% Y2O3-ZrO2electrolyte ceramics[J]. Journal of the European Ceramic Society,2015,35:951-958.
[2] 孙媛媛,屈树国,李建隆. 质子交换膜燃料电池用磺化聚醚醚酮膜的研究进展[J]. 化工进展,2016,35(9):2850-2860.SUN Y Y,QU S G,LI J L. Research progress of the sulfonated poly(ether ether ketone)s membranes for proton exchange membrane fuel cell[J]. Chemical Industry and Engineering Progress,2016,35(9):2850-2860.
[3] KONDOH J. Origin of the hump on the left shoulder of the X-ray diffraction peaks observed in Y2O3-fully and partially stabilized ZrO2[J]. Journal of Alloys and Compounds,2004,375:270-282.
[4] 邹浩斌,侯三英,熊子昂,等. 免增湿型空气自呼吸燃料电池的研究进展[J]. 化工进展,2016,35(1):91-97.ZOU H B,HOU S Y,XIONG Z A,et.al. Progress in the R&D of self-humidifying and air-breathing proton exchange membrane fuel cell[J].Chemical Industry and Engineering Progress,2016,35(1):91-97.
[5] UENO T,HIRATA Y,SHIMONOSONO T. Analysis of compressive deformation behavior of wet powder compacts of nanometer-sized yttria-stabilized zirconia particles[J]. Ceramics International,2016,42:1926-1932.
[6] 张雁玲,王红涛,孟凡飞,等. 微流体燃料电池发展现状[J]. 化工进展,2016,35(1):65-73.ZHANG Y L,WANG H T,MENG F F,et. al. Development status of microfluidic fuel cell[J]. Chemical Industry and Engineering Progress,2016,35(1):65-73.
[7] GESTEL T V,SEBOLD D,BUCHKREMER H P. Processing of 8YSZ and CGO thin film electrolyte layers for intermediate-and low-temperature SOFCs[J]. Journal of the European Ceramic Society,2015,35:1505-1515.
[8] JOO J H,CHOI G M. Open-circuit voltage of ceria-based thin film SOFC supported on nano-porous alumina[J]. Solid State Ionics,2007,178:1602-1607.
[9] KOBAYASHI T,WANG S R,DOKIYA M. Oxygen nonstoichiometry of Ce1–ySm2-0.5y–x(y=0.1,0.2)[J]. Solid State Ionics,1999,126:349-357.
[10] ZHANG L,LAN R,XU X X,et al. A high performance intermediate temperature fuel cell based on a thick oxide-carbonate electrolyte[J].Journal of Power Sources,2009,194:967-971.
[11] DZIEMBAJ R,MOLENDA M,ZAITZ M M,et al. Correlation of electrical properties of nanometric copper-doped ceria materials(Ce1-xCuxO2-δ)with their catalytic activity in incineration of VOCs[J]. Solid State Ionics,2013,251:18-22.
[12] PRASAD D H,SON J W,KIM B K,et al. Synthesis of nano-crystalline Ce0.9Gd0.1O1.95electrolyte by novel sol-gel thermolysis process for IT-SOFCs[J]. Journal of the European Ceramic Society,2008,28:3107-3112.
[13] TADOKORO S K,MUCCILLO E N S. Effect of Y and Dyco-doping on electrical conductivity of ceria ceramics[J]. Journal of the European Ceramic Society,2007,27:4261-4264.
[14] RAJESH S,MACEDO D A,NASCIMENTO R M,et al. One-step synthesis of composite electrolytes of Eu-doped ceria and alkali metal carbonates[J]. International Journal of Hydrogen Energy,2013,38:16539-16545.
[15] SHAWUTI S,GULGUN M A. Solid oxide-molten carbonate nano-composite fuel cells:particle size effect[J]. J. Power Sources,2014,267:128-135.
[16] ZHU B,LI S,MELLANDER B E. Theoretical approach on ceria-based two-phase electrolytes for low temperature(300—600℃)solid oxide fuel cells[J]. Electrochem. Commun.,2008,10:302-305.
[17] RAJESH S,MACEDO D A,NASCIMENTO R M,et al. One-step synthesis of composite electrolytes of Eu-doped ceria and alkali metal carbonates[J]. Int. J. Hydrogen Energy.,2013,38:16539-16545.
[18] KIM J T,LEE T H,PARK K Y,et al. Electrochemical properties of dual phase neodymium-doped ceria alkali carbonate composite electrolytes in intermediate temperature[J]. J. Power Sources,2015,275:563-572.
[19] HUANG J,MAO Z,LIU Z,et al. Performance of fuel cells with proton-conducting ceria-based composite electrolyte and nickel-based electrodes[J]. J. Power Sources,2008,175 :238-243.
[20] HUANG J,GAO Z,MAO Z. Effects of salt composition on the electrical properties of samaria-doped ceria/carbonate composite electrolytes for low-temperature SOFCs[J]. Int. J. Hydrogen Energ.,2010,35:4270-4275.
[21] RONDAO A I B,PATRICIO S G,FIGUEIREDO F M L,et al.Composite electrolytes for fuel cells:long-term stability under variable atmosphere[J]. Int. J. Hydrogen Energ.,2014,39:5460-5469.
[22] MARTINS N C T,RAJESH S,MARQUES F M B. Synthesis and electrochemical assessment of Ce0.5Yb0.5O1.75ceramics and derived composite electrolytes[J]. Mater. Res. Bull,2015,70:449-455.
[23] KOBI S,JAISWAL N,KUMAR D,et al. Ionic conductivity of Nd3+and Y3+co-doped ceria solid electrolytes for intermediate temperature solid oxide fuel cells[J]. Journal of Alloys and Compounds,2016,658:513-519
[24] LIU X,FECHLER N,ANTONIETTI M. Salt melt synthesis of ceramics,semiconductors and carbon nanostructures[J]. Chem. Soc.Rev.,2013,42:8237-8265.
[25] SAMMES N,PHILIPS R,SMIRNOVA A. Proton conductivity in stoichiometric and sub-stoichiometric yittrium doped SrCeO3ceramic electrolytes[J]. J. Power Sources,2004,134:153-159.
Ce0.8Sm0.2O2-αceramic prepared by sol-gel method at low temperature and its composite electrolyte in intermediate temperature fuel cells
GUAN Qingmei,WANG Hongtao
(Anhui Provincial Key Laboratory for Degradation and Monitoring of Pollution of the Environment,School of Chemical and Material Engineering,Fuyang Teachers College,Fuyang 236037,Anhui,China)
Ce0.8Sm0.2O2–αwas synthesized by sol-gel method at 900℃ using Sm2O3,HNO3,(NH4)2Ce(NO3)6,citric acid as raw materials and then compounded with (Li/K)2CO3. The preparation temperature(900℃)is much lower than conventional sintering temperature(1400℃). The sintering temperature of Ce0.8Sm0.2O2–α(SDC) was determined by DSC-TGA. The XRD results showed that there was no reactions between Ce0.8Sm0.2O2–αand (Li/K)2CO3. The SEM examinations revealed that the SDC particle size is uniform,and the surface is uniformly covered by (Li/K)2CO3that act as the SDC particle binder. The conductivity of the composite electrolyte in dry nitrogen was measured using electrochemical analyzer. The highest conductivity was 3.3×10–2S/cm at 600℃,which is higher than that of single CeO2material. The H2/O2fuel cell by the composite electrolyte showed that the electrolyte impedance and polarization impedance under open-circuit condition were 3.13Ω·cm2and 0.81Ω·cm2,respectively,and generated the maximum power density of 130mW/cm2at 600℃.
cerium oxide(CeO2);composites;electrolytes;hydrogen;fuel cells;conductivity
TQ133.3;O614.33
:A
:1000-6613(2017)09-3395-05
10.16085/j.issn.1000-6613.2016-2030
2016-11-07;修改稿日期:2017-05-16。
国家自然科学基金青年项目(51402052)及安徽省高等学校自然科学基金项目(2015KJ010)。
管清梅(1978—),女,副教授,主要从事物理化学和材料化学研究。E-mail:flyssky@163.com。联系人:王洪涛,教授,硕士生导师,主要从事电化学和材料化学研究。E-mail:hongtaoking3 @163.com。
