生物膜层干涉技术在生物分子分析和检测中应用的研究进展
2017-08-31杨国泰李福来王辰时何丽华许恒毅
杨国泰,吴 鑫,李福来,王辰时,何丽华,许恒毅*
(1.南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047;2.江西省食品检验检测研究院,江西 南昌 330046)
综 述
生物膜层干涉技术在生物分子分析和检测中应用的研究进展
杨国泰1,吴 鑫2,李福来1,王辰时1,何丽华1,许恒毅1*
(1.南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047;2.江西省食品检验检测研究院,江西 南昌 330046)
生物膜层干涉技术是基于光干涉信号实现对生物分子动力学分析或快速检测的非标记分析检测技术。因具有实时提供分析物信息、分析速度快和样品耗量少等优点,该技术已被应用于蛋白质、核酸、脂质、糖类及其他生物分子之间相互作用的分析;所需样品量少、特异性强等优点也为该技术应用于快速检测奠定了基础。该文介绍了生物膜层干涉技术的基本原理,综述了其在动力学分析和快速检测领域的相关应用研究,并对其发展趋势和应用前景进行了展望。
生物膜层干涉技术;动力学分析;快速检测;综述
非标记的生物分析方法无需借助人工标签可直接检测、分析生物分子,已被广泛应用于生物分子间相互作用的分析和检测[1]。非标记的生物分析方法具有如下优势[2-3]:①不需选择和设计标签,便于测定;②样品处理简单,分析检测时间短;③避免了化学标签对研究结果的影响。常见的非标记生物分析方法如表1所示。
生物膜层干涉(Biolayer interferometry,BLI)技术是基于光干涉原理的非标记技术,该技术除具有非标记生物分析方法的优势外,还具有操作简单、无损检测、样品耗量少、实时提供分析物的直接信息和相互作用情况等优点。通过对光干涉信号的实时监测,BLI技术能够广泛应用于生物分子相互作用的分析或快速检测。本文对BLI技术在动力学分析和快速检测中的应用进行了综述,旨在为生物分子研究中BLI技术的应用提供参考。

表1 非标记的分析检测技术
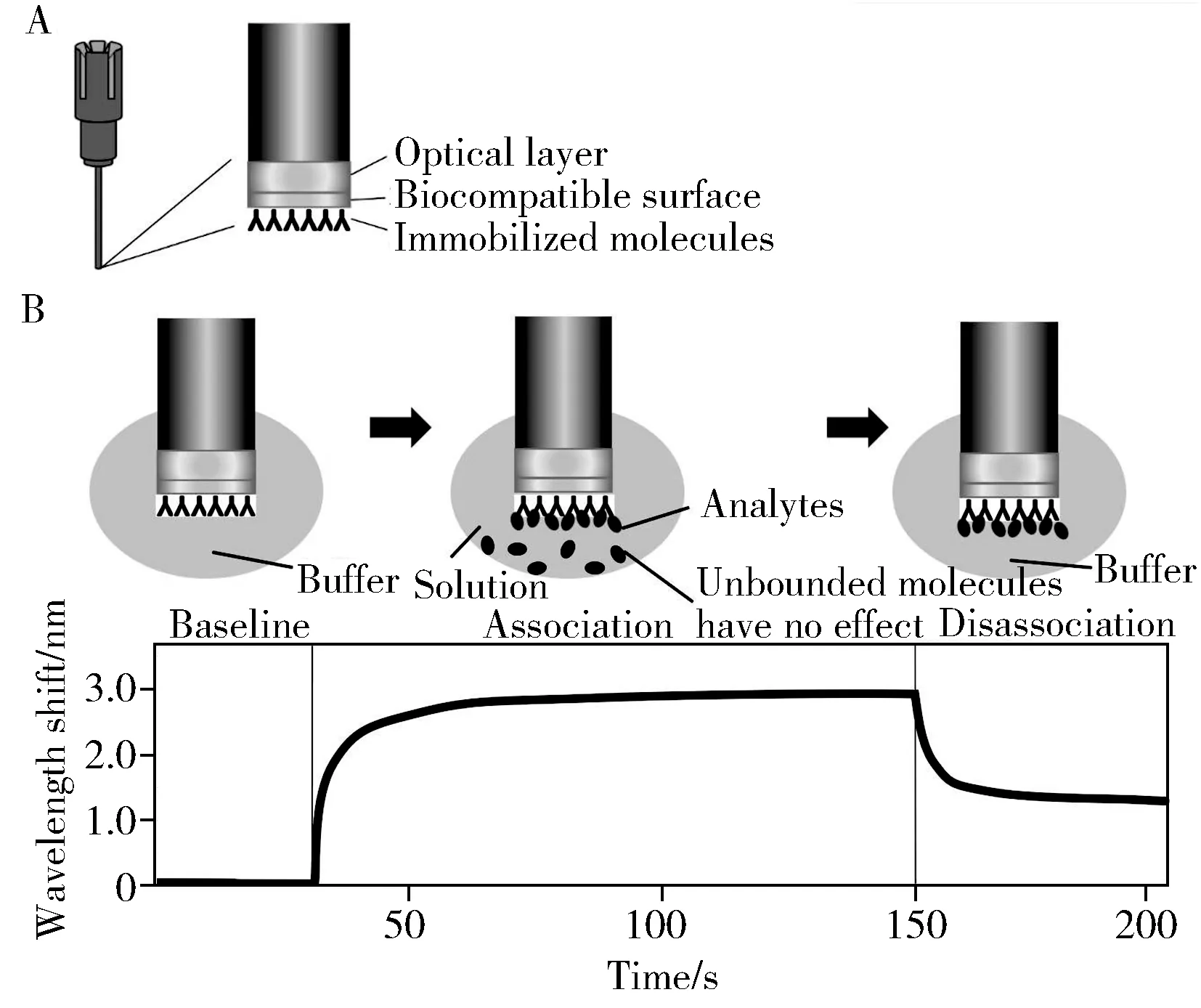
图1 BLI技术传感器(A)及基本检测过程(B)Fig.1 The sensor(A) and the basic detection process(B) of BLI
1 生物膜层干涉技术的原理
BLI通过实时监测光干涉信号的变化来实现生物分子的相互作用分析或检测(图1)。生物分子结合到光纤材质的生物传感器末端形成一层生物膜,当待分析物结合在生物传感器末端时会引起传感器末端分子量的改变,从而导致生物膜厚度的改变。当自然光通过生物膜时会发生反射和透射现象,生物膜厚度的变化导致干涉光波发生相对位移,生物分子结合前后的干涉光波被光谱仪检测到,形成干涉光谱,以干涉光谱的相对位移(nm)实时显示出来[11](图1B)。Octet®和BLItz®是基于BLI原理发展起来的商业化设备[12]。Octet®是多通道检测设备,整个检测过程完全自动化,能够控制检测模块的温度(控制范围为4~40 ℃),并且检测后样品可回收。BLItz®是单通道检测设备,检测过程需手动操作,不能控制检测温度,最少可检测4 μL样品。
2 生物膜层干涉技术在生物分子研究中的应用
2.1 生物膜层干涉技术在生物分子动力学分析中的应用
BLI技术因能实时检测生物分子之间的相互作用且只需少量样品,而被广泛应用于生物分子的筛选纯化、动力学常数的测定、相互作用的实时检测等(表2)。

表2 生物膜层干涉技术在生物分子动力学分析中的应用
aAHQ:anti-murine IgG quantitation;bAMC:anti-mouse IgG Fc capture;cAHC:anti-hIgG Fc capture ;dSA:streptavidin;eSSA:super streptavidin;fAPS:aminopropylsilane
2.1.1 蛋白质的动力学分析 目前,BLI技术对蛋白质动力学分析的研究主要集中于蛋白质的动力学常数测定、相互作用实时监测以及筛选纯化等方面。大量研究显示,应用BLI技术对蛋白质进行动力学分析具有结果准确可靠、样品用量少、检测速度快、无需标记等优点。Wartchow等[25]利用BLI技术测定了3种与人类疾病相关的蛋白质(BCL-2、eIF4E和JNK1)与酶蛋白之间的相互作用,并将该方法与表面等离子共振技术(SPR)以及时间分辨荧光分析法进行比较,结果发现BLI技术在蛋白质与蛋白质相互作用的表征中得出的数据与SPR及时间分辨荧光分析法得出的数据相符,体现了BLI技术的准确性。Sanders等[26]基于BLI技术对小麦及小麦粉中抗体和脱氧雪腐镰刀菌烯醇-卵白蛋白(DON-OVA)的亲和力进行测定,与酶联免疫吸附测定法(ELISA)相比,BLI技术可实现DON-OVA动力学的自动化检测,所需检测时间更短。
BLI技术在蛋白质相互作用分析方面还具有结果明确、灵敏度高等优势,Li等[17]基于BLI技术测定了抗药物抗体的亲和力,并与ELISA及电化学发光免疫法(ECLIA)进行比较,结果显示基于BLI技术的检测方法在低亲和力的抗药物抗体检测方面具有更高的灵敏度,并且在含有药物样品的测定中发现BLI技术更耐循环药物的干扰;该检测结果表明BLI技术在免疫原性评估研究中的巨大应用前景。BLI技术在蛋白质相互作用的实时监测方面也得到了广泛应用。Ciesielski等[18]通过BLI技术对DNA聚合酶γ(Polγ)的两个亚基Polγα、Polγβ的结合和解离进行实时监控,发现二者结合快而解离慢,由此反映出Polγ发生失调而导致线粒体疾病出现的情况与Polγ两个亚基结构之间相互作用情况的关系。此外,BLI技术也可用于蛋白质的筛选纯化。Brenac等[14]应用BLI技术对单克隆抗体进行分离纯化,单克隆抗体的整体回收率达到90%,纯度接近97%,表明BLI技术在提高单克隆抗体的纯度、缩短单克隆抗体提取时间以及降低单克隆抗体的纯化成本等方面具有良好应用价值。Do等[16]通过BLI技术纯化了3种不同树脂中的人免疫球蛋白G,结果显示仅有少量人免疫球蛋白G残留于原有样品中,而负载在传感器上的人免疫球蛋白G的回收率接近100%。
2.1.2 核酸的动力学分析 随着应用范围的不断拓展,BLI技术在核酸的动力学分析中也被越来越多地应用。在核酸与蛋白质的动力学分析中,He等[27]基于BLI技术测定了锌指AN1型结构域5(Zfand5)与肿瘤坏死因子的mRNA序列(ARETNF)、锌指蛋白36(TTP)与ARETNF之间的解离常数KD,发现Zfand5和TTP在与ARETNF结合时,二者之间具有竞争关系。Normand等[28]应用BLItz®研究了有机偶氮苯染料CSB对ssDNA和蛋白质Rad51之间相互作用的影响,发现CSB对ssDNA和Rad51的偶联具有强的抑制作用,表明BLI技术在核酸与蛋白质相互作用的分析中具有好的应用效果。BLI技术也能用于核酸之间的动力学分析,Grieshaber等[29]通过BLI技术研究了衣原体基因组RNA(CTL0322和CTL0097)与参与蛋白质HctA生成的RNA IhtA之间的实时相互作用,结果显示CTL0322、CTL0097对IhtA具有明显的作用效果,表明通过BLI技术能够实现核酸之间的动力学分析,且结果准确。另外,郑欣等[23]将BLI技术应用于核酸与小分子物质相互作用的分析,测得适配体与石房蛤毒素间的亲和常数Kd值为7.44 μmol/L,且该适配体不与河豚毒素结合。
2.1.3 其他生物分子的动力学分析 BLI技术在其他生物分子的动力学分析中也有广泛应用。Wallner等[20]利用BLI技术测定了3种不同脂质体制剂与固定化的重组人促红细胞生成素之间的亲和力常数等动力学数据,结果显示3种脂质体制剂均能与固定蛋白质形成稳定的配合物,此外,脂质体浓度依赖性的结合模式也得到了证明。Niu等[21]基于BLI技术测定了λ-卡拉胶和小分子物质bFGF之间的亲和力常数Kd、偶联常数Kon和解离常数Kdis。Naik等[30]用BLI技术和SPR监测炭疽毒素在pH驱动下发生孔隙易位的结构和动力学变化,该研究成果可进一步用于利用药物调节或抑制炭疽毒素的研究中。随着技术的逐步成熟,BLI技术将会被越来越多地应用于各种生物分子动力学分析的研究中。
2.2 生物膜层干涉技术在生物分子快速检测中的应用
BLI技术除了可对生物分子进行动力学分析以外,还可对蛋白质、核酸、糖类以及其他小分子物质进行快速检测。应用BLI技术对生物分子进行快速检测时,其所需样品量少、特异性强的优点能够得到充分体现。
2.2.1 蛋白质的快速检测 通过BLI技术快速测定蛋白质的方法已见诸报道,为了提高检测的灵敏度,还发展出一系列放大信号的策略。Auer等[31]将诺洛病毒样颗粒固定在Ni-NTA传感器上,再连接诺洛病毒特异性抗体,通过在诺洛病毒特异性抗体上连接经由HRP修饰的二抗、HRP氧化金属螯合剂DAB形成沉淀实现信号放大,从而实现血清样品中诺洛病毒特异性抗体的灵敏检测,该方法能在10~20 min检测出稀释倍数达100 000倍的血清样品中的诺洛病毒特异性抗体。Mechaly等[32]对剧毒蛋白质蓖麻毒素进行了定量检测研究,先在SA传感器上固定抗体,然后与抗原连接,再在抗原上连接修饰有碱性磷酸酶的抗体,最后通过在含有碱性磷酸酶底物BCIP/NBT的溶液中沉浸,使其在传感器表面析出不溶性结晶,实现放大干涉信号的效果,形成显著的干涉现象,该方法可在17 min内完成检测,检测限达10 pg/mL。
2.2.2 核酸的快速检测 核酸是最基本的生命物质之一,它在生长、遗传、变异等一系列重大生命现象中起着决定性作用,开发核酸的检测方法具有重要意义。Zhang等[33]应用BLI技术对目标DNA片段进行了检测,首先在SA传感器上固定DNA探针,随后通过碱基互补配对结合方式将目标DNA捕获在传感器的表面,通过测定光干涉信号的变化实现检测。由于微小核酸片段较小,低浓度时的光干涉信号较弱,检测限较高(20 nmol/L)。为了提高检测的灵敏度,作者设计了四面体结构的DNA探针,通过“吊坠”模式进行信号放大,使检测限提高了100倍。
2.2.3 其他生物分子的快速检测 BLI技术还被用于糖类、小分子以及其他生物分子的快速检测。刘小军等[34]应用BLI技术快速检测牛乳中的β-内酰胺类抗生素残留,结果显示无标记状态下氨苄青霉素的检测灵敏度约为50 ng/mL,金标记状态下灵敏度约为1.56 ng/mL;另外通过对其他β-内酰胺类抗生素进行BLI和胶体金免疫层析试纸条的检测发现,BLI技术的检测灵敏度比胶体金免疫层析试纸条的检测灵敏度高1倍,且具有特异性强、无交叉反应的特点。Zhang等[33]将ATP与DNA四面体结构的探针结合,再通过ATP与SA传感器结合,实现了ATP的定量检测,检出限可达2 mmol/L。Paek等[35]将伴刀豆球蛋白A固定在传感器上,并将传感器浸入到半透膜隔离的含牛血清蛋白的基质中,此时牛血清蛋白与伴刀豆球蛋白A结合,当传感器沉浸到含葡萄糖的样品中时,葡萄糖透过半透膜进入含牛血清蛋白的基质中,并与伴刀豆球蛋白A结合,从而将牛血清蛋白竞争下来,使干涉信号产生变化,实现了葡萄糖的定量检测。此方法能在15 min内对10~500 mg/dL浓度范围内的葡萄糖样品进行实时监测。
3 总结与展望
BLI技术由于具有操作简单、样品耗量少、检测速度快、结果准确等优点,已被广泛应用于生物分子的动力学分析和快速检测。本文聚焦BLI,综述了其在蛋白质、核酸、脂质、糖类及其他生物分子分析检测中的研究进展。目前,BLI技术的应用范围不断扩展:由于SA传感器的固化分子具有与细胞表面受体密度相似的独特优势,BLI技术在病毒与受体直接分析方面崭露头角[36-37];BLI技术也逐渐应用于菌体的直接检测[32]和纳米材料的动力学分析[38]等方面。但随着生物分子分析检测方法的不断升级,BLI技术在提高结果的准确性、操作的简便性、方法的经济性等方面面临巨大挑战。同时,BLI技术作为固液反应技术,仍然存在对实验条件要求严格、应用范围有局限等不足[11]。因此,BLI技术在完善检测方法、拓宽检测范围等方面具有广阔的发展空间。另外,随着市场需求的不断增加,BLI技术在降低使用成本、改进分析技术等方面还有待提升。相信经过不断的发展和完善,BLI技术必将在生物分子的分析检测乃至更广阔的领域发挥更大的价值。
[1] Concepcion J,Witte K,Wartchow C,Choo S,Yao D,Persson H,Wei J,Li P,Heidecker B,Ma W,Varma R,Zhao L S,Perillat D,Carricato G,Recknor M,Du K,Ho H,Ellis T,Gamez J,Howes M,Phi-Wilson J,Lockard S,Zuk R,Tan H.CombinatorialChemistry&HighThroughputScreening,2009,12(8):791-800.
[2] Cooper M A.Nat.Rev.DrugDiscovery,2002,1(7):515-528.
[3] Cooper M A,Whalen C.DrugDiscoveryToday:Technologies,2005,2(3):241-245.
[4] Williams M,Daviter T.Protein-LigandInteractions:MethodsandApplications. 2nd ed.Passaic:Humana Press, 2013:139-165.
[5] Cai J F.ProteinInteractions.Rijeka:InTech,2012:401-427.
[6] Kameyama K,Minton A P.Biophys.J.,2006,90(6):2164-2169.
[7] Wilson J L,Scott I M,McMurry J L.Biochem.Mol.Biol.Edu.,2010,38(6):400-407.
[8] Jerabek-Willemsen M,Wienken C J,Braun D,Baaske P,Duhr S.AssayDrugDev.Technol.,2011,9(4):342-353.
[9] Fu H A.Protein-ProteinInteractions:MethodsandProtocols.Passaic:Humana Press,2004:35-54.
[10] Gao J M,Zhang Z M,Li G K.J.Instrum.Anal.(高嘉敏,张卓旻,李攻科.分析测试学报),2016,35(12):1647-1653.
[11] Coligan J E,Dunn B M,Speicher D W,Wingfield P T.CurrentProtocolsinProteinScience.Hoboken:John Wiley & Sons,Inc.,2015,79:19.25.1-19.25.26.
[12] Maragos C M.MycotoxinRes.,2011,27(3):157-165.
[13] Sun T W,Reid F,Liu Y Q,Cao Y,Estep P,Nauman C,Xu Y.Mabs,2013,5(6):838-841.
[14] Brenac Brochier V,Ravault V.Eng.LifeSci.,2015,16:152-159.
[15] Huang X L,Chen R,Xu H Y,La W H,Xiong Y H.Anal.Chem.,2016,88(3):1951-1958.
[16] Do T,Ho F,Heidecker B,Witte K,Chang L,Lerner L.ProteinExpress.Purif.,2008,60(2):147-150.
[17] Li J,Schantz A,Schwegler M,Shankar G.J.Pharm.Biomed.Anal.,2011,54(2):286-294.
[18] Ciesielski G L,Hytönen V P,Kaguni L S.MitochondrialDNA:MethodsandProtocols,2016,1351:223-231.
[19] Grabherr M G,Pontiller J,Mauceli E,Ernst W,Baumann M,Biagi T,Swofford R,Russell P,Zody M C,Di Palma F,Lindblad-Toh K,Grabherr R M.PlosOne,2011,6(5):e20136.
[20] Wallner J,Lhota G,Jeschek D,Mader A,Vorauer-Uhl K.J.Pharm.Biomed.Anal.,2013,72:150-154.
[21] Niu T T,Zhang D S,Chen H M,Yan X J.Carbohydr.Polym.,2015,125:76-84.
[22] DiGiandomenico A,Warrener P,Hamilton M,Guillard S,Ravn P,Minter R,Camara M M,Venkatraman V,Macgill R S,Lin J,Wang Q,Keller A E,Bonnell J C,Tomich M,Jermutus L,McCarthy M P,Melnick D A,Suzich J A,Stover C K.J.Exp.Med.,2012,209(7):1273-1287.
[23] Zheng X,Hu B,Gao S X,Liu D J,Sun M J,Wang L H.Chin.J.Biochem.Pharm.(郑欣,胡波,高顺祥,刘德婧,孙铭娟,王梁华.中国生化药物杂志),2014,9:17-19.
[24] Braesch-Andersen S,Beckman L,Paulie S,Kumagai-Braesch M.PLoSOne,2014,9(12):e115180.
[25] Wartchow C A,Podlaski F,Li S,Rowan K,Zhang X,Mark D,Huang K S.JournalofComputer-aidedMolecularDesign,2011,25(7):669-676.
[26] Sanders M,McPartlin D,Moran K,Moran K,Guo Y,Eeckhout M,O'Kennedy R,De Saeger S,Maragos C.Toxins,2016,8(4):103.
[27] He G A,Sun D X,Ou Z Y,Ding A H.J.Biol.Chem.,2012,287(30):24967-24977.
[28] Normand A,Rivière E,Renodon-Cornière A.Biochem.Pharmacol.,2014,91(3):293-300.
[29] Grieshaber N A,Tattersall J S,Liguori J,Lipat J N,Runac J,Grieshaber S S.PLoSOne,2015,10(3):e0116593.
[30] Naik S,Brock S,Akkaladevi N,Tally J,McGinn-Straub W,Zhang N,Gao P,Gogol E P,Pentelute B L,Collier R J,Fisher M T.Biochemistry,2013,52(37):6335-6347.
[31] Auer S,Koho T,Uusi-Kerttula H,Vesikari T,Blazevic V,Hytönen V P.Sens.ActuatorsB,2015,221:507-514.
[32] Mechaly A,Cohen H,Cohen O,Mazo O.Anal.Biochem.,2016,506:22-27.
[33] Zhang M,Jiang X Q,Le H N,Wang P,Ye B C.ACSAppl.Mater.Interfaces,2013,5(3):473-478.
[34] Liu X J,Fu H,Xue F,Ma T,Zeng X X,Zhu H.J.AnhuiAgric.Sci.(刘小军,付辉,薛峰,马涛,曾祥翔,朱海.安徽农业科学),2013,41(23):9749-9750.
[35] Paek S H,Cho I H,Kim D H,Jeon J W,Lim G S,Paek S H.Biosens.Bioelectron.,2013,40(1):38-44.
[36] Xiong X,Coombs P J,Martin S R,Liu J,Xiao H,McCauley J W,Locher K,Walker P A,Collins P J,Kawaoka Y,Skehel J J,Gamblin S J.Nature,2013,497(7449):392-396.
[37] Vachieri S G,Xiong X,Collins P J,Walker P A,Martin S R,Haire L F,Zhang Y,McCauley J W,Gamblin S J,Skehel J J.Nature,2014,511(7510):475-477.
[38] Gao D,Zhang Z P,Li F,Men D,Deng J Y,Wei H P,Zhang X E,Cui Z Q.Int.J.Nanomed.,2013,8:2119-2128.
中科院生态环境研究中心在碳纳米管毒理机制方面取得系列进展
中国科学院生态环境研究中心环境化学与生态毒理学国家重点实验室郭良宏研究组在碳纳米管细胞外排生物过程和效应方面取得重要进展,相关研究成果近期发表于国际著名纳米科学期刊Small并作为当期的封底文章(Small,2016,12,5998-6011)。碳纳米管具有独特的理化性质,在电子、环境和纳米医药等领域的应用潜力巨大,而随之带来的潜在环境与健康危害也越来越受到关注。碳纳米管与细胞的相互作用始于物理接触,随后被细胞摄入、外排或者降解,这些生物过程决定了碳纳米管实际的细胞内暴露量,因而对碳纳米管后续的毒性/生物效应至关重要。全面深入了解这个复杂过程中涉及到的分子机制及后续生物效应,有利于揭示和调控碳纳米管的生物活性,促进碳纳米管技术的可持续发展。
郭良宏研究组近年来一直致力于碳纳米管的细胞毒代动力学和热力学过程及其毒理机制的研究。研究组从分子水平、细胞功能和细胞自噬等角度,对碳纳米管的免疫毒性机制进行了系统的研究。其工作中采用基因芯片技术研究了碳纳米管对巨噬细胞全基因组基因表达的影响,通过生物信息学分析,解析出碳纳米管在转录组水平对细胞的线粒体、蛋白酶体等细胞器以及细胞周期/凋亡等多个信号通路的基因表达的调控作用(Nanotoxicology,2012)。以此为线索,研究组以原代小鼠腹腔巨噬细胞(PMQ)和纯化CD4+T淋巴细胞为模型,评价了碳纳米管对PMQ吞噬功能、辅助细胞功能以及分泌细胞因子功能的干扰效应,揭示了碳纳米管在非毒性剂量水平,对免疫细胞功能的影响(Nanotoxicology,2013)。
研究组近期在碳纳米管的细胞内吞、外排动力学过程研究中取得一系列新进展。研究定量分析了细胞累积碳纳米管随时间变化的趋势,发现每个巨噬细胞最大能累积皮克级的碳纳米管,巨胞饮在碳纳米管内吞过程中起主导作用,并存在明显的细胞外排现象(Scientific Reports,2017)。碳纳米管进入细胞后定位于溶酶体,阻碍了细胞自噬体的消解,细胞自噬流被阻断,引起自噬体过度累积,导致细胞毒性。另一方面,通过调控细胞的呼吸爆发能有效控制其在溶酶体中的降解(Toxicology Letters,2013;International Journal of Molecular Sciences,2016)。研究首次发现一种特殊的嘌呤受体-P2X7参与介导了碳纳米管的外排过程: 碳纳米管暴露导致细胞外ATP(eATP)浓度上升,激活了P2X7受体及其后续的一系列信号传导,并引起溶酶体碱化后沿着细胞骨架导轨排出细胞,碳纳米管随溶酶体一起排出(Small,2016)。重金属离子Ni2+能通过抑制P2X7受体活性阻碍碳纳米管的正常外排,造成过量的碳纳米管在细胞内累积,引起碳纳米管毒性的显著上升 (Environmental Science & Technology,2016)。以上工作明确了碳纳米管细胞外排机制,不仅有利于深入了解碳纳米管的毒性机制及提供可能的控制方法,还提出了一个纳米材料与化合物协同毒性效应的新机制,为研究环境中碳纳米管与其他污染物共存状态下的安全性评价提供了新的思路。
以上研究工作得到了国家基金委和中国科学院的资助。
(信息来源:中国科学院生态环境研究中心)
Research Progress in Application of Biolayer Interferometry in Analysis and Detection of Biomolecules
YANG Guo-tai1,WU Xin2,LI Fu-lai1,WANG Chen-shi1,HE Li-hua1,XU Heng-yi1*
(1.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China;2.Jiangxi Institute for Food Control,Nanchang 330046,China)
Biolayer interferometry is an optical system that monitors interactions between biological materials and detects biological materials rapidly for lable-free.Due to its advantages of real-time,rapidness and low sample consumption,biolayer interferometry has been gradually used for detecting interactions between proteins,peptides,nucleic acids,small molecules,and/or lipids.Furthermore,biolayer interferometry could also provide a solid foundation in rapid detection field because of its low sample consumption and strong specificity.In this article,the principle of biolayer interferometry is discussed,and two major application areas including kinetic analysis and rapid detection are investigated and reviewed.The development trend and future application of biolayer interferometry for measuring biological materials are also prospected.
biolayer interferometry;kinetic analysis;rapid detection;review
2017-03-28;
2017-04-27
江西省青年科学家(井冈之星)培养对象项目(2014BCB23004);江西省食品药品监督管理局科技计划(2015SP13)
10.3969/j.issn.1004-4957.2017.08.020
O657.3;G353.11
A
1004-4957(2017)08-1055-06
*通讯作者:许恒毅,博士,副研究员,研究方向:食品生物技术,Tel:0791-88304447-222-9520,E-mail:kidyxu@163.com
