壮药竹节蓼的质量标准研究Δ
2017-08-14曾祥燕唐玉荣颜萍花广西中医药大学药学院南宁530001
曾祥燕,唐玉荣,颜萍花,黎 理(广西中医药大学药学院,南宁 530001)
壮药竹节蓼的质量标准研究Δ
曾祥燕*,唐玉荣,颜萍花,黎 理#(广西中医药大学药学院,南宁 530001)
目的:建立壮药竹节蓼的质量标准。方法:采用薄层色谱法(TLC)对药材样品进行定性鉴别;采用高效液相色谱法对药材样品中槲皮苷进行含量测定:色谱柱为Agilent Zorbax SB-C18,流动相为乙腈-0.1%冰醋酸溶液(20∶80,V/V),流速为1.0 mL/min,检测波长为360 nm,柱温为30℃,进样量为10 μL;参照2015年版《中国药典》测定药材样品水分、灰分和浸出物的含量。结果:竹节蓼药材的TLC图斑点清晰,分离度好。槲皮苷检测质量浓度线性范围为0.023~0.46 mg/mL(r=0.999 1);精密度、稳定性、重复性试验的RSD<2.0%;加样回收率为98.01%~103.05%(RSD=1.71%,n=6)。药材样品水分、总灰分、酸不溶性灰分、浸出物和槲皮苷含量分别为6.39%~9.78%、2.82%~8.07%、0.02%~0.27%、14.14%~28.45%、0.09%~0.50%。结论:该研究所建标准可用于壮药竹节蓼的质量控制。
壮药;竹节蓼;槲皮苷;定性;定量;薄层色谱法;高效液相色谱法
ABSTRACTOBJECTIVE:To establish quality standard for Zhuang medicine Homalocladium platycladum.METHODS:TLC method was used for qualitative identification.HPLC method was used to determine the content of quercetrin in samples:Agilent Zorbax SB-C18column,mobile phase consisted of acetonitrile-0.1%acetic acid(20∶80,V/V),flow rate of 1.0 mL/min,detection wavelength of 360 nm,column temperature of 30℃,injection volume of 10 μL.The contents of moisture,total ash and extract in samples were determined.referring to Chinese Pharmacopiea(2015 edition).RESULTS:TLC spots of H.platycladum were clear and well-separated without interference from negative control.The linear range of quercetin were 0.023-0.46 mg/mL(r=0.999 1). RSDs of precision,stability and repeatability tests were all lower than 2.0%.The average recoveries were 98.01%-103.05%(RSD=1.71%,n=6).The contents of moisture,total ash,extract and quercetrin in samples were 6.39%-9.78%,2.82%-8.07%,0.02%-0.27%,14.14%-28.45%,0.09%-0.50%respectively.CONCLUSIONS:Established trial can be used for quality control of Zhuang medicine H.platycladum.
KEYWORDSZhuang medicine;Homalocladium platycladum;Quercetrin;Qualitative;Quantitative;TLC;HPLC
竹节蓼为蓼科植物竹节蓼Homalocladium platycladum(F.Muell.ex Hook.)L.H.Bailey的全草[1],又名观音竹、飞天蜈蚣、扁竹等,味甘、淡,性平,归肝、肺经,具有清热解毒、祛瘀消肿的功效,主治痈疮肿毒、跌打损伤等症,在民间常作为草方用于治疗肿瘤,效果显著[2-3],但其化学成分研究未见报道。本课题组前期研究发现竹节蓼中含有金丝桃苷和槲皮苷等黄酮类化合物。而研究表明,槲皮苷和金丝桃苷具有抗肿瘤、抗炎、抗菌等作用,与竹节蓼功效主治具有一定相关性[4-7]。笔者采用薄层色谱法(TLC)和高效液相色谱法(HPLC)[8-10]对竹节蓼药材中槲皮苷进行定性定量分析,并对其水分、灰分及浸出物含量进行测定,以期为其质量控制提供科学依据。
1 材料
1.1 仪器
1260型HPLC仪,包括DAD检测器、1260色谱工作站(美国Agilent公司);FA1104型电子分析天平(上海精密科学仪器有限公司);KQ5200B型超声波清洗器(昆山市超声仪器有限公司,功率:250 W,频率:40 kHz);DHG-9070A型电热鼓风干燥箱(上海一恒科学仪器有限公司);H1650-W型高速离心机(长沙湘仪离心机仪器有限公司);HH-S6型电热恒温水浴锅(金坛市医疗仪器厂)。
1.2 试剂
槲皮苷对照品(中国食品药品检定研究院,批号:111538-200504,纯度:>98%);硅胶GF254(青岛海洋化工有限公司,批号:0140828);乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。
1.3 药材
竹节蓼药材采自广西各地(见表1),经广西中医药大学中药鉴定教研室蔡毅教授鉴定为真品。以编号为ZJL-1的药材样品作对照药材。

表1 竹节蓼药材来源Tab 1 Resouce of H.platycladum
2 方法与结果
2.1 定性鉴别
取药材样品粉末1 g,加50%甲醇溶液20 mL,超声处理30 min,滤过,滤液蒸干,浓缩加50%甲醇溶液定容至1 mL,即得供试品溶液。另取槲皮苷对照品,加50%甲醇溶液制成质量浓度为1 mg/mL的对照品溶液。再取竹节蓼对照药材粉末1 g,同供试品溶液制备方法制成对照药材溶液。按TLC法[2015年版《中国药典》(四部)][11]试验,吸取上述3种溶液各10 μL,分别点于同一硅胶GF254薄层板上,以乙酸丁酯-环己烷-甲酸-水(6∶1.2∶1.8∶0.5,V/V/V/V)为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照药材和对照品色谱相应位置上显相同颜色的斑点,详见图1。
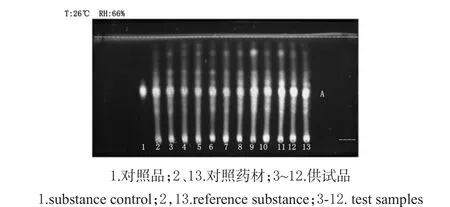
图1 薄层色谱图Fig 1 TLC chromatogram
2.2 含量测定
2.2.1 色谱条件与系统适用性试验 色谱柱:Agilent Zorbax SB-C18(250 mm×4.6 mm,5 μm);流动相为乙腈-0.1%冰醋酸溶液(20∶80,V/V);流速:1.0 mL/min;检测波长:360 nm;柱温:30℃;进样量:10 μL。在上述色谱条件下,理论板数以槲皮苷峰计>3 000;各成分基线分离良好,分离度>1.5,详见图2。
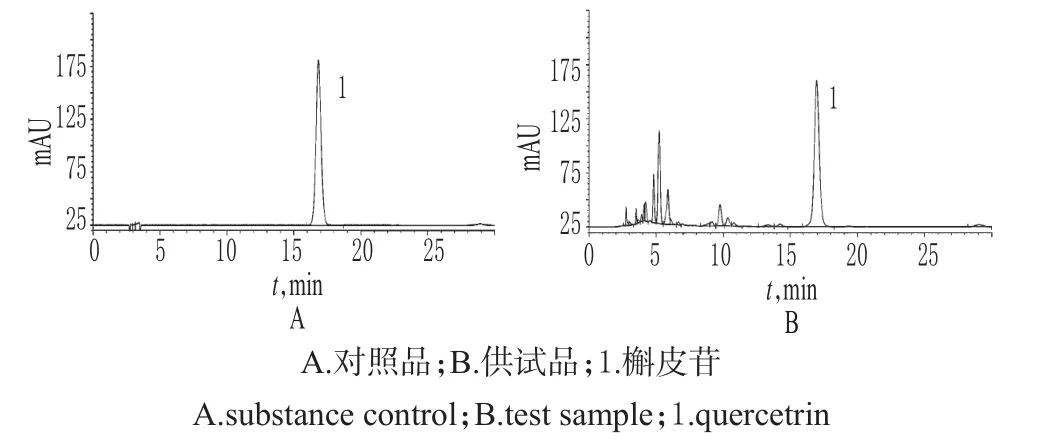
图2 高效液相色谱图Fig 2 HPLC chromatograms
2.2.2 对照品溶液的制备 取槲皮苷对照品适量,精密称定,加甲醇制成质量浓度为0.344 mg/mL的对照品溶液。
2.2.3 供试品溶液的制备 称取药材样品(编号:ZJL-1)约1 g,精密称定,置于具塞锥形瓶中,精密加70%甲醇溶液20 mL,称定质量,超声提取45 min,放至室温,再次称定质量,加70%甲醇溶液补足减失的质量,摇匀,滤过,精密量取滤液约2 mL,以半径为12 cm、10 000 r/ min离心10 min,取上清液,即得。
2.2.4 线性关系考察 分别精密量取“2.2.2”项下对照品溶液0.1、0.2、0.4、0.8、1.6、2.0 mL,分别置于2 mL量瓶中,加甲醇定容,制成系列对照品溶液。精密量取上述系列对照品溶液各10 μL,按“2.2.1”项下色谱条件进样测定,记录峰面积。以槲皮苷质量浓度(x,mg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得槲皮苷回归方程为y=18 165.511 9x-47.969 429(r=0.999 1)。结果表明,槲皮苷检测质量浓度线性范围为0.023~0.46 mg/mL。
2.2.5 精密度试验 取“2.2.2”项下对照品溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,槲皮苷峰面积的RSD=0.08%(n=6),表明仪器精密度良好。
2.2.6 稳定性试验 取“2.2.3”项下供试品溶液(编号:ZJL-1)适量,分别于室温下放置0、4、8、12、16、24 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,槲皮苷峰面积的RSD=0.51%(n=6),表明供试品溶液在室温放置24 h内基本稳定。
2.2.7 重复性试验 精密称取同一批样品(编号:ZJL-1)适量,按“2.2.3”项下方法制备供试品溶液,共6份,再按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,槲皮苷峰面积的RSD=1.73%(n=6),表明本方法重复性良好。
2.2.8 加样回收率试验 取已知含量样品(编号:ZJL-1)适量,每份0.25 g,共6份,分别加入一定质量的槲皮素对照品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.2.9 样品含量测定 取11批样品各适量,分别按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表3。

表2 加样回收率试验结果(n=6)Tab 2 Results of recovery test(n=6)
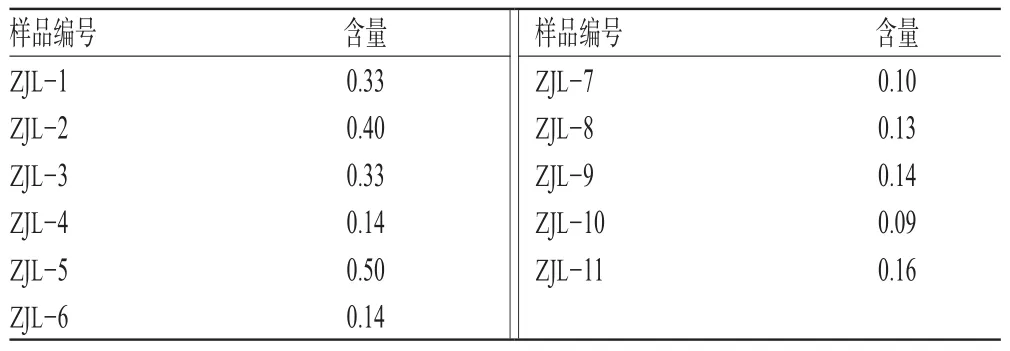
表3 样品含量测定结果(n=3,%)Tab 3 Results of content determination of samples(n=3,%)
由表3可知,11批药材样品中槲皮苷含量为0.09%~0.50%,初步拟定按干燥品计算,本品含槲皮苷不得少于0.08%。
2.3 水分、灰分和浸出物的测定
参照2015年版《中国药典》(四部)通则水分测定法、灰分测定法、浸出物测定法测定药材样品水分、灰分和浸出物[11],结果见表4。

表4 药材样品水分、灰分和浸出物测定结果(n=3,%)Tab 4 Determination of moisture,ash and extract of samples(n=3,%)
由表4可知,11批竹节蓼药材水分含量为6.39%~9.78%,总灰分含量为2.82%~8.07%,酸不溶性灰分含量为0.02%~0.27%,浸出物含量为14.14%~28.45%。从实际应用的角度考虑,初步拟定本品水分不得过10.00%,总灰分不得过8.50%,酸不溶性灰分不得过0.30%,浸出物含量不少于12.60%。
3 讨论
笔者按本试验色谱条件进样分析,测得槲皮苷色谱峰面积的RSD<2.0%,分离度符合含量测定要求,方法稳定、重复性好,杂质干扰小。经测定,11批药材样品中槲皮苷含量在0.09~0.50%之间,说明不同时间竹节蓼中槲皮苷的含量差异较大,地域的差别及采收时间的不同对其含量影响的规律如何,相关研究将另文报道。
在TLC鉴别中,通过对乙酸丁酯-丙酮-甲醇-甲酸(5∶3∶1∶1,V/V/V/V)、氯仿-丙酮-甲酸-水(6∶3∶1∶1,V/V/V/V)、乙酸丁酯-环己烷-甲酸-水(6∶1.2∶1.8∶0.5,V/ V/V/V)等展开系统进行试验,结果显示,各编号药材样品均可检出槲皮苷,以乙酸丁酯-环己烷-甲酸-水(6∶1.2∶1.8∶0.5,V/V/V/V)为展开系统时,展开效果较好,重现性好,斑点清晰且分离较好,比移值适中,故选用乙酸丁酯-乙酸乙酯-甲酸-水(11∶3∶1.5∶1.5,V/V/V/V)为展开系统;此方法稳定性及重复性好,简便、快速,可作为竹节蓼的定性鉴别方法。
本试验通过广泛收集不同产地样品进行研究,结果具有一定的代表性,能够用于评价竹节蓼药材的质量;本研究所建标准可用于壮药竹节蓼的质量控制。
[1] 国家中医药管理局《中华本草》编写委员会.中华本草:第二册[M].上海:上海科技出版社,1999:636.
[2] 梁启成,钟鸣.中国壮药学[M].南宁:广西民族出版社,2005:172.
[3] 方春生,杨燕军,宋卉,等.竹节蓼不同提取部位体外抗肿瘤活性的研究[J].时珍国医国药,2014,25(12):2865-2868.
[4] 朱学鑫,蒋福升,丁志山.槲皮苷生物活性的研究进展[J].蛇志,2012,24(1):47-50.
[5] 李锦松,陈剑鸿,孟民杰.金丝桃苷药理作用及其作用机制的研究进展[J].广东药学院学报,2015,31(2):269-270.
[6] 李泽友,陈峰,任守忠,等.三白草的化学成分和药理作用研究进展[J].中国药房,2007,18(6):473-474.
[7] 黄华艺,查锡良.黄酮类化合物抗肿瘤作用研究进展[J].中国新药与临床杂志,2002,21(7):428-433.
[8] 杨楠,贾晓斌,张振海,等.黄酮类化合物抗肿瘤活性及机制研究进展[J].中国中药杂志,2015,40(3):373-381.
[9]杨月娥,朱恩焕,胡文,等.HPLC-DAD同时测定鸡肉参中芦丁、槲皮苷、槲皮素的含量[J].中国实验方剂学杂志,2013,19(5):120-122.
[10] 罗世恒,李芙蓉,王西芳,等.HPLC法测定不同采集期、不同产地侧柏叶中杨梅苷和槲皮苷[J].药物分析杂志,2013,33(3):399-403.
[11] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:57、103、202、204.
Study on Quality Standard of Zhuang Medicine Homalocladium platycladum
ZENG Xiangyan,TANG Yurong,YAN Pinghua,LI Li(College of Pharmacy,Guangxi University of TCM,Nanning 530001,China)
R927
A
1001-0408(2017)21-2989-03
2016-08-11
2016-10-10)
(编辑:张 静)
广西壮族自治区重点实验室培育基地项目(No.桂科基字〔2014〕32号);广西“2011协同创新中心”项目(No.桂教科研〔2013〕20号);广西重点学科项目(No.桂教科研〔2013〕16号);广西高校中青年教师基础能力提升项目(No.桂教科研〔2016〕3号);《广西壮药质量标准(第三卷)》质量评价与标准研究项目(No.MZY2015001);广西科学研究与技术开发计划项目(No.桂科重1598005-10);广西中医药大学研究生教育创新计划资助项目(YJS201626)
*硕士研究生。研究方向:中药及民族药品种鉴别与开发利用。E-mail:1471090976@qq.com
#通信作者:讲师,硕士。研究方向:中药及民族药品种鉴定与开发利用。E-mail:lijiayou42@163.com
DOI10.6039/j.issn.1001-0408.2017.21.30
