吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌的疗效观察
2017-08-12罗丹凤洪朝欣
罗丹凤 洪朝欣
吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌的疗效观察
罗丹凤 洪朝欣
目的 探讨吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌的疗效。方法 采用回顾性研究方法。选择蒽环类耐药的晚期乳腺癌患者120例作为研究对象,根据治疗方法的不同分为观察组与对照组,各60例。观察组给予吉西他滨辅助治疗,对照组给予长春瑞滨辅助治疗,21 d为1个化疗周期,2组都治疗3个周期。结果 观察组的有效率为70.0%,对照组的有效率为50.0%,观察组的有效率明显高于对照组(P<0.05)。观察组与对照组白细胞下降、恶心呕吐、黏膜反应等不良反应发生率对比,差异无统计学意义(P>0.05),且对症处理后均明显好转。随访至今,观察组的无进展生存时间和总生存期为(16.39±2.19)个月和(19.44±1.87)个月,都明显长于对照组的(13.22±1.89)个月和(16.98±2.22)个月(P<0.05)。结论 吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌具有较好的安全性,能提高治疗效果,从而延长患者的生存时间,有较高的应用价值。
吉西他滨;蒽环类药物;耐药性;晚期乳腺癌;生存时间
(ThePracticalJournalofCancer,2017,32:1358~1360)
乳腺癌是妇女常见的恶性肿瘤,我国近年来乳腺癌发病率正以每年3%的速度递增,在部分城市已成为发病率最高的恶性肿瘤之一[1-2]。虽然乳腺癌的早期诊治效果比较好,但是由于各种因素的影响,仍然有50%左右患者经手术及辅助化疗、辅助内分泌治疗后会发展成晚期乳腺癌[3-4]。化疗是晚期乳腺癌的主要治疗手段,可减轻临床症状,延长患者生存期[5-6]。早期蒽环类对晚期乳腺癌有较好的疗效,也是首选的化疗方案,但是也有部分患者已对蒽环类药物产生耐药,为此还需要推荐更加有效的治疗方案与药物[7]。吉西他滨为去氧胞苷的衍生物,可在细胞内通过核苷酸激酶作用,催化成有活性的三磷酸双氧胞苷,组织DNA的复制,达到抑制肿瘤细胞生长的作用[8-9]。本文探讨了吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌的疗效,现报告如下。
1 资料与方法
1.1 一般资料
采用回顾性研究方法。2009年8月到2016年4月选择在我院诊治的蒽环类耐药的晚期乳腺癌患者120例作为研究对象。纳入标准:均为女性、经病理确诊为晚期乳腺癌;有客观可测量病灶;所有患者既往均接受过蒽环类药物化疗;研究得到医院伦理委员会的批准;临床与随访资料完整,患者知情同意。排除标准:妊娠与哺乳期妇女;临床与随访资料缺失。根据治疗方法的不同分为观察组与对照组,各60例。2组患者的年龄、体重指数、KPS评分、转移病灶数目、病理类型等对比无明显差异(P>0.05)。见表1。

表1 2组一般资料对比
1.2 治疗方法
观察组:给予吉西他滨辅助治疗,选择吉西他滨1 000 mg/m2,静脉滴入,d1、d8;顺铂75 mg/m2,静脉滴入,d1~3。21 d为1个化疗周期。
对照组:给予长春瑞滨辅助治疗,选择长春瑞滨30 mg/m2,静脉滴入d1、d8;顺铂75 mg/m2,静脉滴入,d1~3天。21 d为1个化疗周期。
2组都治疗观察3个周期。
1.3 观察指标
疗效根据WHO实体瘤客观疗效评价标准进行判定,完全缓解(CR):所有可见病变完全消失并至少维持4周以上;部分缓解(PR):肿瘤病灶的最大两径乘积减少≥50%,维持4周以上;疾病稳定(SD):肿瘤病灶两径乘积缩小<50%,或增大<25%,无新病灶出现;疾病进展(PD):肿瘤病灶两径乘积增大≥25%,或出现新病灶。(CR+PR)/总例数×100.0%=总有效率。
不良反应按WHO抗癌药物常见不良反应分级标准进行评价,根据临床观察和实验室指标进行全面评价,主要为白细胞下降、恶心呕吐、黏膜反应等。所有患者都进行随访,记录2组的无进展生存时间和总生存期。
1.4 统计方法
全部病例观察完成后采用SPSS20.00软件进行分析,计量数据采用均数±标准差表示,计数数据采用百分比表示,对比采用配对t检验、卡方分析等,P<0.05代表差异有统计学意义。
2 结果
2.1 疗效对比
治疗后经过疗效评价,观察组的有效率为70.0%,对照组的有效率为50.0%,观察组的有效率明显高于对照组(χ2=5.511,P<0.05)。见表2。

表2 2组有效率对比/例
2.2 不良反应对比
经过观察,观察组与对照组白细胞下降、恶心呕吐、黏膜反应等不良反应发生率对比,差异无统计学意义(P>0.05),且经对症处理后明显好转。见表3。
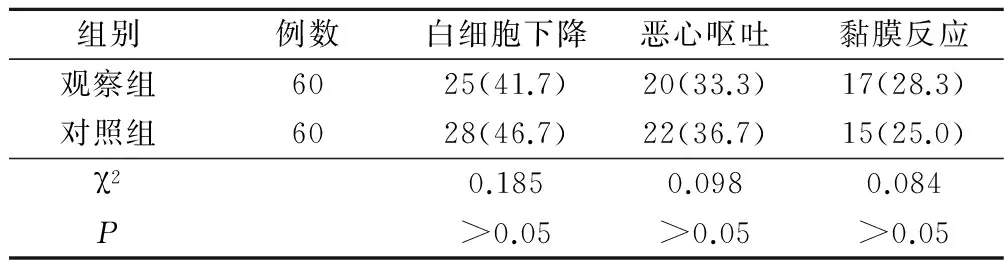
表3 2组不良反应对比(例,%)
2.3 无进展生存时间和总生存期对比
随访至今,观察组的无进展生存时间和总生存期为(16.39±2.19)个月和(19.44±1.87)个月,都明显长于对照组的(13.22±1.89)个月和(16.98±2.22)个月,差异均有统计学意义(t=3.782、4.114,P均<0.05)。
3 讨论
乳腺癌是女性常见的恶性肿瘤,其发病率逐年升高,其中绝经期后发病率呈现明显上升趋势,到60岁可达最高峰,严重威胁到妇女的健康[10]。随着诊疗技术的发展,乳腺癌的预后有了明显进步,早期乳腺癌经过手术治疗、术后放疗、化疗等,90%的早期乳腺癌患者可以获得长期生存。而晚期乳腺癌由于伴发多脏器转移,治疗效果较差,对于治疗的要求也比较高[11]。
蒽环类、紫杉类、烷化剂、抗代谢药为晚期乳腺癌最常使用的化疗药物,但是随着药物的广泛使用,患者的耐药率越来越高[12]。内分泌治疗是晚期乳腺癌患者不可或缺的治疗手段,其疗效明确,应用方便。长春瑞滨为半合成的第四代长春碱类衍生物,可特异性作用于细胞有丝分裂的微管,使肿瘤细胞的分裂增殖停止于有丝分裂中期,从而抑制肿瘤细胞增长,起到抗肿瘤作用[13-14]。吉西他滨和长春瑞滨是2个作用靶点不同,抗瘤谱广,可选择性地抑制DNA拓扑异构酶,继而抑制DNA的合成,影响细胞分裂周期,导致细胞死亡[15]。本研究显示治疗后经过疗效评价,观察组的有效率为70.0%,对照组的有效率为50.0%,观察组的有效率明显高于对照组(P<0.05),也说明吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌能提高治疗效果。
目前乳腺癌的化疗最有效的药物是蒽环类和(或)紫杉类为主的化疗方案,但是大部分患者在术后辅助或者一线方案中已经使用过蒽环类药物,为此寻找更加有效的晚期乳腺癌治疗方案成为临床急需解决的问题[16-17]。靶向治疗是除化疗外对乳腺癌最有前景的治疗方法,很多新的治疗靶点也相继被发现。抗代谢类药物吉西他滨和破坏DNA双链结构的铂类药物的联合使用能够直接破坏DNA双链间的碱基,进而阻碍DNA复制;也可通过发挥细胞毒作用,从而抑制DNA的合成并导致细胞死亡。并且吉西他滨对神经轴突微管影响较小,神经毒性较其他长春碱类药物明显减少[18-19]。本研究显示观察组与对照组白细胞下降、恶心呕吐、黏膜反应等不良反应发生率对比差异无统计学意义(P>0.05),且都对症处理后明显好转,也表明吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌也具有很好的安全性。
晚期乳腺癌具有增殖快、侵袭能力强,恶性程度高,远处及内脏转移率较高,临床预后较差等特点[20]。研究显示吉西他滨单药在晚期乳腺癌有较好的疗效,对蒽环类耐药的晚期转移性乳腺癌也有较好疗效[21-22]。本研究显示观察组的无进展生存时间和总生存期为(16.39±2.19)个月和(19.44±1.87)个月,都明显长于对照组的(13.22±1.89)个月和(16.98±2.22)个月(P<0.05),也说明吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌能延长患者的生存时间。
总之,吉西他滨辅助治疗蒽环类耐药的晚期乳腺癌具有很好的安全性,能提高治疗效果,从而延长患者的生存时间,有很高的应用价值。
[1] 张艳芳,牛春莲,张春珍,等.吉西他滨联合紫杉醇周方案治疗蒽环类耐药的晚期乳腺癌疗效观察〔J〕.中国实用医刊,2016,43(13):51-53.
[2] Ouyang L,Chang W,Fang B,et al.Estrogen-induced SDF-1α production promotes the progression of ER-negative breast cancer via the accumulation of MDSCs in the tumor microenvironment〔J〕.Sci Rep,2016,20(6):541-548.
[3] Tolcher AW,Bendell JC,Patnaik A,et al.A phase Ⅰb study of the MEK inhibitor GSK1120212 combined with gemcitabine in patients with solid tumors:Interim results〔J〕.J Clin Oncol,2011,29(4_suppl):278-284.
[4] 肖雄升,谢洪泼,张远起,等.奥沙利铂联合卡培他滨对蒽环类或紫杉醇耐药性晚期乳腺癌的治疗效果〔J〕.实用医药杂志,2016,33(8):692-694.
[5] 李书平,张阿桥.吉西他滨联合顺铂治疗蒽环类及紫杉类耐药性晚期乳腺癌疗效分析〔J〕.航空航天医学杂志,2016,27(1):17-18.
[6] Maemura K,Mataki Y,Kurahara H,et al.Gemcitabine and S-1 induction chemotherapy followed by chemoradiotherapy for locally advanced pancreatic cancers〔J〕.Anticancer Res,2017,37(1):233-237.
[7] Deflin M,Parthan A,Taylor D,et al.Comparison of the clinical benefit of an adjuvant therapy in gastrointestinal stromal tumors(GIST) with other adjuvant cancer therapies〔J〕.J Clin Oncol,2012,30(4_suppl):129-134.
[8] 田新庆,王文珍,王小娜.吉西他滨联合顺铂治疗三阴性晚期乳腺癌的疗效观察〔J〕.肿瘤研究与临床,2015,27(1):57-59.
[9] Awasthi N,Ostapoff K,Zhang C,et al.Evaluation of combination treatment benefits of nab-paclitaxel in experimental pancreatic cancer〔J〕.J Clin Oncol,2012,30(4_suppl):170-177.
[10] 詹 颖,童远和,陈志勇,等.吉西他滨联合顺铂与多西他赛联合顺铂在晚期三阴乳腺癌化疗中的对比研究〔J〕.中国现代医生,2016,54(17):67-69,74.
[11] 马守成,乔 慧,杨天宁,等.沙利度胺联合GP方案治疗晚期乳腺癌的疗效分析〔J〕.肿瘤学杂志,2016,22(6):518-520.
[12] Kropp L,Siegal GP,Frampton GM,et al.Primary intraosseous smooth muscle tumor of uncertain malignant potential:Original report and molecular characterization〔J〕.Rare Tumors,2016,8(4):6507-6512.
[13] Le Fournis S,Gohier P,Urban T,et al.Corneal graft rejection in a patient treated with nivolumab for primary lung cancer〔J〕.Lung Cancer,2016,102(2):28-29.
[14] 柏 方,陈 青,吴克瑾,等.GP方案与NP方案治疗晚期乳腺癌疗效的Meta分析〔J〕.肿瘤学杂志,2016,22(4):259-264.
[15] 刘 君,肖 扬,郭建雄,等.奥沙利铂联合替吉奥和吉西他滨联合顺铂治疗晚期三阴性乳腺癌的疗效和不良反应比较〔J〕.肿瘤防治研究,2016,43(1):72-77.
[16] 吕红琼,谢 玲,倪明立,等.吉西他滨联合卡培他滨治疗复发转移乳腺癌的疗效观察〔J〕.中国癌症防治杂志,2016,8(4):249-251.
[17] Farr SE,Chess-Williams R,McDermott CM.Gemcitabine:Selective cytotoxicity,induction of inflammation and effects on urothelial function〔J〕.Toxicol Appl Pharmacol,2016,19(2):1-9.
[18] 林秀欣,周 颖,余更生,等.吉西他滨联合奈达铂治疗紫杉类耐药的三阴乳腺癌疗效观察〔J〕.中国药物评价,2016,33(3):150-152.
[19] Hong S,Zhang L.Gemcitabine improves survival in patients with recurrent or metastatic nasopharyngeal carcinoma〔J〕.Chin J Cancer,2016,35(1):100-109.
[20] 常桂花.多西他赛联合吉西他滨治疗复发转移乳腺癌临床疗效观察〔J〕.中国医师杂志,2016,18(6):908-909.
[21] Maemura K,Mataki Y,Kurahara H,et al.Gemcitabine and S-1 induction chemotherapy followed by chemoradiotherapy for locally advanced pancreatic cancers〔J〕.Anticancer Res,2017,37(1):233-237.
[22] 王俊斌,杨 燕,汪子书,等.长春瑞滨或吉西他滨联合顺铂治疗转移性三阴性乳腺癌的临床疗效与安全性评价〔J〕.中国临床药理学杂志,2016,32(1):24-26.
(编辑:甘 艳)
Efficacy of Gemcitabine Adjuvant Therapy for Anthracycline Resistant AdvancedBreast Cancer
LUO Danfeng,HONG Chaoxin.
The 180th Hospital of PLA,Quanzhou,362000
Objective To investigate the efficacy of gemcitabine adjuvant therapy for anthracycline resistant advanced breast cancer.Methods A retrospective study was conducted,120 advanced breast cancer patients with anthracycline drug resistance were selected as the research object,all the patients were divided into the observation group and the control group,with 60 patients in each group according to the different treatment methods,the observation group was given adjuvant gemcitabine treatment,the control group was given vinorelbine adjuvant therapy,21 d for 1 cycle,the 2 groups were observed for 3 cycles of treatment.Results The effective rates of the observation group was 70.0%,the effective rate of the control group was 50.0%,and the effective rate of the observation group was significantly higher than that of the control group(P<0.05).There were no significant difference between the 2 groups in the incidence of leukopenia,nausea and vomiting,mucosal reaction and other adverse reactions(P>0.05),and all the adverse reactions after symptomatic treatment significantly improved.Up to now,the progression free survival and overall survival in the observation group were(16.39±2.19) months and(19.44±1.87) months,which were significantly longer than those of the control group of(13.22±1.89) months and(16.98±2.22) months(P<0.05).Conclusion Gemcitabine adjuvant therapy for anthracycline resistant advanced breast cancer has good safety,it can improve the therapeutic effect,prolong the survival time of patients,and it has high application value.
Gemcitabine;Anthracycline;Drug resistance;Advanced breast cancer;Survival time
362000 解放军第180医院
10.3969/j.issn.1001-5930.2017.08.041
R737.9
A
1001-5930(2017)08-1358-03
2017-02-22
2017-04-20)
