培美曲赛联合铂类密集化疗治疗肺腺癌的疗效观察
2017-08-12杨庚武张午临
杨庚武 张午临 李 静 刘 峥
培美曲赛联合铂类密集化疗治疗肺腺癌的疗效观察
杨庚武 张午临 李 静 刘 峥
目的 分析培美曲赛联合铂类密集化疗治疗肺腺癌疗效和不良反应。方法 60例经病理检查确诊的晚期肺腺癌患者,分别接受培美曲赛联合奈达铂非密集化疗(对照组28例)和培美曲赛联合奈达铂密集化疗(实验组32例),观察两组近期疗效和不良反应并进行比较分析。结果 纳入的60例患者中,对照组28例,总有效率ORR为14.3%,疾病控制率DCR为57.2%;实验组32例,总有效率ORR为25.0%,疾病控制率DCR为78.1%;不良反应实验组与对照组相比有差异(P<0.05),有统计学意义;实验组患者治疗后2年累积死亡率明显低于对照组患者(χ2=4.63,P=0.032<0.05),且差异有统计学意义。结论 培美曲赛联合铂类密集化疗治疗肺腺癌疗效相对较好,不良反应相对低,值得临床应用。
培美曲赛;铂类密集化疗;肺腺癌
(ThePracticalJournalofCancer,2017,32:1298~1300)
肺腺癌是肺癌的1种,属于非小细胞癌(NSCLC)。肺腺癌已经取代鳞癌成为最常见的组织学类型[1]。现将2013年1月至2016年1月共60例经病理确诊的晚期肺腺癌患者,分别接受培美曲赛和培美曲赛联合铂类密集化疗治疗分析报告如下。
1 资料与方法
1.1 研究对象
2013年1月至2016年1月共60例经病理检查确诊的晚期肺腺癌患者,分别接受培美曲赛联合奈达铂非密集化疗(对照组28例)和培美曲赛联合铂类密集化疗(实验组32例)。对照组男性12例,女性16例,平均年龄(65±10.3)岁,ECOG PS 评分 0~1 分 20例,2 分 8 例;吸烟者 10 例,不吸烟者 18 例;临床分期 Ⅲb期3 例,Ⅳ 期25例;实验组男性13例,女性19例,平均年龄(64±11.2)岁,ECOG PS 评分 0~1 分 20例,2 分 12例;吸烟者 10 例,不吸烟者 22例;临床分期 Ⅲb期5例,Ⅳ 期27例;对照组和实验组的一般临床资料,差异均不明显,统计学没有意义(P>0.05),具有可比性。
1.2 纳入标准以及排除标准[2-4]
纳入标准:①符合病理确诊肺腺癌疾病诊断标准;②PS评分为0分~2分,重要脏器功能可耐受化疗;③中性粒细胞>1.5×109/L 、白细胞>3.0×109/L 、血小板>6×1010/L,红细胞>2×1012/L且血红蛋白不得低于8.0 g/dl的肺腺癌患者;④实验室指标未超过正常值的2倍,且肝、肾功能正常或者没有感染、发热,出血倾向者和严重并发症;⑤既往未接受过培美曲赛化疗;⑥告知家属及患者并签署知情同意书。排除标准:①对培美曲赛或铂类药不耐受以及过敏者;②感染严重、出血倾向未能控制者;③心、肝、肾脏功能严重损坏者。
1.3 方法
对照组采用曲赛联合奈达铂非密集化疗:给予培美曲赛(江苏扬子江药业)500 mg/m2,奈达铂(南京先声药业)80 mg/m2,第1天;实验组采用培美曲塞联合铂类化疗治疗:患者在治疗前7天口服叶酸 400 μg/d,持续到治疗结束;用药前 7天给予肌肉注射维生素B121 000 μg/次;用药3天(前天、当天和后天)口服地塞米松 4.5 mg/次,每天 2 次。培美曲塞:250 mg/m2;奈达铂:40 mg/m2;连续3周后停一周,化疗中给予常规预防性止吐及必要处理。
1.4 疗效评定
治疗14天后评价疗效。化疗3~10个周期,其中位周期为 6个周期。采用1999 年实体瘤疗效评价标准(RECIST)作为依据,将其分为4大类,完全缓解(complete response,CR):肿瘤完全消失且维持4周以上;部分缓解(partial response,PR):肿瘤最大径总和缩小30%以上,并且维持4周以上;疾病稳定(stable disease,SD):肿瘤最大径总和缩小在30%以下或增加但未出现新病灶;进展(progres-sive disease,PD);肿瘤最大径总和超过20%,或者出现新的病灶。其中总有效率(ORR)=(CR+PR)/总例数×100%,疾病控制率(DCR)为(CR+PR+SD)。随访截至 2016 年1月31日,随访24个月,观察患者的不良反应及生存情况。
1.5 统计学方法
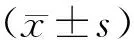
2 结果
2.1 疗效评价
共60例纳入最后疗效分析,其中对照组28例,实验组32例。每例患者至少完成2个周期全身化疗,中位化疗周期为4个。可评价疗效的60例患者中,对照组:无CR,PR 4例(14.3% ),SD 12例(42.9%),PD 12例(42.9%),ORR为14.3%,DCR为57.2%;实验组:无CR,PR 8例(25% ),SD 17例(53.1%),PD 7例(21.9%),ORR为25.0%,DCR为78.1%,见表1。
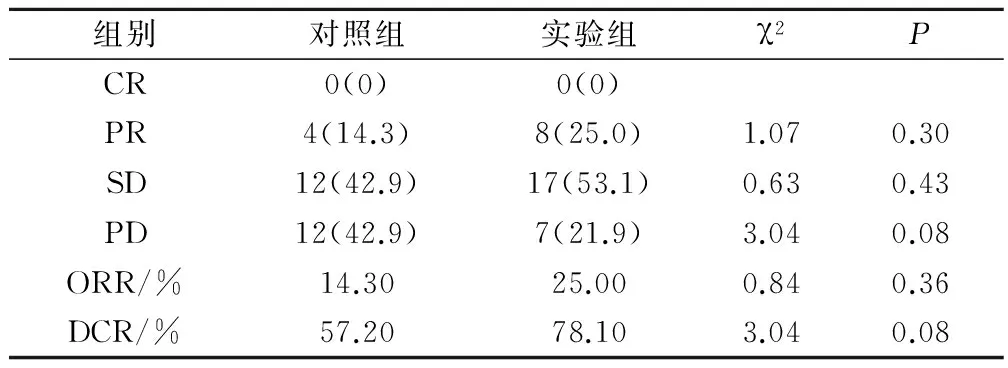
表1 76例肺腺癌患者的近期疗效(例,%)
2.2 不良反应
不良反应主要为肝肾损害和胃肠道反应,对照组不良反应总发生率为60.7%(17/28),实验组为21.9%(7/32)。两组相比,对照组略高于实验组,且差异有统计学意义(P<0.05),见表2。

表2 76例肺腺癌患者的不良反应比较/例
2.3 两组患者治疗后2年累积死亡率的比较
实验组32例患者中有4例死亡,对照组28例患者中有9例死亡。经统计学分析,实验组患者治疗后2年累积死亡率明显低于对照组(12.5%,4/32 vs 32.1%,9/28;χ2=4.63,P=0.032<0.05),见图1。
3 讨论
肺腺癌作为肺癌的1种,在肺癌的比例中高居首位,在女性及不抽烟者容易出现 。早期临床症状特殊性不高,仅出现呼吸系统疾病共有的一些症状:低热、咳嗽、痰血、胸闷、胸痛等,比较容易被忽略[5-6]。治疗原则采取综合治疗方法:依据患者的总体状况分析,病理学、肿瘤的细胞学、侵及范围、临床分期和发展趋向等,采取综合治疗(MDT )模式涉及多个学科,有步骤、有目的、合理地应用手术、化疗、放疗和生物靶向等治疗手段[7],使得患者达到完全缓解或者部分缓解,达到治愈的目的,从而提高其生活质量,延长患者生存期。临床上对肺癌的治疗仍然以手术治疗、药物治疗和放射治疗为主。相比于其他类型的肺癌,肺腺癌的预后相对要好[8-9]。具体情况和临床分期有关。晚期乳腺癌化疗主要采用蒽环类、紫杉类药物等一线及卡培他滨、 吉西他滨等二、 三线的标准治疗方案。而培美曲塞被 FDA 批准为恶性胸膜间皮瘤(无法手术) 的一线治疗药物以及局部晚期肺癌或转移性非小细胞肺癌的二线药物。大量研究显示,在肺癌、乳腺癌、胃癌、头颈部癌、结肠癌等治疗中培美曲塞均取得较好疗效[10]。

图1 两组患者2年累积复发率比较
培美曲塞是1种新型多靶点抗叶酸制剂,一方面抑制胸甘酸合成酶,另一方面抑制叶酸依赖性酶(二氢叶酸还原酶和甘氨酸核糖核甘甲酰基转移酶等),进而干扰胸腺嘧啶核苷和嘌呤核苷的生物合成,阻止肿瘤细胞DNA和RNA的合成,最终实现抗肿瘤的目的。王丽等[2]结果显示培美曲塞联合铂类一线治疗晚期肺腺癌疗效中,培美曲塞联合顺铂或卡铂疗效较好,安全性高无完全缓解病例,部分缓解27例,稳定21例,进展14例,总有效率为43.5%,疾病控制率为77.4%。所有患者无进展生存期5.7个月。陈艳等[11]对培美曲塞联合铂类治疗晚期乳腺癌研究中,培美曲赛+顺铂与培美曲赛+奥沙利铂的疗效和不良反应相当,疗效较好,不良反应较轻。
本研究为回顾性分析,通过对既往的研究比较发现联合铂类密集化疗治疗肺腺癌疗效相对较好,本文研究两组一般资料因素不足以对两组比较产生明显影响,差异均不具有统计学意义(P>0.05)。纳入的60例病人中,对照组28例,总有效率ORR为14.3%,疾病控制率DCR为57.2%;实验组32例,总有效率ORR为25.0%,疾病控制率DCR为78.1%;不良反应实验组与对照组相比出现差异(P<0.05),有统计学意义;实验组患者治疗后2年累积死亡率明显低于对照组患者(12.5%,4/32 vs 32.1%,9/28;Log-rank χ2=4.63,P=0.032<0.05),且差异有统计学意义。
综上所述,培美曲赛联合铂类密集化疗治疗肺腺癌疗效相对于对照组相对近期疗效较好,毒性反应相对低,值得临床进一步应用和观察。
[1] 朱雄增,张 杰.肺腺癌iaslc/atS/erS国际多学科分类解读〔J〕.临床与实验病理学杂志,2012,28(3):241-243.
[2] 王 丽,史美祺.培美曲塞联合铂类一线治疗晚期肺腺癌疗效〔J〕.江苏医药,2012,38(11):1290-1292.
[3] 邱 冬,李 杭,姜桂林,等.培美曲塞联合铂类治疗晚期非小细胞肺癌的临床疗效及安全性观察〔J〕.山东医药,2013,53(33):40-42.
[4] 陈文怡,王韡旻,姜丽岩,等.培美曲塞联合铂类一线治疗晚期非鳞非小细胞肺癌的临床观察〔J〕.中国癌症杂志,2014,24(8):610-614.
[5] 刘 伟.肺腺癌2011年国际新分类〔J〕.实用癌症杂志,2012,27(4):432-434.
[6] 樊英瑞,王朝霞,陆彬彬,等.培美曲塞联合铂类二线及以上治疗晚期非小细胞肺癌的临床观察〔J〕.中国医药科学,2012,2(19):42-43,56.
[7] 刘小红,万林林,丁 伟,等.培美曲塞联合铂类药治疗晚期复发性肺癌的临床疗效观察〔J〕.现代中西医结合杂志,2013,22(18):1995-1997.
[8] 黄 芳,姜 达,李 颖,等.晚期肺腺癌化疗方案的优化〔J〕.肿瘤防治研究,2015,42(7):687-692.
[9] 赵文华,宋向群,于起涛,等.培美曲塞及吉西他滨联合铂类一线治疗有吸烟史的晚期非小细胞肺癌患者的疗效观察〔J〕.广西医科大学学报,2014,31(4):601-603.
[10] 赵大海,陆友金.抑制自噬促进培美曲塞对A549细胞的增殖抑制作用〔J〕.中国药理学通报,2015,31(5):664-668.
[11] 陈 艳,陈 平,陈苏蓉,等.培美曲塞联合铂类治疗晚期乳腺癌的疗效〔J〕.中国肿瘤临床与康复,2016,23(6):698-701.
(编辑:吴小红)
Clinical Observation of Pemetrexed Combined with Platinum Intensive Chemotherapy for Lung Adenocarcinoma
YANG Gengwu,ZHANG Wulin,LI Jing,et al.
Handan Central Hospital,Handan,056000
Objective To analyze the efficacy and toxicity of pemetrexed combined with platinum intensive chemotherapy for lung adenocarcinoma.Methods A retrospective analysis of 60 cases of advanced lung adenocarcinoma confirmed by pathology were conducted,they were treated with pemetrexed combined with nedaplatin non-intensive chemotherapy(control group 28 cases) and pemetrexed combined with nedaplatin intensive chemotherapy(experimental group 32 cases),curative effect and toxicity of the 2 groups were observed and compared.Results A total of 60 patients were enrolled in clinical evaluation:the control group had 28 cases,the total efficiency was 14.3%,the disease control rate was 57.2%;the experimental group had 32 cases,the total efficiency was 25%,the disease control rate was 78.1%;the adverse reaction of the 2 groups had significant difference(P<0.05),there was statistical significance;2-year cumulative mortality in the experimental group after treatment was significantly lower than the control group(4/32 12.5%,vs 32.1%,9/28;Log-rank χ2=4.63,P=0.032<0.05),and the difference was statistically significant.Conclusion The curative effect of pemetrexed combined with platinum intensive chemotherapy for lung adenocarcinoma is relatively good,and the toxicity is relatively low,it is worthy of clinical application.
Pemetrexed;Platinum intensive chemotherapy;Lung adenocarcinoma
邯郸市科技局研究项目(编号:1423108108)
056000 邯郸市中心医院
10.3969/j.issn.1001-5930.2017.08.023
R734.2
A
1001-5930(2017)08-1298-03
2017-03-24
2017-05-02)
