蒸汽灭菌过程挑战装置有效性验证综述
2017-08-10龚琬玲邱纬宇广东省医疗器械质量监督检验所广东广州510663
龚琬玲 邱纬宇 广东省医疗器械质量监督检验所 (广东 广州 510663)
蒸汽灭菌过程挑战装置有效性验证综述
龚琬玲 邱纬宇 广东省医疗器械质量监督检验所 (广东 广州 510663)
过程挑战装置(PCD)广泛应用于灭菌过程有效性的评价中,当PCD被用来评价特定的灭菌过程的有效性时,应对其本身的可靠性进行验证。本文主要介绍了国内外对蒸汽灭菌过程挑战装置有效性验证的研究现状,简述国内相关标准的内容。
过程挑战装置 蒸汽灭菌
医院感染是当今国内外医学界普遍重视的一个问题,已成为感染性疾病领域的一个具有挑战性的难题。医院消毒工作质量直接影响到医院感染控制的水平,尤其是出现多起与医疗感染的事故后,国家相关部门对医疗感控的重视程度明显提高。为提高医院感染控制管理水平,做好消毒灭菌的过程确认和监测工作是必不可少的。不同的国家和国际质量体系标准中,灭菌是一个“特殊”过程的代表,然而灭菌过程的有效性不能通过对产品的检查和测试来确认,只能够通过间接的方法来对灭菌过程进行监测。近年来,得到广泛认可的方法是采用灭菌过程挑战装置(PCD)进行监测,本文结合国内外现状,综述验证过程挑战装置(PCD)有效性的方法。
1.过程挑战装置(PCD)
过程挑战装置(PCD)是对灭菌过程有预定抗力的模拟装置,由测试装置及检测器(生物或化学指示物,或物理测量系统)组成,用于评价灭菌过程的有效性[1]。当PCD被用来评价特定的灭菌过程的有效性时,应对其本身的可靠性进行验证[2]。
2.国内外研究现状
在管腔类医疗器械普遍使用前,最常用的过程挑战装置是B-D试验标准包,B-D试验标准包专门用于预真空(包括脉冲)压力蒸汽灭菌器空气排除效果的检测。但是随着医疗技术的不断发展,医疗领域出现了许多管腔类器械,如内镜和微创外科器械等结构复杂的管腔器械。经大量试验证明,管腔器械比标准的测试布包更难实现灭菌,即使某个灭菌过程能够通过B-D试验,也并不一定能将管腔器械灭菌,因此出现了一种新的过程挑战装置——管腔型PCD。管腔型PCD在国外已被应用于压力蒸汽灭菌过程的验证。
PCD的结构和外观形式可能多种多样,但其构成基本一致,包括3个部分:1、对灭菌介质的穿透具有一定抵抗力的部分;2、能够装载生物或化学指示物的舱;3、内部的生物或化学指示物[3]。PCD根据包裹类型可分为两类:一种是敷料型PCD,另一种是管腔型PCD。敷料型PCD分为标准包和测试包两种,管腔型的PCD有紧凑型PCD和螺旋型PCD两种。根据PCD中放置的指示物分类可分为生物PCD、化学PCD及生物和化学混合PCD[2],如图1所示:
目前欧洲大部分国家都有相关标准对PCD进行了详细规定,如EN285、EN867-4和EN867-5等对蒸汽灭菌过程监测的PCD提出明确要求。欧洲大部分国家倾向于按照灭菌物品的不同难度采用不同的过程挑战装置进行监测,在过程挑战装置的选择和设计过程时,灭菌难度必须要经过测试保证比所监测的物品更难灭菌。而美国传统上采用标准的过程挑战装置,即不管灭菌物品复杂程度如何,所使用的过程挑战装置只有一个,这一点并不太科学,因此目前美国也逐渐向欧洲标准靠拢,例如ANSI/AAMI/ ISO17665-1标准中强调过程挑战装置的灭菌难度必须要经过测试保证比所监测的物品更难灭菌。德国标准DIN58921对PCD适用性验证提供了明确的方法。

图1. 常见过程挑战装置
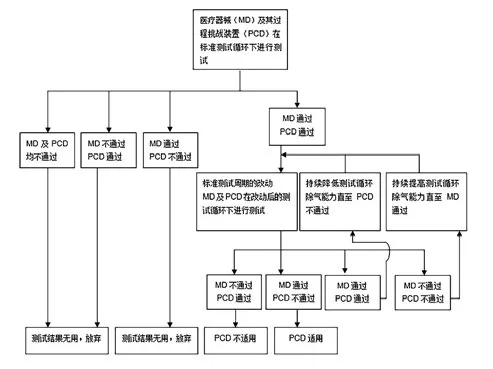
图2. 试验原理图[4]
国内相关卫生部门和国内灭菌器、医疗保健产品制造商等大多采用国外的生产商提供的过程挑战装置,本身对过程挑战装置的研究并不多。国家食品药品监督管理总局于2016年发布了一份过程挑战装置有效性验证相关的行业标准,即YY/T 1402-2016《医疗器械蒸汽灭菌过程挑战装置适用性的测试方法》[4]。
3.YY/T 1402-2016标准简述
YY/T 1402-2016标准规定了证实过程挑战装置在除气及蒸汽渗透方面比其模拟的医疗器械更难达到灭菌条件的测试方法[4]。该标准中描述的测试过程,主要通过在标准测试周期的基础上降低灭菌器除气能力,逐步降低灭菌器的灭菌能力,从而实现验证过程挑战装置有效性的目的,试验原理如图2所示。
医疗器械(MD)及其过程挑战装置(PCD)首先在标准测试周期下进行“通过-测试”的测试过程,当MD及PCD均通过该测试时(例如生物指示物培养呈阴性或化学指示物变色完全),可进行下一步“失败-测试”的测试。
“失败-测试”的测试过程主要通过修改标准测试周期中的灭菌器除气能力(如:预真空阶段的预设真空压力值),使灭菌器的灭菌能力逐步降低,直至出现MD通过测试而PCD不能通过测试的试验结果,此时说明该PCD有效(即比其模拟的MD更难灭菌)。
4.小结
综上所述,通过改变灭菌过程中的主要参数(如:真空度、维持时间、灭菌温度等),不断提高灭菌难度直至过程挑战装置(PCD)无法达到预期灭菌效果而被模拟的医疗器械可达到预期灭菌效果的方法是目前验证过程挑战装置(PCD)有效性较为可行实用的方法。
[1] ISO 17665-1:2006.Sterilization of health care products -Moist heat -Part 1:Requirements for the development,validation and routine control of a sterilization process for medical devices.
[2] 曹原,张流波.压力蒸汽灭菌过程验证装置(PCD)的进展[J].中国护理管理,2008,8(5):34-37.
[3] 钱英杰.灭菌过程挑战装置简介[J].中国护理管理,2008,8(1):69-71.
[4] YY/T1402-2016医疗器械蒸汽灭菌过程挑战装置适用性的测试方法[S].国家食品药品监督管理总局,2016.
Summary of the Verifcation of the Effectiveness of PCDs Used in the Steam Sterilization Process
GONG Wan-ling QIU Wei-yu Guang dong Medical Devices Quality Surveillance and Test Institute (Guang dong Guangzhou 510663)
The process challenge device (PCD) is widely used in the evaluation of the effectiveness of the sterilization process. When PCD is used to evaluate the effectiveness of a particular sterilization process, its reliability should be verifed. This paper mainly introduces the research status of the verifcation of the effectiveness of PCDs used in the steam sterilization process at home and abroad, and briefy describes the contents of the relevant domestic standards.
process challenge device, steam sterilization
1006-6586(2017)12-0019-02
R-1
A
2017-03-10
