β-1,3-葡聚糖酶的结构与催化性质研究进展
2017-08-09大连理工大学生命科学与技术学院辽宁大连116024
王 瑞,杨 君,杨 青(大连理工大学生命科学与技术学院,辽宁大连 116024)
β-1,3-葡聚糖酶的结构与催化性质研究进展
王 瑞,杨 君*,杨 青
(大连理工大学生命科学与技术学院,辽宁大连 116024)
β-1,3-葡聚糖酶广泛存在于细菌、真菌、植物和无脊椎动物中,因来源的差异,β-1,3葡聚糖酶的生理功能多样,如参与植物生长发育、提高或诱导抗病性、提供菌体营养、调节真菌细胞壁稳定性和刚性、参与病毒释放和入侵等。酶的结构研究是探索酶催化反应机理、挖掘酶催化特性以及酶理性设计改造的基础。本文对晶体结构研究最充分的GH16家族细菌β-1,3-葡聚糖酶的结构特征及催化机理进行综述,并通过与GH17家族植物来源β-1,3-葡聚糖酶的结构比较,揭示细菌β-1,3-葡聚糖酶的作用机制,为进一步改造和利用该酶,实现其在植物保护、食品和制药等领域的应用提供重要参考。
β-1,3-葡聚糖酶,晶体结构,催化机制,底物特异性
β-1,3-葡聚糖酶是一类能够水解以β-1,3-糖苷键连接的葡聚糖的酶系,广泛存在于细菌、真菌、植物和无脊椎动物中。自发现自然界生物体内存在β-1,3-葡聚糖酶以来,人们长期不懈地对其进行研究,研究内容涵盖β-1,3-葡聚糖酶的分离纯化、生理生化特性、在生物体内的作用、编码β-1,3-葡聚糖酶的基因等。目前,对β-1,3-葡聚糖酶的应用研究多集中于工业废料的综合利用、精益啤酒和葡萄酒酿造工程中酒的过滤工艺且抑制潜在真菌的污染[1]、饲料添加剂[2-3]、活性多糖的改性增溶[4-5]、果蔬的绿色保鲜[6]、植物病害防治[7]与真菌细胞壁结构分析[8]等。
目前为止,CAZY数据库共收集8个来源于细菌和4个来源于植物的β-1,3-葡聚糖酶晶体结构(http://www.cazy.org/)。这两个来源不同的酶能够催化相同的底物,但二者无论在氨基酸序列上还是在三维空间结构上都没有相似性。植物β-1,3-葡聚糖酶属于糖苷水解酶17家族,拥有一个(β/a)8桶状结构,而细菌β-1,3-葡聚糖酶属于糖苷水解酶16家族,其三级结构为典型的“β-jelly-roll”结构,表面形成凹槽结构,易于和底物结合。此外,由于大部分细菌本身不含有β-1,3-葡聚糖,β-1,3-葡聚糖酶的主要功能是分解周围环境中的葡聚糖,起到营养作用[9],因而细菌β-1,3-葡聚糖酶可能具有更为广泛的底物谱。因此,本文对GH16家族细菌β-1,3-葡聚糖酶的结构特征及催化机理进行综述,并通过与GH17家族植物来源β-1,3-葡聚糖酶的结构比较,理解细菌β-1,3-葡聚糖酶的作用机制,为进一步改造和利用该酶,实现其在食品、制药和植保等领域的应用提供重要参考。
1 细菌β-1,3-葡聚糖酶的结构特征和水解机制
1.1 细菌β-1,3-葡聚糖酶的序列特征
目前,人们已经分离得到了许多细菌β-1,3-葡聚糖酶,这些物种包括环状芽孢杆菌(Bacilluscirculans)[10]、解淀粉芽孢杆菌(Bacillusamyloliquefaciens)[11]、类芽孢杆菌(Paenibacillussp.)[12]、盐屋链霉菌(Streptomycessioyaensis)[13]以及诺卡土壤菌F96(Nocardiopsissp. F96)[14]等。以海栖热袍菌MSB8(ThermotogamaritimaMSB8)β-1,3-葡聚糖酶催化域的结构(3AZX)[15]为模板,利用MEGA5.1与来源于嗜碱性的诺卡土壤菌F96(alkaliphilicNocardiopsissp. strain F96)的内切β-1,3-葡聚糖酶(2HYK)[16]、来源于嗜热古细菌(Pyrococcusfuriosus)的内切β-1,3-葡聚糖酶(2VY0)、来源于盐屋链霉菌(Streptomycessioyaensis)的内切β-1,3-葡聚糖酶(3DGT)[13]、来源于海洋红嗜热盐菌(Rhodothermusmarinus)的β-1,3-葡聚糖酶(3ILN)、来源于结合分支杆菌(Mycobacteriumtuberculosis)的β-1,3-葡聚糖酶(4WZF)[17]、来源于海洋细菌Zobelliagalactanivorans的β-1,3-葡聚糖酶ZgLamA(4BOW)[18]和ZgLamC(4CRQ)[19]以及来源于热袍菌Thermotogapetrophila的内切β-1,3-葡聚糖酶(4DFS)[20]进行序列比对,并将结果经ESPript 3.0修饰。基于结构的序列分析表明,这些来源于不同细菌的酶具有相似的二级结构,其中包括β-链和α螺旋的数目和长度。以ThermotogamaritimaMSB8海带多糖酶(Laminarinase)为例,该酶催化域的二级结构包含18个β-链(形成2个扭曲的β折叠片)、2个短α-螺旋以及2个310螺旋。序列对比的结果表明,除了与同样来源于热袍菌属的Thermotogapetrophilaendo-β-1,3-glucanase的序列一致性达到99%之外,TmLamCD与其它蛋白之间的序列一致性只有28%~50%左右(图1)。尽管GH16家族β-1,3-葡聚糖酶彼此之间的同源性不高,但这些酶的折叠方式和某些氨基酸残基却高度保守,尤其是该家族特征性的EIDIXE序列在酶的催化作用中发挥着非常重要的作用,其中靠前的Glu通常在催化过程中作为亲核试剂,而靠后的Glu则是催化酸/碱。
1.2 细菌β-1,3-葡聚糖酶的整体结构
为了表现GH16家族细菌来源的β-1,3-葡聚糖酶之间结构的异同,本文将PDB数据库中已知结构的酶(包括2HYK、3AZX、3DGT、3ILN、4BOW、4CRQ、4DFS以及4WZF)催化域部分重叠,得到图2(A)的结果。细菌β-1,3-葡聚糖酶富含β-折叠,这些链弯曲折叠成两个面对面反向平行的片层结构,形成典型的类似三明治的“β-jelly roll”结构,并呈现出一定的弯曲以形成一个供底物结合的凹槽(图2B)。催化域结构非常保守,其中两个反向平行的折叠片的结构尤为保守,每条β-链的长度和弯曲走向都基本保持一致。同时,在已知结构的β-1,3-葡聚糖酶中都发现一个与酶结合的Ca2+,这一现象在GH16家族糖苷水解酶中也是非常保守的[21]。该钙离子在细菌葡聚糖酶中可能起到提升热稳定性的作用[22]。根据晶体结构,钙离子位于酶催化凹槽的背面,而底物则与酶沿着凹槽相互结合,二者的空间距离较远,说明钙离子对酶的催化作用没有直接影响[15]。钙离子的结合位点也非常一致,都是由两个氨基酸序列相距较近的Glu和Gly以及一个距离较远的Asp的骨架羰基氧和Asp的羰基侧链氧与钙离子相互作用,从而使钙离子稳定结合。
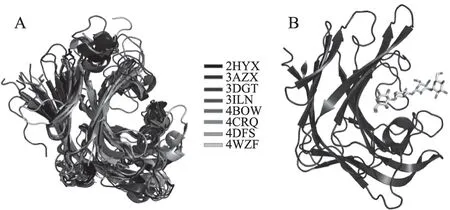
图2 细菌β-1,3-葡聚糖酶的整体结构[13,15-20,23-24]Fig.2 The overall structure of bacterial β-1,3-glucanase[13,15-20,23-24]注:A. GH16家族已知晶体结构的所有细菌 β-1,3-葡聚糖酶三维结构叠加对比; B.来源于Zobellia galactanivorans的β-1,3-葡聚糖酶 ZgLamA与一个海带四糖的复合物晶体结构。
1.3 催化域的活性位点
细菌β-1,3-葡聚糖酶的活性位点包括作为亲核试剂、催化酸/碱的催化关键残基和一系列为底物结合和稳定过渡态提供结构和功能支撑的辅助残基。研究发现细菌β-1,3-葡聚糖酶的催化活性依赖于位于一个高度保守单元(EXDXXE)的2个谷氨酸残基和1个天冬氨酸残基[25]。Wen-Yih Jeng等[15]用环状的己糖类似物葡糖酸内脂与TmLamCD共结晶并得到复合物晶体结构揭示在催化位点周围的氨基酸残基中,Asn-45、Glu-132、Glu-137和His-151与葡萄糖酸内酯形成了直接的氢键,Oδ2原子与His-151的Nε2形成氢键的Asp-134也参与了稳定配体,同时Trp-116残基和Ala114残基与底物形成了疏水作用力。为了模拟长链底物在TmLamCD中的位置,他们又用一种具有一个极性头部和16个C尾部的表面活性剂分子CTAB与酶进行了共结晶,发现Ile-40、Trp-43、Asn-45、Arg-85、Ala-114、Trp-116、Trp-127、Glu-132和Glu-137等残基都与CTAB分子形成了疏水作用。
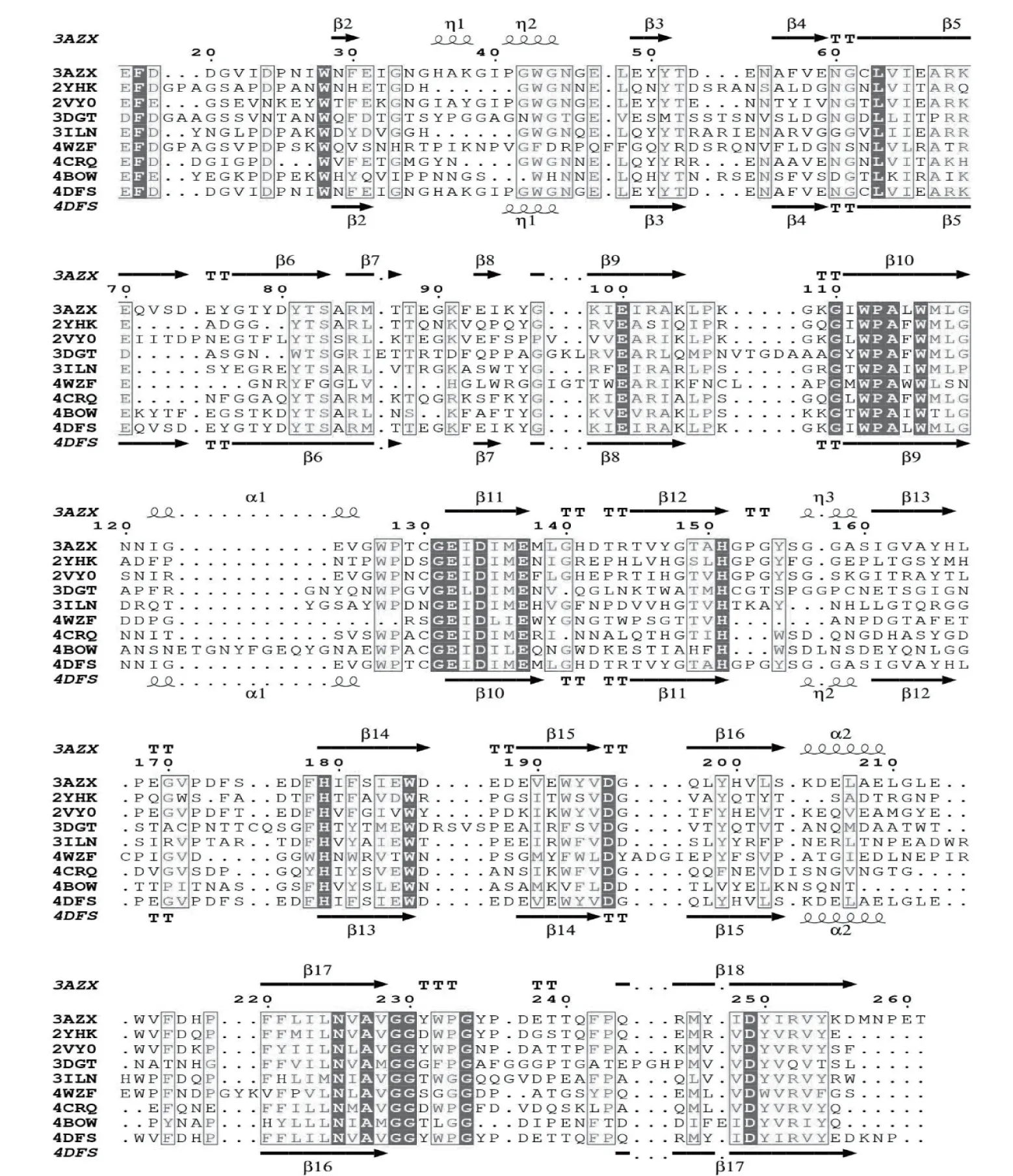
图1 GH16家族β-1,3-葡聚糖酶以结构为基础的序列对比Fig.1 Structure-based sequence alignment of family GH16 β-1,3-glucanase
1.4 水解机制
糖苷水解酶的水解机制主要分为反向水解机制(inverting mechanisms)和保留水解机制(retaining mechanisms),而GH16家族的糖苷水解酶所采取的水解机制是保留水解机制[26]。该家族酶的整个催化过程分为两个步骤。首先,Glu-132作为亲核试剂攻击糖环上的C1原子从而使两个糖环之间的β-1,3-糖苷键断裂。然后Glu-137作为催化酸接受电子,进而将电子转移给邻近的水分子,接着该水分子攻击之前β位置的C1原子,最终Glu-132和产物得以释放(图3)。
2 细菌β-1,3-葡聚糖酶的底物特异性
虽然同属一个糖苷水解酶家族,且结构相似,但GH16家族β-1,3-葡聚糖酶相互之间具有不同的底物特异性。根据Aurore Labourel等人的研究,来源于海洋细菌Zobelliagalactanivorans的β-1,3-葡聚糖酶ZgLamA对底物β-1,3-葡聚糖海带多糖(laminarin)的催化效率要比对混合链葡聚糖MLG(β-1,3-1,4-葡聚糖)高将近22倍左右。对比ZgLamA与两种底物的复合物晶体发现,酶与两种底物的相互作用在底物结合位点-1和-2位置非常相似(图4A和B),两个糖残基分别与酶的Glu-274、Trp-238、Asp-271、Glu-250、Arg-213、Asn-171和Ser-269等氨基酸残基形成氢键,同时还与Trp-238、Trp-242、Trp-264以及His-170等氨基酸残基形成疏水作用。因为MLG中β-1,4-糖苷键的存在,使得其在底物结合位点-3位置的糖残基相较于海带六塘发生了180°的翻转,最终导致Glu-263代替Trp-264与糖残基形成氢键。
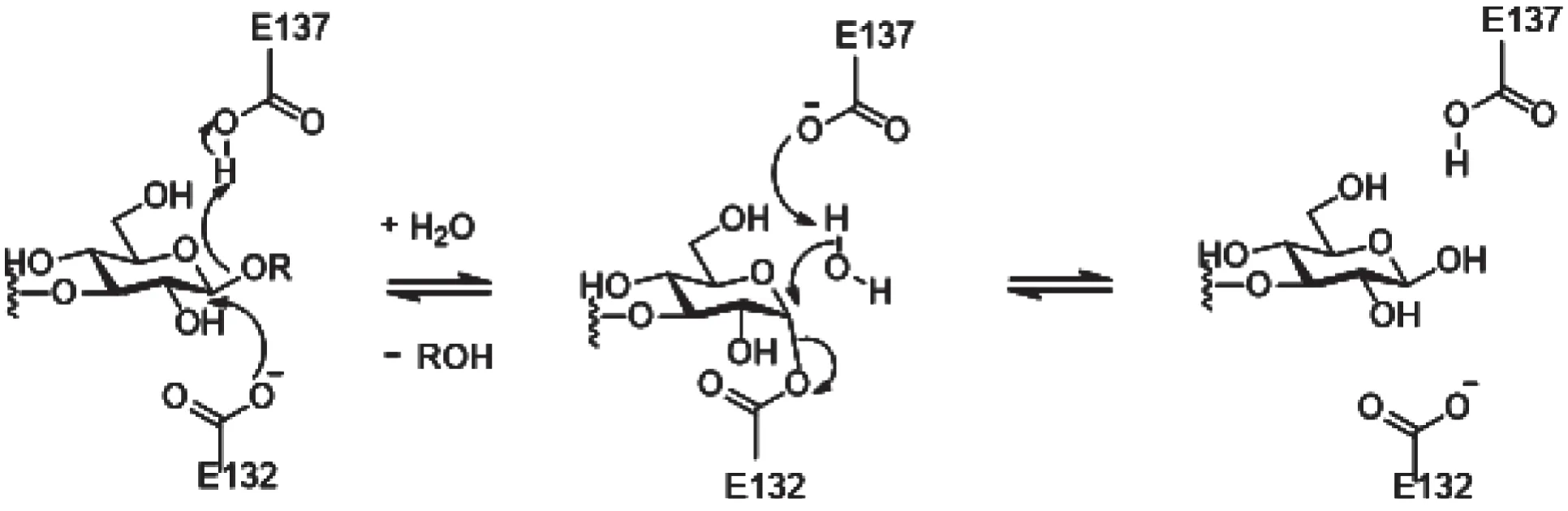
图3 β-1,3-葡聚糖酶的保留催化机制[26]Fig.3 The retaining mechanisms of β-1,3-glucanase[26]
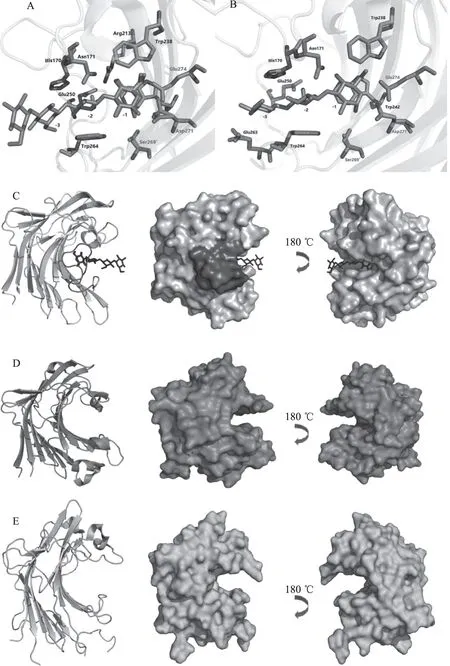
图4 细菌β-1,3-葡聚糖酶的底物特异性[17-19]Fig.4 The substrate specificity of bacterial β-1,3-glucanases[17-19]注:A和B,ZgLamA催化凹槽分别与海带四糖(A)和G3G4G(B)的相互作用;C,ZgLamA与海带四糖复合物晶体结构的 卡通模型和疏水表面(图中深灰色部位为ZgLamA特有的环结构);D,ZgLamC晶体结构的 卡通模型和疏水表面;E,Rv0315晶体结构的卡通模型和疏水表面。
从晶体结构图中可以看出(图4A和B),海带己糖由于β-1,3-糖苷键的不断延伸使其在催化凹槽中呈现出螺旋型构象,而混合链的G3G4G则由于β-1,4-糖苷键的出现使其表现出直线型构象。通过二级序列对比发现,ZgLamA拥有一个由17个氨基酸(从Ala-246到Ala-262)组成的长环(loop)(图4C),而这个环结构在其他同家族已知结构的β-1,3-葡聚糖酶中是不存在的。该环结构存在于催化凹槽中,堵塞了酶的负结合位点从而使ZgLamA的催化中心呈现出弯曲凹槽的构象(图4C)。这种构象非常有利于酶结合具有螺旋型构象的β-1,3-葡聚糖,同时妨碍直线型的混合链葡聚糖的结合。这也解释了ZgLamA对β-1,3-葡聚糖的催化效率远高于对MLG的催化效率的原因。
随后,Aurore Labourel等人得到了同样来源于海洋细菌Zobelliagalactanivorans且与ZgLamA同源性为37%的另一个GH16家族β-1,3-葡聚糖酶ZgLamC的晶体结构。ZgLamC同样既可以水解β-1,3-葡聚糖海带多糖又可以水解混合链葡聚糖MLG,但与ZgLamA不同的是,它对海带多糖的催化效率比对MLG的催化效率高3倍。对比二者总体的晶体结构发现,因为缺少ZgLamA特有的环结构,ZgLamC的催化中心呈现出直线型的凹槽(图4D)。Aurore Labourel等人对比了这两种酶与底物复合物晶体的区别,发现底物结合位点-1和-2位置的糖残基与酶的相互作用基本相同,相关氨基酸残基也很保守。但是-3位置因为没有环的堵塞,从而使ZgLamC具有一个相对大的空间来结合海带多糖和MLG两种底物。这解释了ZgLamC对两种底物催化效率相差不大的原因。
Wanyu Dong等人[17]得到了结核分支杆菌(Mycobacteriumtuberculosis)来源的β-1,3-葡聚糖酶Rv0315的晶体结构。与前两个酶不同的是,Rv0315不管在何种pH条件下,都不具备水解海带多糖的能力,即使增加酶浓度也检测不到任何活力。为了找到Rv0315没有水解活力的原因,Wanyu Dong等人对比了其与ZgLamA结构的差异。相比之下,两个酶的总体结构是非常相似的,但Rv0315具有一个更大的催化凹槽(图4E),进一步对比二者与底物复合物晶体之间的差异,发现在底物结合位点-1处,Rv0315和ZgLamA与底物的结合非常相似,但Rv0315缺失了所有在ZgLamA中与-2和-3位置的糖残基相互作用的氨基酸残基,例如Asn-171、Glu-250、Arg-213、Trp-264和His-170等,并因此导致Rv0315的催化凹槽的尺寸明显偏大,这可能是Rv0315没有明显催化活性的原因。
综上所述,虽然GH16家族β-1,3-葡聚糖酶的结构总体上非常相似,但是酶与底物结合残基的差异,仍会影响酶对不同类型底物的选择性和催化活性,这使得细菌β-1,3-葡聚糖酶的底物谱具有多样性。
3 细菌β-1,3-葡聚糖酶与植物β-1,3-葡聚糖酶结构对比
植物β-1,3-葡聚糖酶属于糖苷水解酶17家族,其结构特征是拥有一个(β/α)8TIM桶状结构。迄今为止,人们已经得到4个植物β-1,3-葡聚糖酶的晶体结构(http://www.cazy.org/)。序列对比分析结果表明,桶状结构核心区域的β-链是高度保守的,主要的差异都发生在蛋白外围的环结构和螺旋结构处,而且都是由于序列的插入或者删除引起的。2013年,Agnieszka Wojtkowiak等人获得了马铃薯内切-β-1,3-葡聚糖酶(GLUB20-2)突变体E259A与一个海带六糖共结晶的晶体结构,这是人们首个得到的GH17家族糖苷水解酶与寡糖分子的复合晶体结构。虽然将其活性位点突变,但GLUB20-2E259A仍具有剩余活性,质谱分析揭示该突变体用两种方式切割了海带六糖,分别产生了一个海带三糖分子和一个海带四糖分子[27](图5A、B)。
结构显示三糖分子被固定在酶的底物结合位点-1、-2和-3处,具有较高的结合亲和力,其非还原端位于催化凹槽的远端。其中,底物两个糖分子与-1和-2的结合高度保守,且与参与水解活性的关键残基Asn117、Glu310、Lys313和Glu319有相互作用,共形成8个直接的氢键和2个水分子介导的氢键[28]。此外,Tyr58的芳香环与-2位的糖形成疏水作用,而Phe305和Phe322的芳香环则与-1位的糖相互作用。底物结合位点-3处的糖与Gln82形成两个直接的氢键及水分子介导的氢键,以稳固三糖分子与酶的结合。除可结合三糖分子外,酶的催化凹槽也可容纳一个海带四糖,但由于在+1和+2结合位点底物与酶的低亲和力导致电子云混乱,该研究未能解析出对应的葡萄糖分子(如图5A、B)。尽管如此,+1位置的糖很可能会与Phe204形成疏水相互作用,而+3和+4底物结合位点处的糖可与Thr166形成直接的氢键。
GLUB20-2催化凹槽形成两端开口中间弯曲的峡谷型几何构象。该构象排除了任何直线型β-1,4-葡聚糖在-3到+4底物结合位点结合的可能性,而针对β-1,6-糖苷键,该酶也仅可能提供+1和+2结合位点。这也解释了植物β-1,3-葡聚糖酶主要水解由β-1,3-糖苷键相连的葡聚糖分子[29],而对混合链的β-1,3-1,4-葡聚糖[30]和具有分支的β-1,3-1,6-葡聚糖[31]仅有非常有限的催化活性。
植物β-1,3-葡聚糖酶与细菌β-1,3-葡聚糖酶采用相同的水解机制(retaining mechanism)来催化以β-1,3-糖苷键相连的葡聚糖分子的水解。二者在催化过程中作为质子供体和亲核试剂的都是两个严格保守的谷氨酸残基。但是,二者在序列和蛋白结构上有着巨大的差异。序列比对发现,植物β-1,3-葡聚糖酶中,参与催化的两个谷氨酸残基分别位于相距较远的两个β-链的末端,而细菌酶中相应的两个谷氨酸残基则处于同一条β-链上,彼此之间只有5个氨基酸残基的距离。以底物分子为基准,将马铃薯β-1,3-葡聚糖酶(StLam)与底物的复合物晶体结构和海洋细菌Zobelliagalactanivoransβ-1,3-葡聚糖酶(ZgLamA)与底物的复合物晶体结构进行对接(图5C)发现,两个酶重合部分较少,植物酶与细菌酶的催化凹槽差异较大且底物在催化凹槽中的结合方向也不同(图4和图5)。植物酶体积要大于细菌酶,催化凹槽更长且具有独特的几何构象,而细菌酶的催化凹槽中底物结合位点少于植物酶,并且绝大多数呈现两端开口的直线型构象,这使得植物酶相比于细菌酶具有更突出的底物专一性。
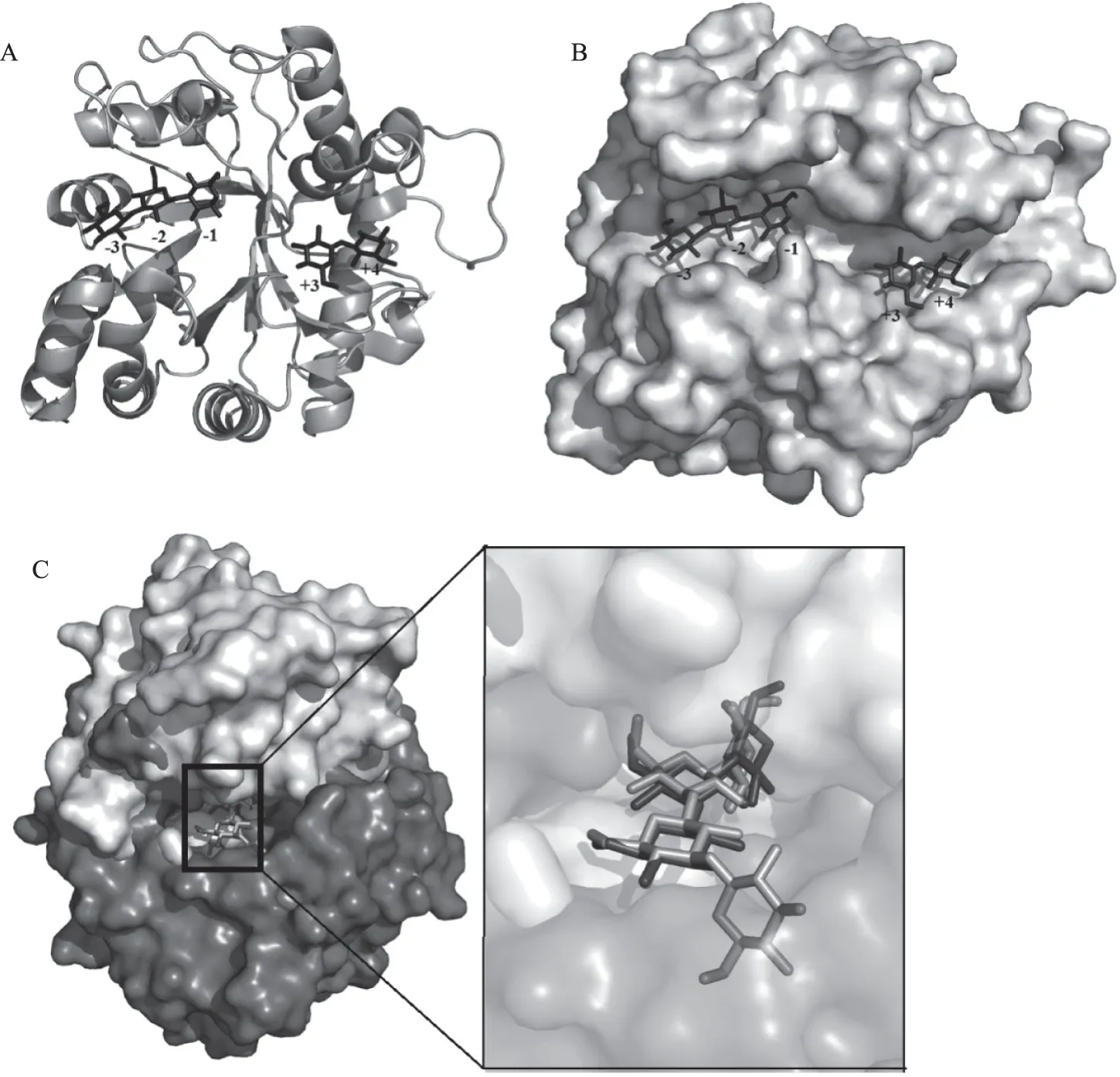
图5 植物β-1,3-葡聚糖酶的结构及其与细菌β-1,3-葡聚糖酶结构的对比[18]Fig.5 Three-dimensional structure of plant β-1,3-glucanase and structural comparison of plant β-1,3-glucanase and bacterial β-1,3-glucanase[18]注:A.StLam晶体结构的卡通模型;B.StLam与底物复合物晶体的疏水表面模型; C.ZgLamA和StLam分别与底物的复合物晶体结构以底物分子为基准对接(图中ZgLamA为白色,StLam为黑色)。
4 展望
酶结构与功能的研究是探索酶催化反应机理、挖掘酶催化特性以及酶理性设计改造的重要基础。β-1,3-葡聚糖酶因其特异性水解β-1,3-葡聚糖的能力,在食品工业和植物保护研究中受到广泛关注。但一些新型β-1,3-葡聚糖酶(如GH64、GH81、GH128及GH132家族)因缺乏晶体结构信息,其催化机制和底物选择性的分子机制尚不清楚,限制了酶的工程化改造和工业化应用。本研究通过对细菌β-1,3-葡聚糖酶结构和催化性质的总结和分析,有助于理解该酶所呈现的底物选择和催化活性多样性的分子基础,使我们可以基于比较结构生物化学,调控或改造β-1,3-葡聚糖酶的性质,以实现其在水果保鲜、植物抗病及活性小分子多糖制备等多领域的应用。
[1]Jadhav SB,Gupta A. Studies on application ofβ-1,3 glucanase in the degradation of glucans produced by Botrytis cinerea and inhibition of fungal growth[J]. Biocatalysis and Agricultural Biotechnology,2016,7:45-47.
[2]Blättel V,Larisika M,Pfeiffer P.β-1,3-Glucanase from Delftia tsuruhatensis strain MV01 and its potential application in vinification[J]. Applied and Environmental Microbiology,2011,77(3):983-990.
[3]李孝辉,钱玉英. 大麦饲料的开发及β—葡聚糖酶的应用[J]. 粮食与饲料工业,1997(8):19-20.
[4]徐敏,李晶,郑志永. 哈茨木霉产水解热凝胶的内切β-1,3-葡聚糖酶的分离纯化[J]. 食品工业科技,2014,35(12):157-161.
[5]畅晓洁,郑必胜,赵欣. 裂褶菌产内切β-1,3-葡聚糖酶的分离纯化[J]. 食品工业科技,2012,33(4):227-229.
[6]陈小云,李坚斌,林莹.β-1,3-葡聚糖酶和几丁质酶在热带水果保鲜中的应用[J]. 食品工业科技,2008(5):96.
[7]Fujimori N,Enoki S,Suzuki A. Grape apoplasmicβ-1,3-glucanase confers fungal disease resistance in Arabidopsis[J]. Scientia Horticulturae,2016,200:105-110.
[8]Mouyna I,Aimanianda V,Latgé JP. GH16 and GH81 familyβ-(1,3)-glucanases in Aspergillus fumigatus are essential for conidial cell wall morphogenesis[J]. Cellular Microbiology,2016,18(9):1285-1293.
[9]Fuchs K-P,Zverlov VV,Velikodvorskaya GA. Lic16A of Clostridium thermocellum,a non-cellulosomal,highly complex endo-β-1,3-glucanase bound to the outer cell surface[J]. Microbiology,2003,149(4):1021-1031.
[10]Yamamoto M,Ezure T,Watanabe T. C-Terminal domain ofβ-1,3-glucanase H in Bacillus circulans IAM1165 has a role in binding to insolubleβ-1,3-glucan[J]. FEBS Letters,1998,433(1-2):41-43.
[11]Kim PI,Chung K-C. Production of an antifungal protein for control of Colletotrichum lagenarium by Bacillus amyloliquefaciens MET0908[J]. FEMS Microbiology Letters,2004,234(1):177-183.
[12]Hong T-Y,Meng M. Biochemical characterization and antifungal activity of an endo-1,3-β-glucanase of Paenibacillus sp. isolated from garden soil[J]. Applied Microbiology and Biotechnology,2003,61(5-6):472-478.
[13]Hong T-Y,Hsiao Y-Y,Meng M. The 1.5Å structure of endo-1,3-β-glucanase from Streptomyces sioyaensis-evolution of the active-site structure for 1,3-β-glucan-binding specificity and hydrolysis[J]. Acta Crystallographica Section D Biological Crystallography,2008,64(9):964-790.
[14]Masuda S,Endo K,Koizumi N. Molecular identification of a novelβ-1,3-glucanase from alkaliphilic Nocardiopsis sp. strain F96[J]. Extremophiles,2006,10(3):251-255.
[15]Jeng WY,Wang NC,Lin CT. Crystal structures of the laminarinase catalytic domain from Thermotoga maritima MSB8 in complex with inhibitors-essential residues for beta-1,3-and beta-1,4-glucan selection[J]. The Journal of Biological Chemistry,2011,286(52):45030-45040.
[16]Fibriansah G,Masuda S,Koizumi N. The 1.3 A crystal structure of a novel endo-beta-1,3-glucanase of glycoside hydrolase family 16 from alkaliphilic Nocardiopsis sp. strain F96[J]. Proteins,2007,69(3):683-690.
[17]Dong W,Huang J,Li Y. Crystal structural basis for Rv0315,an immunostimulatory antigen and inactive beta-1,3-glucanase of Mycobacterium tuberculosis[J]. Scientific Reports,2015,5:15073.
[18]Labourel A,Jam M,Jeudy A. The beta-glucanase ZgLamA from Zobellia galactanivorans evolved a bent active site adapted for efficient degradation of algal laminarin[J]. The Journal of Biological Chemistry,2014,289(4):2027-2042.
[19]Labourel A,Jam M,Legentil L. Structural and biochemical characterization of the laminarinase ZgLamCGH16 from Zobellia galactanivorans suggests preferred recognition of branched laminarin[J]. Acta Crystallographica Section D,Biological Crystallography,2015,71(Pt 2):173-184.
[20]Cota J,Alvarez TM,Citadini AP. Mode of operation and low-resolution structure of a multi-domain and hyperthermophilic endo-beta-1,3-glucanase from Thermotoga petrophila[J]. Biochemical and Biophysical Research Communications,2011,406(4):590-594.
[21]Michel G,Chantalat L,Duee E. The κ-carrageenase of P. carrageenovora features a tunnel-shaped active site-a novel insight in the evolution of Clan-B glycoside hydrolases[J]. Structure,2001,9(6):513-525.
[22]Welfle K,Misselwitz R,Welfle H. Influence of Ca2+on conformation and stability of three bacterial hybrid glucanases[J]. European Journal of Biochemistry,1995,229(3):726-735.
[23]Bleicher L,Prates ET,Gomes TC. Molecular basis of the thermostability and thermophilicity of laminarinases-X-ray structure of the hyperthermostable laminarinase from Rhodothermus marinus and molecular dynamics simulations[J]. The Journal of Physical Chemistry B,2011,115(24):7940-7949.
[24]Ilari A,Fiorillo A,Angelaccio S. Crystal structure of a family 16 endoglucanase from the hyperthermophile Pyrococcus furiosus-structural basis of substrate recognition[J]. The FEBS Journal,2009,276(4):1048-1058.
[25]Krah M,Misselwitz R,Politz O. The laminarinase from thermophilic eubacterium Rhodothermus marinus[J]. European Journal of Biochemistry,1998,257(1):101-111.
[26]Davies G,Henrissat B. Structures and mechanisms of glycosyl hydrolases[J]. Structure,1995,3(9):853-859.
[27]Wojtkowiak A,Witek K,Hennig J. Structures of an active-site mutant of a plant 1,3-β-glucanase in complex with oligosaccharide products of hydrolysis[J]. Acta Crystallographica Section D-Biological Crystallography,2013,69(1):52-62.
[28]Chen L,Garrett TP,Fincher GB. A tetrad of ionizable amino acids is important for catalysis in barleyβ-glucanases[J]. Journal of Biological Chemistry,1995,270(14):8093-8101.
[29]Witek AI,Witek K,Hennig J. Conserved Cys residue influences catalytic properties of potato endo-(1→3)-β-glucanase GLUB20-2[J]. Acta Biochimica Polonica,2008,55(4):791-797.
[30]Akiyama T,Shibuya N,Hrmova M. Purification and characterization of a(1→3)-β-D-glucan endohydrolase from rice(Oryza sativa)bran[J]. Carbohydrate Research,1997,297(4):365-374.
[31]Peumans WJ,Barre A,Derycke V. Purification,characterization and structural analysis of an abundantβ-1,3-glucanase from banana fruit[J]. European Journal of Biochemistry,2000,267(4):1188-1195.
Progress in the structure and catalytic mechanism ofβ-1,3-glucanases
WANG Rui,YANG Jun*,YANG Qing
(School of Life Science and Biotechnology,Dalian University of Technology,Dalian 116024,China)
β-1,3-glucanases are widespread throughout bacteria,fungi,plants and invertebrates. They play various physiological roles due to the diversity of origin,such as participating in plant growth and development,defending against pathogens in plant,providing nutrients for bacteria,regulating fungal cell wall stability and rigidity,and involving in the release and invasion of virus. The research of enzyme structure is the basis to explore the mechanism of enzyme catalyzed reaction,to characterize enzyme catalytic properties and to design and transform the enzyme. The structure and catalytic mechanism of GH16 bacterialβ-1,3-glucanase were thoroughly reviewed. By comparing with the structure of GH17 plantβ-1,3-glucanases,this study was attempted to reveal how bacterialβ-1,3-glucanases hydrolyze polysaccharide,and provides an important reference for further modification and utilization of bacterialβ-1,3-glucanases in plant protection,food and pharmaceutical fields.
β-1,3-glucanases;crystal structure;catalytic mechanism;substrate specificity
2017-01-05
王瑞(1991-),男,硕士研究生,研究方向:糖苷水解酶的结构功能研究,E-mail:raywangbio@gmail.com。
*通讯作者:杨君(1972-),女,博士,副教授,研究方向:蛋白质结构与功能研究,E-mail:junyang@dlut.edu.cn。
国家重点研发计划(2016YFD0200502);辽宁省自然科学基金(2015020782)。
TS201.1
A
1002-0306(2017)14-0314-07
10.13386/j.issn1002-0306.2017.14.062
