药物涂层球囊在冠状动脉分支开口病变中的应用
2017-08-09翟东东高炬张萌刘鸿宇王斌曲涛
翟东东 高炬 张萌 刘鸿宇 王斌 曲涛
·临床研究·
药物涂层球囊在冠状动脉分支开口病变中的应用
翟东东 高炬 张萌 刘鸿宇 王斌 曲涛
目的 评价药物涂层球囊在经皮冠状动脉介入治疗分支开口病变(Medina 0,0,1型)的有效性和近期疗效。方法 符合入选条件的患者共48例,随机分为药物涂层球囊(drug coated balloon,DCB)血管成形术治疗组(DCB组)和切割球囊(cutting balloon,CB)血管成形术治疗组(CB组)。DCB组应用DCB扩张治疗靶病变,CB组用CB扩张治疗靶病变,分析比较术中即刻效果及远期预后。结果 术前两组临床资料比较,差异无统计学意义。术中两组间均无冠状动脉穿孔、心脏压塞、急性血栓事件发生。两组病变血管最小内径(minimal lumen diameter,MLD)术前及术后即刻比较,差异无统计学意义;DCB组的随访MLD[(1.8±0.2)mm比(1.5±0.3)mm,P=0.006]明显优于CB组,差异有统计学意义;随访期间无死亡、非致死性心肌梗死、血运重建发生。结论 在冠状动脉分支开口病变治疗中,DCB与CB治疗相比,即刻效果相似,但近期疗效优于CB。
经皮冠状动脉介入治疗; 切割球囊; 药物涂层球囊; 分支开口病变
冠状动脉分支开口病变属于冠状动脉分叉病变中的0,0,1型(Medina分型)[1],分支血管管径一般较小,多在3 mm以下,病变多位于开口部位,因特殊的解剖特点,目前的介入治疗方式存在诸多困难。支架置入术较常用,但因病变血管直径较小、易形成支架内血栓,同时因定位困难,极易影响到主支血管,甚至需要额外置入支架,增加术后支架内再狭窄发生率[2-4]。单纯普通球囊扩张易造成不规则内膜损伤和严重撕裂,而且扩张后易弹性回缩,再狭窄发生率高[5]。切割球囊(cutting balloon,CB)血管成形术的低压扩张具有减轻血管弹性回缩及血管内膜损伤较轻的优点。既往研究显示,与单纯普通球囊扩张及支架置入术相比,CB血管成形术优势明显,但再狭窄发生率仍高达37.5%~41.0%[5-6]。近年来,药物涂层球囊(drug coated balloon,DCB)在我国已逐渐应用,目前主要应用于支架内再狭窄[7-10]及小血管病变[11-14]等治疗,因其能明显降低再狭窄发生率,为临床处理冠状动脉分支开口病变提供了新的思路。本研究旨在探讨DCB治疗分支开口病变的有效性及近期疗效。
1 对象与方法
1.1 研究对象
纳入2015年6月至2016年6月在航天中心医院心脏医学部住院的冠心病且拟行经皮冠状动脉介入治疗( percutaneous coronary intervention,PCI)患者。入选标准:(1) 符合1979年世界卫生组织(WHO)关于缺血性心脏病的命名和诊断标准[13];(2)年龄<80岁;(3)存在客观的心肌缺血证据,如心电图(静息、动态或负荷试验)出现典型性ST段改变,心肌核素或超声心动图检查显示灌注缺损和(或)室壁运动异常等;(4)经选择性定量冠状动脉造影(quantitative coronary angiography,QCA)判断分支开口狭窄至少>70%,且相应主支血管无明显狭窄,符合Medina分型0,0,1型病变;(5)同意接受PCI。排除标准:(1)年龄>80岁患者;(2)急性心肌梗死行急诊PCI患者;(3)心源性休克患者;(4)严重肾功能不全患者;(5)碘过敏及PCI禁忌证患者;(6)预期寿命<3年且合并其他疾病患者;(7) QCA提示病变长度>10 mm,狭窄程度<70%,靶病变部位处主支血管存在病变,支架内再狭窄。共入选患者48例,采用随机数字表法随机分组,分为DCB组及CB组。
1.2 研究方法
两组患者术前常规服用阿司匹林100 mg、每日1次,氯吡格雷75 mg、每日1次,持续7 d以上,如未达7 d,在术前24 h给予负荷剂量阿司匹林300 mg,氯吡格雷300 mg。手术开始时患者均给予肝素100 U/kg,术中每小时追加1000 U。患者均采用经右侧桡动脉或股动脉入径穿刺,均常规体位行冠状动脉造影(coronary angiography,CAG)检查,判断血管管腔口径以QCA为准,根据情况可以应用普通球囊进行预扩张。DCB组术中使用的球囊为紫杉醇DCB(德国贝朗医疗),CB组术中使用的球囊为CB(波士顿科学国际有限公司)。DCB选择直径与血管直径的比值为(0.8~1)∶1,尽快到达病变部位后,扩张时以每5秒递增l atm(1 atm=101.325 kPa)速度扩张至6 atm,最大扩张压力为8 atm,在最高压力时持续30~60 s。CB使用方法为到达病变部位后以每5秒递增l atm的速度缓慢扩张至4~6 atm,在最高压力时持续10~15 s,必要时可以重复扩张。术后均服用阿司匹林100 mg、每日1次,氯吡格雷75 mg、每日1次,持续12个月以上;术后6个月复查CAG。术后病变血管狭窄程度减少>20%,残余狭窄<50%,主支血管未受影响,无死亡、急性心肌梗死或需急诊冠状动脉旁路移植术定义为球囊扩张成功。
1.3 观察指标
收集患者临床基线资料包括年龄、性别、冠心病家族史、病史及用药情况等。经QCA判断并记录病变部位、病变长度及基准血管直径。记录术前及术后即刻病变血管最小内径(minimal lumen diameter,MLD)、最大扩张压及扩张时间等资料。术后6个月以专科门诊或电话方式进行随访。临床观察终点为主要不良心血管事件(major adverse cardiovascular events,MACE),包括心源性死亡、非致死性急性心肌梗死、靶病变血运重建(target lesion revaseularization,TLR)。患者术后6个月后复查CAG,以QCA判断并记录靶病变MLD。
1.4 统计学分析
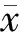
2 结果
2.1 两组患者基线资料比较(表1)
两组患者年龄、性别、体重指数,病史(冠心病家族史、高脂血症、高血压病、糖尿病)、吸烟、用药情况(他汀类、硝酸酯类、血管紧张素转化酶抑制药/血管紧张素Ⅱ受体拮抗药、β阻滞药)比较,差异均无统计学意义(均P>0.05)。
2.2 两组患者靶血管造影结果比较(表2)
两组患者均成功完成了CAG及PCI术,其中DCB组22例患者23处靶血管病变、CB组26例患者28处靶血管病变,QCA结果提示两组的靶血管病变情况,包括病变部位、平均病变长度、基准血管直径等指标,两组比较,差异均无统计学意义(均P>0.05)。
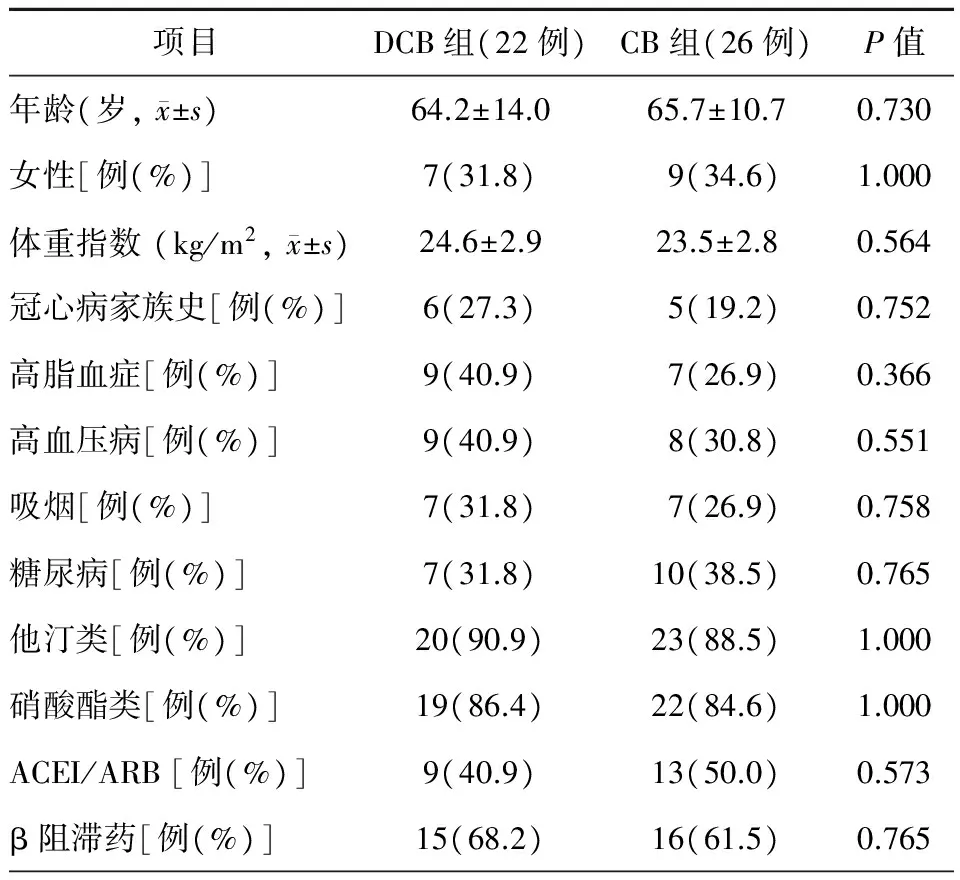
表1 两组患者基线资料比较
注:DCB,药物涂层球囊;CB,切割球囊;ACEI,血管紧张素转化酶抑制药;ARB,血管紧张素Ⅱ受体拮抗药
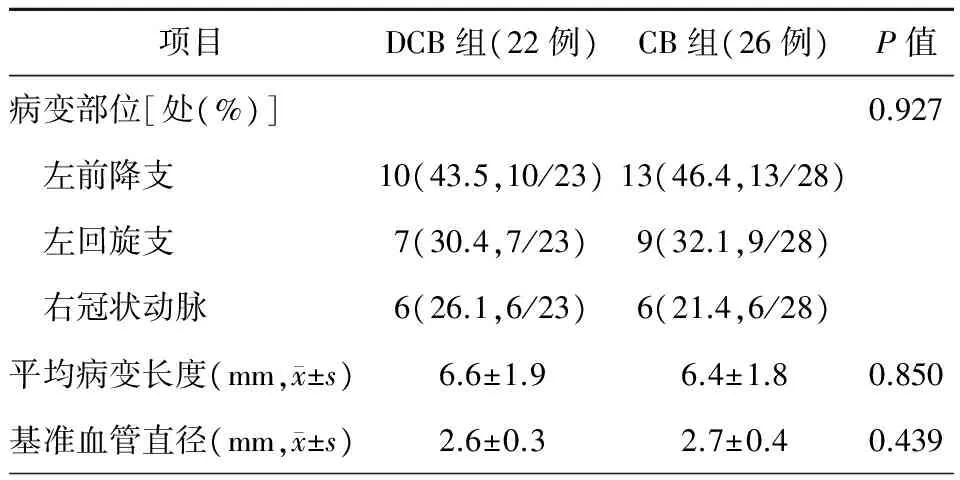
表2 两组患者术中造影情况对比
注:DCB,药物涂层球囊;CB,切割球囊
2.3 两组患者手术结果及随访情况比较(表3)
DCB组和CB组手术成功率比较,差异无统计学意义。DCB组手术失败1例,为球囊扩张术后内膜撕裂,行置入支架术后成功。CB组手术失败2例,其中1例为CB术后内膜撕裂、术中观察未影响血流,1例CB未通过病变,考虑与原病变钙化严重有关。两组在扩张前MLD及扩张后即刻MLD比较,差异均无统计学意义 (均P>0.05)。两组患者住院期间各有1例不典型胸痛发作,但心电图未见明显改变。临床随访6个月,两组患者平均CAG随访率及CAG随访时间比较,差异均无统计学意义 (均P>0.05),且均未发生死亡、非致死性心肌梗死、TLR。DCB组随访MLD明显优于CB组[(1.8±0.2)mm比(1.5±0.3)mm,P=0.006],差异有统计学意义。
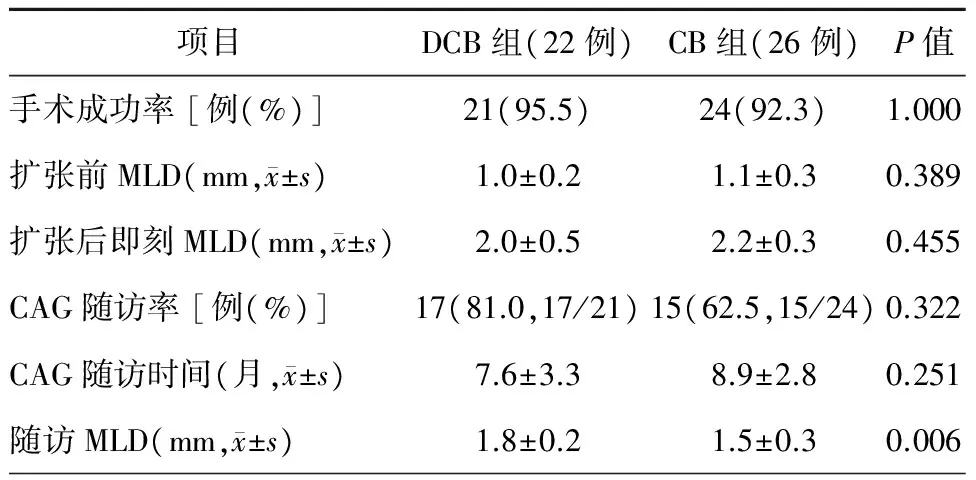
表3 两组患者手术结果及随访情况对比
注:DCB,药物涂层球囊;CB,切割球囊;MLD,病变血管最小内径; CAG,冠状动脉造影
3 讨论
冠状动脉分支开口部位有较丰富的胶原纤维,因此,对分支开口病变进行介入治疗时,其弹性回缩明显高于冠状动脉其他部位的病变,同时存在靶病变直径较小、定位困难等解剖特点。目前常用的介入治疗方法术中风险大、远期再狭窄率高,冠状动脉分支开口病变介入治疗是目前棘手的问题。近年来,DCB作为一种新的介入治疗技术在欧洲逐渐广泛应用于冠状动脉及外周介入领域,在国内也有多个 DCB 产品已经或即将投入临床使用。DCB 的出现为我国冠状动脉疾病的治疗提供了新的选择[7]。
本研究中,应用DCB血管成形术治疗分支开口病变,与CB血管成形术治疗相比,手术即刻效果两者相似,但随访复查CAG发现DCB组6个月疗效明显优于CB组,提示DCB治疗有效降低晚期血管丢失率,既往研究也证实了这一点[14-15]。CB扩张压力小、能减少血管内膜的无序撕裂,手术即刻效果较好,但血管内膜撕裂后,刺激血管平滑肌细胞(smooth muscle cells,SMC)向内膜发生增殖、覆盖,而SMC的过度增生,是造成血管内再狭窄的重要因素[16]。同时,内膜损伤后胶原暴露,诱发局部炎症反应,促使白细胞和血小板在损伤部位的内皮黏附、聚集,导致血管支架内再狭窄,虽然CB血管成形术炎症反应较普通球囊扩张轻,但仍会导致支架内再狭窄[17]。DCB的表面为对比剂及抗增殖药物混合物,短时间的球囊扩张就可以引起持续的抗增殖作用。Scheller等[18]进行了DCB预防支架内再狭窄的动物实验,结果显示了紫杉醇DCB与血管壁接触1 min可显著降低支架内再狭窄发生率,与单纯普通球囊相比,紫杉醇DCB组的新生内膜面积减少63%;涂层药物在送入冠状动脉循环系统扩张前仅丢失6%,扩张后大约80%的药物快速从球囊传递至血管壁并保留较长时间,抗增殖药物的短期暴露即可明显阻断早期的增生启动因子,抑制细胞骨架生成,阻断有丝分裂,有效抑制细胞快速增殖,还可抑制SMC迁移和表型改变,抑制内膜增生性炎症反应,从而明显减少晚期管腔丢失[19-20]。因此,DCB血管成形术远期效果优于CB血管成形术。
本研究中,DCB治疗未出现冠状动脉穿孔等严重并发症,手术失败l例,为球囊扩张后内膜严重撕裂,原因考虑为术中患者不能耐受球囊扩张且术中扩张速度偏快、造成内膜撕裂。本研究DCB使用过程中应注意:DCB为一次性使用装置,不能重复使用,要尽可能快地到达病变部位,应用DCB前应该使用普通球囊充分预扩张,同时可以增加患者缺血预适应能力。如狭窄严重、普通球囊预扩张效果不满意、可使用CB预处理。为减少夹层发生,无论普通球囊、CB还是DCB,操作时均应遵循“低压扩张、慢起慢放”原则,对术者操作的要求较高,当压力升到4 atm后,稍停顿,然后以1 atm/5 s速度慢慢扩张球囊,扩张至6~8 atm,维持30~60 s(视患者耐受情况而定),扩张结束后再缓慢减压。
综上所述,在冠状动脉分支开口病变治疗中,与CB相比,DCB同样具有成功率高、安全、并发症发生率低等优点,同时远期再狭窄率进一步减低,DCB适用于分支开口病变的PCI术。 尽管如此,DCB 仍存在一些问题有待解决, 例如: 关于 DCB 治疗冠状动脉原发病变的研究较少,观察时间短,其证据强度还有待进一步加强; DCB 虽然能有效地抑制血管内膜增生,但不能克服管壁弹性回缩,后者在再狭窄中起着重要作用。因此,目前对DCB需积累更多的临床数据,尤其是中国人群中的研究证据,并在未来不断完善产品的设计。由于本研究样本量小,未进行长期随访,试验结果具有一定局限性,DCB的使用是否具有更大获益尚需进一步的研究。
[1] Medina A, Suárez de Lezo J, Pan M. A new classification of coronary bifurcation lesions. Rev Esp Cardiol, 2006,59(2):183.
[2] Muramatsu T,Tsukahara R,Ho M,et al.Efficacy of directional coronary atherectomy before stent implantation for coronary ostial lesions.J Invasive Cardiol,2000,12(9):440-445.
[3] Brunel P, Martin G, Bressollette E, et al. “Inverted” provisional T stenting, a new technique for Medina 0,0,1 coronary bifurcation lesions: Feasibility and follow-up. EuroIntervention,2010,5(7):814-820.
[4] Zimarino M, Corazzini A, Ricci F, et al. Late thrombosis after double versus single drug-eluting stent in the treatment of coronary bifurcations: A meta-analysis of randomized and observational Studies. JACC Cardiovasc Interv,2013,6(7):687-695.
[5] Muramatsu T, Tsukahara R, Ho M, et al.Effectiveness of cutting balloon angioplasty for small vessels less than 3.0 mm in diameter. J Interv Cardiol,2002,15(4):281-286.
[6] Chung CM, Nakamura S, Tanaka K,et al.Comparison of cutting balloon vs stenting alone in small branch ostial lesions of native coronary arteries. Circ J,2003,67(1):21-25.
[7] 陈韵岱,王建安,刘斌,等.药物涂层球囊临床应用中国专家共识.中国介入心脏病学杂志,2016,24(2):61-67.
[8] Windecker S, Kolh P, Alfonso F, et al. 2014 ESC/EACTS guidelines on myocardial revascularization: the Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS) Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J,2014,31(4):264-267.
[9] Siontis GC, Stefanini GG, Mavridis D, et al. Percutaneous coronary interventional strategies for treatment of in-stent restenosis: a network meta-analysis. Lancet,2015,386(9994):655-664.
[10] Scheller B, Ong PJ, Kleber F. Drug-coated balloon treatment as default strategy for DES-ISR. J Am Coll Cardiol,2016,67(3):346-347.
[11] Unverdorben M, Kleber FX, Heuer H, et al. Treatment of small coronary arteries with a paclitaxel-coated balloon catheter. Clin Res Cardiol,2010,99(3):165-174.
[12] Latib A, Colombo A, Castriota F, et al. A randomized multicenter study comparing a paclitaxel drug-eluting balloon with a paclitaxel-eluting stent in small coronary vessels: the BELLO (Balloon Elution and Late Loss Optimization) study. J Am Coll Cardiol,2012,60(24):2473-2480.
[13] Nomenclature and criteria for diagnosis of ischemic heart disease.Report of the Joint International Society and Federation of Cardiology/World Health Organization Task Force on Standardization of Clinical Nomenclature. Circulation,1979, 59(3):607-609.
[14] Agostoni P, Belkacemi A, Voskuil M,et al. Serial morphological and functional assessment of drug-eluting balloon for in-stent restenotic lesions: mechanisms of action evaluated with angiography, optical coherence tomography, and fractional flow reserve. JACC Cardiovasc Interv,2013,6(6):569-576.
[15] Nishiyama N, Komatsu T, Kuroyanagi T, et al. Clinical value of drug-coated balloon angioplasty for de novo lesions in patients with coronary artery disease. Int J Cardiol,2016,222:113-118.
[16] Gutman D, Golomb G. Liposomal alendronate for the treatment of restenosis. J Control Release,2012,161(2):619-627.
[17] Inoue T, Sakai Y, Hoshi K, et al. Lower expression of neutrophil adhesion molecule indicates less vessel wall injury and might explain lower restenosis rate after cutting balloon angioplasty. Circulation,1998,97(25):2511-2518.
[18] Scheller B, Speck U, Abramjuk C,et al. Paclitaxel balloon coating, a novel method for prevention and therapy of restenosis.Circulation,2004,110(7):810-814.
[19] Bahl R, Indermuehle A, Froehlich GM,et al. Drug-eluting balloon for instent restenosis--the author′s reply. Heart,2013,99(24):1874-1875.
[20] Byrne RA, Neumann FJ, Mehilli J,et al.Paclitaxel-eluting balloons, paclitaxel-eluting stents, and balloon angioplasty in patients with restenosis after implantation of a drug-eluting stent (ISAR-DESIRE 3): a randomised, open-label trial.Lancet,2013,38l (9865):461-467.
Drug-coated balloon in small branch ostial lesions of coronary arteries
ZHAIDong-dong,GAOJu,ZHANGMeng,LIUHong-yu,WANGBin,QUTao.
DepartmentofCardiology,AerospaceCentralHospital,Beijing100049,China
Correspondingauthor:QUTao,Email:qutaol@126.com
Objective To evaluate the safety and efficacy of drug-coated balloon in small branch ostial lesions of coronary arteries(Medina type 0,0,1 lesion). Methods A total of 48 patients were enrolled in the study and they were randomly divided into the Drug-Coated Balloon (DCB) angioplasty group (22 cases) and the Cutting Balloon (CB) angioplasty group (26 cases). They underwent percutaneous coronary intervention ( PCI) with either DCB or with CB in small branch ostial lesions of coronary arteries respectively,The immediate outcomes and long-term efficacy were investigated. Results There were no statistical differences between the two groups in baseline clinical date before PCI. There were no coronary perforation, pericardial tamponade, acute thrombotic events in the two groups. There was no significant difference in minimal lumen diameter (MLD) immediately after PCI between the two groups.During follow-up angiography,the MLD in the DCB group was significantly larger than in the CB group [(1.8±0.2)mmvs. (1.5±0.3) mm,P=0.006]. There were no death, nonfatal myocardial infarction or revascularization recorded in the groups during 6 months of follow-up. Conclusion The immediate outcomes between DCB and CB were similar in small branch ostial lesions for coronary arteries angioplasty.The long-term efficacy of DCB angioplasty is better than CB angioplasty.
Percutaneous coronary intervention; Cutting balloon; Drug coated balloon; Small branch ostial lesions
10.3969/j.issn.1004-8812.2017.07.005
中国航天科工集团公司医疗卫生科研项目(2016-LCYL-005)
100049 北京,航天中心医院心脏医学部
曲涛,Email: qutaol@126.com
R541.4
2017-01-23)
