C@MnO2复合材料的制备及电化学性能研究
2017-08-07王建芳徐杰王君
王建芳,徐杰,王君
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
C@MnO2复合材料的制备及电化学性能研究
王建芳,徐杰,王君
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
采用微孔纳米碳球为硬模板,KMnO4为锰源,制备了具有核壳结构的纳米复合材料C@MnO2。首先以八苯基倍半硅氧烷为前驱体制得微孔含硅碳球xph-C-Si,除硅后得到微孔碳球xph-C。其次将所得微孔碳球xph-C在0.5 mol·L-1KMnO4溶液中进行氧化锰壳层包覆反应,最终制得C@MnO2复合材料。该复合材料为球形颗粒,尺寸约为200 nm左右。材料具有良好的分散性,其内部呈现出有序的微孔结构。采用三电极体系,在1 mol·L-1硫酸钠电解液中对C@MnO2电极材料进行循环伏安测试,该材料表现出较高的比电容值,在5 mV·s-1的扫速下,C@MnO2电极材料的电容值为286 F·g-1。
氧化锰;微孔碳;核壳结构;复合材料
随着全球人口增长和经济快速发展,环境污染问题(温室效应、酸雨、雾霾)及能源短缺问题相继而生,急需开发清洁、高效、可再生的新型能源替代传统化石能源(煤炭、石油、天然气)[1-2]。超级电容器是一种新型的储能器件,具有超高比电容和较大的功率密度、充放电效率高、循环寿命长、使用温度范围宽、环境友好等优点,成为当前最重要的储能器件之一[3-4]。寻找价格低廉、结构稳定、性能优异的电化学电容器电极材料是该领域研究的热点之一。
氧化锰是过渡金属氧化物之一,在自然界储量丰富、环境友好、结构多样,具有较高的赝电容而用作超级电容器电极材料。但由于其电子传导率低、电荷转移电阻大、循环可逆性差,影响了该类物质效能的发挥[5-6]。作为超级电容器电极材料之一,碳材料比表面积大,具有良好的导电性和机械性能,基于双电层储能机理将电荷存储在电极与电解质溶液界面处的双电层中,但其质量比电容较低[7-9]。大量的研究工作表明,通过不同的反应技术将碳材料与氧化锰材料进行复合,有效发挥了二者的赝电容和双电层电容的协同效应,材料的电导率和循环稳定性得到大幅提高[10-11]。作为负载基体碳材料,研究多数选择碳纳米管、石墨烯、碳黑颗粒,而具有微孔结构且大比表面积的碳材料却少有研究。
在本研究中,选择大比表面积的有序微孔结构碳球为反应基体,运用氧化还原反应原理制备了具有核壳结构的C@MnO2的纳米复合材料。采用三电极体系,通过循环伏安法测试了C@MnO2电极材料的比电容。
1 材料与方法
1.1 试剂与仪器
实验中所用试剂均为分析纯。八苯基笼型倍半硅氧烷购自梯希爱试剂公司,1,2-二氯乙烷,四氯化碳,无水氯化铝,无水乙醇,高锰酸钾均购自上海国药试剂有限公司。所有试剂原料均未经过预处理直接使用。
1.2 材料的制备
1.2.1 微孔纳米碳球的制备
根据文献[12],将0.5 g的八苯基笼型倍半硅氧烷(ph-Poss)溶解于50 mL的1,2-二氯乙烷中,80℃磁力搅拌条件下进行回流。加入2 g无水氯化铝(AlCl3)催化剂,20 mL四氯化碳(CCl4)作为交联剂,经过Friedel-Crafts交联反应。回流反应12 h后,加入95%乙醇/水混合溶液100 mL(乙醇/水=80 mL:20 mL)终止反应。将所得沉淀过滤,95%乙醇/5%稀盐酸(150 mL/50 mL)和纯水洗涤,100℃干燥8 h,得到聚合物聚八苯基笼型倍半硅氧烷,标记为xph-Poss。将所得xph-Poss在N2气流中900℃碳化3 h,加热速率为5℃·min-1,得到含硅的纳米碳球xph-C-Si,进一步在HF(40%)处理8 h,得到有序微孔纳米碳球xph-C。
1.2.2 C@MnO2复合材料的制备
取0.018 g xph-C微孔纳米碳球,分散到浓度为0.06 mol·L-150 mL的高锰酸钾(KMnO4)溶液中,室温搅拌4 h,抽滤,50℃干燥12 h,得到最终产物C@MnO2复合材料。
1.3 分析与表征
采用D/Max–3cX射线粉末衍射仪对样品进行XRD物相分析,测试条件:Cu靶Kα线,Ni滤波,电压40 kV,电流30 mA,扫描范围3°~70°(2θ),扫描速度8°·min-1;样品的表面形貌观察所用的仪器是日本日立公司TM 3000;透射电镜(TEM)图像采用JEM-2100仪器进行观察。
将制备的C@MnO2复合材料作为活性物质(80%)、乙炔炭黑和导电剂进行均匀混合,聚偏二氟乙烯乳液为粘结剂,电极活性物质、乙炔黑和粘结剂的质量比为80:15:5,研磨混合均匀的黑色浆状物质,将其吸附至孔泡沫镍基体上进行干燥形成工作电极。采用三电极体系在电化学分析工作站上进行测试。
2 结果与分析
2.1 C@MnO2的形貌与晶相结构
图1为所得目标产物C@MnO2复合材料的SEM图与XRD图谱。

图1 所得产物C@MnO2
从图1(a)可以看出,所得材料呈现球形分布,颗粒大小基本均匀,尺度约为350 nm。在XRD图谱中,出现于2θ=23.9°的宽化衍射峰对应于石墨碳(002)晶面[13],说明聚八苯基笼型倍半硅氧烷在高温热处理过程中形成了石墨碳结构的纳米碳球。在2θ=36°出现的微弱衍射峰对应于层状氧化锰的(002)晶面[14],说明在室温搅拌过程中高锰酸钾与碳材料反应形成了二氧化锰,宽化且微弱的衍射峰表明C@MnO2复合材料中二氧化锰结晶度较低。
2.2 所得产物的微观结构分析
图2为包覆前后材料的透射电镜图。从图2(a)可以看出,碳材料xph-C中可观察到纳米孔洞结构,说明硅去除以后形成了均匀分布的微孔结构。通过氧化锰包覆以后,可以看到球形表面附近附着了一层颗粒状异质结构材料,说明碳材料与KMnO4溶液反应后形成了一层氧化锰(图2(b))。

图2 所得产物的TEM图
2.3 不同阶段所得产物的表征分析
对不同阶段产物的形貌和结构变化进行了跟踪分析。图3为不同反应阶段产物的SEM图。

图3 不同阶段所得产物的SEM图
由图3可见,对比观察表明,产物的形态均呈现球形颗粒,分布较为均匀。图3(a)为单体八苯基笼型倍半硅氧烷(ph-Poss)发生交联聚合反应后生成产物聚八苯基笼型倍半硅氧烷(xph-Poss)的SEM图,球形颗粒的聚合有利于后续纳米碳球的形成。经过900℃碳化处理3 h,球形形貌保持但尺寸显著减小,说明碳化过程中有机骨架发生塌陷而使体积皱缩(图3(b))。xph-Poss在HF(40%)中处理除硅过程中,所得产物微孔纳米碳球xph-C为大小分布均匀的球形形貌(图3(c))。通过在KMnO4溶液中对微孔纳米碳球进行氧化锰的包覆,保持了前驱体微孔纳米碳球的球形形貌,具有较好的分散性且尺寸略有增大(图3(d))。
进一步对不同阶段所得产物进行了晶相结构分析,结果如图4所示。从图4中可以看出含硅的纳米碳球xph-Poss-Si表现为Si以无定形SiO2形态存在(图3(a))[12]。在HF溶液中对硅进行去除后,2θ=24°左右的衍射包强度发生显著降低,同时衍射峰向低角度方向移动,说明SiO2得到有效去除同时形成了纳米碳球xph-C(图3(b))。二氧化锰的包覆后,碳材料的衍射峰几乎完全消失,说明氧化锰对纳米碳球xph-C进行了较大程度的包覆(图3(c))。
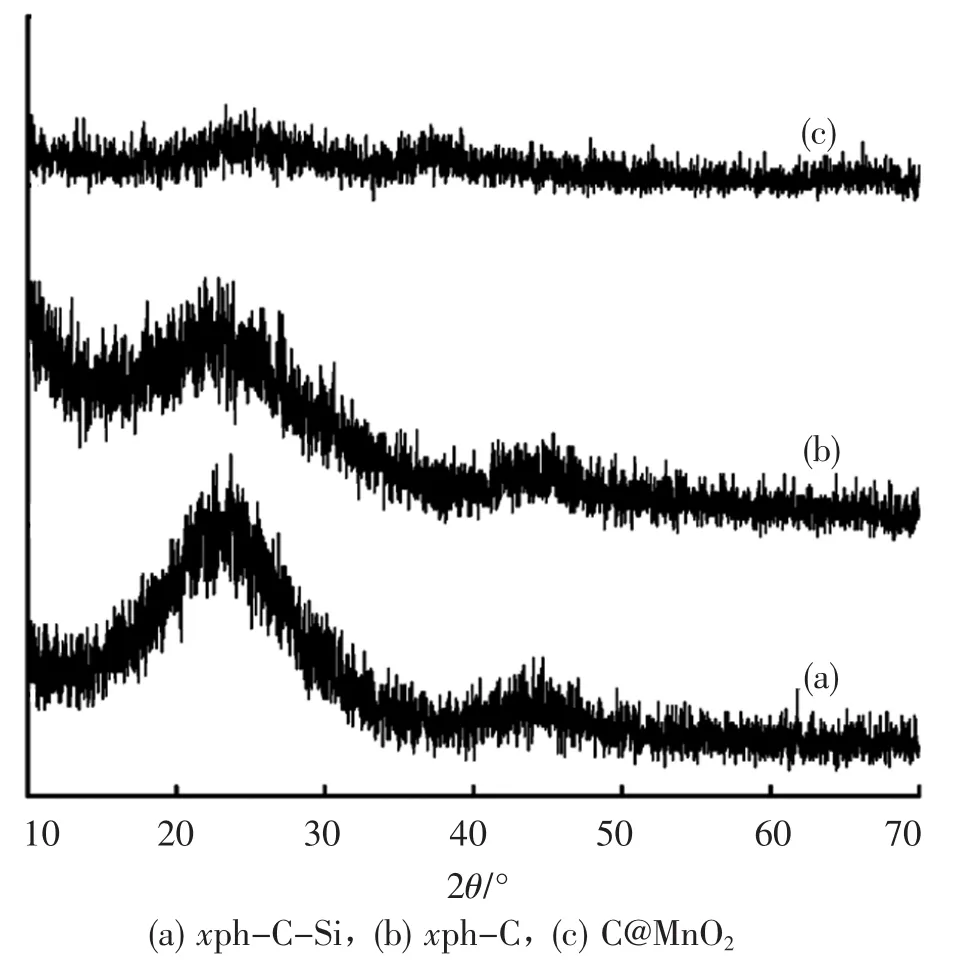
图4 不同阶段所得产物的XRD图谱
2.4 所得产物的电化学分析
在5 mV·s-1的扫速下,采用三电极体系在1 mol·L-1Na2SO4电解质溶液中对电极材料xph-C、C@MnO2进行循环伏安测试,所得循环伏安曲线如图5所示。计算结果表明二者的电容值分别为40 F·g-1和286 F·g-1。包覆二氧化锰后,电容值大大提高,循环伏安曲线接近于矩形,说明C@MnO2具有很高的反应活性和高倍率可逆性,微孔碳球的存在使赝电容特性的氧化锰材料兼具了双电层电容的特征,丰富且均匀的孔道结构有利于电解液向电极表面的扩散,从而提高电极材料的有效利用率。

图5 MnO2包覆前后所得材料的循环伏安测试
不同扫速下的循环伏安曲线如图6(a)所示,当扫速增加到10、20、50 mV·s-1时,电容值分别依次减小为256、220、161 F·g-1,扫速增加使得电解液中的Na+来不及进入C@MnO2复合材料的内部孔道结构,电极反应仅仅发生在材料的外表面,从而使电容量降低[15]。为进一步研究C@MnO2复合电极材料的充放电可逆性,进行了充放电测试,其结果如图6(b)所示。电流密度分别为0.5、1、2、5 A·g-1时,电容值分别为144、134、124、105 F·g-1。充放电曲线表现为较对称的三角形,说明充放电时间基本均等,电极材料具有良好的充放电可逆性。
3 结论
以八苯基倍半硅氧烷(ph-Poss)为碳源,通过先交联后碳化的方式制备了尺度均一的微孔纳米碳球。之后在高锰酸钾溶液中反应制备了C@MnO2复合材料。研究结果表明C@MnO2复合材料的形貌基本呈球形,相比碳球尺寸有所增大,具有较好的分散性。采用三电极体系在1 mol·L-1Na2SO4电解质中对电极材料xph-C-Si、C@MnO2进行循环伏安测试,计算结果表明二者的电容值分别为40 F·g-1和286 F·g-1,氧化锰与微孔碳球的包覆结合,显著增大了碳材料的比电容值,提高了电极材料的有效利用率,为组装超级电容器提供了一类新的电极材料。
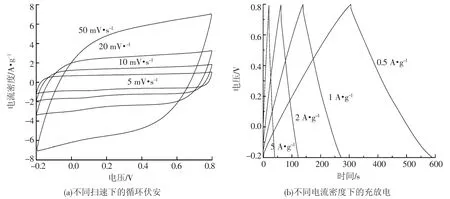
图7 所得产物C@MnO2电化学测试
[1]YANG Z G,ZHANG J L,KINTNER-MEYER M C W,et al.Electrochemical energy storage for green grid[J].Chemical Reviews,2011,111:3577-3613.
[2]YU G H,XIE X,PAN L J,et al.Hybrid nanostructured materials for high-performance electrochemical capacitors[J].Nano Energy,2013,2:213-234.
[3]WEI W,CUI X,CHEN W,et al.Manganese oxidebased materials as electrochemical supercapacitor electrodes[J].Chemistry Society Review,2011,40:1697-1721.
[4]DYER A,PILLINGER M,NEWTON J,et al.Sorption behavior of radionuclides on crystalline synthetic tunnel manganese oxides[J].Chemistry of Materials,2000,12:3798-3804.
[5]MAS,AHNK,LEEE,etal.Synthesisand characterization of manganese dioxide spontaneously coated on carbon nanotubes[J].Carbon,2007,45:375-382.
[6]FISCHER A,PETTIGREW K,ROLISON D,et al.Incorporation of homogeneous,nanoscale MnO2with in ultraporous carbon structures via self-limiting electroless deposition:implications for electrochemical capacitors[J].Nano Letters,2007,7:281-286.
[7]LEI Z,CHRISTOV N,ZHAO X S.Intercalation of mesoporous carbon spheres between reduced graphene oxide sheets for preparing high-rate supercapacitor electrodes[J].Energy&Environmental Science,2011,4:1866-1873.
[8]YAN J,WEI T,SHAO B,et al.Electrochemical properties of graphene nanosheet/carbonblack composites as electrodes for supercapacitors[J].Carbon,2010,48:1731-1737.
[9]WANG G,SUN X,LU F,et al.Flexible pillared graphene-paper electrodes for high-performance electrochemical supercapacitors[J].Small,2012,8:452-459.
[10]LEI Z,SHI F,LU L.Incorporation of MnO2-coated carbon nanotubes between graphene sheets as supercapacitor electrode[J].ACS Applied Materials&Interfaces,2012,4:1058-1064.
[11]QU D,WEN J,LIU D,et al.Hydrogen ion supercapacitor:a new hybrid configuration of highly dispersed MnO2in porous carbon coupled with nitrogen-doped highly ordered mesoporous carbon with enhanced H-insertion[J].ACS Applied Materials&Interfaces,2014,6:22687–22694.
[12]LI Z H,WU D C,LIANG Y R,et al.Synthesis of welldefined microporous carbons by molecular-scale[J].Journal of the American Chemical Society,2014,136:4805-4808.
[13]LEI Z B,SHI F H,LU L,et al.Incorporation of MnO2-coated carbon nanotubes between graphene sheets as supercapacitor electrode[J].ACS Applied Materials Interfaces,2012,4:1058-1064.
[14]WANG J F,ZHANG G N,REN L J,et al.Topochemical oxidation preparation of regular hexagonal manganese oxide nanoplates with birnessite-type layered structure[J].Crystal Growth&Design,2014,14:5626-5633.
[15]YANG X,WANG Y,XIONG H,et al.Interfacial synthesis of porous MnO2and its application in electrochemical capacitor[J].Electrochimica Acta,2007,53:752-757.
(责任编辑:张国春)
The Synthesis of C@MnO2Composite and Its Capacitance Performance
WANG Jian-fang,XU Jie,WANG Jun
(College of Chemical Engineering and Modern Materials/Shaanxi Key Laboratory of Comprehensive Utilization of Tailings Resources,Shangluo University,Shangluo 726000,Shaanxi)
The nanocomposite materials C@MnO2with core-shell structure are prepared by adopting microporous carbon nanosphere in KMnO4solution.Firstly,microporous carbon spheres are prepared by using eight phenyl silsesquioxane as precursor,then microporous carbon are reacted with 0.5 mol·L-1KMnO4to form C@MnO2.The nanocomposite C@MnO2shows sphere-like morphology with the particle size about 200 nm,which shows good dispersity and regular microporous structure.The electrochemical property of as–prepared C@MnO2has been tested by cyclic voltammetry in 1 mol·L-1Na2SO4solution,which exhibits high specific capacitance of 286 F·g-1at 5 mV·s-1.
manganese oxide;microporous carbon;core-shell structure;composite materials
TB33
:A
:1674-0033(2017)04-0028-05
10.13440/j.slxy.1674-0033.2017.04.007
2017-05-13
国家级大学生创新创业训练计划项目(201611396022);商洛学院科研基金项目(16SKY017)
王建芳,女,山西曲沃人,博士,副教授
