内镜下切除巨大胃间质瘤8例分析
2017-08-07邹白仓马师洋
张 莉,邹白仓*,马师洋,董 蕾,杨 军
(1西安交通大学第二附属医院消化内科,西安 710004;2西安交通大学第二附属医院病理科;*通讯作者,E-mail:zoubaicang@sohu.com)
内镜下切除巨大胃间质瘤8例分析
张 莉1,邹白仓1*,马师洋1,董 蕾1,杨 军2
(1西安交通大学第二附属医院消化内科,西安 710004;2西安交通大学第二附属医院病理科;*通讯作者,E-mail:zoubaicang@sohu.com)
目的 探讨内镜下切除胃巨大间质瘤的可行性。 方法 回顾分析2014-07~2016-07在西安交通大学第二附属医院接受内镜下切除治疗的胃巨大间质瘤(直径>3 cm)患者的临床资料,所有患者术前均行EUS检查,对手术方式、完整切除率及术中、术后并发症情况进行分析。 结果 8例(男性5例,女性3例)标本最大直径均超过3 cm的患者接受了内镜下黏膜下挖除术(ESE)、内镜下全层切除术(EFTR)治疗或内镜下经隧道切除术(STER)。其中7例(87.5%)完整切除,1例因出血术中转外科行手术治疗。完整切除的患者中,有1例标本因体积过大难以通过贲门,在胃腔内进行切割后取出,2例患者因标本质脆,通过贲门时发生破裂,1例患者因术后迟发出血接受内镜止血。 结论 内镜下切除直径超过3 cm的巨大胃间质瘤,技术上可行,但可能无法保证标本的完整,对术中出现严重并发症的患者,需外科手术补救治疗。
胃间质瘤; 消化内镜; 超声内镜
随着内镜下黏膜切除术(endoscopic submucosal dissection,ESD)技术的发展,胃的黏膜下肿瘤也可经内镜下切除[1]。对于起源于黏膜肌层及黏膜下层的肿瘤可直接采用ESD切除,而对于位于固有肌层及向浆膜生长的肿瘤,则需采用内镜下黏膜下挖除术(endoscopic submucosal excavation,ESE)及内镜下全层切除术(endoscopic full-thickness resection,EFTR)来完成;对于位于贲门附近的肿瘤,还可借助隧道技术,予以内镜下切除(sub-tunnel endoscopic resection,STER)[1,2]。我院内镜中心对8例超过3 cm的巨大胃间质瘤(gastrointestinal stromal tumor,GIST)行内镜下切除,分析如下。
1 资料及方法
1.1 材料及设备
内镜下切除及复查采用PANTAX EG29-i10内镜,超声内镜采用PANTAX EG-3270UK(线阵)、EG-3670UK(环扫),频率5-10 Hz(常用频率7.5 Hz)(Pantax medical Corporation,Tokyo Japan);超声主机为HITACHI EZU-MT-29-S1(Hitachi medical Corporation,Tokyo Japan),电切刀采用KD-650L Duer Knife及KD-611L IT2 Knife,热止血钳为FD-410LR Coagspur (Olympus Co.,Ltd,Tokyo Janpan);ERBE高频电工作站(ERBE,Tübingen,German),HXROCC-D-26-195和谐夹(南京微创Micro-Tech(Nanjing)Co.,Ltd),CO2气泵供气,黏膜下注射液为5%果糖氯化钠溶液250 ml+肾上腺素2 mg+亚甲蓝溶液0.5 ml。
1.2 纳入患者
回顾分析2014-07~2016-07在西安交通大学第二附属医院消化内科因胃巨大间质瘤行内镜下切除术的8例患者的临床资料,对手术方式、完整切除率及术中、术后并发症情况进行分析。纳入标准为:①术后病理证实为间质瘤;②病变最大直径超过3 cm。所有患者入院后完成包括心电图、血常规、凝血功能,肝肾功能等术前常规检查,术前行超声内镜(endoscopic ultrasonography,EUS)检查,术前告知手术大致操作流程及风险并签署知情同意书。
1.3 手术方法
均在气管插管全身麻醉下进行,对于靠近贲门病变采用STER,手术步骤为:①以病变上方3-5 cm食管下段为隧道入口,黏膜下注射液体后,纵行切开黏膜;②黏膜下分离形成隧道;③隧道内切除瘤体;④瘤体自隧道取出;⑤钛夹封闭隧道口。对于不宜采用STER的患者,根据病变深度选用ESE或EFTR。手术步骤:①点状标记病变范围;②黏膜下注射后,环周切开病变表面黏膜;③对主要位于黏膜下层或固有肌浅层的病变,黏膜下完整剥离病变,即为ESE;起源于固有肌层深层或向腔外生长的病变,采用全层切除,即为EFTR;④缝合创面。切除标本回收、固定,行组织病理学检查。
术后所有患者禁饮食,ETFR患者予以胃肠减压;预防性抗感染,原则上时间不超过72 h;质子泵抑制剂(proton pump inhibitor,PPI)静滴2次/d;退热、止痛等对症处理。术后48-72 h复查内镜,如无异常情况,患者逐步恢复饮食。
1.4 随访
术后1月、3月、6月、1年行内镜复查,以后每年复查胃镜1次。对于复发风险中度以上的患者建议口服甲磺酸伊马替尼,并于复查时行胸部、腹部及盆腔CT检查,排除复发及转移。
2 结果
2.1 患者资料
8例患者包括男性5例,女性3例,平均年龄(55.5±15.2)岁(42-73岁),临床资料见表1。
表1 纳入的8例患者的临床资料
Table 1 The clinical data of 8 patients with GIST
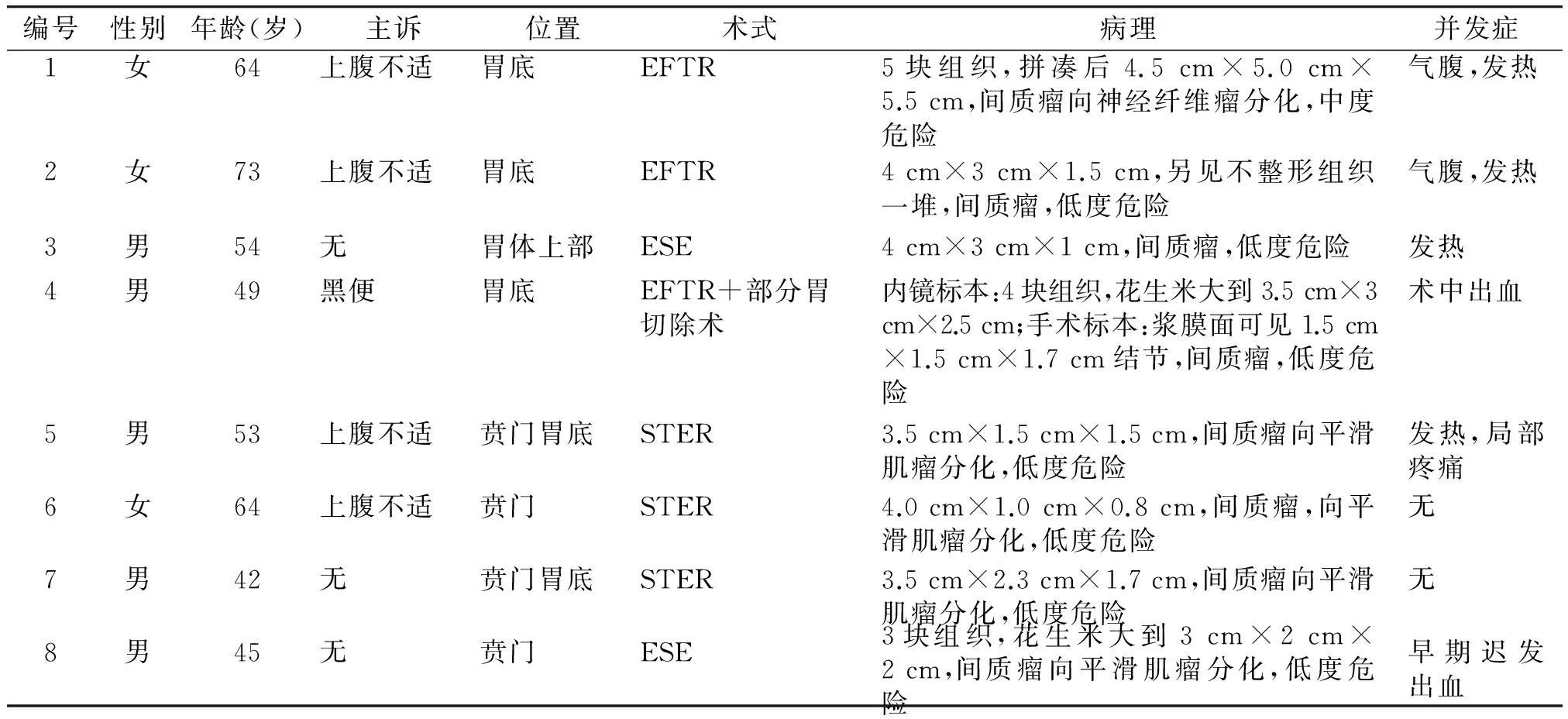
编号性别年龄(岁)主诉位置术式病理并发症1女64上腹不适胃底EFTR5块组织,拼凑后4.5cm×5.0cm×5.5cm,间质瘤向神经纤维瘤分化,中度危险气腹,发热2女73上腹不适胃底EFTR4cm×3cm×1.5cm,另见不整形组织一堆,间质瘤,低度危险气腹,发热3男54无胃体上部ESE4cm×3cm×1cm,间质瘤,低度危险发热4男49黑便胃底EFTR+部分胃切除术内镜标本:4块组织,花生米大到3.5cm×3cm×2.5cm;手术标本:浆膜面可见1.5cm×1.5cm×1.7cm结节,间质瘤,低度危险术中出血5男53上腹不适贲门胃底STER3.5cm×1.5cm×1.5cm,间质瘤向平滑肌瘤分化,低度危险发热,局部疼痛6女64上腹不适贲门STER4.0cm×1.0cm×0.8cm,间质瘤,向平滑肌瘤分化,低度危险无7男42无贲门胃底STER3.5cm×2.3cm×1.7cm,间质瘤向平滑肌瘤分化,低度危险无8男45无贲门ESE3块组织,花生米大到3cm×2cm×2cm,间质瘤向平滑肌瘤分化,低度危险早期迟发出血
2.2 手术情况
2.2.1 手术方式及切除率 3例患者采用STER,2例ESE,3例EFTR,7例完全切除,1例EFTR患者因术中出血转外科手术治疗(病例4,见图1),切除率为87.50%。3例患者完整切除肿瘤后,在标本取出胃腔过程中出现标本破裂,其中1例为标本过大(直径约5 cm),无法通过贲门,在胃腔内以圈套器切割(病例1,见图2)后经食管取出,另2例均因标本质脆,圈套器取出时破裂(病例2,病例8)。
2.2.2 EUS结果与手术相符情况 均为固有肌层的低回声占位,其中3例回声不均,7例(87.50%)测量的肿瘤大小与术后标本相符(相差<5 mm),1例差别较大,最大直径相差2 cm(病例1)。
2.2.3 并发症及处理 严重并发症主要包括穿孔和出血(各2例)。ETFR为主动穿孔,均术中缝合,对于较大的类圆形创面,采用钛夹与尼龙圈的荷包缝合(见图2)。出血2例,1例为术中出血(病例4),开腹后发现腹腔积血约400 ml,转外科手术治疗;另1例为24 h内出现早期迟发出血,内镜下成功止血(病例8);轻微不良反应有发热、术后局部疼痛等,均对症处理后消失。
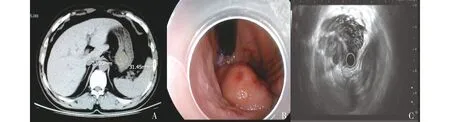
A.上腹CT平扫见近贲门处瘤体,大小约27 mm×31 mm;B.内镜下见胃底穹窿部巨大隆起性病变,表面黏膜充血、糜烂;C.EUS示固有肌层低回声不均质占位,边缘呈高回声,中央有坏死区。图1 病例4的胃巨大间质瘤的CT、内镜及EUS图像Figure 1 The CT scan,endoscopic and EUS views of the large gastric GIST in case 4
2.3 随访
平均随访14±11.3月(3-28个月),所有患者未发现复发及转移。
2.4 典型病例
2.4.1 病例1资料 女,62岁,以上腹不适10余天主诉入院。胃镜检查发现胃底近前壁巨大隆起,超声内镜检查提示固有肌层最大截面约35 mm×25 mm,回声欠均匀的低回声占位。与主管医生、患者家属及外科沟通后行内镜下切除术。术中见瘤体位于固有肌层,胃腔内瘤体约3 cm,并向腔外生长,全层切除瘤体及胃壁,透过创面可见腹腔脏器及网膜;以钛夹、尼龙圈行双荷包缝合。但标本太大且质硬,无法通过贲门,遂以圈套器在胃腔内将标本分割为5块后取出。拼凑复原瘤体形态,测量大小约4.5 cm×5.0 cm×5.5 cm。术后4 d复查胃镜见创面无出血、穿孔,嘱患者进流食,1周后出院。术后病理示中危间质瘤。患者拒绝服用靶向药物,密集随访未见复发。
分析:①超声胃镜因探头方向等因素,有时对间质瘤大小的判断不够准确;②巨大间质瘤内镜下切除技术可行,术后的巨大创面可内镜下完全缝合,患者禁食时间及住院周期与一般患者差距不大;③过于巨大的标本,会出现贲门、食管通过困难,人为切割标本理论上增加了复发的风险。
2.4.2 病例4 男,47岁,以间断黑便20余天主诉入院。入院后行上腹CT检查示胃底占位,直径约3 cm。胃镜检查见胃底穹窿部隆起性病变,EUS示固有肌层低回声不均质病变,中央坏死、边缘高回声。考虑该病变超过2 cm,且有症状(黑便),并有超声内镜可见的危险因素(回声不均一,有坏死),有外科手术指征。但患者要求内镜下治疗,术中见病变向腔内及腔外生长,切除腔内部分,已经出现穿孔,且浆膜面出血难以控制,立即转外科行手术治疗。术中见腹腔积血400 ml,胃壁有直径4 cm的穿孔,创面边缘有2 cm的残留肿瘤组织。术后病理提示中度危险,建议予以c-kit靶向甲磺酸伊马替尼口服,定期复查胃镜及上腹CT。
分析:随着瘤体体积的增大,内镜下切除的难度增加,且术后复发风险增加。对于较大的尤其向腔内及腔外生长的病例,全层切除几乎不可避免。术前与患者及外科充分沟通,做好遇到内镜下难以处理的情况,转外科手术的准备。
3 讨论
GIST为起源于胃肠道肌层的最常见间叶性肿瘤,其中60%的GIST分布于胃,其次为小肠(30%)、直肠(5%),其余为结肠和食管[3-5]。GIST常无症状,而在胃镜检查时偶然发现,也有患者有消化道出血、腹痛、腹部包块等临床表现[6]。根据细胞类型,GIST可分为梭状细胞型、上皮样细胞型及混合细胞型[3-7]。GIST的危险度主要指手术切除后的复发风险,2008年后,美国国立卫生研究院(National Institute of Health,NIH)根据肿瘤部位、直径、核分裂像和肿瘤破裂将GIST分为极低危险、低度危险、中度危险和高度危险4级,中度以上的患者较低度及极低度患者存在明显的预后差异,并建议中危以上的应接受靶向药物治疗[8,9]。国外及我国的外科治疗专家共识[8,10-12]均未将内镜治疗作为推荐的方案,主要考虑有出血、穿孔、肿瘤残余及破裂的风险。但随着ESD相关技术的发展,出现了大量的黏膜下肿瘤内镜下切除的报道[13-17]。有学者认为内镜治疗GIST指征为:肿瘤直径<3 cm;边界清晰、质地均匀;腔内型生长为主;无消化道外侵及转移征象[4]。然而内外专家[17,18]均报道了无腹腔镜辅助的内镜切除巨大黏膜下肿瘤的经验,其中Zhou等[16]报道的间质瘤直径达到4.6 cm,Bona等[17]报道的最大肿瘤达12 cm。本研究中直径超过3 cm的间质瘤内镜下切除率为87.5%,切除的最大标本为5.5 cm,说明内镜下切除技术上可行,腔外生长、穿孔风险都不再是内镜治疗的禁忌。
标本取出困难是直径超过3 cm的肿瘤内镜下切除后所面对的主要问题,因此有学者建议对此类肿瘤应考虑内镜-腹腔镜联合操作。本研究中有3例患者虽然完整切除,但在标本回收时出现了主动或被动的破裂,按照NIH标准及NCCN指南,复发风险即应划为高度危险[8,11]。但在严密缝合后的胃腔内发生破裂,其种植、复发的风险是否等同于开腹手术,有待探讨。标本取出时采用网篮,通过贲门时向一个方向旋转镜身,是减少肿瘤破裂的有效手段。
GIST的诊治需要多学科的参与(multiple disciplinary team,MDT)[18],团队中除了要有外科与肿瘤科医师外,内镜师也应参与到整个诊断与治疗过程中来。内镜下切除比外科手术具有创伤小、恢复快、住院时间短。本研究表明对于较大的间质瘤内镜下可以根据病变的位置及深浅,通过选择合适的术式而达到完整切除,但术后标本的回收方法仍可进一步改进。对于较大的、内镜下切除可能存在困难的患者,可在术前与外科取得联系,以便外科及时补救治疗。
[1] 许昌芹,张澍田.上消化道黏膜下肿瘤内镜治疗进展[J].中国内镜杂志,2015,21(3):279-283.
[2] 钟芸诗,齐志鹏,时强.胃肠间质瘤内镜治疗值得关注的几个问题[J].中国实用外科杂志,2015,35(4):378-381.
[3] Miettinen M,Lasota J.Gastrointestinal stromal tumors(GISTs):definition,occurrence,pathology,differential diagnosis and molecular genetics [J].Pol J Pathol,2003,54(1):3-24.
[4] Miettinen M,Lasota J.Gastrointestinal stromal tumors:pathology and prognosis at different sites[J].Semin Diagn Pathol,2006,23(2):70-83.
[5] 侯英勇,朱雄增.胃肠道间质瘤的组织发生及命名[J].中华病理学杂志,2000,29(6):453-454.
[6] 赵海潞,李红芬,王淑琴,等.162例胃肠道间质瘤的临床病理学及免疫表型特征[J].中华肿瘤杂志,1998,20(4):313-315.
[7] CSCO胃肠间质瘤专家委员会.中国胃肠间质瘤诊断治疗专家共识(2013年版)[J].临床肿瘤病学杂志,2013,18(11):1025-1032.
[8] Joensuu H.Risk stratification of patients diagnosed with gastrointestinal stromal tumor[J].Hum Pathol,2008,39(10):1411-1419.
[9] Fletcher CD,Beman JJ,Corless C,etal.Diagnosis of gastrointestinal stromal tumors:a consensus approach[J].Hum Pathol,2002,33(5):459-465.
[10] 曹晖,汪明.NCCN《软组织肉瘤——胃肠间质瘤临床实践指南(2015年第1版)》更新介绍与解读[J].中国实用外科杂志,2015,35(6):599-603.
[11] 中华医学会外科学分会胃肠外科学组.胃肠间质瘤规范化外科治疗专家共识[J].中国实用外科杂志,2015,35(6):593-598.
[12] Nishida T,Kawai N,Yamaguchi S,etal.Submucosal tumors:comprehensive guide for the diagnosis and therapy of gastrointestinal submucosal tumors[J].Dig Endosc,2013,25(5):479-489. [13] Chun SY,Kim KO,Park DS,etal.Endoscopic submucosal dissection as a treatment for gastric subepithelial tumors that originate from the muscularis propria layer:a preliminary analysis of appropriate indications[J].Dig Dis Sci,2013,58(6):1710-1716.
[14] Catalano F,Rodella L,Lombardo F,etal.Endoscopic submucosal dissection in the treatment of gastric submucosal tumors:results from a retrospective cohort study[J].Gastr Cancer,2013,16(4):563-570.
[15] Liu BR,Song JT,Qu B,etal.Endoscopic muscularis dissection for upper gastrointestinal subepithelial tumors originating from the muscularis propria[J].Surg Endosc,2012,26(11):3141-3148.
[16] Zhou PH,Yao LQ,Qin XY,etal.Endoscopic full-thickness resection without laparoscopic assistance for gastric submucosal tumors originated from the muscularis propria[J].Surg Endosc,2011,25(9):2926-2931.
[17] Bona D,Aiolfi A,Siboni S,etal.Giant leiomyoma of thegastroesophageal junction:technique and results of endoscopicfull-thickness resection[J].Clin Exp Gastroenterol,2011,1(4):263-267.
[18] Mullady DK,Tan BR.A multidisciplinary approach to the diagnosis and treatment of gastrointestinal stromal tumor[J].J Clin Gastroenterol,2013,47(7):578-585.
Endoscopic ultrasonograpy-assisted endoscopic resection for large gastric gastrointestinal stromal tumor in 8 cases
ZHANG Li1,ZOU Baicang1*,MA Shiyang1,DONG Lei1,YANG Jun2
(1DepartmentofGastroenterology,SecondAffiliatedHospitalofXi’anJiaotongUniversity,Xi’an710004,China;2DepartmentofPathology,SecondAffiliatedHospitalofXi’anJiaotongUniversity;*Correspondingauthor,E-mail:zoubaicang@sohu.com)
ObjectiveTo explore the feasibility of endoscopic ultrasonography(EUS)-assisted endoscopic resection in treatment of large gastric gastrointestinal stromal tumor(GIST).MethodsClinical and pathological records of 8 patients with large gastric GIST(diameter of the tumor >3 cm)who underwent endoscopic resection from July 2014 to July 2016 were analyzed retrospectively. All the patients accepted EUS before endoscopic surgery.The methods of resection,en block resection rate and complications during and after surgeries were analyzed.ResultsEight patients(5 male and 3 female)underwent sub-tunnel endoscopic resection(STER),endoscopic submucosal excavation(ESE)or endoscopic full-thickness resection(EFTR).Seven patients accomplished the surgery,and one was transferred to open surgery(partial gastrectomy)due to hemorrhage during operation.Among the patients with en block resection,one specimen was too big to get though cardia,so snare incision was performed,and two fragile specimens were ruptured during getting through cardia.Late hemorrhage occurred in one case and endoscopic homeostasis was performed.ConclusionIt is feasible to perform endoscopic resection of large gastric GIST,but the wholeness of the specimen could not be guaranteed.For those who suffer from severe adverse events,the salvage surgery would be necessary.
gastrointestinal stromal tumor; endoscopy; endosonograpgy
国家星火计划项目(2011GAB5001)
张莉,女,1976-09生,博士,主治医师,E-mail:spinesurgeon@126.com
2016-12-24
R735.2
A
1007-6611(2017)04-0357-05
10.13753/j.issn.1007-6611.2017.04.012
