有关艾滋病的常见认识误区与最新发现
2017-08-07许凡
许 凡
(广东省深圳第二外国语学校 518110)
中国疾控中心数据显示,截至2016年9月,我国报告存活HIV感染者和病人65.4万例,累计死亡20.1万例;国内目前仍有32.1%的感染者未被发现;近5年我国大中学生HIV感染者年增35%。对于传染病而言,预防胜于治疗,预防的关键在于疾病预防及治疗知识的普及,而学校教育是最有效的普及途径之一。本文对5个广为误解的艾滋病知识进行分析,并介绍一些最新研究成果,以期加深对艾滋病的认识和了解。
1 对艾滋病的常见认识误区
1.1 误认为HIV感染者就是艾滋病(AIDS)患者 HIV(human immunodeficiency virus)即人类免疫缺陷病毒,是一种逆转录病毒,它通过入侵人类免疫细胞,摧毁或损害其功能,使人逐步丧失免疫功能,但感染初期没有症状。HIV包含HIV-1和HIV-2两种类型。HIV-1是引起全世界绝大多数HIV感染的病毒类型。
AIDS(human immunodeficiency virus infection and acquired immune deficiency syndrome)即艾滋病,中文名是获得性免疫缺陷综合征,是HIV病毒感染的最后阶段。发病后,患者体内CD4+T淋巴细胞已经少于200个/μL,免疫系统无法正常工作,此时患者极易受到病原体感染,最终死于严重感染或恶性肿瘤等疾病。
成年HIV携带者在疾病进展到AIDS之前常有较长的潜伏期,HIV-1侵入机体后潜伏期为2~10年左右,HIV-2侵入机体后潜伏期可能更长,这期间HIV携带者称为HIV感染者。HIV感染者与AIDS患者都具有传染性。不同之处是后者已经出现了明显的病症,而前者尚未出现明显症状。值得注意的是,处于HIV感染窗口期(即已感染HIV病毒,但未能用检测方法测出病毒的一段时期)的感染者也具有传染性。
1.2 误认为蚊子叮咬、共用马桶也可能传播HIV 大多数师生都了解HIV的一般传播途径(性接触、血液、母婴),但当问及蚊虫叮咬、共用马桶是否有可能传染HIV时,许多人显得有些迟疑。这主要是其对HIV的生存能力与传播途径认识不透彻所造成的。
HIV病毒主要通过血液、精液传播,还可能通过阴道分泌物、母乳及任何可能含有血液的体液传播。其他的体液(如唾液),如果不混有血液,理论上并不会含有HIV病毒。且离体后的HIV病毒仅暴露在空气中几个小时,90%~99%的病毒都将丧失感染能力。
有些人担心蚊子叮咬艾滋病患后,残留在蚊子口器中的血可能造成感染,但事实上必须有一定数量的HIV进入人体才可能造成感染。有科学家估算,蚊子口器上残留的血液仅有4×10-5mL,若要有足量的病毒引起感染,至少需要被同一只蚊子反复叮咬2800次才有可能发生。且根据蚊子的生理特点,蚊子在叮咬某人后,须待血液消化后才会去寻找下一个目标,HIV在蚊子体内无法繁殖,所以无需担心被蚊子叮咬会感染HIV。另外,蚊子虽能传播疟疾、登革热等疾病,但其致病原(疟原虫、登革热病毒)的传播途径与HIV不同,并非经血液传染。
同理,若马桶没有被HIV携带者的精液、月经血或阴道分泌物沾污或已足够干燥,接触马桶的皮肤没有损伤或皮肤病时,是没有感染风险的。
1.3 误认为同性性接触更容易感染HIV 艾滋病最早于1981年在美国被报道,当时的艾滋病患者主要为男同性恋者,因此同性性接触被认为是一种高HIV感染风险的途径。直到1985年科学家才发明检测HIV感染的办法,在这几年间,美国出现越来越多输血患者感染HIV的病例,说明血库已经被感染。美国食品药品监督管理局迫于社会压力下达禁令:感染HIV风险较高的性活跃男同性恋者不得献血。除了美国,法国、德国、瑞士、丹麦、挪威等国陆续也颁布了类似的法律法规。 这在某一程度上加强了民众的刻板印象——同性性行为较异性性行为更容易感染HIV。
经性接触传播是目前全球主要的HIV传播途径,全球大约70%~80%的感染者是通过性接触感染HIV的。其中,异性间性接触传播占70%以上,而男同性恋性接触传播占5%~10%。同样,在我国异性性传播才是艾滋病的主要传播途径。依据中国疾控中心的数据显示,每年新报告HIV感染者中,经异性性传播的比例从2011年的 46.5% 上升到 2015 年的 66.5%。
虽然同性性接触确实是高感染性行为,但这并不意味着民众可以忽视异性性接触的风险。澄清这一事实是为了避免公众误以为异性性接触比同性性接触更安全而忽略了应有的保护措施。
1.4 误认为感染HIV后没有治疗方法 事实上,对HIV是有预防措施和治疗措施的:①暴露后预防措施。当个人由于职业原因(医生、护士等)或高危性接触而可能暴露于HIV后,可通过暴露后预防措施(post-exposure prophylaxis,PEP)减少感染的可能。2014年始,WHO建议HIV感染的暴露后预防的疗程措施包括咨询、急救护理和HIV检测,并施以28 d抗逆转录病毒药物疗程,且第一剂药物应在暴露后72 h内尽早使用。因此,在经历高感染风险行为之后,应及时联系当地传染病医院或疾控中心,寻求帮助。②感染后的治疗措施。自2013年起,WHO不再将感染HIV归为不可治愈的“绝症”,而是“慢性、可以控制的疾病”。若及时治疗,HIV感染者甚至可以比同时期患上糖尿病的人活得更久。确诊感染HIV后,可以通过由3种或3种以上抗病毒药物组成的抗病毒联合疗法(antiretroviral therapy,ART)抑制HIV增殖。抗病毒治疗虽无法治愈HIV感染,但可以控制体内病毒复制,并增强人体免疫系统,恢复其抗感染能力。通过抗逆转录病毒治疗,HIV感染者可以过上健康有益的生活。针对不同人群(儿童、青少年及成年人)的药物使用,建议参考WHO于2013年发布的《使用抗病毒药物治疗和预防艾滋病毒感染的综合指南》[1]。
根据联合国的SDG可持续发展目标,至2030年底,世界范围内应实现90%的确诊HIV感染者接受ART或其他治疗的目标。但截至2014年底,我国仅有59%的感染者接受了治疗,若加上估测的实际感染者数量(某些感染者在未发生症状前尚未确诊),ART的覆盖率可能只有35.8%。如果HIV感染的预防及治疗措施更广为人知,相信一定能够提高ART覆盖率。
1.5 误认为HIV感染者不能结婚生子 如果不及时进行治疗,患者感染HIV病毒后的平均存活年限为9~11年左右。相反,若及时进行药物干预,感染者不仅可以正常生活,还可与HIV阴性的人结婚生子。
WHO建议对所有HIV携带者启用抗逆转录病毒药物治疗,这将大大减少HIV的传播。2011年的一项实验已经证实,当HIV阳性者坚持采用有效的抗逆转录病毒药物治疗时,将病毒传给其没有受到感染的性伙伴的危险性可降低96%。同时,对HIV阴性伴侣开展暴露前预防用药(pre-exposure prophylaxis, PrEP)。预防方法就是使没有受到HIV感染的人员每天服用抗逆转录病毒药物,以防止染上HIV。在一系列人群中开展的十多项随机对照研究已经证明,暴露前预防方法在减少HIV传播方面的有效性。因此,若阳性伴侣可以规范使用抗病毒药物进行ART,降低传播风险;另一方阴性伴侣使用药物进行PrEP,降低被感染风险,夫妻双方是有可能拥有自己的健康后代的。通过对孕期或哺乳期妇女实施类似的预防性干预措施,也可以预防母婴传播和保证母亲的生命。
2 关于艾滋病的新发现
2.1 HIV正在进化成更“温和”的版本 HIV是“伪装高手”,它可以毫不费力地躲过人体免疫系统的监控,并对免疫细胞发起猛攻。但近来研究表明,HIV在传播的过程中致病性可能会有所下降。
牛津大学的一项研究指出,相对于较早出现艾滋病例的博茨瓦纳(非洲中南部国家)来说,南非地区的HIV复制能力更弱一些(10%左右)。研究团队对该现象的解释是:当HIV感染一些免疫功能极强的人时,它只有两个选择:一是被消灭,一是通过变异使得自己在增殖过程中不易被免疫系统发现,从而能够存活下来。若HIV通过变异使自己不易被发现并清除时,它们的增殖能力也会减弱,致病性降低,潜伏期延长。而这种“温和型”病毒侵入另一人体后,又进入不断“弱化”的循环中。与此同时,抗逆转录药物的普及也促使病毒向此方向进化,即药物使增殖能力强的病毒死亡,而“温和型”的病毒有更高几率存活并增殖。
但这并不意味着“温和型”的HIV对人类没有威胁,它依然可能使感染者发展成艾滋病,只是所需的时间更长些而已。
2.2 艾滋疫苗新思路——对人体细胞进行“转基因” 美国加州斯克里普斯研究所的科学家们找到了对抗HIV的一种方案:对细胞进行“转基因”操作。首先,设计一种经过改造的无害腺病毒的DNA片段作为载体,然后将其注入肌肉组织,载体会以类似普通病毒入侵细胞的方式对肌肉组织中的细胞进行“改造”,肌肉细胞就可以不断生产某种保护性蛋白质。该保护性蛋白质极好地模拟了CD4和CCR5两种受体,并与HIV紧密结合,阻止其进入CD4细胞。其机理是:HIV表面的每一包膜蛋白含有与T细胞表面的CD4、CCR5受体的结合位点,可识别并攻击T细胞。一般的抗体只能与病毒的一个结合位点相结合,而肌肉细胞产生的保护性蛋白质在结构上与抗体相似,但能同时与HIV的两个结合位点结合,从而保护CD4细胞免受HIV攻击(图1)。经“改造”后的肌肉细胞可以大量、持久地产生这种保护性蛋白质[2]。
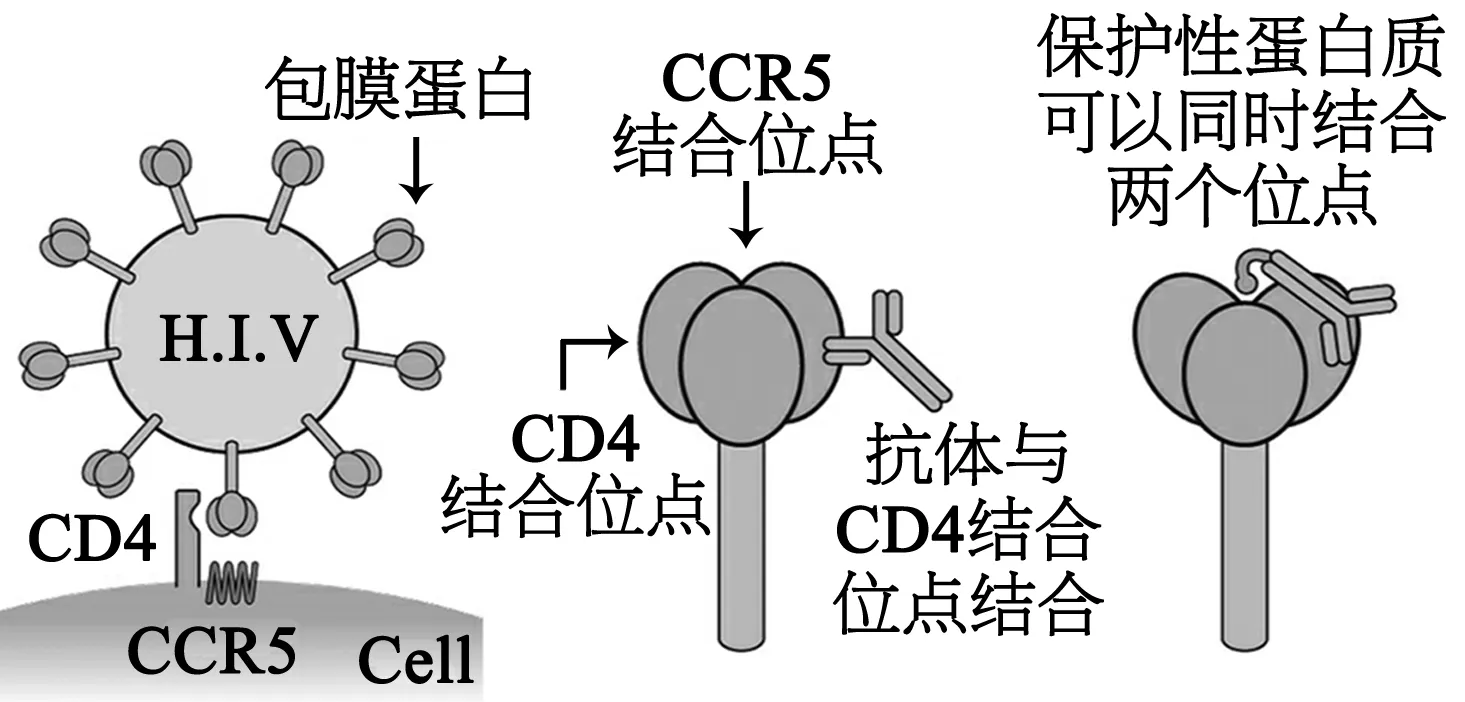
图1 经改造的肌肉细胞产生的保护性蛋白质作用机理
目前这一治疗手段仅在动物身上取得不错的效果:实验猴接受“转基因”注射后8个月未受HIV感染。虽然尚未知道人体临床实验结果如何,但这种新颖的治疗方案仍让科学家及患者充满期待。
2.3 清除HIV的新方法在动物实验中获得成功 2016年,德国德累斯顿工业大学与汉堡海因里希·佩特研究所的研究人员合作,利用蛋白质改造的重要工具“分子定向进化”法开发出一种名为 Brec1 的重组酶。试管细胞标本和实验鼠实验显示,这种重组酶可以准确定位识别 90% 以上临床常见的HIV病毒株,并能安全准确地在受感染细胞的染色体组中完全“剪除”整合的原病毒(指存在于宿主染色体内的、潜在的病毒基因组)。实验还显示,这种方法并没有破坏寄主细胞和正常基因的功能。原病毒被清除后,受HIV遗传物质干扰而失灵的免疫系统有望恢复正常。
HIV与其他逆转录病毒一样,在繁殖时其遗传物质会整合到人体基因组上进行复制。虽然目前的抗逆转录病毒疗法可有效抑制HIV的繁殖,但却不能根除这类整合性病毒。因此病毒可以在治疗期间潜伏休眠,一旦治疗中止,又重新开始复制。而上述清除HIV的新方法有望给艾滋病治疗带来根本性变化,使彻底根治成为可能。在目前动物实验的基础上,研究人员已获准下一步在患者身上进行初步的临床试验。
