进出口食品中89Sr和90Sr的快速检测
2017-07-18迪于成龙马思政杜瑶芳陆
尚 迪于成龙马思政*杜瑶芳陆 地
(1.烟台出入境检验检疫局 山东烟台 264000;2.山东核电有限公司)
进出口食品中89Sr和90Sr的快速检测
尚 迪1于成龙2马思政1*杜瑶芳1陆 地1
(1.烟台出入境检验检疫局 山东烟台 264000;2.山东核电有限公司)
为对进出口食品中89Sr和90Sr进行快速检测,本研究针对多种食品样品进行分析,建立一种快速分析方法。通过消解预处理、碳酸盐沉淀对食品样品中Sr进行富集;采用新型Sr·Spec萃取树脂,对89Sr和90Sr进行分离纯化;结合低本底α/β测量法,在Y自生长一定时间后通过测量90Y含量得出90Sr含量,从而得到89Sr含量。该方法优化了传统检测流程,满足对进出口食品中89Sr和90Sr的快速检测需求,极大缩短检测时间。
食品;89锶;90锶;快速检测
1 前言
90锶(Sr)是进出口食品中重点监测核素之一,主要来源于人类从事的核活动及核事故带来的污染,其半衰期长,在放射性核素毒性分组中属于高毒组,主要通过食入或吸入途径进入人体,积聚在人体骨骼和牙齿中,可对人体造成内照射伤害,带来致癌风险[1]。
现行90Sr检测标准中,主要有3种方法:发烟硝酸法、二-(2-乙基已基)磷酸萃取法[2-4]和离子交换法[5-7]。发烟硝酸法是我国食品中分析90Sr的传统标准方法之一,该方法操作繁琐,检测周期长,且高浓度酸会对实验人员身体造成一定损伤。二-(2-乙基已基)磷酸(HDEHP)是一种用途很广的磷型萃取剂,在水相高酸度时对高价金属离子保持良好的萃取率。弋昌厚等[8]报道了硝酸体系中HDEHP萃取分离和测定环境样品中90Sr的分析流程,该方法需将90Sr放置 14 d以上,等待90Sr与90钇(Y)达到平衡后,再用HDEHP萃取分离90Y。该方法操作时间长,无法满足进出口食品快速检测的要求。Horwitz等[9-11]制备了一种负载冠醚的萃取色层树脂——Sr·Spec树脂,该树脂对Sr具有高效的选择性,对Sr的分离取得了非常好的效果。Rodriguez等[12]则利用该树脂成功地分离了中低活度放射性废物中的90Sr。由于Sr·Spec树脂的优异性能,国外已广泛应用于环境样品中90Sr的分析,并且已经发布了使用Sr·Spec树脂测定水和土壤中90Sr含量的标准[13,14]。本研究采用新型Sr·Spec树脂,结合碳酸盐共沉淀,对进口食品样品中Sr进行富集分离,通过对自生长的90Y的测量,得到样品中90Sr含量以及89Sr含量,从而建立一种对样品中89Sr及90Sr含量的快速检测方法。
2 材料与方法
2.1 材料
2.1.1 试剂
Sr·Spec 树脂:粒径 50-100 μm,天津博纳艾杰尔科技有限公司;90Sr-90Y标准溶液:5.73 Bq/mL,25 μg/mL Sr载体+25 μg/mL Y 载体,0.1 mol/L HNO3介质,中国计量科学研究院;硝酸锶、硝酸钇[Y(NO3)·6H2O]、浓硝酸、二水合草酸:均为分析纯,国药集团化学试剂有限公司;其他试剂:均为分析纯。
2.1.2 仪器
MPC-9604型低本底α/β分析仪:美国Ortec公司;分析天平:AB265-S,瑞士梅特勒托利多公司。
2.2 方法
2.2.1 实验方法
2.2.1.1 Sr载体溶液的配制和标定
取12.1 g硝酸锶溶解于水中,用水定容至1 L,即为Sr载体溶液(5mg Sr/mL)。
取4份2mL Sr载体溶液分别置于烧杯中,用氨水调节溶液pH至8.0,加入5mL饱和碳酸铵溶液,加热至近沸腾,冷却沉淀。用已称重的G4玻璃砂芯漏斗抽滤,分别用10mL水和无水乙醇洗涤沉淀。沉淀在105℃烘干。冷却后称重,直至恒重。
2.2.1.2 Y载体溶液的配制和标定
取21.55g硝酸钇溶解于水中,用水定容至1 L,即为Y载体溶液(5mg Y/mL)。
取4份2mL Y载体溶液分别置于烧杯中,加入5mL饱和草酸溶液,用氨水调节溶液pH至1.5,水浴加热,冷却沉淀至室温。在有定量滤纸的三角漏斗中过滤沉淀,分别用10mL水和无水乙醇洗涤沉淀。取下滤纸置于瓷坩埚中在电炉上烘干后再置于马弗炉中900℃灼烧30min,在干燥皿中冷却后称重,直至恒重。
2.2.1.3 硝酸(3 mol/L)-草酸(0.05 mol/L)溶液
取191mL浓硝酸和6.3 g二水合草酸,溶解于800mL水中,最后用水稀释定容至1 L。
2.2.1.4 Sr·Spec 树脂预处理
将色谱柱固定于色谱柱架上,在色谱柱下放置50mL离心管以盛接滤液,取下色谱柱底部活塞或盖子,使色谱柱流通。用5mL 8.0 mol/L硝酸溶液润洗色谱柱。
2.2.1.5 样品预处理
取样品可食部分,称重,干燥,灰化,再次称重,计算样品灰鲜比G。称取1-10 g(精确至0.001 g)灰样于烧杯中,加入1mL Sr载体,用少量水将灰润湿,将样品消解并蒸干。加入5mL浓硝酸,轻微加热将沉淀溶解,调节样品液pH=2。加入 0.5mL 1.25 mol/L硝酸钙溶液。加盖表面皿,并加热至沸腾,冷却至室温后调节pH=8。加入30mL饱和碳酸钠溶液,沸水浴0.5 h,加几滴饱和碳酸钠溶液检查沉淀是否完全。冷却静置后离心,用10%碳酸钠溶液洗涤沉淀2次,弃去上清液,用5mL浓硝酸溶解沉淀并蒸干。同时做5个平行样。
2.2.1.6 Sr分离
向上述蒸干烧杯中加入10mL 8.0 mol/L硝酸溶液,溶解析出物。将重新溶解的样品液转移到色谱柱上,排液。用5mL 8.0mol/L硝酸溶液冲洗烧杯,重复上步操作。向色谱柱中加入5mL硝酸(3 mol/L)-草酸(0.05 mol/L)溶液,并排液。再次加入5mL 8.0 mol/L硝酸溶液,排液。向色谱柱中加入10mL 0.05 mol/L硝酸溶液洗脱Sr,排液并收集洗脱液,流速控制在1mL/min。加入5mL 0.05 mol/L硝酸溶液于色谱柱中,保持树脂处于湿润状态,盖好色谱柱顶盖,并置于安全的地方直到完成90Y自生长,后续将再次使用色谱柱。
2.2.1.7 回收率测定
重量法测定Sr的化学回收率。对于被分析的样品,用乙醇润湿的纸巾清洁样品盘,擦拭样品盘并干燥。样品盘称重,记录重量。将上述收集洗脱液逐滴加入样品盘中,红外灯下蒸干。用2mL 0.05 mol/L HNO3冲洗盛有洗脱液的烧杯,一并转移到样品盘中蒸干。将样品盘冷却,称重并记录质量。将样品测量足够长时间,以获得计数统计和最小检测浓度。
2.2.1.8 低本底 α/β计数器效率刻度
用于测量90Sr/90Y活度的计数器必须进行校准,即确定测量装置对已知活度90Sr/90Y源的响应,它可用探测效率来表示。向烧杯中分别加入1.00mL Sr载体溶液、1.00mL Y载体溶液和5.00mL90Sr-90Y标准溶液,蒸至近干,再溶于10mL 8.0 mol/L硝酸溶液。将溶液转移到色谱柱上,并排液。分别收集洗液和洗脱液,按照2.2.1.7进行操作。将排液开始至排液完毕的中间时刻作为Sr、Y的分离时刻。在和试样相同条件下测量90Sr源及90Y源的计数率。
2.2.1.9 监督源制备
在样品盘内均匀滴入2.50mL90Sr-90Y标准溶液,红外灯下烘干,制成与校准源相同活度大小的监督源。在校准测量仪器的探测效率时,同时测定监督源的计数率。在测量样品时也定期测量其计数率,以便确定测量仪器是否正常工作。
2.2.1.10 自生长90Y的分离
残留Sr的样品盘置于干净处等待Y自生长7 d,将样品盘置于一干净烧杯中,加入5mL 8.0mol/L硝酸溶液重新溶解残留物,缓慢加热,再次用酸冲洗样品盘,洗液收集于烧杯中。将样品液转移至2.2.1.6中留用的色谱柱,并排液。加入5mL 8.0 mol/L硝酸溶液冲洗烧杯后排液,收集洗液。记录最后一次淋洗时间作为Y自生长的终止时间。将洗液在样品盘中蒸干,上机检测。该过程可假设Y的回收率为100%。
2.2.2 结果计算
2.2.2.1 重量法测Sr的回收率YSr
根据2.2.1.6中方法测定回收率公式如下:

式中:YSr-Sr的回收率;
RW-残留物与样品盘质量,mg;
TW-样品盘净质量,mg;
BW-空白质量(萃取剂从色谱柱上的损失量),mg;
CW-加入的 Sr(NO3)2质量,mg。
2.2.2.290Sr的探测效率
采用低本底α/β计数器测量90Sr,其探测效率计算公式如下:

式中:E-90Sr的探测效率;
Ns-90Sr标源的计数率,s-1;
Nb-本底计数率,s-1;
D-1.00mL 5.73 Bq/mL90Sr-90Y标准溶液中90Sr的活度,Bq;
YSr-Sr的化学回收率,算法同式(1);
e-λ×(t1-t2)为90Sr的衰变因子。此处 t1为 Sr、Y 的分离时刻(d),t2为测量90Sr源进行到一半的时间(d),λ 为90Sr的衰变常数,等于 0.693/T,T 为90Sr的半衰期(d)。
2.2.2.390Y的探测效率
公式同2.2.2.2。
2.2.2.4 样品中89Sr+90Sr的总活度浓度
用低本底α/β计数法计算样品中89Sr+90Sr的总活度浓度,计算公式如下:

式中:C-样品中89Sr与90Sr的总含量,Bq/kg;
Nt-样品的计数率,s-1;
Nb-本底计数率,s-1;
G-灰鲜比,g/kg;
J0-校准测量仪器的探测效率时测得的90Sr监督源的净计数率,s-1;
J-测量样品时90Sr监督源的净计数率,s-1;
mh-称取的灰样的质量,g;
YSr-Sr的化学回收率;
E-90Sr的探测效率。
2.2.2.590Sr活度浓度计算
通过90Y-自生长计算90Sr活度浓度,计算公式如下:
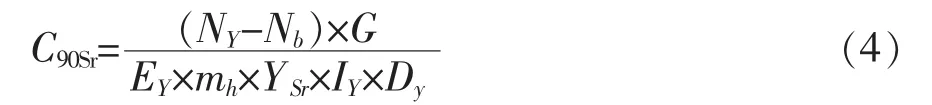
式中:C90Sr-样品中90Sr活度浓度,Bq/kg;
NY-Y 的计数率,s-1;
Nb-本底计数率,s-1;
G-灰鲜比,g/kg;
EY-90Y的计数效率;
mh-称取的灰样的质量,g;
IY-90Y的自生长因子=1-exp[(-ln2/2.6708)×(T2-T1)];
Dy-90Y 的衰变校正=exp[(-ln2/2.6708)×(T3-T2)];
T1-90Y自生长的起始时间(最后冲洗Sr开始分离);
T2-90Y自生长的终止时间(最后冲洗-自生长后去除Sr);
T3-样品测量的中点时刻。
2.2.2.689Sr活度浓度的计算
通过扣除总Sr中的90Sr来计算89Sr,计算公式如下:
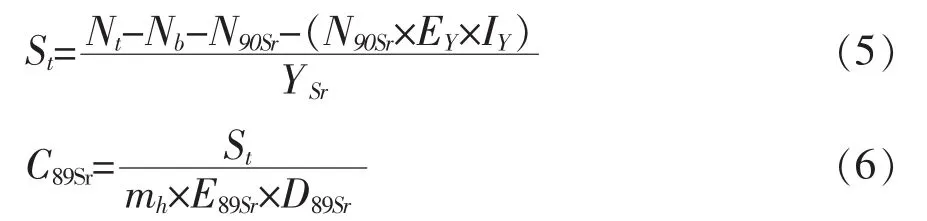
式中:St-89Sr的计数率,s-1;
Nt-样品的计数率,s-1;
Nb-本底计数率,s-1;
N90Sr-90Sr的计数率,N90sr=NY×E,s-1;
NY-Y 的计数率,s-1;
E-90Sr的探测效率;
EY-90Y的计数效率;
IY-90Y的自生长因子=1-exp[(-ln2/2.6708)×(T2-T1)];
C89Sr-89Sr的活度浓度,Bq/kg;
mh-称取的灰样的质量,g;
E89Sr-89Sr的计数效率;
D89Sr-89Sr的衰变校正=exp[(-ln2/50.5)×(T3-T0)];
T0-采样时间;
T3-样品测量的中间时刻。
2.2.2.7 探测下限的确定
本方法探测下限计算公式如下:
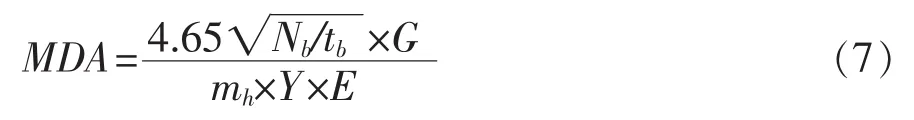
式中:MDA-探测下限,Bq/kg;
tb-本底测量时间,s。
3 结果分析与讨论
3.1 回收率的确定
本研究以4种不同食品样品为例,分别取4种样品的空白测试样,每个样品添加含有5mg Sr的载体溶液,以重量法计算样品中Sr的回收率。相同实验条件下,每中样品做5组平行样。Sr回收率、样本标准偏差(SD)及变异系数(CV%)结果见表1。由实验结果分析得知,对于植物样品,平均回收率较高,约为83%-86%;对于动物性样品,回收率接近80%。实验证实该方法准确可靠。
3.2 探测效率确定
本研究通过对90Sr-90Y标准溶液进行萃取分离得到90Sr标源,用该标源对仪器进行效率刻度,计算得到仪器对90Sr探测效率平均值为38.4%,对90Y的探测效率为32.6%。
3.3 探测下限确定
针对4种不同样品测量5组平行样,计算该方法针对不同样品的探测下限。以90Sr为例,通过测量本底计数率,计算每种样品的的探测下限。其中,苹果的检出限为0.09 Bq/kg,大豆检出限为0.39 Bq/kg,青虾检出限为0.28 Bq/kg,鲑鱼检出限为0.34 Bq/kg。分析数据可以得出,该方法检出限低,可快速准确测量低比活度样品。
4 结语
建立了一种快速简便测量食品样品中89Sr和90Sr的分析方法。样品分析流程简便,分析周期仅为9 d左右,约为传统分析方法所需时间的一半,极大地缩短检测时间。在进出口检验领域,对鲜活水产品、保鲜期要求较高的水果等食品的检测,本方法有较高的推广应用价值。Sr·Spec树脂对Sr选择性好,本方法采用该树脂对进出口食品样品进行检测,结果稳定,准确度高,证实该方法可靠。
[1]舒复君,杨金玲,杨志红,等.一种快速分析土壤样品中90Sr的方法[J].核化学与放射化学,2013,35(1):14-18.
[2]党磊,吉艳琴.低水平90Sr的分析方法研究进展[J].核化学与放射化学,2010,32(3):129-144.
[3]GB 11222.1-89生物样品中锶-90的放射化学分析方法二-(2-乙基己基)磷酸酯萃取色层法[S].
[4]陈飞,尹亮亮,孔祥银,等.生物样品中锶-90分析的不确定度评定[J].辐射研究与辐射工艺学报,2016,34(1):59-64.
[5]Heilgeist M.Use of extraction chromatography,ion chromatography and liquid scintillation spectrometry for rapid determination of strontium-89 and strontium-90 in food in cases of increased release ofradionuclides [J].JournalofRadianalyticaland Nuclear Chemistry,2000,245(2):249-254.
[6]Inan S,NostarE.Structure and ion exchangebehaviorof zirconium antimonates for strontium[J].SeparationScience and Technology,2013,48(9):1364-1369.
[7]孔祥银,邵宪章,陈飞,等.冠醚包覆聚苯乙烯磁性颗粒的合成、表征及其对锶离子的吸附性能 [J].辐射研究与辐射工艺学报,2016,34(2):49-56.
[8]弋昌厚,李福德,刘飙,等.环境样品中锶-90的测定[J].生物化学与生物物理学报,1978,10(1):59-70.
[9]Horwitz E P,Dietz M L,Fisher D E.SREX:a newprocess for the extraction and recoveryofstrontium fromacidic nuclear waste streams[J].Solvent Extraction and Ion Exchange,1991,9(1):1-25.
[10]Horwitz E P,Chiarizia R,Dietz M L.Novelstrontium-selective extraction chromatographic resin[J].Solvent Extraction and Ion Exchange,1992,10(2):313-336.
[11]Horwitz E,Dietz M,Fisher D.Extraction of strontiumfrom nitric acid solutions using dicyclohexano-18-crown-5 and its derivatives[J].Solvent Extraction and IonExchange,1990,8(4-5):557-572.
[12]Rodriguez M,Suhrez J A,Espartero A G.Separation of radioactive strontium by extraction using chromatographic resin[J].Nuclear Instruments&Methods in Physics Research,1996,369(2-3):348-352.
[13]ASTM D 5811-2000 2008.Standard test method for strontium-90in water[S].
[14]Vajda N,Ghoda-Esphahani A,Cooper E,et al.Determination of radio strontium in soil samples using a crown ether[J].Journal of Radio analytical&Nuclear Chemistry,1992,162(2):307-323.
Rapid Detection of89Sr and90Sr in Food Imported and Exported
SHANG Di1, YU Chenglong2, MA Sizheng1*, DU Yaofang1, LU Di1
(1.Yantai Entry-Exit Inspection and Quarantine Bureau, Yantai, Shandong, 264000;2.Shandong Nuclear Power Company Ltd.)
This paper aims to build a new rapid detection method of89Sr and90Sr in import and export food.A new Sr·Spec solid phase extraction resin is used to separate and purify89Sr and90Sr in this method,combined with digestion pretreatment,carbonate precipitation,low background alpha and beta measurement.The contentof90Srcan be determined by measuring the contentof90Y afterits self-growth,and the content of89Sr is also available.This method optimizes the traditional experimental procedure and shortens the detection time,which greatly satisfies the requirement of rapid detection of89Sr and90Sr.
Food;89Sr;90Sr;Rapid Detection
TS201.6;R144
E-mail:ciqshangdi@163.com;*通信作者E-mail:masz122@163.com
山东出入境检验检疫局科技计划项目(SK201601)
2016-12-30
