金纳米簇高效绿色制备及其对汗潜指印的显现
2017-06-27陈虹宇
黄 锐, 陈虹宇
(1.西南政法大学刑事侦查学院, 重庆 401120; 2.物证技术重庆高校工程研究中心, 重庆 401120;3.重庆大学生物工程学院, 重庆 400044)
金纳米簇高效绿色制备及其对汗潜指印的显现
黄 锐1,2,3, 陈虹宇1
(1.西南政法大学刑事侦查学院, 重庆 401120; 2.物证技术重庆高校工程研究中心, 重庆 401120;3.重庆大学生物工程学院, 重庆 400044)
目的 制备性能优良的金纳米簇,构建荧光金纳米簇粉末显现汗潜指印的新方法,并将荧光金纳米簇粉末、金粉、磁性粉对陈旧指印显现效果进行比较,探究新方法的优点与不足。方法 基于微波辐射与超声方法的优点,采用超声- 微波协同制备方法,以牛血清白蛋白为稳定剂和还原剂绿色合成了金纳米簇,对金纳米簇制备条件进行优化后,将其制成粉末应用于潜指印显现。借助自主搭建汗潜指印显现观察系统,用多波段光源紫外光激发,观察汗潜指印显现效果。结果 金纳米簇的制备耗时约1 h,过程高效绿色,荧光性能好,量子产率高达7.1%,平均粒径约为3.3 nm,最佳激发波长为521 nm,最强发射峰为633 nm。其显现的汗潜指印发出橙红色荧光,细节特征明显。结论 以超声- 微波协同制备方法制备的金纳米簇可应用于模拟案件现场指印的显现观察,其显现效果优于传统粉末显现试剂,是一种快捷、环保的汗潜指印显现方法。
金纳米簇; 牛血清白蛋白; 超声- 微波协同法; 荧光; 汗潜指印显现
0 引言
金纳米簇(Gold nanoclusters,Au NCs)作为一种新型的发光材料,是指由几个到几十个金原子所组成的粒径在2 nm左右的团簇[1],具有强稳定的光物理性质、高生物相容性、低毒性等优点[2]。近十年来,Au NCs的荧光性质主要应用于荧光探针检测金属离子[3]、活细胞荧光成像[4]、荧光传感器等[5]。但Au NCs在刑事科学技术领域的研究与应用鲜有文献报道,仍处起步阶段。指纹具有人各不同、终生不变、触物留痕的特性,有“人体身份证”和“证据之王”的美称,对揭露、证实犯罪和识别案犯有不可忽视的作用。指印显现技术已有上百年的历史,传统显现方法有502熏显法[6]、茚三酮法[7]、DFO法[8]等。随着纳米技术的飞速发展,新型纳米材料应用于潜指印显现引起了科研工作者的关注,出现了利用金属[9]、上转换发光[10]、磁性纳米材料[11]显现指印等方法,Au NCs因其能与蛋白质、氨基酸中的巯基(—SH)结合且具有良好的荧光特性,在潜指印显现领域也具有研究价值。2013年,柴芳等人[12]制得谷胱苷肽功能化的荧光Au NCs,并将其应用于硅片、玻璃上汗潜指印、血指印显现,拓宽指印显现的应用范围。上述研究方法在制备过程中采用传统水浴加热方法,耗时较长(12 h~72 h)、操作繁琐,不具备绿色高效的优点,合成效率较低。
目前,Au NCs的合成多采用传统加热法和孵育法,如Ying课题组[13]在孵育12 h条件下,利用BSA为保护剂和稳定剂制备了荧光量子效率为6%的Au NCs,但该法时间消耗长、耗能较大、反应速度慢、制备的产物粒径较大、性能低,在实际工作中难以得到推广。随着科技发展,环境友好型的超声技术与微波技术作为新兴技术在纳米材料制备中得到应用。超声作用能推动微粒往复振动,增强产物分散性,有效阻止粒子团聚[14];微波辐射最先受热的内部向外传热,比传统加热迅速均匀,加热效率高,能缩短制备时间,降低能耗,并保持BSA生物活性[15]。
本文采取超声- 微波协同法,以BSA为保护基团绿色合成了尺寸小、荧光性能优良的Au NCs。通过Au NCs形貌及光学性质的表征和对超声微波协同时间的优化,将其成功地应用于不同客体表面汗潜指印显现。在自组装汗潜指印显现观察系统中检见清晰可辨的橙红色荧光纹线。其显现效果显著优于传统粉末显现试剂金粉、磁粉,是优质便捷的汗潜指印显现试剂。
1 实验部分
1.1 试剂与仪器
氯金酸(HAuCl4)购于天津市光复精细化工研究所;牛血清白蛋白(BSA)购于磐安县鸿瑞生物科技有限公司;氢氧化钾(KOH)、乙醇溶液(C2H5OH)购于中国医药上海化学试剂公司;所有化学试剂均为分析纯。
D8023CSL-K4家用微波炉(格兰仕),JP-040超声洗涤仪(上海精宏实验设备有限公司),UV-2450紫外- 可见分光光度计(日本岛津公司)测得,S-4800场发射扫描电子显微镜(日本日立公司),RF-5301PC荧光光谱仪(日本岛津公司),VECTOR22傅里叶变换红外光谱仪(德国布鲁克公司),ZataPALS电位及粒度分析仪(美国布鲁克海文仪器公司),AXIS UL TRA DLDX射线光电子能谱仪(日本岛津公司),Milli-Q超纯水机(美国密理博公司),BK-360B超声波洗涤仪(济南巴克超声波科技有限公司),ESJ200-4B分析天秤(沈阳龙腾电子有限公司),自组装汗潜指印显现观察系统用于显现指印的观察固定。
1.2 金纳米簇的制备
采用新型超声- 微波协同法加热,将20 mLHAuCl4溶液(0.01 mol/L)加入到20 mLBSA溶液(50 mg/mL)中,混合均匀,加入2 mL KOH溶液(1 mol/L),搅拌,先置于超声波洗涤仪超声1 h,再置于家用微波炉,高火条件下(800 W)微波辐射50 s,溶液呈亮棕色。
1.3 金纳米簇的表征
通过透射电子显微镜观察各溶液微粒状态;用电位及粒度分析仪测定Au NCs粒子半径。分别对Au NCs制备过程中一系列溶液进行紫外光谱扫描,扫描波长范围设定为250~500 nm,绘制各组紫外光谱图;用傅里叶变换红外光谱仪对Au NCs进行测试,测试红外图谱波数范围在4 000~500 cm-1;取样品进行稀释,通过荧光光谱仪采集荧光光谱,扫描范围450~800 nm,入射和出射狭缝均为5 nm,并测定Au NCs的荧光量子产率。
1.4 汗潜指印的显现与固定
所有指印样本均由同一志愿者提供。志愿者将手洗净晾干后,在客体上捺印汗潜指印,获得指印样本。为模仿案件现场上汗潜指印,本实验指印样本在自然条件下存放在干净托盘内。将Au NCs溶液制成粉末,用毛刷分别取适量Au NCs粉末沿指印乳突纹线顺时针刷显。用自主搭建汗潜指印显现观察系统在黑暗条件下进行汗潜指印显现并拍照固定,然后用Photoshop图像处理软件对照片采用“曲线”等命令增强处理[16],使得图片中荧光指印纹线更加清晰可辨,更利于检验鉴定。
2 结果与讨论
2.1 金纳米簇的合成
2.1.1 金纳米簇的合成原理
图1为Au NCs合成原理图。BSA含有酪氨酸、半胱氨酸等氨基酸,分子结构复杂。BSA能与Au形成稳定的结构原因在于:半胱氨酸组成了二硫键以及自由巯基[17],具有可与金离子结合并且还原金离子的巯基(—SH)等庞大的结合位点,是合成Au NCs的理想模板;酪氨酸有还原性,在强碱性环境下可将Au3+还原成金原子或者Au+。
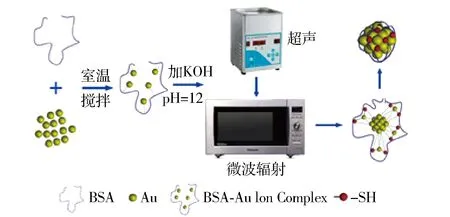
图1 Au NCs合成原理图
2.1.2 超声- 微波协同制备
考察传统水热法、超声法、微波法、超声- 微波协同法对Au NCs荧光强度和平均粒径的影响。如图2所示,超声- 微波协同加热法制备的Au NCs荧光强度与粒径大小明显优于其他制备方法;微波法制备的Au NCs粒径较小,这与微波加热能使溶液均匀受热有关;超声法制备的粒子粒径比微波法略大,但荧光性能优异;传统加热法制备的Au NCs性能最差。超声- 微波协同加热法将超声法与微波法各自优点结合,充分体现了高效绿色的特点。其高效性体现在不仅能使粒子粒径减小,分散效果和荧光性能增强,还能使反应时间大大降低,反应效率提高,即在相同反应时间内能制备更多的性能优良的Au NCs;其绿色性体现在BSA在合成过程中生物活性未发生改变,整个反应过程安全,反应时间降低使得耗能减少,同时使制备同样量Au NCs需要的试剂量减少。

图2 不同方法制备对Au NCs的影响
为使超声- 微波协同作用达到最优,设计9组试验,保持超声功率和微波功率不变,改变超声时间与微波辐射时间,考察不同反应时间对Au NCs荧光量子产率和平均粒径以及粒子分散程度的影响,实验方案及结果如表1所示。
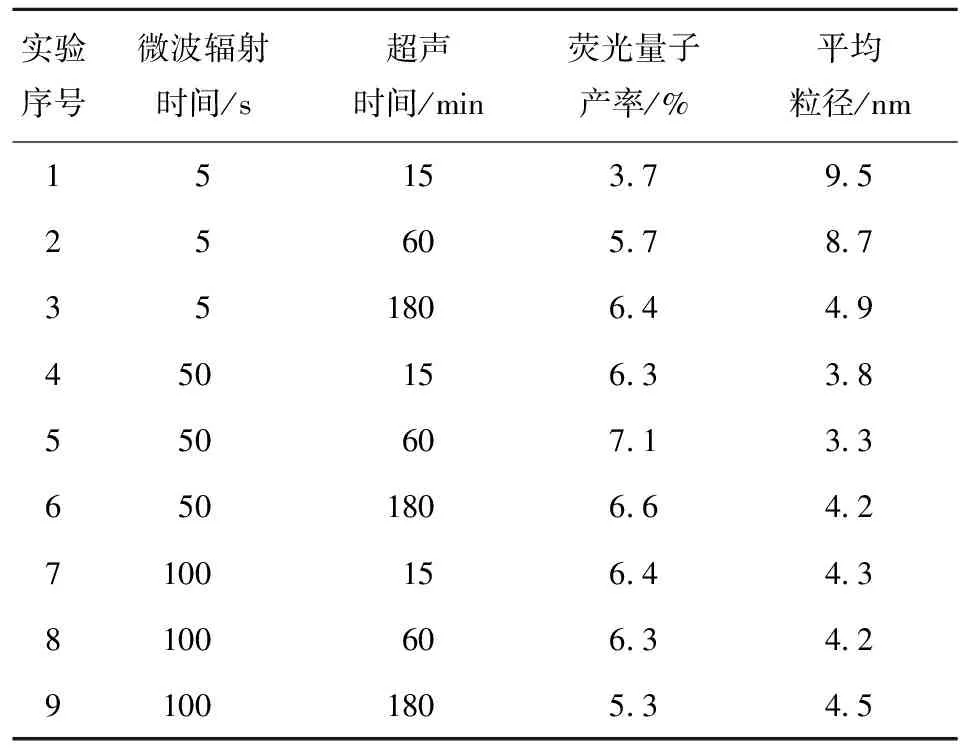
表1 超声时间与微波辐射时间对合成Au NCs的影响
从实验结果分析可知,超声与微波时间的最优组合为超声1 h,微波辐射50 s。超声时间由少至多,粒径逐渐减少,分散程度逐渐增强。当超声到一定程度后,粒径减小不再明显。而Au NCs的荧光性能随着粒径的减小而增大。在超声作用下,产生的空化效应使局部出现高温高压,加快了Au NCs生成速率,有利于减小颗粒尺寸,空化气泡和高温能降低产物表面自由能,防止Au NCs团聚[3-4]。但超声时间过长,未冷却足够时间,会导致溶液局部过热,使蛋白质变性,作为保护剂和稳定剂的BSA失活,反而使得Au NCs荧光性能降低。同样微波辐射是指在微波能量的作用下,分子运动从杂乱无章的状态变成有序高频地振动,将动能转化成热能,从分子水平上进行搅拌,以达到均匀迅速加热的目的[18]。辐射时间较少,Au NCs生成速率低,易团聚;辐射时间长,温度过高会导致BSA变性。
2.2 金纳米簇的表征
2.2.1 电镜表征
通过在电镜下观察Au NCs的粒径形貌大小及分布发现,Au NCs是由几至几十个金原子组成,形态为球形,与纳米金粒子形态相近(如图3所示)。从图3(a)中任意抽取一个粒子用Photoshop进行测量,其半径为1.6 nm。用电位及粒度分析仪测量,发现Au NCs分散均匀性好,其平均粒径为3.3 nm。与2013年杜娟[19]报道的粒径为13.3 nm的传统金纳米粒子相比,Au NCs尺寸远小于纳米金。因此Au NCs相较于金纳米粒子能级不连续性更大,电子发生跃迁的能力越强,产生的荧光更强[20]。

图3 Au NCs电子显微镜及粒径分布图
2.2.2 光谱表征
如图4所示,在280 nm左右紫外辐射下,Au NCs有较强的紫外吸收峰,而BSA中的色氨酸和酪氨酸残基紫外吸收峰也位于280 nm左右[21]。BSA缠绕在Au外面,起保护稳定作用,因此Au NCs的紫外光谱性质与BSA相近,这说明超声- 微波加热协同技术未破坏BSA的生物活性。
为进一步证明Au NCs的生成,分别对BSA溶液、BSA+ HAuCl4、Au NCs的红外光谱进行比较。如图5所示,这3种溶液的特征吸收峰未发生明显变化,但Au NCs在2 300 cm-1左右处的巯基特征吸收峰消失,说明通过超声加热反应BSA分子已经成功修饰至Au NCs的表面。而BSA自身的特征吸收峰在反应前后未有明显的变化,说明蛋白质的构象无明显改变。
图6为Au NCs荧光光谱图,激发波长为521 nm,最大发射波长为633 nm。将多波段光源调至365 nm波段,Au NCs在滤光镜下检见橙红色荧光。以罗丹明B的乙醇溶液为标准参考物测定Au NCs的量子产率进一步表征它的荧光性能[22],测得荧光量子产率为7.1%。这与Ying课题组[13]报道的Au25NCs的荧光量子产率相比提高了1.1%,说明本研究制备的Au NCs荧光性能更优,采用高效绿色超声-微波协同法,既加快了合成时间,又使制备Au NCs尺寸和分散性达到最佳,粒子能级间隔增大,荧光量子产率相应提高[17]。
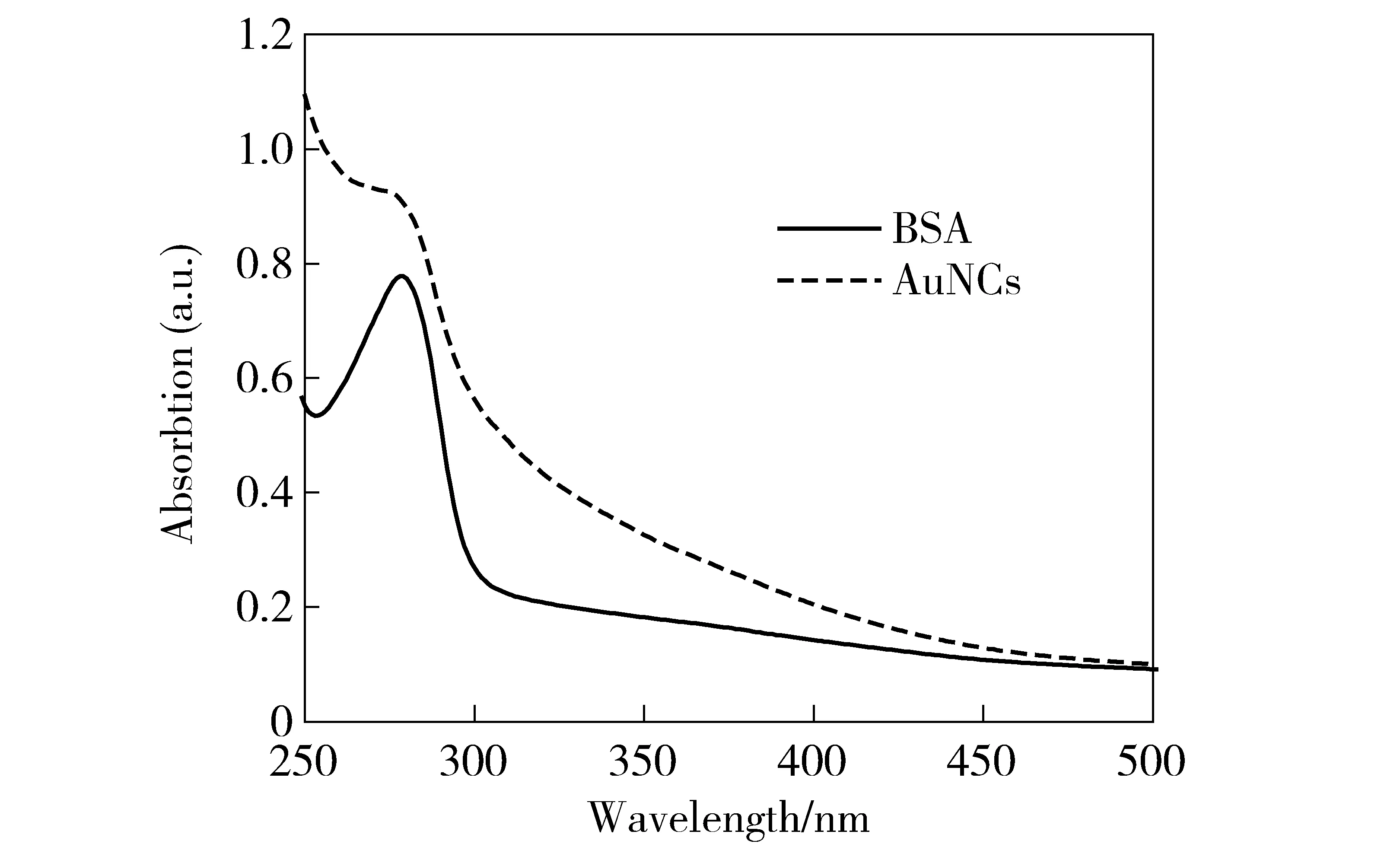
图4 Au NCs紫外可见光谱图
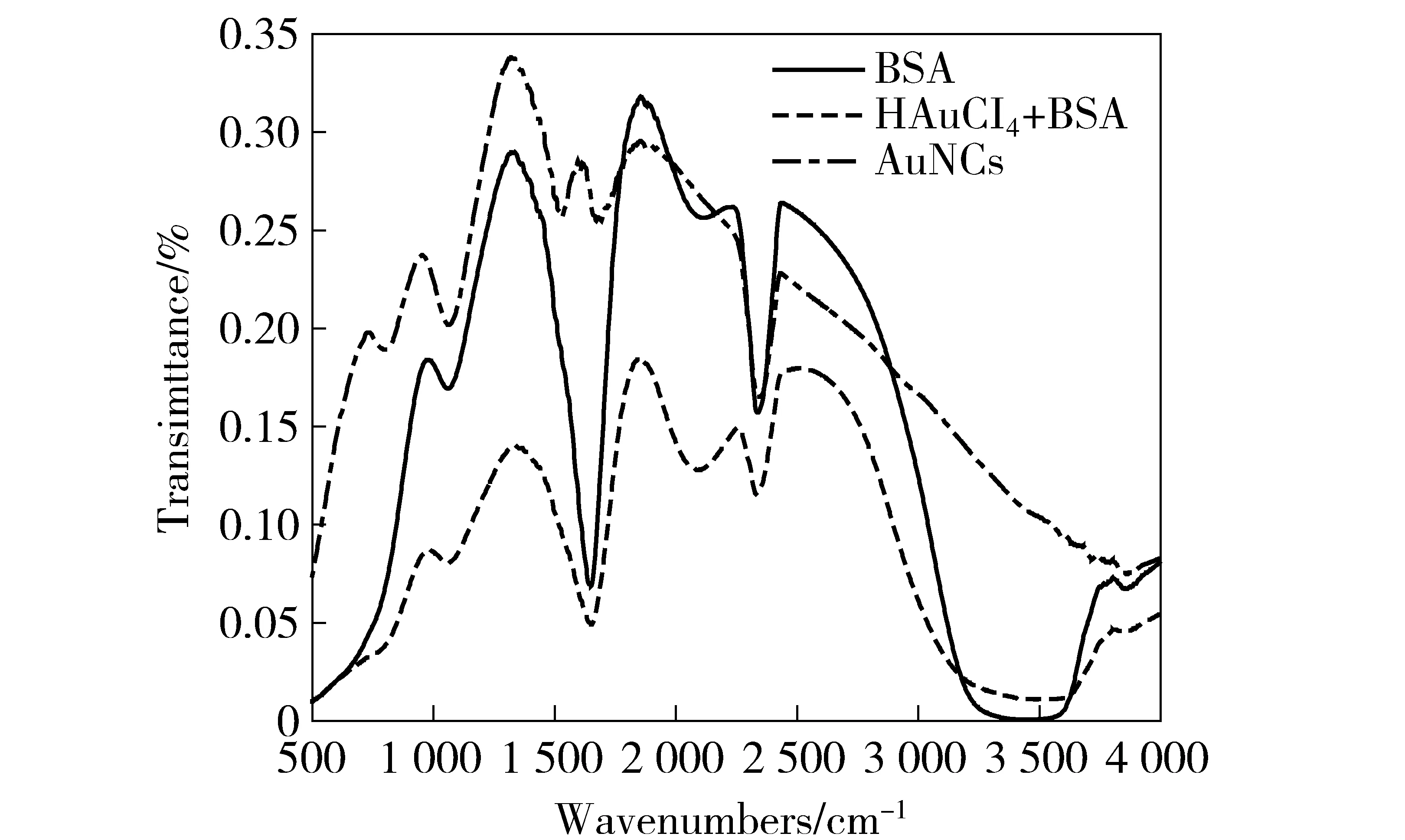
图5 Au NCs红外光谱图

图6 Au NCs荧光光谱图,内嵌图荧光变化图,(a) (b)分别为在白炽灯、在多波段光源照射下的照片
2.3 汗潜指印显现的应用
人双手手指指头的乳突花纹上分布有汗孔,汗孔分泌的汗液常含有油脂以及其他微小物质[23],因此遗留在客体上的汗潜指印成分包含少量的水、少量的无机物、蛋白质、油脂等有机物。
Au NCs显现汗潜指印的原理是利用金粒子与汗潜指印中的蛋白质、油脂等物质中的—SH结合,增大指印纹线与透明玻璃客体背景反使汗潜指印的乳突纹线得以显现,从而达到显现潜在指印的目的。如图7所示,参照前期对自主搭建汗潜指印显现系统的研究[24],利用多波段光源、有色滤光镜、数码单反相机自主搭建汗潜指印显现观察系统对汗潜指印进行观察固定。在黑暗条件下,将多波段光源调365 nm波段,照射被Au NCs粉末显现的汗潜指印,指印产生的橙红色荧光透过有色滤光镜被数码单反相机记录,将指印乳突纹线及其细节特征固定下来。不反映指印特征的其他杂光因无法透过有色滤光镜而不能被相机记录。

图7 自主搭建汗潜指印显现观察系统示意图
2.3.1 不同载体上的显现效果比较
如图8所示,Au NCs粉末对不同载体上汗潜指印的显现效果有明显差异:玻璃上粉显的指印显现纹线细节特征清晰可辨,具备比对条件;保鲜膜和金属上的显现效果相差不大,但由于保鲜膜具有粘附性,小梨沟部位易黏附粉末而形成干扰特征;塑料上的显现效果最差,能基本显现指印,但纹线与背景的反差不大;在纸类载体上,表面光滑的衬垫纸、相纸显现效果较A4纸显现效果好。由此可说明Au NCs在非渗透性客体上的显现效果优于渗透性客体。
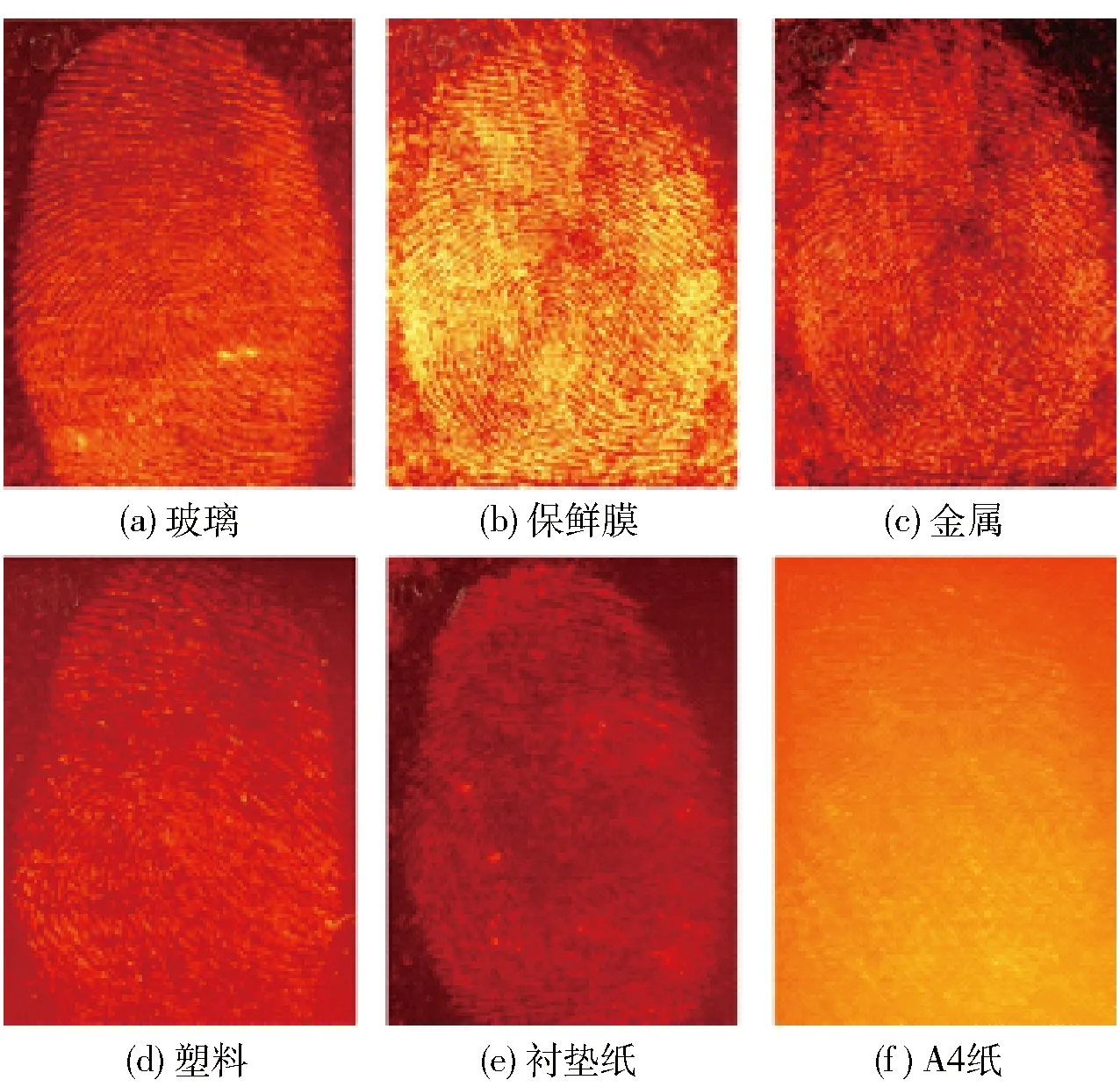
图8 Au NCs在不同载体上的显现效果
2.3.2 与传统粉显试剂比较
金粉、磁性粉为目前常用的指印显现粉末,本研究将Au NCs制成粉末(如图9),比较Au NCs与磁性粉、金粉的对陈旧指印(15d)显现效果。如图10所示,Au NCs对于非渗透客体上(玻璃、保鲜膜、塑料)陈旧指印的显现效果比磁性粉、金粉佳,且显现的指印有荧光。磁性粉、金粉无荧光,指印遗留物质挥发降低了磁粉、金粉对纹线的吸附能力,使得纹线模糊、与背景反差下降。他们对于纸张等渗透客体上陈旧指印的显现效果较好。

图9 粉末荧光图

图10 Au NCs、金粉、磁性粉在不同载体上的显现效果;左:Au NCs;中:传统金粉;右:传统磁性粉
Au NCs对于非渗透性客体上的指印显现效果好于渗透性客体。传统粉显试剂存在以下几个问题:一是由于与纹线结合原理仅靠静电引力等微小作用力易使背景客体着色;二是对陈旧指印的显现效果不好,一旦指印物质减少,显现效果就会变差;三是无荧光,背景客体与纹线反差不鲜明,显现指印效果不佳,对拍摄条件有较高要求。
2.3.3 金纳米簇粉末对纹线特异性分析
采用能谱仪,进一步探究Au NCs粉末对指印乳突纹线的特异性,任意选取Au NCs粉末刷显的指印的乳突纹线和背景客体作为AB两点。对AB两点的元素进行检测,检测结果显示,Au NCs粉末对乳突纹线的特异性良好,Au NCs出现在A点,即指印乳突纹线上;B点处于指印小梨沟位置,未检测到Au NCs。

图11 能谱仪检测; A点:乳突纹线处;B点:小梨沟处
3 结论
本文利用超声- 微波协同新技术,在1 h左右(微波50 s,超声1 h)成功制备了Au NCs,较其他方法更加绿色、高效。在安全低耗的合成环境中既保持了BSA生物活性,同时也高效性地制备了粒子分散性好、粒径小、荧光性能优良的Au NCs。通过不同表征方法对Au NCs性能进行了测定,并获得了最优超声微波时间,即超声1 h,微波辐射50 s,最终将粒径为3.3 nm、荧光量子产率为7.1%的Au NCs成功应用于指印显现,并与传统粉显试剂进行全面比较,构建了自主搭建汗潜指印显现观察系统对新型纳米材料显现指印的高效新方法。相信在本研究的基础上,金属乃至贵金属纳米团簇的优越性会在法庭科学领域中发挥越来越重要的作用。
[1] WILCOXON J P, ABRAMS B L. Synthesis structure and properties of metal nanoclusters[J]. Chem. soc. rev, 2006, 35(5): 1162-1194.
[2] ZHENG J, NICOVICH P R, DICKSON R M. Highly fluorescent noble metal quantum dots[J]. Annual review of physical chemistry, 2007, 58: 409.
[3] YANG S, JIANG Z, CHEN Z, et al. Bovine serum albumin-stabilized gold nanoclusters as a fluorescent probe for determination of ferrous ion in cerebrospinal fluids via the Fenton reaction[J]. MicrochimicaActa, 2015:1-6.
[4] LI SHANG, G. ULRICH NIENHAUS. Gold nanoclusters as novel optical probes for in vitro and in vivo fluorescence imaging[J]. Biophysical Reviews. 2012. 4(4): 313-322.
[5] CHEN Z, QIAN S, CHEN J, et al. Highly fluorescent gold nanoclusters based sensor for the detection of quercetin[J]. Journal of Nanoparticle Research, 2012, 14(12):1-8.
[6] REHN B W, KENDALL F G. Rapid method of super glue®fuming application for the development of latent fingerprints[J]. Journal of Forensic Science, 1983, 28(3): 777-780.
[7] WANG M C, LUO Y P. A comparative study of the use of genipin or ninhydrin in fingerprints development[J]. Forensic Science & Technology, 2013, 6: 33-35.
[8] POUNDS A C, PHIL M, GRIGG R, et al. The use of 1,8-diazafluoren-9-one (DFO) for the fluorescent detection of latent fingerprints on paper[J]. A preliminary evaluation. Journal of Forensicences, 1990, 35(1):169-175.
[9] BECUE A, CHAMPOD C, MARGOT P. Use of gold nanoparticles as molecular intermediates for the detection of fingermarks[J]. Forensic Science International, 2007, 168(2):169-176.
[10] JIE WANG, TING WEI, XINYANG LI, et al. Near-Infrared-Light-Mediated imaging of latent fingerprints based on molecular recognition[J].Angew. Chem., 2014(53): 1616-1620.
[11] ZHANG L Y, CHU T. Synthesis of composite particles with Fe3O4core and Ag shell for the development of fingerprints[J]. Bulletin-Korean Chemical Society, 2013, 34(5):1457-1461.
[12] 柴芳, 代起君, 吴红波. 一种荧光金纳米簇用于潜指印显现的方法:201210443554.X[P]. 2013-05-01.
[13] JIANPING X, YUANGANG Z, YING J Y. Protein-directed synthesis of highly fluorescent gold nanoclusters[J]. Journal of the American Chemical Society, 2009, 131(3):888-889.
[14] 李凡修. 超声/微波辅助制备纳米TiO2及光催化性能研究[D]. 武汉: 华中科技大学, 2008.
[15] 杜军, 林亮, 刘作华,等. 微波对TiO2溶胶低温晶化影响的研究[J]. 压电与声光, 2009, 31(5):703-705.
[16] CHEN Y F, FENG L. The application of image processing technology in the standardization of physical evidence photos[J]. Image Technology, 2005.
[17] JIN R. Quantum sized,thiolate-protected gold nanoclusters[J]. Nanoscale, 2010, 2(3): 343-362.
[18] 杨霞, 王胜平, 马新宾.微波技术在催化剂制备中的应用[J].化学通报, 2004, 641-647.
[19] 杜娟. 金纳米粒子微波及水热反应合成研究及其在光谱分析中的应用[D]. 重庆: 重庆大学, 2013.
[20] BALL & AMP P, GARWIN L. Science at the atomic scale[J]. Nature, 1992, 355(355):761-766.
[21] ZHANG M, DANG Y Q, LIU T Y, et al. Pressure-induced fluorescence enhancement of the BSA-Protected gold nanoclusters and the corresponding conformational changes of protein[J]. J. Phys. Chem. C, 2012, 117(1):639-647.
[22] KUBIN R F, FLETCHER A N. Fluorescence quantum yields of some rhodaminedyes[J]. Journal of Luminescence, 1983, 27(4):455-462.
[23] MCKENNISJR H, TURNBULL L B, BOWMAN E R. Bowman E R. γ-(3-PYRIDYL)-γ-methylaminobutyric acid as a urinary metabolite of nicotine1[J]. Journal of the American Chemical Society, 1957, 79(23): 6342-6343.
[24] 黄锐, 刘睿. 荧光铂纳米簇对汗潜指印的显现研究[J]. 刑事技术, 2017.
(责任编辑 陈小明)
重庆市科学技术委员会基础与前沿研究计划项目(cstc2016jcyjA0503);重庆市教育委员会科学技术研究项目(KJ1500111);物证技术重庆高校工程研究中心研究项目(LCFS1421);2015年西南政法大学资助项目(2015XZQN-27)。
黄 锐(1982—), 女, 重庆人, 博士, 讲师。 研究方向为物证技术学、分析化学。
D918.91
