复方桑菊口服液的质量标准研究
2017-06-19魏娜于莉尹茂山徐建江
魏娜,于莉,尹茂山,徐建江
药学
复方桑菊口服液的质量标准研究
魏娜,于莉,尹茂山,徐建江*
目的建立复方桑菊口服液的质量控制方法并考察其稳定性,为临床用药提供理论指导。方法用高效液相色谱法测定绿原酸和连翘苷的含量,色谱柱为YMC-Pack ODS-AQL(250 mm×4.6 mm,5 μm)流动相为乙腈-水25∶75,柱温为25℃,检测波长为220 nm流速为1.0 ml/min采用留样观察法进行初步稳定性试验。结果通过探索性试验建立该药的色谱测量方法。绿原酸、连翘苷分别在0.011~0.22,0.02~0.4 μg线性关系良好,平均回收率分别为99.7%和99.5%,RSD为1.6%,2.1%,n=6,比较该制剂放置6个月3批样品与新样品间的各项指标均无明显变化。结论所用测定方法简单,准确度高,药物的质量稳定可靠,可作为该复方制剂质量标准的参考。
高效液相色谱;绿原酸;连翘苷;质量控制;复方桑菊口服液
复方桑菊口服液处方是由桑叶、野菊花、连翘、甘草、桔梗、芦根、苦杏仁、薄荷叶等组成。具有清热解毒、辛凉解表、利咽消肿等作用,主要是用于病毒感染或者病毒混合感染的呼吸道感冒[1]。
笔者参照中国药典2015年版中药复方口服制剂的质量标准,采用薄层层析鉴定复方桑菊口服液,并用高效液相色谱法(HPLC)测定该复方制剂中连翘苷含量,为完善复方桑菊口服液质量标准提供参考。
1 材料与仪器
1.1 药材及试药复方桑菊口服液,桑叶、野菊花、连翘、苦杏仁、桔梗、甘草、芦根和薄荷对照药材,绿原酸、连翘苷、甘草酸对照品(购自上海麦克林生化试剂),乙腈为色谱纯,水为纯净水,其余试剂为分析纯。
1.2 主要仪器Agilent 1260型高效液相色谱仪(配有低压四元泵、柱温箱、自动进样器、DAD检测器、ChemStations色谱工作站);UVProbe-2450紫外可见分光光度仪(日本岛津公司);BP211D电子天平(德国赛多利斯公司);PHSJ-4A酸度计(上海雷磁仪器厂)。
2 方法与结果
2.1 含量测定方法学建立
2.1.1 色谱条件色谱柱YMC-Pack ODS-AQL1(250 mm×4.6 mm,5 μm)流动相:乙腈-水(25∶75),流速:1.0 ml/min,柱温:25℃,检测波长:230 nm,进样量:20 μl。
2.1.2 对照品溶液的配制取连翘苷对照品约14.00mg,绿原酸对照品7.50mg,甲醇溶解,置100 ml棕色容量瓶中定容,得到含0.11 mg/ml的绿原酸和0.20 mg/ml连翘苷混合对照品储备液。精密量取5.00ml溶液置100ml量瓶中,加甲醇定容,经0.45μm微孔滤膜过滤即得5.5 g/ml绿原酸和10 g/ml连翘苷的混合对照品溶液。
2.1.3 供试品溶液的制备取复方桑菊清热口服液0.3 ml,过10%甲醇溶液活化的Sep-Peck18小柱,用2 ml 30%甲醇以1滴/s的速度推出淋洗液定容于5 ml量瓶中,摇匀经0.45μm微孔滤膜滤过即得。
2.1.4 空白对照液的制备将处方中的桑叶、野菊花和连翘除去,根据制剂工艺的制备方法制备复方桑菊口服液阴性样品溶液。准确吸取溶液0.5 ml,然后按供试品制备方法制备空白对照液。
2.1.5 方法可行性考察准确取对照品液和供试品液各20μl,进样,结果表明绿原酸、连翘苷理论塔板数>4000,对称因子为0.98,信噪比>3.0。
2.1.6 标准曲线准确吸取混合对照品溶液2、4、6、8、10、20、40 μl,进样,结果表明绿原酸进样量在0.011-0.22 μg、连翘苷在0.02~0.4 μg具有良好的线性关系。绿原酸回归方程为Y=6.211X103+98.70(相关系数0.9999,线性范围0.011~0.22μg);连翘苷回归方程为Y=4.357X103+12.30(相关系数0.9999,线性范围0.02~0.4μg)。
2.1.7 绿原酸与连翘苷加样回收率测定精密吸取已知含量的复方桑菊清热口服液样品6 ml[3-7],含0.059 mg/ml绿原酸和0.106 mg/ml连翘苷6份分别加入混合对照品储备液4 ml,混合均匀再取0.3 ml,经Sep-PackC18小柱处理,定容到5 ml按含量测定条件测定,计算回收率。结果见表1。
2.1.8 精密度实验分别吸对照品溶液20 μl,注入色谱仪,1日以内连续进样6回,测3日,记下色谱图。结果表明绿原酸和连翘苷的日内RSD分别是0.67%和0.45%(n=6),日间RSD分别是0.95%和0.68%(n=3),说明本方法精密度较高。
2.1.9 稳定性试验精密吸取供试品溶液20 μl,然后在室温下于0、2、4、6、8、12、24 h分别注入高效液相色谱仪,测定并记录峰面积。结果显示,绿原酸和连翘苷的RSD分别是0.56%和0.19%(n=6),说明供试品稳定性良好。
2.1.10 重复性试验样品制作3份供试品溶液,准确吸取供试品溶液15 μl注入液相色谱仪,记录峰面积。采用峰面积外标法来算连翘苷和绿原酸含量,结果绿原酸与连翘苷的RSD分别为0.79%和0.48%,n=6,说明本试验方法重复性较优。
2.2 样品含量测定取3批样品,然后每批取6份样,制备供试品溶液,测定样品中绿原酸与连翘苷的含量,外标法计算,结果见表2。

表2 样品含量测定结果(n=3)
2.3 影响试验与加速试验
2.3.1 影响因素试验取样品,分别在低温(4℃)和高温(60℃)条件下进行实验,于0、5、10 h时间点取样测定各指标,结果见表3。

表3 影响因素试验
2.3.2 加速试验把3批样品放置在45℃下6个月,分别用1、2、3表示,其性状、pH以及含量都没有明显变化,绿原酸为A,连翘苷为B。结果见表4。
2.4 薄层定性检查结果样品的相对密度1.12~1.50,pH6.0~8.0。检查结果见图1~3,分析结果见表5。
2.5 含量测定结果据查阅的相关资料和复方桑菊口服液的实验结果[2-14],本研究初步可定复方桑菊口服液中的绿原酸和连翘苷的含量标准为每1 ml含分别不低于0.06 mg和0.12 mg,目前测定的3个批次的复方桑菊口服液中的绿原酸和连翘苷中的含量都符合规定,测定结果见表6。

表4 加速试验及长期试验结果

图1 桑叶
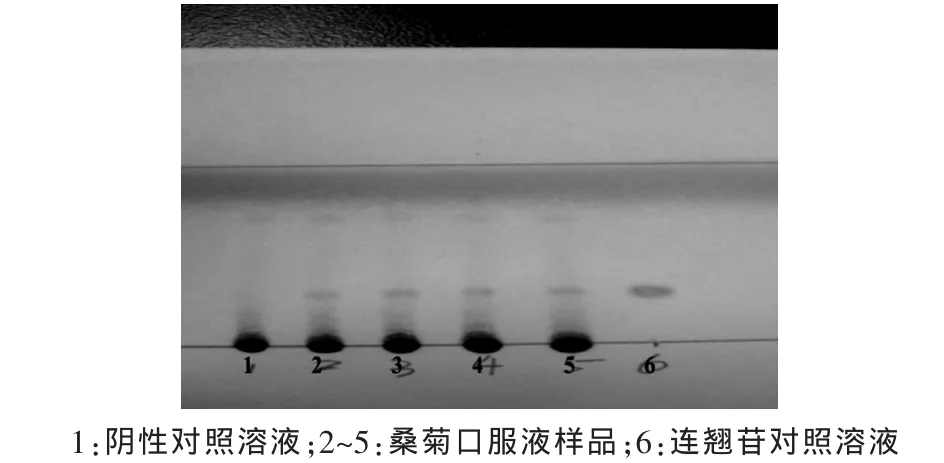
图2 连翘

图3 甘草

表5 相对密度、pH值测定结果

表6 样品含量测定结果(n=3,%)
3 讨论
复方桑菊口服液是传统中成药,该实验采用薄层色谱法(TCL)进行系统的质量标准研究,建立科学高效的薄层色谱(HPLC)鉴别方法[15]。用高效液相色谱法(HPLC)对连翘苷和绿原酸含量进行了含量测定,并开展线性关系分析、精密度、重复性以及稳定性试验等,这种方法简便、结果稳定、行之有效,对复方桑菊口服液进行质量控制;通过薄层色谱法(TCL)对桑菊感冒颗粒的系统研究发现,桑叶、连翘、甘草和薄荷的TLC所得检测斑点显色理想,与样品相应位置上的斑点显色清晰,较大呈现圆斑状,且阴性对照无斑点干扰,通过测定3个不同批号的复方桑菊口服液样品,结果是每1 ml样品中平均含绿原酸和连翘苷分别为0.045 mg和0.112 mg,RSD为0.45%和0.65%,结合桑叶、连翘、甘草的薄层色谱(HPLC)鉴别方法和连翘苷含量的高效液相色谱(HPLC)测量法,是一种高效,简便,重复性好,精确度高的质量标准检测方法,具有推广性。
复方桑菊口服液作为一种新型的口服制剂,结合了传统中药理论和现代制剂工艺。在中医药基础理论的指导下,利用现代研究方法对复方桑菊处方中的君药桑叶和野菊花进行进一步的系统研究,如新剂型的开发、药效研究等,具有重要的社会价值和经济价值[16-18]。
中药制剂的质量控制是关乎其疗效、安全性和稳定性的关键问题,最终影响中医药的健康发展,到目前为止,我国乃至全世界中成药的质量控制标准的研究仍然停留在较低的水平。随着高科技的引入,对于中成药的质量标准研究得到了一定的发展,但是一味地依靠西医、西药等科技手段,不是解决建立科学有效的中成药质量标准体系最佳途径,笔者所在课题组通过相关文献的阅读和相关实验开展的所见所思,对更好建立中成药质量标准体系的思考体现为两方面:一是中药制剂质量控制的前提是中医药理论为指导,结合大数据的不断验证。由于中成药制剂是整个中医文化的一部分,中成药的根本依据是传统的中医理论,有必要加强中医理论的研究、完善以及推广。而中药文化其本质就是中华民族经过几千年的长期实践的文化瑰宝,长期的实践过程其实就是一个大数据的不断验证的过程,最终形成类似《神农本草》《黄帝内经》《本草纲目》等优秀典籍,现阶段可借助大数据在中成药质量标准体系中得以应用,将会得到更为科学的质量标准体系[19]。二是合理利用现代技术。中药由于其种类多,成分复杂,个体差异加大等,都为中成药的质量标准的建立带来困难,随着高科技的发展,一些先进的检测手段对于中成药的研究就有明显的促进作用,如生物免疫技术、电子计算机技术以及中药数字化图谱指纹技术等,但一味地依赖这些手段将会丧失中医文化的根本,不利于中成药质量标准的建立[20]。
[1]吴晓慧.桑菊饮加减治疗上呼吸道感染40例[J].陕西中医2009,30(4):401-402.
[2]李元林,吴群,陈瑶.桑菊口服液抗菌活性成分研究[J].中国医药导报,2015,12(6):38-39.
[3]彭凯丽,李新民,李元林,等.正交试验优选复方桑菊口服液中药材的提取工艺[J].中国药房,2014,29(6):50-51.
[4]侯飞燕,周全彩.复方桑菊口服液的质量控制研究[J].中南药学,2014,25(5):431-432.
[5]王志东,梁荣瑞.中药野菊花的药理作用研究进展[J].医学综述,2009,15(6):906-909.
[6]张振亚,方学平.野菊花提取物抑制呼吸道合胞病毒作用的体外实验研究[J].解放军药学学报,2006,22(4):245-247.
[7]蔡蓁蓁.中成药的传统剂型与新剂型[J].现代中医药,2014(1):46-50.
[8]郑璐璐,张贵君.野菊花药效组成抗炎的生物效应研究[J].天津中医药,2011,1(1):70.
[9]吴石磊.桑叶中东莨菪素提取分离,含量分析及体外抗菌活性研究[D].重庆:西南大学,2009.
[10]姜丽霞.HPLC法测定野菊花中绿原酸的含量[J].中国药品标准,2003,4(6):54-56.
[11]尉芹,马希汉.绿原酸及其提取分离方法评述[J].中成药,2001,23(2):135-137.
[12]国家药典委员会.中华人民共和国药典:一部[S].北京:化学工业出版社,2010:279.
[13]彭凯丽.复方桑菊口服液的制备工艺及其质量标准研究[D].衡阳:南华大学,2014.
[14]李元林,吴群,彭凯丽,等.RP-HPLC法对复方桑菊口服液中的绿原酸蒙、花苷、连翘苷的含量测定[J].湖南师范大学学报:医学版,2013,10(3):90-93.
[15]孙莲,胡尔西单.薄层-紫外分光光度法测定桑叶中的绿原酸[J].时珍国医国药,2006,17(7):1199-1201.
[16]沈梅芳,李小萌,单琪媛.薄荷化学成分与药理作用研究新进展[J].中华中医药学刊,2012,30(7):1484-1487.
[17]李海英,文毅.桑菊感冒片标准研究[J].辽宁中医药杂志,2005,32(8):829-830.
[18]林丽美,许招懂,姚江雄,等.夏桑菊口服液质量标准研究[J].中成药,2012,34(8):1500-1505.
[19]王荣到,苏鹏,李哲.浅谈杏仁和苦杏仁的药理作用及临床应用[J].基层中药杂志,2009,45(9):45-49.
[20]王春芳,张卫兵.HPLC测定抗病毒口服液中连翘苷的含量[J].中国药品标准,2004,5(3):44-46.
[2016-11-15收稿,2016-12-12修回][本文编辑:刘一洋]
Study on the quality standard of Compound Sangjü oral liquid
WEI Na,YU Li.Dept.of Pharmacy,the General Hospital of Jinan Military Region,Jinan,Shandong 250031,China
ObjectiveTo establish a quality control method Compound Sangjü oral liquid and inspect its stability,so as to provide the basis for clinical use.It was important to analyze the content of Sangju oral liquid. MethodsA HPLC was used to determination the content of chlorogenic and phillyrin.The YMC-Pack ODS-AQL column(250 mm×4.6 mm,5 μm)was used,the mobile phase was acetonitribe-water(75∶25),the temperature was 25℃,and the detection wavelength was 220 nm,the flow rate was 1.0 ml/min.Storage observation method was used to determine its stability.ResultsThe linear ranges of chlogenic acid and phillyrin were 0.011-0.22 and 0.02-0.4 μg,The average recoveries of chlorogenic acid and phillyrin were 99.7%and 99.5%respectively.Comparing the preparation placed for 6 months,it was found the 3 samples had all no obvious change.ConclusionThe abovementioned method is simple,reliable,and can be used as a reference for the quality standard.The preparation is stable during the inspected time.
High performance liquid chromatography;Quality control;Chlogenic acid;Phillyrin;Compound Sangjü oral liquid
R927.1
A
10.14172/j.issn1671-4008.2017.06.025
250031山东济南,原济南军区总医院药剂科(魏娜,于莉,徐建江);山东省医学科学院药物所(尹茂山)
徐建江,Email:xjj8605@163.com
