盐酸左氧氟沙星注射液灭菌前已灌封样品微生物限度检查方法学的建立
2017-06-19乔龙娟王林黄加秀田颖王君
乔龙娟,王林,黄加秀,田颖,王君
盐酸左氧氟沙星注射液灭菌前已灌封样品微生物限度检查方法学的建立
乔龙娟,王林,黄加秀,田颖,王君
盐酸左氧氟沙星为氧氟沙星的左旋体,其抗菌活性约为氧氟沙星的两倍,主要作用机制为抑制细菌 DNA 旋转酶的活性,阻碍细菌 DNA 复制,对大多数革兰阴性菌和革兰阳性菌均有较强的抗菌作用[1]。因其抗菌谱广,抗菌作用强,维持时间长,疗效高,不良反应轻微,临床应用范围广泛[2]。
根据新版 GMP 的要求,应当依据所用灭菌方法的效果确定灭菌前产品微生物污染水平的监控标准,并定期监控[3-4]。检验方法的可靠直接决定产品日常监测的结果,笔者据此建立了盐酸左氧氟沙星注射液灭菌前已灌封样品的微生物限度检查方法,并进行了方法学验证。
1 材料与方法
1.1 材料
1.1.1 供试品 盐酸左氧氟沙星注射液配制液(规格:0.1 g/ml,批号:16062231、16071131、16071331)为扬子江药业集团有限公司产品。
1.1.2 试验用菌种 金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、大肠埃希菌[CMCC(B)44102]、白色念珠菌[CMCC(F)98001]、黑曲霉菌[CMCC(F)98003]均来自中国菌种保藏中心。
1.1.3 稀释液和缓冲液 0.9% 无菌氯化钠溶液、pH 7.0的无菌氯化钠-蛋白胨缓冲液均为自制。
1.1.4 培养基 胰酪大豆胨液体培养基(批号:20160310)、胰酪大豆胨琼脂培养基(批号:20160308)、沙氏葡萄糖琼脂培养基(批号:20160310)、沙氏葡萄糖液体培养基(批号:20160318),均由北京三药科技开发有限公司提供。
1.1.5 仪器 ZH-2 型旋涡混合仪购自上海沪西医疗仪器厂;HTY-601 型集菌仪和全封闭集菌培养器均购自浙江泰林生物技术股份有限公司;KB400 型恒温培养箱购自德国宾得公司。
1.2 方法
1.2.1 菌液制备 分别接种大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的新鲜培养物至胰酪大豆胨液体培养基,接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,30 ~35 ℃ 培养 18 ~ 24 h;接种白色念珠菌的新鲜培养物至沙氏葡萄糖液体培养基中,20 ~ 25 ℃ 培养 24 ~ 48 h。上述培养物用 0.9% 无菌氯化钠溶液稀释成含菌数小于 100 cfu/ml的菌悬液。接种黑曲霉的新鲜培养物至胰酪大豆胨琼脂斜面培养基中,培养 5 ~ 7 d,产生大量孢子,加入 3 ~ 5 ml 含 0.05%(v/v)聚山梨酯 80 的 0.9% 无菌氯化钠溶液,将孢子洗脱,然后吸出孢子悬液(管口带有薄的无菌棉花过滤菌丝)至灭菌试管内,用含 0.05%(v/v)聚山梨酯 80 的 0.9%无菌氯化钠溶液将菌液稀释至含 50 ~ 100 cfu/ml 的菌悬液,备用[4]。
1.2.2 需氧菌检查方法
1.2.2.1 需氧菌检查方法的预验证一 盐酸左氧氟沙星对大多数细菌均有较强的抗菌作用,但对厌氧菌和肠球菌的抑菌作用较差,故采用薄膜过滤法通过冲洗液及冲洗液加中和剂的方法[5]分别对铜绿假单胞菌、金黄色葡萄球菌及枯草芽孢杆菌进行实验,以确定最终的验证方法。
试验组:
A:取供试液 19.9 ml 和小于 10 000 cfu 的铜绿假单胞菌菌悬液 0.1 ml 混匀,然后取上述混匀后的样品 2 ml 至含有 100 ml pH 7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,然后用 pH 7.0 的无菌氯化钠-蛋白胨缓冲液900 ml 冲洗,每次 100 ml,冲洗结束后取出滤膜,菌面朝上贴至胰酪大豆胨琼脂培养基平板上,于 30 ~ 35 ℃ 倒置培养 3 d,逐日点计菌落数。金黄色葡萄球菌、枯草芽孢杆菌同法操作。
B:采用每 250 ml 含 1 ml 聚山梨酯 80 的缓冲液冲洗,其余操作同“A”。
C:采用每 250 ml 含 1 ml 3 mol/L 氯化镁溶液的缓冲液冲洗,其余操作同“A”。
菌液组:以稀释液代替供试液,其余按照“试验组”项下 A、B、C 试验组方法进行操作。
1.2.2.2 需氧菌检查方法的预验证二
试验组:
D:取供试液 2 ml 至含有 100 ml pH7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,然后用 pH 7.0 的无菌氯化钠-蛋白胨缓冲液 900 ml 冲洗,每次 100 ml,在最后一次冲洗液中加入不大于 100 cfu/ml 的铜绿假单胞菌菌悬液,冲洗结束后取出滤膜,菌面朝上贴至胰酪大豆胨琼脂培养基平板上,于 30 ~ 35 ℃ 倒置培养 3 d,逐日点计菌落数。金黄色葡萄球菌、枯草芽孢杆菌同法操作。
E:采用每 250 ml 含 1 ml 3 mol/L 氯化镁溶液的缓冲液冲洗,其余操作同“D”。
F:采用每 250 ml 含 1 ml 聚山梨酯 80 和 1 ml 3 mol/L 氯化镁溶液的缓冲液冲洗[6-8],其余操作同“D”。
菌液组:以稀释液代替供试液,按照“试验组”项下D、E、F 方法进行操作。
1.2.2.3 需氧菌检查方法的验证
取 3 批进行验证。
试验组:取供试液 2 ml 至含有 100 ml pH 7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,然后用每 250 ml含 1 ml 聚山梨酯 80 和 1 ml 3 mol/L 氯化镁溶液的 pH 7.0的无菌氯化钠-蛋白胨缓冲液 900 ml 冲洗,每次 100 ml,在最后一次冲洗液中加入不大于 100 cfu/ml 的铜绿假单胞菌菌悬液,冲洗结束后取出滤膜,菌面朝上贴至胰酪大豆胨琼脂培养基平板上,于 30 ~ 35 ℃ 倒置培养 3 d,逐日点计菌落数。金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌及黑曲霉同法操作。
菌液组:以稀释液代替供试液,照“试验组”项下方法进行操作。
供试品对照组:以稀释液代替菌悬液,照“试验组”项下方法进行操作。
稀释剂对照组:取试验菌 1 ml 至含 100 ml pH 7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,照“试验组”项下方法进行操作。
1.2.3 霉菌及酵母菌检查方法
1.2.3.1 霉菌及酵母菌检查方法的预验证
试验组:
H:取供试液 19.9 ml 和小于 10 000 cfu 的白色念珠菌菌悬液 0.1 ml 混匀,然后取上述混匀后的样品 2 ml 至含有 100 ml pH7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,用 pH 7.0 的无菌氯化钠-蛋白胨缓冲液 200 ml冲洗,每次 100 ml,冲洗结束后取出滤膜,菌面朝上贴至沙氏葡萄糖琼脂培养基平板上,于 20 ~ 25 ℃ 倒置培养 5 d,逐日点计菌落数。黑曲霉同法操作。
I:采用 pH 7.0 的无菌氯化钠-蛋白胨缓冲液 500 ml冲洗,其余操作同“H”。
菌液组:以稀释液代替供试液,其余照“试验组”项下H、I 方法进行操作。
1.2.3.2 霉菌及酵母菌检查方法的验证
取 3 批进行验证。
试验组:取供试液 19.9 ml 和小于 10 000 cfu 的白色念珠菌菌悬液混匀,然后取上述混匀后的样品 2 ml 至含有100 ml pH7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,然后用 pH7.0 的无菌氯化钠-蛋白胨缓冲液 200 ml冲洗,每次 100 ml,冲洗结束后取出滤膜,菌面朝上贴至沙氏葡萄糖琼脂培养基平板上,于 20 ~ 25 ℃ 倒置培养 5 d,逐日点计菌落数。黑曲霉同法操作。
菌液组:以稀释液代替供试液,照“试验组”项下方法进行操作。
供试品对照组:以稀释液代替菌悬液,照“试验组”项下方法进行操作。
稀释剂对照组:取试验菌 1 ml 至含 100 ml pH 7.0 的无菌氯化钠-蛋白胨缓冲液的集菌培养器中过滤,照“试验组”项下方法进行操作。
2 结果
2.1 需氧菌检查方法的验证
2.1.1 需氧菌检查方法的预验证一结果采用方法 A、B、C 的试验组在培养 3 d 后,铜绿假单胞菌、金黄色葡萄球菌及枯草芽孢杆菌的平板上均无菌产生,试验组的回收率为0,三种方法均不适用该样品的需氧菌检查。
2.1.2 需氧菌检查方法的预验证二结果当试验组采用方法 F 时,在培养 3 d 后,铜绿假单胞菌、金黄色葡萄球菌及枯草芽孢杆菌的试验组的回收率均大于 90%(表 1)。初步判定方法 F 适用于该供试品的需氧菌检查,故采用该方法进行正式验证。

表 1 需氧菌预验证二结果(回收率 %)
2.1.3 需氧菌检查方法的验证结果经过 3 批样品的验证,铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的试验组回收率均在 50% ~ 200% 之间,且对应稀释剂对照组的回收率也符合要求(表 2)。

表 2 需氧菌验证结果(回收率 %)
2.2 霉菌及酵母菌检查方法的验证
2.2.1 霉菌及酵母菌方法的预验证结果当冲洗量分别为200、500 ml 时,白色念珠菌和黑曲霉的回收率均符合试验要求且相差不大(表 3)。故采用冲洗量为 200 ml 进行正式验证。

表 3 霉菌及酵母菌预验证一结果(回收率 %)
2.2.2 霉菌及酵母菌方法的验证结果3 批样品的白色念珠菌、黑曲霉的试验组回收率均在 50% ~ 200% 之间,且稀释剂对照组的回收率也符合要求(表 4)。
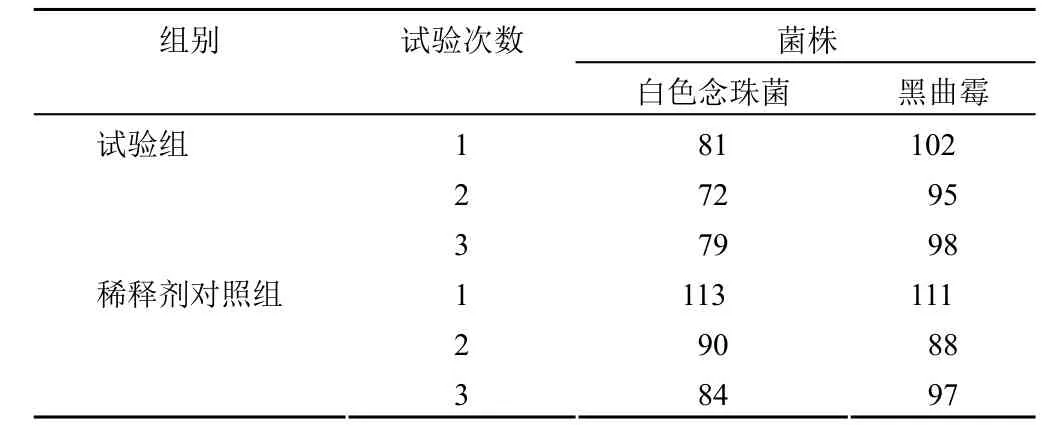
表 4 霉菌及酵母菌验证结果(回收率 %)
2.3 盐酸左氧氟沙星注射液灭菌前已灌封样品微生物限度检查方法
需氧菌检查:配制液进行薄膜过滤后采用每 250 ml 含1 ml 聚山梨酯 80 和 1 ml 3 mol/L 氯化镁溶液的 pH 7.0无菌氯化钠-蛋白胨缓冲液 900 ml 冲洗,每次 100 ml。
霉菌及酵母菌检查:配制液进行薄膜过滤后用 pH 7.0的无菌氯化钠-蛋白胨缓冲液冲洗 2 次,每次 100 ml。
3 讨论
由于盐酸左氧氟沙星有较强的抑菌性,单纯采用薄膜过滤法不能消除其抑菌性。根据对喹诺酮类药物化学性质的分析,该类药品能够与部分金属离子(Fe2+、Mg2+、Mn2+等)进行络合反应形成稳定的六元环络合物,最终能达到消除抑菌活性的目的[6]。本文采用薄膜过滤法通过冲洗液及冲洗液加中和剂的方法分别进行了验证,通过在冲洗液中添加适量的中和剂(聚山梨酯 80 和氯化镁)能有效地消除抑菌活性。
本文将菌悬液和供试液混匀后进行验证时,试验组的回收率始终为 0。而根据《中国药典》(2015 版)的规定:如果供试品对微生物生长的抑制作用无法以其他方法消除,供试液可经过中和、稀释或薄膜过滤处理后再加入试验菌悬液进行方法适用性试验[5]。据此在最后一次冲洗液中加入符合要求的菌悬液进行多次试验,确立了盐酸左氧氟沙星注射液灭菌前已灌封样品需氧菌、霉菌及酵母菌的微生物限度检查方法。
聚山梨酯 80 和氯化镁作为中和剂加入到冲洗液后,试验结果对菌株无影响。在制备含聚山梨酯 80 和氯化镁的冲洗液时,建议采用将聚山梨酯 80、氯化镁溶液与缓冲液混合均匀、分装后进行灭菌,用于供试品的检测。
[1] Tang YH, Wu CR, Wei Y, et al. In vitro and in vivo antibacterial activities of levofloxac in against clinic isolates. Herald Med, 2007, 26(9):983-986. (in Chinese)唐映红, 伍参荣, 魏云, 等. 盐酸左氧氟沙星体内外抗菌作用研究.医药导报, 2007, 26(9):983-986.
[2] Tananka M, Otsuk IM, Une T, et al. In-vitro and in-vivo activity of DR-3355, an optically active isomer of ofloxacin. J Antimicrob Chemother, 1990, 26(5):659-666.
[3] Cao Y, Liang Y. Study on microbial control of aseptic drug before sterilization. China Pharm, 2009, 18(22):9-11. (in Chinese)曹元, 梁毅. 无菌药品灭菌前微生物控制研究. 中国药业, 2009, 18(22):9-11.
[4] Huang JX, Xie CJ, Wang L, et al. Methodology validation for microbial limit test of liquid preparation of pantoprazole sodium for injection before filtration sterilization. China Pharm, 2013, 24(45): 4307-4309. (in Chinese)黄加秀, 谢春娟, 王林, 等. 注射用泮托拉唑钠过滤除菌前配制液的微生物限度检查方法学验证. 中国药房, 2013, 24(45):4307-4309.
[5] Chinese Pharmacopoeia Commission. Pharmacopoeia of the People’s Republic of China. Volume 4, 2015. Beijing: China Medical Science Press, 2015. (in Chinese)国家药典委员会. 中华人民共和国药典. 2015年版四部. 北京: 中国医药科技出版社, 2015.
[6] Zhang GH, Yu L, Liu WJ. Application of manganese sulfate in sterility test of several quinolones. Drug Stand China, 2008, 9(1):35-38. (in Chinese)张光华, 余立, 刘文杰. 硫酸锰在几种喹诺酮类药物无菌检查中的应用. 中国药品标准, 2008, 9(1):35-38.
[7] Song ZM, Shi L, Li LY. Study on the in-vitro antibacterial activity of levofloxacin against 325 bacteria isolates from patients. Guizhou Med J, 2001, 25(10):677-678. (in Chinese)宋振民, 石磊, 李凌云. 盐酸左氧氟沙星对325株分离细菌的体外抗菌活性. 贵州医药, 2001, 25(10):677-678.
[8] Yang XC, Xie JJ. Validation of microbial limit test for levofloxacin hydrochloride capsules. J Practical Med Tech, 2011, 18(11):1173-1175. (in Chinese)杨小春, 谢家军. 盐酸左氧氟沙星胶囊微生物限度检查方法的建立. 实用医技杂志, 2011, 18(11):1173-1175.
10.3969/j.issn.1673-713X.2017.03.016
225321 泰州,扬子江药业集团有限公司
王林,Email:wanglin@yangzijiang.com
2017-03-11
