东海海水和大气中挥发性卤代烃的分布、来源和海-气通量研究*
2017-06-19杨桂朋李冠霖
袁 达, 何 真, 杨桂朋,2**, 李冠霖
(1.中国海洋大学化学化工学院,海洋化学与理论教育部重点实验室,山东 青岛 266100;2.海洋国家实验室海洋生态与环境科学功能实验室,山东 青岛 266071)
东海海水和大气中挥发性卤代烃的分布、来源和海-气通量研究*
袁 达1, 何 真1, 杨桂朋1,2**, 李冠霖1
(1.中国海洋大学化学化工学院,海洋化学与理论教育部重点实验室,山东 青岛 266100;2.海洋国家实验室海洋生态与环境科学功能实验室,山东 青岛 266071)
于2014年10月和2015年6月对东海海水和大气中挥发性卤代烃(VHOCs)的浓度分布、来源及海-气通量进行了系统的研究。结果表明:秋季东海海水中二氟二氯甲烷(CFC-12)、三氯氟甲烷(CFC-11)、三氟三氯乙烷(CFC-113)的浓度普遍高于夏季。秋季和夏季3种CFCs的水平分布均呈现近岸高,外海低的趋势,其分布主要受到陆源输入和长江冲淡水的影响。海水中碘甲烷(CH3I)的分布表现出明显的季节变化,浓度高值出现在夏季。CH3I的分布受到陆源输入、浮游植物释放和光化学合成的影响。夏季东海大气中3种氟氯烃CFC-12、CFC-11和CFC-113的浓度分布主要受陆源气团输送和气象条件的影响;CH3I的来源除陆源释放外,海洋释放也十分重要。总体来说夏季东海海域是大气中CFC-12和CFC-11的汇,是CH3I的源。
挥发性卤代烃;分布;海洋大气;东海
挥发性卤代烃(Volatile halogenated organic compounds,VHOCs)是大气中普遍存在的一类重要的痕量温室气体和主要的损耗臭氧层物质(Ozone-depleting Substances,ODS),具有影响对流层气候和破坏平流层臭氧层的双重效应[1-3]。其中氟氯烃(CFCs)作为一类人为来源的卤代烃,在工业生产和社会生活中被广泛的用作制冷剂、发泡剂、溶剂和喷雾剂。CFCs被认为是极地臭氧消耗最主要的贡献者,所以被《蒙特利尔议定书》列为受控物质,但是目前CFCs在不同的地区,特别是在发展中国家仍被大量的使用,其每年的释放量仍很显著[4]。碘甲烷(CH3I)是大气中碘自由基最主要的天然来源,其活性高于CH3Cl和CH3Br,目前已成为VHOCs研究的新热点[5]。
海洋和大气在VHOCs的生物地球化学循环过程中有显著的作用。海洋边界层大气是运输陆源污染物进入海洋的载体,构成陆地和海洋之间构成一个重要的环节。海洋是VHOCs的一个巨大储库,是大气VHOCs的重要天然来源,海洋释放的VHOCs对于大气中VHOCs的浓度水平和大气环境具有重要影响[6]。正是由于海洋和大气VHOCs对全球气候变化所起的重要作用,国际上针对其浓度时空分布,源与汇和海-气交换通量及其影响因素等进行了大量研究,研究领域已涉及世界各大洋及部分近海和海湾等若干海域及其相应的大气。已有的研究表明海水中VHOCs的浓度分布一般近岸海域大于大洋区[6],海-气通量同海水浓度相似一般呈现近岸海域大于大洋区[7];多年连续的观测数据表明,大气中VHOCs的浓度在近些年经过人为调控正在逐渐降低[1],而且近岸海域上层大气中VHOCs浓度一般高于大洋区[8],高纬度海区低于低纬度海区低于热带[5, 9]。然而国内对于有关海洋VHOCs的研究工作仍处于初步阶段[10-14],特别是缺少关于近岸海洋边界层大气中VHOCs的研究,缺少这些研究会严重阻碍中国和全球VHOCs的数据库的建立,而且会对中国近岸海域VHOCs源汇平衡的估算造成很大的误差,进而对于估算中国近岸海域对全球变暖和臭氧层空洞的贡献造成很大的误差。因此本文选择东海作为研究海域,对东海海水和大气中VHOCs的分布、来源和季节变化进行了系统的研究,首次讨论了浮游植物丰度和种类对海水中VHOCs分布的影响。此研究有助于了解中国近岸海域对东海海水和大气中VHOCs的贡献以及中国近岸海域的污染情况,为更加深入地认识中国海域VHOCs的生物地球化学循环过程以及东海对全球VHOCs的区域性贡献提供一定的科学依据,进而发展建立VHOCs的生物地球化学模型,了解VHOCs的释放对区域和全球环境气候变化的影响。
1 样品采集和分析
1.1 样品采集
分别于2014年10月18日-11月1日(秋季)和2015年6月11日-6月21日(夏季)搭乘“科学3号”科学考察船对东海进行了取样调查(见图1)。并选取3000断面进行VHOCs的垂直分布研究。每个站位不同深度的海水样品通过调查船上的Niskin采水器采集获得,之后将海水分装到100 mL的注射器中,尽快现场分析。大气样品由经过电弧抛光的真空不锈钢罐采集,为了防止来自船体的污染,在将要停船时(船速一般大于2节)将真空不锈钢罐置于船的最顶层甲板,迎着风向,用手轻轻打开罐体上开关进行采样,等到响声停止,迅速关闭开关,旋紧螺母,采样时间平均约为2 min。样品采集后密封保存,待返回实验室进行测定。环境参数和水文参数,如海水温度、盐度及溶解氧由船上的CTD(conductivity, temperature, and depth)设备采集海水样品时同步测定完成。经纬度、气温等气象数据由船载气象观测仪(Young公司,美国)时时观测。在水面上方大约10 m处测定风速。
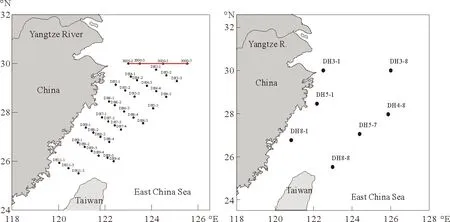
图1 2014年秋季和2015年夏季东海航次采样站位图
1.2 大气样品中VHOCs的分析方法
采用三阶冷凝的方法,对大气样品进行预浓缩预处理,能有效去除样品中的干扰气体,如H2O(g)、CO2、惰性气体、N2等。第一阶段:通过将大气采样罐和预浓缩仪进样口连接,用泵将400 mL大气样品抽至第一个捕集肼中(吸附剂为玻璃微珠),用液氮将捕集肼冷却至-150 ℃,样品中的目标化学物VHOCs和一部分挥发性化合物(H2O(g)、CO2等)就被捕集在吸附肼中,而O2和N2因无法被捕集而去除,之后预加热捕集肼至-30 ℃再加热至10 ℃,可以使水保持液态不被解吸,而又能够使目标化合物充分解吸出来。第二阶段:第一阶段捕集肼里解吸出的化合物在高纯He气的输送下进入第二阶段捕集肼中(吸附剂为Tenax TA),H2O则留在第一阶段捕集肼中被去除。将第二级捕集肼用液氮冷冻至-30℃,使CO2很快通过捕集肼不被吸附而去除,而目标化合物VHOCs则因吸附被阻流在第二阶段捕集肼中。然后加热第二级捕集肼至190℃,使目标化合物VHOCs解吸下来。第三阶段:高纯He气将第二级捕集肼中的目标化合物VHOCs输入第三级捕集肼中,为了获得更好的分离效果和色谱图,用液氮将第三级捕集肼冷却至-170℃使目标化合物VHOCs进行低温聚焦,之后加热第三级捕集肼至100℃,使目标化合物VHOCs进行热解吸,之后输送进入色谱柱分离,使用气相色谱-质谱联用仪(GC-MSD)分析检测。本实验测定VHOCs的方法检出限为0.1~0.5 ppt,精密度均在3%之内。
1.3 海水样品中VHOCs的分析方法
首先用玻璃注射器将体积为100 mL的海水样品注入吹扫室,通过吹扫-捕集系统对海水样品进行预浓缩预处理,然后经色谱柱分离,用气相色谱-电子捕获检测器进行测定,通过外标法进行定量分析,具体分析方法见文献[15]。
1.4 叶绿素(Chl-a)含量的测定
于小于15 kPa压力下用Whatman GF/F玻璃纤维滤膜(直径47 mm)过滤300 mL海水。在温度4 ℃以下并且避光的条件下,用10 mL 90%的丙酮对Chl-a滤膜进行24 h萃取,之后使用F-4500荧光仪(日本日立)采用荧光法测定Chl-a,具体分析方法见文献[16]。
1.5 浮游植物丰度和种类的测定
在浮游植物定量分析中,通常使用光学显微镜对定量分析样品进行细胞计数和体积测量,最后计算出浮游植物丰度。具体分析方法见文献[17]。
2 结果与讨论
2.1 秋季东海表层海水中4种VHOCs的浓度分布
调查期间秋季东海表层海水温度范围介于21.1~25.8 ℃,平均值为(24.0±0.9)℃,表层温度分布如图2A所示,呈现从近岸向外海逐渐增加的趋势。秋季东海航次调查结果显示,东海表层海水中Chl-a浓度平均值为(1.18±0.97)μg·L-1,浓度范围为0.09~3.63 μg·L-1,水平分布如图2B所示,高值区主要分布在浙江近岸水域,可能是受到沿海陆源径流输入和长江冲淡水输入大量营养盐的影响。Chl-a浓度最高值3.63 μg·L-1和次高值3.58 μg·L-1分别出现在浙江近岸的DH6-1和DH4-1站位,该海域对应东海赤潮高发海域[18]。

图2 秋季东海海水温度 (℃)、Chl-a (μg·L-1)和4种VHOCs (pmol·L-1)浓度的水平分布图
调查期间东海表层海水中二氟二氯甲烷(CFC-12)、三氯氟甲烷(CFC-11)、三氟三氯乙烷(CFC-113)浓度范围分别为2.4~55.4、2.3~76.5和0.3~24.3 pmol·L-1,平均值分别为(15.3±12.8)、(18.5±15.9)和(6.9±5.0)pmol·L-1。CFC-11和CFC-113的浓度高于加拿大海盆中CFC-11和CFC-113的浓度平均值(CFC-11:5.98 pmol·L-1;CFC-11:0.57 pmol·L-1)和楚科奇海海水浓度平局值(CFC-11:6.38 pmol·L-1;CFC-11:0.58 pmol·L-1)[19]。通过浓度差异推测中国东海CFCs的污染比较严重。秋季东海表层海水中CFC-12、CFC-11和CFC-113的浓度水平分布如图2C、D、E所示,3种CFCs的浓度水平分布特征十分相似,均呈现由近岸向远海逐渐减小的趋势,可能是受到浙江沿海人类活动释放的CFCs大量输入的影响。如CFC-11和CFC-113浓度的最高值,CFC-12浓度的次高值均出现在浙江沿海的DH8-1站位,明显与浙江的陆源输入有关。相关性分析结果(见表1)表明CFC-12,CFC-11和CFC-113之间存在显著的正相关关系,推测它们可能存在相似的来源。CFC-12和CFC-113与温度均表现出显著的负相关关系,可能是温度通过影响CFC-12和CFC-113的溶解度,从而影响其浓度。温度越高,CFC-12和CFC-113的溶解度越低,说明东海表层海水中CFC-12和CFC-113分布的受到温度的影响,与Yuan[20]报道的长江口及其邻近海域CFC-12和CFC-113的分布与温度的相关性结果相同。而CFC-11与温度没有表现出显著的关系,可能是由于近岸陆源CFC-11的大量输入,根据Yuan[20]报道可知长江径流对于CFC-11的年输入量远高于CFC-12和CFC-113的年输入量;同时表层海水中CFC-11和大气中CFC-11持续不断的交换也会影响温度与CFC-11的相关关系[21]。
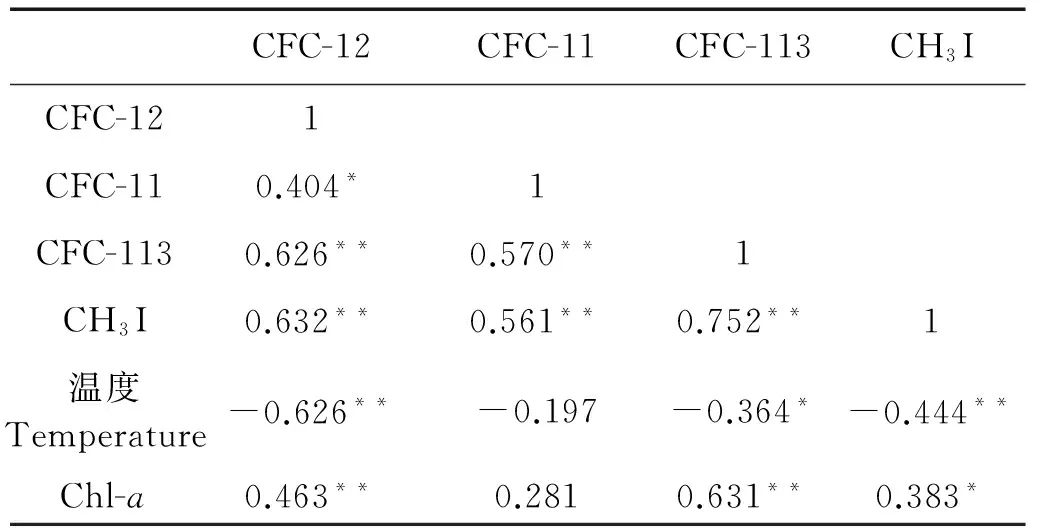
表1 秋季东海海水中4种VHOCs浓度与环境参数的相关性分析
注:**. 在 0.01 水平(双侧)上显著相关。*. 在 0.05 水平(双侧)上显著相关。**: Correlation is significant at the 0.01 level (2-tailled).*: Correlation is significant at the 0.05 level (2-tailled).
秋季东海表层海水中CH3I的浓度平均值为(4.4±3.0)pmol·L-1,对应的浓度范围介于1.0~13.7 pmol·L-1。CH3I浓度的水平分布大致呈现近岸高,外海低的趋势,高值区出现在浙江沿海(见图2F),与Chl-a浓度的水平分布特征相似,所以秋季东海海水中CH3I浓度的水平分布可能受到生物释放的影响。本研究同时测定了东海航次各站位的物种组成和浮游植物丰度,秋季东海的浮游植物优势藻种是硅藻(如角毛藻、菱形藻、骨条藻、根管藻、圆筛藻、链藻等),每个站位硅藻丰度所占比例均在90%以上。浮游植物丰度较高的站位出现在台湾海峡附近的DH11-1和DH11-5站位以及浙江沿海的DH7-1和DH8-1站位。CH3I浓度的最大值出现在浙江沿海的DH8-1站位,伴随着较高的叶绿素浓度(3.22 μg·L-1),同时测得DH8-1站位的优势藻种为尖刺菱形藻(Nitzschia pungens)、浮动弯角藻(Eucampia zodiacus)、角毛藻(Chaetoceros)和劳氏角毛藻(Chaetoceros lorenzianus),丰度分别为28 500、19 000、19 000和19 000 cells·L-1。在DH7-1站位观测到CH3I浓度的次高值,DH7-1站位的优势藻种和其丰度分别为丹麦细柱藻(Leptocylindrus danicus)(32 760 cells·L-1),旋链角毛藻(Chaetoceros curvisetus)(25 740 cells·L-1),中肋骨条藻(Skeletonema costatum)(22 620 cells·L-1)、角毛藻(Chaetoceros)(17 160 cells·L-1)和尖刺菱形藻(Nitzschia pungens)(10 920 cells·L-1)。而CH3I浓度的低值区出现在DH9-2附近海域,但该站位浮游植物丰度较高(106 470 cells·L-1),优势藻种为旋链角毛藻(Chaetoceros curvisetus),丰度为31 200 cells·L-1。这些结果说明CH3I的生物生产释放受到浮游植物丰度和种类的影响,旋链角毛藻不是CH3I的主要生产者,尖刺菱形藻和角毛藻可能是CH3I的重要生产者。从表1可知,CH3I与3种CFCs均表现出显著的正相关关系,而CFCs作为一种人为合成的卤代烃只有人为来源,不具有生物活性,在海水中相对稳定,CFCs可以表征VHOCs的人为陆源输入,说明在调查海域CH3I的分布同样受到近岸陆源输入和长江径流输入的影响。所以秋季东海表层海水中CH3I浓度的水平分布可能受到陆源输入和生物释放的共同作用。
2.2 夏季东海表层海水中4种VHOCs的浓度分布
夏季东海表层海水中CFC-12、CFC-11和CFC-113浓度范围分别为9.9~22.4、3.4~14.6和1.4~16.2 pmol·L-1,平均值分别为(14.4±4.3)、(9.2±4.3)和(6.1±5.7) pmol·L-1,本研究测定的3种CFCs的浓度高于文献报道的相同季节长江口及其邻近海域CFCs的浓度[20]。CFC-11和CFC-113浓度显著高于它们在白令海中的浓度(CFC-11:4.15 pmol·L-1;CFC-11:0.40 pmol·L-1)[19]。CFC-12、CFC-11和CFC-113浓度的高值区出现在近岸地区,可能是由于CFCs主要来源于陆源输入。如图3所示,CFC-12、CFC-11和CFC-113的浓度最大值分别出现在浙江近岸的DH5-1和DH8-1站位,是由于当地人为活动和工业活动输入大量VHOCs导致的。
CH3I浓度范围为1.65~8.9 pmol·L-1,对应的平均值为(5.7±2.6) pmol·L-1。CH3I浓度分布整体比较复杂,可能是由于夏季CH3I的分布受到陆源输入、生物释放和光化学释放的共同作用。CH3I浓度的高值区出现在台湾北部海域(DH8-8),一方面可能是由于DH8-8纬度较低,充足光照会促进表层海水CH3I的光化学生产[7];另一方面可能是由于黑潮水携带台湾近岸海水输入的结果。本研究测定的CH3I的浓度水平分布与丁琼瑶[22]报道的相同季节东海海域CH3I的分布特征相似。CH3I浓度在近岸海域的DH5-1和DH8-1站位出现高值区,对应高的Chl-a浓度,推测可能是由于陆源输入和浮游植物释放的共同作用。
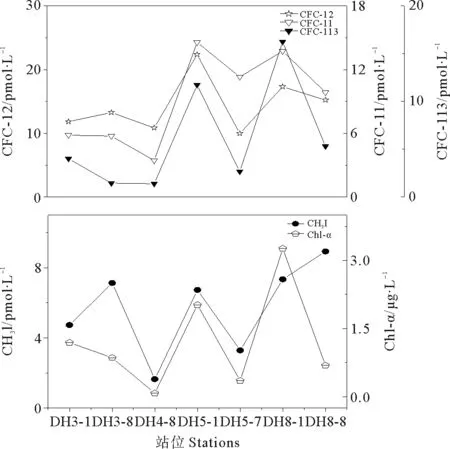
图3 夏季东海海水中4种VHOCs的浓度(poml·L-1)
2.3 东海表层海水中4中VHOCs的季节变化
夏季海水中CFC-12、CFC-11和CFC-113的浓度普遍略微低于秋季它们各自在东海表层海水中的浓度,一方面是由于CFCs在秋季较低的温度下有较高的溶解度,另一方面可能是在夏季盛行的东南季风和台湾暖流的共同作用下,长江冲淡水转向东偏北方向,向浙闽沿岸输送的VHOCs相较于秋季减少,且夏季长江径流量增大,对3种CFCs的浓度有一定的稀释作用,共同导致CFC-12、CFC-11和CFC-113的浓度较小。在调查海域,观察到CH3I的浓度分布存在强烈的季节变化。夏季CH3I浓度的平均值比其秋季的浓度平均值略高一些,可能是由于夏季东海Chl-a的浓度略高于秋季Chl-a的浓度(见表2),浮游植物初级生产力大于秋季,导致夏季浮游植物生产释放VHOCs的能力较强;而且根据Moore[8]报道的光照会促进表层海水CH3I的光化学生产,推测夏季CH3I浓度的平均值略高可能还与夏季的光照强度较高有关。秋季CH3I浓度的水平分布大致呈现近岸高,外海低的趋势,而夏季CH3I浓度的最大值出现在外海,说明影响夏季和秋季CH3I浓度分布的因素有很大不同,秋季CH3I主要来源于陆源输入和夏季CH3I来源于浮游植物的生产释放,光化学合成和陆源输入的共同作用。
2.4 夏季东海大气中VHOCs的分布及海-气通量
2.4.1 夏季东海大气中VHOCs的分布 在夏季东海调查航次中,为了确证东海海洋边界层大气中VHOCs的污染程度以及准确估算夏季东海VHOCs的海-气通量,所以夏季调查航次同时对东海大气中4种VHOCs的分布和来源进行了系统的研究。夏季东海大气中CFC-12、CFC-11、CFC-113和CH3I 的浓度分布如图4所示。根据这4种VHOCs在大气中的寿命和来源,分类讨论它们在大气中的浓度分布特征。
夏季东海大气中CFC-12、CFC-11和CFC-113的浓度平均值分别为(463.3±41.7)、(222.9±8.6)和(100.4±4.8)ppt,对应的浓度范围分别为406.9~522.9、211.6~235.9和96.8~110.5 ppt。本研究中测定的CFC-12和CFC-11的浓度均显著低于它们的全球平均值,而CFC-113的大气浓度高于其全球背景值(CFC-12:537.4; CFC-11:243.4;CFC-113:76.5 ppt)[23]。研究区域CFC-12和CFC-11的大气浓度低于Qin[24]报道的北京大气中CFC-12和CFC-11的浓度平均值681和300 ppt;同样低于Barletta[25]测定的中国43个城市大气中CFC-12和CFC-11的浓度平均值564和284 ppt。CFC-113则高于中国城市大气中CFC-113大气浓度平均值90 ppt[25]和北京地区CFC-113的大气浓度平均值79 ppt[24]。本研究中测定的CFC-12和CFC-11的大气浓度值低于文献值,一方面可能是由于我国于1999开始的对CFCs生产与消费的控制取得了一定的效果,另一方面本研究调查的海域位于受到陆源气团和海洋气团影响显著的近岸区,夏季主要受到海洋气团的影响,陆地气团被海上的活跃气团快速稀释的结果。夏季东海海洋边界层大气中CFC-113的浓度主要受到海洋清洁气团的影响,然而其浓度却高于中国工业城市上空CFC-113的浓度,说明近年来CFC-113仍被大量使用,在持续向大气释放,与Chan[26]报道的珠江三角洲CFC-113的大量使用和释放结果相似。
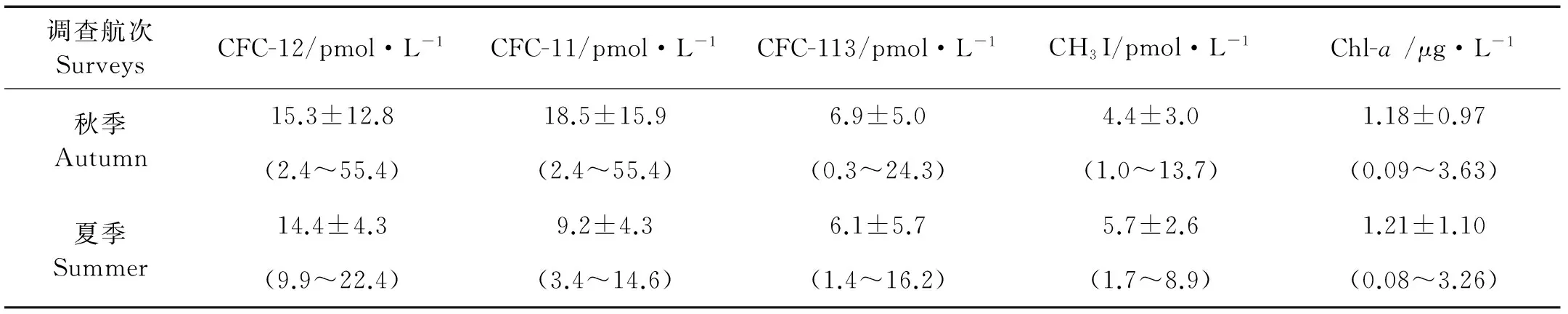
表2 秋季和夏季东海表层海水中4种VHOCs浓度对比

图4 夏季东海大气中4种VHOCs的浓度(ppt)
夏季东海CFC-12、CFC-11和CFC-113大气浓度的空间分布明显受到陆源气团输送的影响。如表3所示CFC-12、CFC-11和CFC-113与气温和风速没有表现出显著的相关关系,而且3种CFCs的分布趋势与气温和风速有很大差异(见图4),推测气温和风速不是影响其分布的主要因素。CFC-12高值区均出现在浙江东部和台湾北部海域,气团的后向轨迹图表明这可能是由于陆地空气团输送的影响(见图5)。例如CFC-12大气浓度的最高值均出现在DH5-7站位,72 h气团后向轨迹图表明DH5-7站位CFC-12浓度的高值主要来自于朝鲜半岛和日本空气团的远距离输送(见图5),表明朝鲜半岛和日本沿海存在较高的CFCs释放。CFC-11和CFC-113大气浓度的最大值分别出现在DH4-8和DH5-1站位,可能与台湾岛工业活动释放的VHOCs的长距离输送有关。CFC-12、CFC-11和CFC-113均没有表现出显著的正相关关系,可能与复杂气团的输送有关,根据各站位的气团后向轨迹图可知,调查区域的气团来源复杂,导致CFC-12、CFC-11和CFC-113的来源不尽相同。
夏季东海海域CH3I的大气浓度比率平均值为(1.5±0.6) ppt,对应的浓度范围为1.0~2.9 ppt。CH3I的浓度平均值高于它们的全球平均值(CH3I: 0.6 ppt)[27]。本研究中CH3I的浓度值显著低珠江三角洲城市上空CH3I浓度平均值(CH3I: 3.22 ppt)[26];CH3I大气浓度范围在Yokouchi报道的北半球范围0.01~5.5 ppt之内[28]。CH3I大气浓度也在东南印度洋和太平洋CH3I大气浓度范围0.46~4.9 ppt之内,但显著高于这两个海区CH3I大气浓度的平均值(CH3I: 1.1 ppt)[5]。上述浓度差异的原因可能是由于本论文调查海域属于近岸海域,一方面受到陆地气团的影响;另一方面由于近岸陆源输入的影响,水体有机污染物含量较高,导致近岸海域浮游植物大量生长,进而导致VHOCs的生物释放量增加,从而通过VHOCs海-气交换进入大气的通量增加,所以CH3I的测定值较城市低而较大洋区要高。
大气中CH3I浓度的最大值出现在台湾北部的DH8-8站位,与本研究海水中CH3I的浓度分布特征相类似。与文献报道的海域上层大气中CH3I浓度受到其表层海水浓度的影响结果相似[29]。如在台湾北部的DH8-8站位发现CH3I大气浓度的最大值,一方面该站位表层海水中CH3I的浓度值也相对较高;另一方面Li[6]通过对不同纬度大气中CH3I浓度的调查报道热带地区海岛附近海域由于高等植物的释放和太阳辐射导致其在大气中的浓度较高纬度地区高,通过气团后向轨迹图可知DH8-8站位大气中CH3I的高值受到来自热带气团远距离输送的影响。CH3I的大气浓度与3种CFCs均没有表现出显著的相关性,可能是由于CH3I与CFCs的来源有较大差异,CFCs主要是人为释放,而CH3I除了陆源气团输送,还与海-气通量有关[29]。
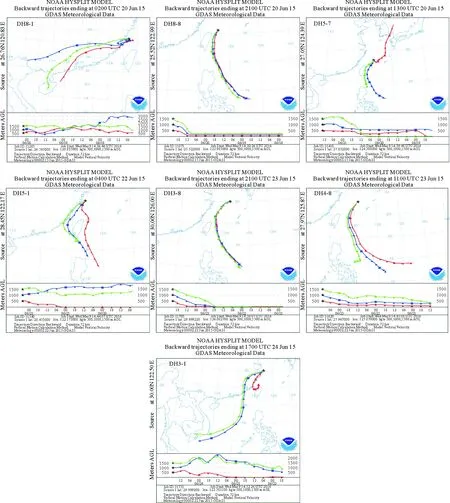
图5 通过NOAA HYSPLIT model (http://www.arl.noaa.gov/ready.php)计算得到夏季东海每个站位的气团后向轨迹图
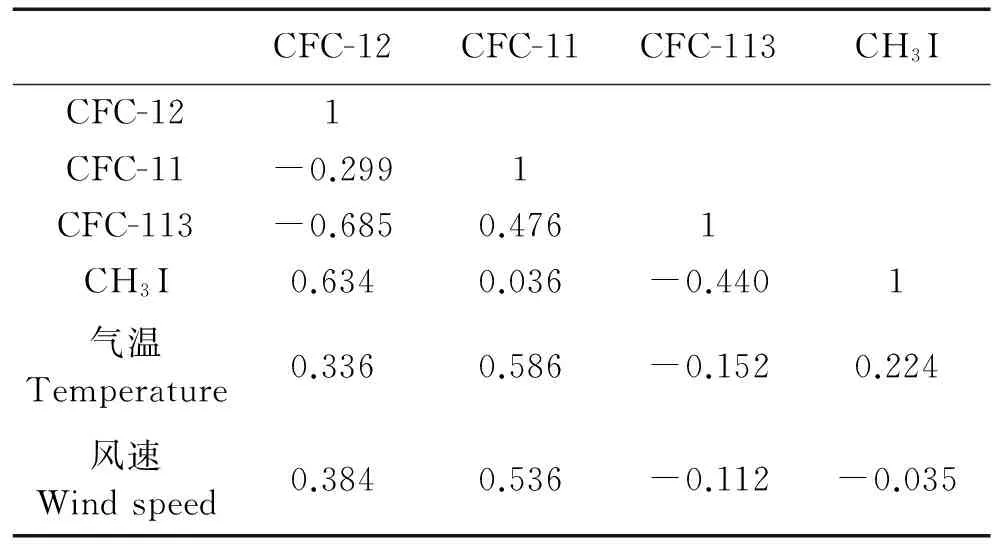
CFC-12CFC-11CFC-113CH3ICFC-121CFC-11-0.2991CFC-113-0.6850.4761CH3I0.6340.036-0.4401气温Temperature0.3360.586-0.1520.224风速Windspeed0.3840.536-0.112-0.035
注: **. 在0.01 水平(双侧)上显著相关。*. 在 0.05 水平(双侧)上显著相关。**. Correlation is significant at the 0.01 level (2-tailled).*. Correlation is significant at the 0.05 level (2-tailled).
2.4.2 夏季东海VHOCs的海-气通量 根据夏季东海海水中和大气中CFC-12、CFC-11和CH3I浓度,可以通过Liss和Slater提出的方程对其夏季东海海-气通量加以估算:
F=Kw(Cw-Ca/H)。
其中:F为通量;kw是气体交换常数;Cw(pmol·L-1)代表气体在表层海水的浓度;Ca(pmol·L-1)为气体在气相的浓度[30],根据气体摩尔体积将五种气体在大气中的浓度由ppt转换为pmol·L-1;H是亨利定律常数,CFC-12和CFC-11的亨利定律常数由Warner and Weiss[31]的公式进行计算,CH3I的亨利定律常数由Moore[32]报道的公式进行计算。
Kw被认为是风速(u,m·s-1)和气体施密特常数Sc(Schmidt number)的函数。Kw的计算可用经验公式得到,本文选择W92[33]公式计算的Kw值:
Kw= 0.31u2(Sc/660)-1/2。
其中:CFC-12,CFC-11和CH3I的Sc由文献报道的公式进行计算[34-35]。
根据通量计算公式可知,海-气通量与海水和大气中VHOCs的浓度有关,引用不同季节的大气的数据,在估算海-气通量时,会造成很大的误差,所以本研究对秋季东海海域VHOCs的海-气通量没有进行估算,只选取夏季航次进行海-气通量计算。夏季调查海域CFC-12、CFC-11和CH3I的海-气通量平均值(范围)分别为(-457.2±273.7)(-801.9~-25.2)、(-182.5±114.8)(-345.4~-17.7)和(97.4±98.0)(9.9~296.3) nmol·m-2·d-1。东海海域CFC-12、CFC-11和CH3I通量的空间差异较大,规律性不明显,海-气通量的计算公式说明其主要是受到风速的影响,其分布在大部分站位与风速保持一致(见图6)。其中CFC-12、CFC-11和CH3I的海-气通量显著高于相同季节它们在长江口及其邻近海域的通量值(平均风速为2.5 m·s-1)[20]。CH3I的海-气通量平均值与丁琼瑶[23]报道的相同季节东海海域CH3I的通量值124.58 nmol·m-2·d-1非常接近(平均风速为9.3 m·s-1),但显著高于在相同纬度Chuck[36]估算的结果15 nmol·m-2·d-1(30°N ~10°N)。造成这种差异的原因,可能是由于本研究中风速较大CH3I的海-气通量也较高。从上述结果可以看出,总的来说夏季东海是CFC-12和CFC-11的汇,是CH3I的源。
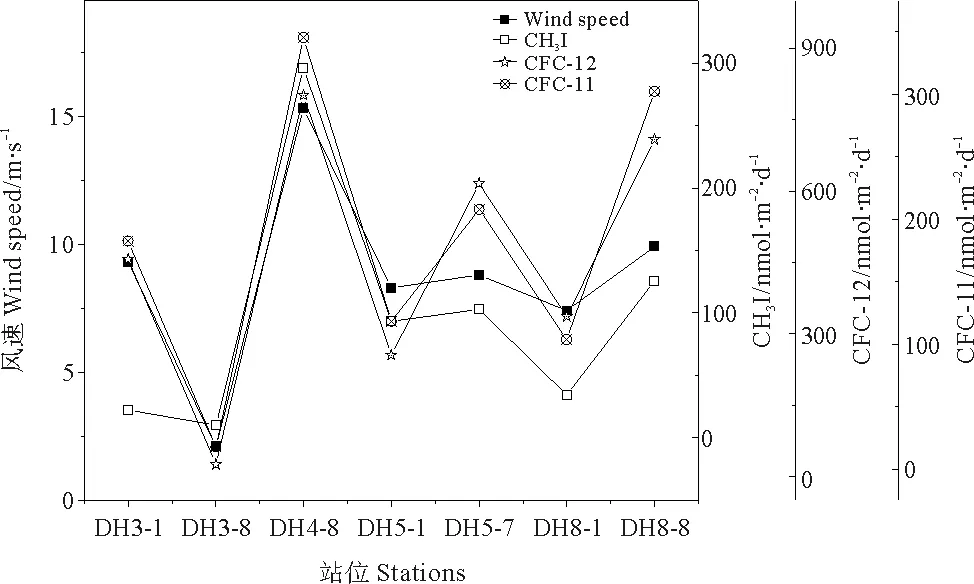
图6 夏季东海3种VHOCs的通量变化与风速的关系
3 结语
东海海域海水中3种CFCs的浓度呈现秋季普遍高于它们在夏季海水中的浓度。3种CFCs水平分布明显受到陆源输入和长江冲淡水的影响,均呈现由近岸向远海逐渐减小的趋势。东海海域海水CH3I的浓度分布表现出明显的季节变化,高值出现在夏季,与Chl-a浓度的季节变化相似,CH3I的分布受到浮游植物丰度和种类、陆源输入和光化学合成的共同影响,尖刺菱形藻、角毛藻可能是CH3I的重要生产者。
除了CFC-113,本研究中CFC-11和CFC-12的大气浓度普遍低于其全球平均值。3种CFCs的分布没有明显的规律,这可能与不同地区空气团的输送有关。CH3I的空间分布表现出远海高,近岸低的特点,浓度高值可能与海洋释放和热带地区空气团的远距离输送有关。海-气通量的计算结果表明夏季调查海域是大气中CFC-12和CFC-11的汇,是CH3I的源。
[1] World Meteorological Organization, Switzerland: (WMO). Scientific Assessment of Ozone Depletion: 2006[R].Switzerland: Global Ozone Research and Monitoring Project-Rep. No. 47, 2007.
[2] Montzka S A, Dlugokencky E J, Butler J H. Non-CO2greenhouse gases and climate change[J]. Nature, 1989, 476(7358): 43-50.
[3] Liu Y, Yvon-Lewis S A, Thornton D C O, et al. Spatial distribution of brominated very short-lived substances in the eastern Pacific[J]. Journal of Geophysical Research, 2013, 118(118): 2318-2328.
[4] Blake N J, Blake D R, Simpson I J, et al. NMHCs and halocarbons in Asian continental outflow during the Transport and Chemical Evolution over the Pacific (TRACE-P) Field Campaign: Comparison With PEM-West B[J]. Journal of Geophysical Research Atmospheres, 2003, 108(D20): 1301-1336.
[5] Li H J, Yokouchi Y, Akimoto H, et al. Distribution of methyl chloride, methyl bromide, and methyl iodide in the marine boundary air over the western Pacific and southeastern Indian Ocean[J]. Geochemical Journal, 2001, 35(2): 137-144.
[6] Yokouchi Y, Ooki A, Hashimoto S, et al. A Study on the Production and Emission of Marine-derived Volatile Halocarbons[M].[s.1.]:Western Pacific Air-Sea Interaction Study, 2014: 1-25.
[7] Moore R M, Groszko W. Methyl iodide distribution in the ocean and fluxes to the atmosphere[J]. Journal of Geophysical Research, 1999, 104(C5): 11163-11171.
[8] Abrahamsson K, Lorén A, Wulff A, et al. Air-sea exchange of halocarbons: the influence of diurnal and regional variations and distribution of pigments[J]. Deep-Sea Research II, 2004, 51(22-24): 2789-2805.
[9] Yokouchi Y, Osada K, Wada M, et al. Global distribution and seasonal concentration change of methyl iodide in the atmosphere[J]. Journal of Geophysical Research Atmospheres, 2008, 113(D18): 1044-1044.
[10] 杨桂朋, 尹士序, 陆小兰, 等. 吹扫-捕集气相色谱法测定海水中挥发性卤代烃[J]. 中国海洋大学学报, 2007, 37(2): 299-304. Yang G P, Yin S X, Lu X L, et al. Determination of volatile halocarbons in seawater using purge and trap gas chromatography[J]. Journal of Ocean University of China, 2007, 37(2): 299-304.
[11] 杨斌, 陆小兰, 杨桂朋, 等. 北黄海海水中挥发性卤代烃的分布和海-气通量研究[J]. 海洋学报, 2010, 32(1): 47-55. Yang B, Lu X L, Yang G P, et al. Distributions and sea-air fluxes of volatile halocarbons in the seawater of the northern Huanghai Sea[J]. Acta Oceanologica Sinica, 2010, 32(1): 47-55.
[12] Lu X L, Yang G P, Song G S, et al. Distributions and fluxes of methyl chloride and methyl bromide in the East China Sea and the Southern Yellow Sea in autumn[J]. Marine Chemistry, 2010, 118: 75-84.
[13] Yang G P, Lu X L, Song G S, et al. Purge-and-Trap Gas Chromatography method for analysis of methyl chloride and methyl bromide in seawater[J]. Chinese Journal of Analytical Chemistry, 2010, 38(5): 719-722.
[14] Yang G P, Yang B, Lu X L, et al. Spatio-temporal variations of sea surface halocarbon concentrations and fluxes from southern Yellow Sea[J]. Biogeochemistry, 2014, 121(2): 369-388.
[15] 何真, 陆小兰, 杨桂朋. 冬季中国东海海水中挥发性卤代烃的分布特征和海-气通量[J]. 环境科学, 2013, 34(3): 849-856. He, Z, Lu X L, Yang G P. Distributions and sea-air fluxes of volatile halocarbons in the East China Sea in Winter[J]. Environmental Science, 2013, 34(3): 849-856.
[16] Parsons T R, Maita Y, Lalli C M. A Manual for Chemical and Biological Methods for Seawater Analysis[M]. Oxford: Pergamon Press, 1984.
[17] 陈纯, 李思嘉, 胡韧, 等. 四种浮游植物生物量计算方法的比较分析[J]. 湖泊科学, 2013, 25(6): 927-935. Chen C, Li S J, Hu R, et al. Comparative analysis of four methods for calculating biomass of phytoplankton community[J]. Journal of Lake Sciences, 2013, 25(6): 927-935.
[18] 徐韧, 洪君超, 王桂兰, 等. 长江口及其邻近海域的赤潮现象[J]. 海洋通报, 1994, 13(5): 25-29. Xu R, Hong J C, Wang G L, et al. On red tide in Yangtse estuary and adjacent sea area[J]. Marine Science Bulletin, 1994, 13(5): 25-29.
[19] 孙娜. 北冰洋、白令海、南海南部海域氟氯烃分布特征及其水团示踪研究[D]. 厦门大学, 2006. Sun N. Distribution of Chlorofluorocarbon and Its Tracer Study of Water Masses in the Arctic Ocean, Bering Sea and the Southern South China Sea[D]. Xiamen University, 2006.
[20] Yuan D, Yang G P, He Z. Spatio-temporal distributions of chlorofluorocarbons and methyl iodide in the Changjiang (Yangtze River) estuary and its adjacent marine area[J]. Marine Pollution Bulletin, 2015, 103(1-2): 247-259.
[21] 孙娜, 李文权. 加拿大海盆氟氯烃的分布及其示踪研究[J]. 极地研究, 2006, 18(1): 21-29. Sun N, Li W Q. Distribution of chlorofluorocarbons in Canada basin and their tracer study[J]. Chinese Journal of Polar Research, 2006, 18(1): 21-29.
[22] 丁琼瑶. 东海、黄海碘甲烷的浓度分布与海-气通量及藻类释放研究[D]. 青岛: 中国海洋大学, 2015. Ding Q Y. The Distributions and Sea-to-Air Fluxes of Methyl Iodide and Production by Marine Phytoplankton[D]. Qingdao: Ocean University of China, 2015.
[23] World Meteorological Organization, (WMO). Scientific Assessment of Ozone Depletion: 2010[R].Switzerland: Global Ozone Research and Monitoring Project-Rep. No. 52, 2011.
[24] Qin D. Decline in the concentrations of chlorofluorocarbons (CFC-11, CFC-12 and CFC-113) in an urban area of Beijing, China[J]. Atmospheric Environment, 2007, 41(38): 8424-8430.
[25] Barletta B, Meinardi S, Rowland F S, et al. Volatile organic compounds in 43 Chinese cities[J]. Atmospheric Environment, 2005, 39(32): 5979-5990.
[26] Chan C Y, Tang J H, Li Y S, et al. Mixing ratios and sources of halocarbons in urban, semi-urban and rural sites of the Pearl River Delta, South China[J]. Atmospheric Environment, 2006, 40: 7331-734
[27] Ko M K W, Poulet G. Very short-lived halogen and sulfur substances, in Scientific Assessment of Ozone Depletion: 2002, Global Ozone Research and Monitoring Project, Report No 47, chapter 2[R]. Switzerlard: World Meterological Organization, 2003.
[28] Yokouchi Y, Ooki A, Hashimoto S, et al. A Study on the Production and Emission of Marine-Derived Volatile Halocarbons[M].[s.1.]: Western Pacific Air-Sea Interaction Study, 2014: 1-25.
[29] Kato S, Watari M, Nagao I, et al. Atmospheric trace gas measurements during SEEDS- II over the northwestern pacific[J]. Deep-Sea Research II, 2009, 56: 2918-2917.
[30] Liss P S, Slater P G. Flux of gases across the air-sea interface[J]. Nature, 1974, 27: 181-184.
[31] Warner M J, Weiss R F. Solubilities of chlorofluorocarbons 11 and 12 in water and seawater[J]. Deep Sea Research Part A Oceanographic Research Papers, 1985, 32(12): 1485-1497.
[32] Moore L R, Goericke R, Chisholm S W. Comparative physiology of Synechococcus and Prochlorococcus: Influence of light and temperature on growth, pigments, fluorescence and absorptive properties[J]. Marine Ecology Progress, 1995, 116(1-3): 259-275.
[33] Wanninkhof R. Relationship between wind speed and gas exchange over the ocean[J]. Journal of Geophysical Research, 1992, 9(7): 7373-7382.
[34] Zheng M, De Bruyn W J, Saltzman E S. Measurements of the diffusion coefficients of CFC-11 and CFC-12 in pure water and seawater[J]. Journal of Geophysical Research, 1998, 103(C1): 1375-1379.
[35] Groszko W. An Estimate of the Global Air-Sea Flux of Methyl Chloride, Methyl Bromide and Methyl Iodide[D]. Halifax, N. S., Canada: Dalhousie Univ, 1999.
[36] Chuck A L, Turner S M, Liss P S. Oceanic distributions and air-sea fluxes of biogenic halocarbons in the open ocean[J]. Journal of Geophysical Research, 2005, 110: C10022.
责任编辑 徐 环
Volatile Halocarbons in the Seawater and Marine Atmosphere of the East China Sea
YUAN Da1, HE Zhen1, YANG Gui-Peng1, 2, LI Guan-Lin1
(1. Key Laboratory of Marine Chemistry Theory and Technology, College of Chemistry and Chemical Engineering, Ocean University of China, Qingdao 266100, China;2. Laboratory for Marine Ecology and Environmental Science, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071, China)
The spatial distributions of volatile halogenated organic compounds (VHOCs) in the surface seawater and marine atmosphere of the East China Sea (ECS) were investigated during two cruises from 18 October to 1 November, 2014 and from 11 to 21, June 2015. Seasonal variation in CFCs concentrations was observed in the study area, with high values in autumn. Concentrations of dichlorodifluoromethane (CFC-12), trichlorofluoromethane (CFC-11), and trichlorotrifluoroethane (CFC-113), in the surface seawater displayed a significant decrease from inshore to offshore. The results of this study suggested that terrestrial input and the Changjiang diluted water were the major factors influencing the distributions of CFCs in the study area. The spatial distribution of CH3I was related to terrestrial input, the biomass and species of phytoplankton in and the photochemical production the study area, with high values in summer. The distribution characteristics of CFC-12, CFC-11, and CFC-113 in the marine atmosphere of the ECS were influenced by long-range transportation of air-masses and meteorological conditions. Both the terrestrial input and sea-air exchange played important roles as the source of CH3I. Our results confirmed that the study area was a net sink for CFC-11 and CFC-12, but an important source of atmospheric CH3I during the study period.
volatile halogenated organic compounds; distribution; marine atmosphere; East China Sea
国家自然科学基金项目(41320104008;41506088);山东省博士后创新基金项目(82214237);山东省 “泰山学者”建设工程项目资助 Supported by the National Natural Science Foundation of China (41506088;41320104008); the Postdoctoral Innovation Fund of Shandong Province (82214237 ); the Taishan Scholars Program of Shandong Province
2016-04-28;
2016-05-23
袁 达(1988-),男,博士。E-mail: yuanda1988@126.com
** 通讯作者:E-mail: gpyang@ouc.edu.cn
P734.4
A
1672-5174(2017)08-093-10
10.16441/j.cnki.hdxb.20160149
袁达, 何真, 杨桂朋, 等. 东海海水和大气中挥发性卤代烃的分布、来源和海-气通量研究[J]. 中国海洋大学学报(自然科学版), 2017, 47(8): 93-102.
YUAN Da, HE Zhen, YANG Gui-Peng, et al. Volatile Halocarbons in the seawater and marine atmosphere of the East China Sea[J]. Periodical of Ocean University of China, 2017, 47(8): 93-102.
