非均匀取代淀粉衍生物手性固定相的制备及其手性识别能力
2017-06-15王宝存鲍明辉林素妃马婕妤唐守万
王宝存, 鲍明辉, 林素妃, 马婕妤, 唐守万
(台州学院医药化工学院, 浙江 台州 318000)
研究论文
非均匀取代淀粉衍生物手性固定相的制备及其手性识别能力
王宝存, 鲍明辉, 林素妃, 马婕妤, 唐守万*
(台州学院医药化工学院, 浙江 台州 318000)
通过区域选择性方法制备了两种新型淀粉衍生物,分别为淀粉2-苯甲酸酯-3-(4-甲基苯基氨基甲酸酯)-6-(3,5-二氯苯基氨基甲酸酯)和淀粉2-苯甲酸酯-3-(3,5-二氯苯基氨基甲酸酯)-6-(4-甲基苯基氨基甲酸酯),将二者分别涂覆于氨丙基硅胶后用作液相色谱手性固定相。研究表明:所制备的手性固定相显示出特异的手性识别能力,其手性识别能力明显高于均匀取代淀粉衍生物——淀粉三(3,5-二氯苯基氨基甲酸酯),取代基的性质及在葡萄糖单元上的位置对手性固定相的手性识别能力有较大的影响。一些未在商品化的手性柱Chiralpak AD上得到有效分离的手性化合物在所制备的固定相上得到了更好的分离。所测试的8对对映体在淀粉2-苯甲酸酯-3-(4-甲基苯基氨基甲酸酯)-6-(3,5-二氯苯基氨基甲酸酯)固定相上均得到了分离,因而此固定相的手性识别能力较强,具有潜在的应用价值。
高效液相色谱;手性固定相;淀粉衍生物;手性分离;多糖
多糖类衍生物手性固定相(chiral stationary phases, CSPs)因其强大的手性识别能力在液相色谱直接拆分对映体中应用广泛[1-8]。通常这类衍生物是均匀取代的,即葡萄糖单元2-、3-、6-位具有相同的取代基[1-8]。为了拓展同一种手性固定相的应用范围,研究者[9-12]研究了基于葡萄糖单元6-位与2-、3-位为不同取代基的非均匀取代多糖类衍生物手性固定相。研究表明,非均匀取代多糖类衍生物具有特异性的手性识别能力,其手性识别能力并不是相应均匀取代衍生物手性识别能力之和,一些手性化合物在此类衍生物上得到了比在均匀取代衍生物上更好的分离[9-12]。最近,Shen等[13]制备了18种葡萄糖单元2-、6-位与3-位为不同苯基氨基甲酸酯基团的淀粉衍生物,并评价了其手性识别能力。基于Dicke[14]报道的选择性酯化淀粉2-OH的方法,2008年Okamoto研究小组[15]制备了两种葡萄糖单元2-、3-、6-位均为不同取代基的新型淀粉衍生物,其2-位为苯甲酸酯基团,3-、6-位分别为3,5-二甲基苯基氨基甲酸酯或3,5-二氯苯基氨基甲酸酯,所制备的衍生物的手性识别能力高于商品化手性柱Chiralpak AD或与之相当。此后,Okamoto研究小组[16]拓展了此项工作,他们合成了一系列淀粉(2-取代苯甲酸酯)衍生物。2012年,Sun等[17]将手性基团(S)-1-苯基乙基氨基甲酸酯引入到淀粉的3-或6-位,制备了4种非均匀取代淀粉衍生物。2015年,徐红月等[18]评价了淀粉2-苯甲酸酯-3-(3,5-二甲基苯基氨基甲酸酯)-6-((S)-1-苯基乙基氨基甲酸酯)手性固定相在反相液相色谱下的手性识别能力。2016年,沈军等[19]合成了5种非均匀取代淀粉衍生物,并评价了其手性识别能力。但到目前为止,在淀粉葡萄糖单元的2-、3-、6-位引入3个不同取代基的研究相对较少,这在一定程度上制约了淀粉衍生物手性固定相及其手性识别机理的研究。本研究合成了两种葡萄糖单元2-、3-、6-位均为不同取代基的新型非均匀取代淀粉衍生物,对其结构进行了表征,评价了其作为高效液相色谱手性固定相的手性识别能力,并与淀粉三(3,5-二氯苯基氨基甲酸酯)(ADCPC)及商品化手性柱Chiralpak AD的手性识别能力进行了比较。
1 实验部分
1.1 仪器与试剂
Agilent 1200系列高效液相色谱仪主要包括G1322A在线脱气装置、G1311A四元泵和G1314B紫外检测器(美国安捷伦公司),同时配备了圆二色检测器(CD 2095,日本Jasco公司); FTIR-8400红外光谱仪(日本岛津公司); Avance Ⅲ核磁共振波谱仪(美国布鲁克公司)。
苯甲酸乙烯酯(纯度99.0%)、无水二甲基亚砜(DMSO,纯度99.7%)购于美国Acros公司;手性样品(纯度95%~98%)购于美国Sigma-Aldrich公司;3,5-二氯苯基异氰酸酯(纯度98%)购于浙江同丰医药化工有限公司;吡啶(pyridine,分析纯,纯度99.5%)购于国药集团化学试剂有限公司;无水磷酸氢二钠(分析纯,纯度99%)、三苯基氯甲烷(纯度97%)、三乙氧基氨丙基硅烷(纯度99%)、三光气(纯度98%)、氢化钙(CaH2,纯度95%)、4-甲基苯胺(纯度99.0%)购于上海阿拉丁生化科技股份有限公司;硅胶(平均直径7 μm,平均孔径100 nm)购于日本Daiso公司;正己烷(色谱纯)购于韩国SK Chemicals公司;异丙醇(色谱纯)购于美国Tedia公司;直链淀粉(聚合度约300)由日本名古屋大学Okamoto教授提供。
吡啶与CaH2回流2 h后,蒸出使用。氨丙基硅胶通过硅胶与三乙氧基氨丙基硅烷在含少量吡啶的干燥甲苯中反应24 h制得,反应温度为80 ℃。4-甲基苯基异氰酸酯通过4-甲基苯胺与三光气反应制得。
1.2 非均匀取代淀粉衍生物手性固定相的制备
1.2.1 非均匀取代淀粉衍生物的合成

图 1 淀粉衍生物A1和A2的合成Fig. 1 Synthesis of amylose derivatives A1 and A2
基于Dicke[14]2004年报道的区域选择性酯化淀粉2-OH的方法,本研究合成了葡萄糖单元上2-、3-、6-位分别为不同取代基的淀粉衍生物A1和A2(见图1)。为了只选择性酯化淀粉2-OH,首先,在80 ℃下于15 min内将6.0 g干燥淀粉溶于120 mL无水DMSO中;然后降温至40 ℃,加入2.3倍(物质的量比,以2-OH物质的量为基准)苯甲酸乙烯酯和2%(质量分数)的Na2HPO4(120 mg,作为催化剂),并在40 ℃下缓慢电磁搅拌反应216 h。反应结束后,将反应液倾入约1 000 mL异丙醇中,析出的不溶物为2-苯甲酸酯淀粉,不溶物用异丙醇充分洗涤并干燥后备用。取4.0 g干燥产物,加入80 mL吡啶,搅拌使其溶解,随后加入2倍(物质的量比,以6-OH物质的量为基准)三苯基氯甲烷,于80 ℃下搅拌反应24 h以选择性保护6-OH。反应完成后,反应液倾入约1 500 mL甲醇中,析出的不溶物为2-苯甲酸酯-6-O-三苯甲基淀粉,不溶物用甲醇充分洗涤并干燥后备用。取干燥的2-苯甲酸酯-6-O-三苯甲基淀粉0.88 g,加入30 mL吡啶使其溶解,后加入过量的R1NCO(3倍,物质的量比,以2-OH物质的量为基准;R1为4-甲基苯基或3,5-二氯苯基),并于80 ℃下搅拌反应24 h,将3-OH转化为3-苯基氨基甲酸酯。将得到的2-苯甲酸酯-3-苯基氨基甲酸酯-6-O-三苯甲基淀粉悬浮于含少量浓盐酸(体积分数为2%)的甲醇溶液中,于50 ℃下搅拌反应24 h,水解脱去三苯甲基。最后,2-苯甲酸酯-3-苯基氨基甲酸酯淀粉中的6-OH与过量的R2NCO(R2为3,5-二氯苯基或4-甲基苯基)于80 ℃下反应24 h。反应结束后,反应液倾入约300 mL甲醇中,析出不溶物,经甲醇洗涤、干燥得2-、3-、6-位均为不同取代基的淀粉衍生物A1和A2。
1.2.2 手性固定相的制备
称取淀粉衍生物0.20 g,溶于6 mL四氢呋喃中,将其涂覆于0.80 g氨丙基硅胶上。以正己烷-异丙醇(90∶10, v/v)为顶替液,在约40 MPa下采用匀浆法将上述固定相装入不锈钢柱中(25 cm×0.2 cm)。手性固定相的手性识别能力由图2所示的8种手性化合物进行评价。

图 2 对映体的结构Fig. 2 Structures of racemates 1. tröger’s base; 2. trans-stilbene oxide; 3. benzoin; 4. 2-phenyl-cyclohexanone; 5. 2,2,2-trifluoro-1-(9-anthryl) ethanol; 6. cobalt (Ⅲ) tris(acetylacetonate); 7. flavanone; 8. trans-cyclo-propane dicarboxylic acid diamide.
1.3 色谱条件和色谱分离参数的测定
色谱分离在室温下进行,流动相使用前经0.22 μm有机相滤膜过滤并超声脱气,流速为0.1 mL/min,检测波长为254 nm。死时间(t0)以1,3,5-三叔丁基苯为不保留化合物测定。保留因子(k)按k1=(t1-t0)/t0,k2=(t2-t0)/t0计算,分离因子(α)按α=k2/k1计算。其中,t1、t2分别为第一个和第二个洗脱的对映异构体的保留时间,k1、k2分别为第一个和第二个洗脱的对映异构体的保留因子。
2 结果与讨论
2.1 衍生物及固定相的表征
2.1.1 衍生物的表征
对2-苯甲酸酯淀粉的结构进行了1H和13C NMR(核磁共振)表征,谱图见图3。13C NMR(500 MHz, DMSO-d6)(10-6,下同):δ165 (C=O), 127~132 (Ar-C), 60~95 (glucose-C);1H NMR (500 MHz, DMSO-d6):δ7.4~8.1 (Ar-H), 3.5~5.9 (glucose-H)。13C NMR谱图中,在δ=165处的峰归属为在葡萄糖单元2-位引入的苯甲酸酯基团中的C=O峰[14],由于此处只出现了一个C=O峰,因此淀粉只在葡萄糖单元的2-位被选择性酯化,即确证了2-苯甲酸酯淀粉的结构。由1H NMR谱图中芳环上质子(Ar-H)与糖单元上质子(glucose-H)的峰面积计算得到2-苯甲酸酯基团的取代度约为0.96。

图 3 2-苯甲酸酯淀粉的(a)13C和(b)1H NMR谱图(500 MHz, DMSO-d6, 80 ℃)Fig. 3 (a)13C and (b)1H NMR spectra of amylose 2-benzoate (500 MHz, DMSO-d6, 80 ℃)
图4为淀粉衍生物A1和A2的1H NMR谱图。1H NMR: A1,δ2.1 (Ar-CH3), 4.3~6.2 (glucose-H), 6.8~8.2 (Ar-H), 10.2~10.8 (NH); A2,δ2.5 (Ar-CH3), 4.3~6.2 (glucose-H), 6.8~8.2 (Ar-H), 9.4~10.8 (NH)。图4a中,在约2.1出现的峰为葡萄糖单元3-位引入的4-甲基苯基氨基甲酸酯基团中的-CH3的质子峰,而图4b中在约2.5出现的峰为葡萄糖单元6-位引入的4-甲基苯基氨基甲酸酯基团中-CH3的质子峰。这与衍生物A1的3-位取代基为4-甲基苯基氨基甲酸酯基团,A2的6-位取代基为4-甲基苯基氨基甲酸酯基团的结构相符。此外,衍生物结构中的其他特征峰也得到了归属,证明图1所示结构是正确的。同时对衍生物进行了元素分析表征:A1的理论值为C 57.05、H 4.09、N 4.77;实测值为C 56.38、H 4.11、N 4.90; A2的理论值为C 57.05、H 4.09、N 4.77;实测值为C 56.68、H 4.24、N 4.72。理论值与实测值非常接近,进一步证明了所合成的衍生物结构与图1所示结构相符。
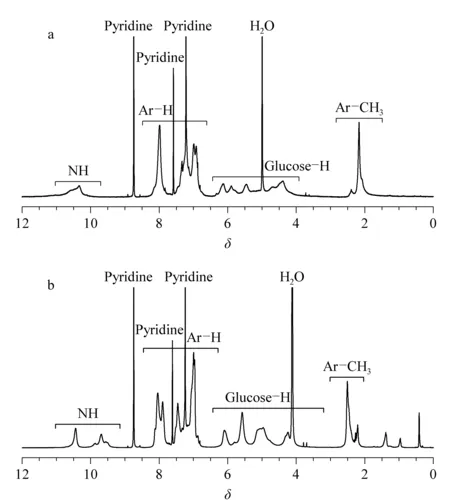
图 4 (a)A1和(b)A2的1H NMR谱图(500 MHz,吡啶-d5, 80 ℃)Fig. 4 1H NMR spectra of (a) A1 and (b) A2 (500 MHz, pyridine-d5, 80 ℃)
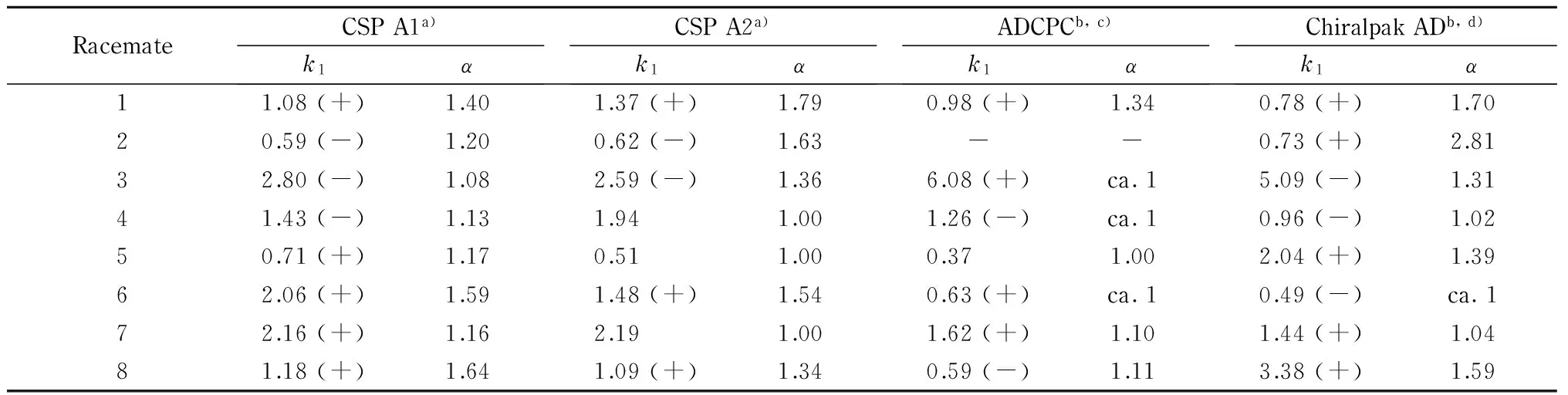
RacemateCSPA1a)k1αCSPA2a)k1αADCPCb,c)k1αChiralpakADb,d)k1α11.08(+)1.401.37(+)1.790.98(+)1.340.78(+)1.7020.59(-)1.200.62(-)1.63--0.73(+)2.8132.80(-)1.082.59(-)1.366.08(+)ca.15.09(-)1.3141.43(-)1.131.941.001.26(-)ca.10.96(-)1.0250.71(+)1.170.511.000.371.002.04(+)1.3962.06(+)1.591.48(+)1.540.63(+)ca.10.49(-)ca.172.16(+)1.162.191.001.62(+)1.101.44(+)1.0481.18(+)1.641.09(+)1.340.59(-)1.113.38(+)1.59
ADCPC: amylose tris(3,5-dichlorophenylcarbamate). ca. 1: in the separation of a racemate, one peak was observed using UV detection, while two peaks were observed with circular dichroism or optical rotation detection. The signs in the parentheses represent the circular dichroism (CD) detection of the first eluted enantiomer. a) Column size, 25 cm×0.2 cm; flow rate, 0.1 mL/min. b) Column size, 25 cm×0.46 cm; flow rate, 0.5 mL/min. c) Data taken from reference [20]. d) Data taken from reference [15]. -: not detected. Eluent: hexane-2-propanol (90∶10, v/v).
2.1.2 手性固定相的表征
用傅里叶变换红外光谱仪对制备的手性固定相进行了表征。发现在约1 740 cm-1处出现羰基(C=O)的吸收峰,在约1 630 cm-1处出现苯环(-C6H5)的吸收峰。由于氨丙基硅胶的红外谱图在此两处没有明显的吸收峰,故羰基及苯环吸收峰的出现说明多糖衍生物被成功地涂覆于氨丙基硅胶上。
2.2 手性固定相的手性识别能力
以正己烷-异丙醇(90∶10, v/v)为流动相考察了CSP A1、CSP A2的手性识别能力,结果见表1。表1还包含了ADCPC及Chiralpak AD的分离数据。
衍生物A1、A2具有相同的2-位取代基,而它们在3-、6-位的取代基正好相反,分别为4-甲基苯基氨基甲酸酯和3,5-二氯苯基氨基甲酸酯基团,但如表1所示,它们的手性识别能力却相差巨大。例如,在CSP A1上得到部分分离的对映体4(α=1.13)、对映体5(α=1.17)、对映体7(α=1.16)在CSP A2上却未能得到分离(α=1.00)。然而,对映体1~3在CSP A2上的分离(对映体1的α=1.79、对映体2的α=1.63、对映体3的α=1.36)却明显好于在CSP A1上的分离(对映体1的α=1.40、对映体2的α=1.20、对映体3的α=1.08)。以上分析说明对于非均匀取代淀粉衍生物,取代基在糖单元上的位置(3-位或6-位)对直链淀粉衍生物的二级结构有较大的影响,进而影响其高级有序结构,从而导致其手性识别能力与立体选择性有较大的差异。这与文献[16,17,19]报导的结论相吻合。此外,取代基在糖单元上的位置不同,也会对衍生物部分区域的极性产生影响,从而影响其手性识别能力。所测试的8对对映体在CSP A1上均得到了分离,说明其具有较高的手性识别能力,并具有潜在的应用价值。
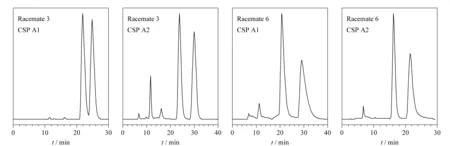
图 5 对映体3和6在CSP A1和CSP A2上的分离色谱图Fig. 5 Chromatographic resolution of racemates 3 and 6 on CSP A1 and CSP A2Mobile phase: hexane-2-propanol (90∶10, v/v); column size (25 cm×0.2 cm); flow rate: 0.1 mL/min.
与均匀取代的淀粉衍生物ADCPC相比,除对映体7在CSP A2上的分离变差外,CSP A1、CSP A2对其余手性化合物的手性识别能力均高于ADCPC或与之相当。特别是未能在ADCPC上得到分离的对映体3~6(对映体3、4、6的α为ca. 1(表示在紫外检测器上未观察到外消旋化合物的分离(1个峰),而在圆二色或旋光检测器上观察到了分离(2个峰))。对映体5的α=1.00),在CSP A1上得到了不同程度的分离(对映体3的α=1.08、对映体4的α=1.13、对映体5的α=1.17、对映体6的α=1.59),同时对映体3、6也在CSP A2上得到了基线分离(α>1.20)。由表1可知,对映体3、6在CSP A1、CSP A2与在ADCPC上的保留因子有较大差异。这表明,2-、3-位或2-、6-位取代基的不同会影响固定相与对映体分子之间形成的瞬间配合物的稳定性。ADCPC与CSP A1、CSP A2手性识别能力的差异进一步说明,糖单元2-、3-位及2-、6-位取代基的性质会对淀粉衍生物的高级有序结构产生影响,从而影响其立体选择性和手性识别能力。此外,ADCPC在糖单元2-位上的-NH基团也会与某些对映体产生氢键相互作用,从而使其表现出与CSP A1、CSP A2(2-位取代基为苯甲酸酯基团)不同的手性识别能力。
与目前液相色谱手性分离中应用最广泛的Chiaralpak AD手性柱相比,对映体4、6和7在CSP A1上得到了更好的分离;而对映体1、2、3和5在CSP A1上的α值明显小于其在Chiralpak AD上的值;对于对映体8,两者表现出相近的手性识别能力。对于CSP A2,在Chiralpak AD未得到分离的对映体6(Chiralpak AD上的α为ca. 1; CSP A2上的α为1.54)在其上得到了完全分离;对于对映体1和3, CSP A2的手性识别能力稍高于Chiralpak AD;而对于对映体2、4、5、7和8, CSP A2的手性识别能力明显弱于Chiralpak AD。需要指出的是,通常在商品化多糖类衍生物手性柱上很难分离的对映体6在CSP A1(α=1.59)、CSP A2(α=1.54)上都得到了完全分离。对映体3和6的分离谱图见图5。此外,与Chiralpak AD柱相比,对映体2和6在CSP A1和CSP A2上的洗脱顺序发生了翻转,说明它们在固定相上的分离机理不同。与Chiralpak AD手性识别能力的对比进一步说明,所制备的非均匀取代淀粉衍生物手性固定相显示出特异的手性识别能力,一些手性化合物在此类衍生物上可获得比在均匀取代淀粉衍生物上更好的分离。
3 结论
制备了两种葡萄糖单元2-、3-、6-位均为不同取代基的新型非均匀取代淀粉衍生物,对其进行了表征,将其涂覆于氨丙基硅胶后用作液相色谱手性固定相。研究表明:所制备的衍生物显示出特异的手性识别能力,其手性识别能力明显高于均匀取代的淀粉衍生物——淀粉三(3,5-二氯苯基氨基甲酸酯)。一些在商品化手性柱Chiralpak AD上未能得到有效分离的手性化合物在所制备的新型衍生物上得到了更好的分离。取代基的性质及在糖单元上的位置影响非均匀取代衍生物的手性识别能力。所测试的8对对映体在淀粉2-苯甲酸酯-3-(4-甲基苯基氨基甲酸酯)-6-(3,5-二氯苯基氨基甲酸酯)上得到了不同程度的分离,表明其具有较高的手性识别能力和潜在的应用价值。
[1] Ward T J, Ward K D. Anal Chem, 2012, 84(2): 626
[2] Jin Z L, Hu F F, Wang Y B, et al. Chinese Journal of Chromatography, 2011, 29(11): 1087
金召磊, 胡芳芳, 汪一波, 等. 色谱, 2011, 29(11): 1087
[3] Luo A, Wan Q, Fan H J, et al. Chinese Journal of Chromatography, 2014, 32(9): 1013
罗安, 万强, 范华均, 等. 色谱, 2014, 32 (9): 1013
[4] Wang M. Chinese Journal of Chromatography, 2014, 32(2): 198
王敏. 色谱, 2014, 32(2): 198
[5] Peluso P, Mamane V, Cossu S. Chirality, 2015, 27(10): 667
[6] Kurka O, Kucera L, Bednar P. J Sep Sci, 2016, 39(14): 2736
[7] Li D Y, Wu X, Hao F L, et al. Chinese Journal of Chromatography, 2016, 34(1): 80
李冬艳, 吴锡, 郝芳丽, 等. 色谱, 2016, 34(1): 80
[8] Li L Q, Fan J, Zhang J, et al. Chinese Journal of Chromatography, 2016, 34(1): 107
李丽群, 范军, 张晶, 等. 色谱, 2016, 34(1): 107
[9] Kaida Y, Okamoto Y. Bull Chem Soc Jpn, 1993, 66(8): 2225
[10] Qu H T, Li J Q, Shen J, et al. Chinese Journal of Analytical Chemistry, 2011, 39(4): 461
屈海涛, 李峻青, 沈军, 等. 分析化学, 2011, 39(4): 461
[11] Tang S W, Li X F, Wang F, et al. Chirality, 2012, 24(2): 167
[12] Shen J, Liu S Y, Zhao Y Q, et al. Acta Polymerica Sinina, 2013(3): 293
沈军, 刘双燕, 赵勇强, 等. 高分子学报, 2013(3): 293
[13] Shen J, Li G, Yang Z Z, et al. J Chromatogr A, 2016, 1467: 199
[14] Dicke R. Cellulose, 2004, 11(2): 255
[15] Kondo S, Yamamoto C, Kamigaito M, et al. Chem Lett, 2008, 37(5): 558
[16] Shen J, Ikai T, Okamoto Y. J Chromatogr A, 2010, 1217: 1041
[17] Sun B S, Li X F, Jin Z L, et al. Chromatographia, 2012, 75(23/24): 1347
[18] Xu H Y, Tang S W, Pan F Y, et al. Science Technology and Engineering, 2015(3): 5
徐红月, 唐守万, 潘富友, 等. 科学技术与工程, 2015(3): 5
[19] Shen J, Li G, Li P, et al. Chinese Journal of Chromatography, 2016, 34(1): 50
沈军, 李庚, 李平, 等. 色谱, 2016, 34(1): 50
[20] Okamoto Y, Aburatani R, Fukumoto T, et al. Chem Lett, 1987, 16(9): 1857
Zhejiang College Students’ Science and Technology Innovation Project (Xinmiao Talents Program) (No. 2016R430020).
Preparation and chiral recognition of heterosubstituted amylose derivatives-based chiral stationary phases
WANG Baocun, BAO Minghui, LIN Sufei, MA Jieyu, TANG Shouwan*
(CollegeofPharmaceuticalandChemicalEngineering,TaizhouUniversity,Taizhou318000,China)
Two novel amylose derivatives, namely amylose 2-benzoate-3-(4-methylphenylcarbamate)-6-(3,5-dichlorophenylcarbamate) and amylose 2-benzoate-3-(3,5-dichlorophenylcarbamate)-6-(4-methylphenylcarbamate), were prepared utilizing a serial regioselective process. After coated onto aminopropyl silica gel, they were utilized as chiral stationary phases (CSPs) for high performance liquid chromatography. Investigations indicated that the CSPs exhibited characteristic chiral recognition and their chiral recognition abilities were much higher than those of amylose tris(3,5-dichlorophenylcarbamate) (ADCPC), a homosubstituted derivative. The nature and position of the substituents at 3-, and 6-positions of a glucose unit had great influence on the chiral resolution abilities of the amylose derivatives. Some chiral compounds which were not effectively resolved on the commercial column Chiralpak AD were effectively separated on the new CSPs. Moreover, with all the eight tested racemates resolved, amylose 2-benzoate-3-(4-methylphenylcarbamate)-6-(3,5-dichlorophenylcarbamate) exhibited relatively high chiral recognition and might be a potential useful CSP.
high performance liquid chromatography (HPLC); chiral stationary phase (CSP); amylose derivative; chiral separation; polysaccharide
10.3724/SP.J.1123.2017.02011
2017-02-13
浙江省大学生科技创新计划(新苗人才计划)项目(2016R430020).
O658
A
1000-8713(2017)06-0572-06
* 通讯联系人.E-mail:tangswtz@163.com.
