粉煤灰基层状金属氧化物对水中活性红X-3B的吸附
2017-06-15周绍杰刘明照
周绍杰,刘明照,钱 翌
(1. 青岛科技大学 环境与安全工程学院,山东 青岛 266042;2. 青岛市环境保护局 崂山分局,山东 青岛 266061)
Zhou Shaojie1,Liu Mingzhao2,Qian Yi1
(1. College of Environment and Safety Engineering,Qingdao University of Science & Technology,Qingdao Shandong 266042,China; 2. Laoshan Branch of Qingdao Environmental Protection Bureau,Qingdao Shandong 266061,China)
粉煤灰基层状金属氧化物对水中活性红X-3B的吸附
周绍杰1,刘明照2,钱 翌1
(1. 青岛科技大学 环境与安全工程学院,山东 青岛 266042;2. 青岛市环境保护局 崂山分局,山东 青岛 266061)
以粉煤灰(FA)为原料,采用共沉淀法制备了层状双金属氢氧化物(LDH)和层状金属氧化物(LMO,也称LDO),并采用XRD和BET技术进行了表征。比较了FA、LDH、LMO对活性红X-3B染料(X-3B)的吸附效果;考察了LMO吸附X-3B的影响因素,并探讨了吸附机理。XRD表征结果表明,LMO在吸附X-3B后重新恢复LDH层状结构。BET表征结果表明,LMO的比表面积大于LDH。吸附实验结果表明,3种吸附剂对X-3B吸附效果的优劣顺序为:LMO>LDH>FA;在初始X-3B质量浓度为50 mg/L、LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附pH为7、吸附时间为30 min的条件下,X-3B去除率可达98.1%;LMO对X-3B的吸附符合Langmuir等温吸附方程,饱和吸附量为129.53 mg/g,且吸附过程可用准二级动力学方程描述。
粉煤灰;层状双金属氢氧化物;层状金属氧化物; 吸附;活性红X-3B
粉煤灰(FA)是燃煤电厂排出的主要固体废弃物,主要含有Al2O3,Fe2O3,SiO2等物质[1-3]。近年来,随着电力工业的快速发展,粉煤灰排放量逐年增加,已成为我国当前排放量较大的工业废渣之一[4]。若FA得不到合理利用,不仅会占用大量的土地,而且会严重威胁大气、水体和土壤环境,并危害人类健康[5]。但目前FA的综合利用率较低,主要作为土建工程基料、土壤改良剂等,且利用速率远赶不上FA的产生速率[6]。
层状双金属氢氧化物(LDH),包括水滑石和类水滑石两类化合物,是一类具有典型双层结构的新型无机功能材料,主要由带正电荷的主体层板、层间阴离子和层间水分子组成[7-8]。由于LDH具有特殊的结构“记忆效应”、层间阴离子的可交换性、催化性和较大的比表面积等特点,常被用作催化剂和吸附剂等[7,9-10]。LDH经焙烧后可得比表面积更大的层状金属氧化物(LMO,也称LDO)[11]。近些年,以LDH和LMO作为吸附剂的研究较多,主要用于吸附水体中的重金属离子[12]、有机污染物[13]、阴离子[14-15]等。
基于FA富含Al2O3和Fe2O3的特点,本工作利用FA制备LDH和LMO,比较了FA、LDH和LMO对活性红X-3B(X-3B)的吸附效果,考察了LMO吸附X-3B的影响因素,并探讨了吸附机理,以期为FA的综合利用以及染料废水的治理提供一种新思路。
1 实验部分
1.1 试剂、材料和仪器
氯化镁、碳酸钠、氢氧化钠、盐酸、活性红X-3B:均为分析纯。
FA:取自昌乐盛世热电有限公司,去除杂质、研磨、过200目筛,得粒径约为75 μm的超细化粉末。其金属元素组成(w,%)为:Al 35.400,Fe 9.540,Mg 3.700,Ni 0.011,Zn 0.008,Pb 0.008,Cu 0.007,Hg 0.005。
模拟X-3B废水:称取1 g X-3B,溶于1 000 mL蒸馏水中,再稀释至不同浓度。
SX2-4-10型箱式电阻炉:龙口市电炉制造厂;Prodigy XP型电感耦合等离子体原子发射光谱仪:美国利曼公司;XQM-20型行星球磨机:长沙天创粉末技术有限公司;D/max-2500/PC型X射线衍射(XRD)仪:日本理学公司;ASAP2020型全自动比表面积及孔隙分析仪:美国麦克仪器公司;SP-722E型分光光度计:上海光谱仪器有限公司。
1.2 吸附剂的制备
1.2.1 LDH的制备
按照m(FA)∶m(Na2CO3)=2∶1的比例将一定量的FA与Na2CO3混合均匀,置于950 ℃的箱式电阻炉中焙烧3 h,取出自然冷却;再将焙烧物与7 mol/L盐酸混合均匀,固液比(焙烧物质量与盐酸体积之比,g/mL)为1∶4,置于85 ℃恒温水浴中回流搅拌2 h,自然冷却即得酸浸液;最后按照n(Mg)∶n(Al+Fe)=3∶1的比例将氯化镁溶液与酸浸液混合,采用双滴共沉淀法将混合液和碱液(含0.5 mol/L Na2CO3和2 mol/L NaOH)同时滴加到反应器中,并保持反应器处于85 ℃、pH=8~9、充分搅拌的条件下,待反应完全后冷却、静置,沉淀物水洗至中性,抽滤、烘干即得LDH。
1.2.2 LMO的制备
将LDH置于500 ℃的箱式电阻炉中焙烧4 h,自然冷却后球磨、过200目筛,即得LMO。
1.3 吸附实验
取50 mL一定浓度的模拟X-3B废水置于150 mL锥形瓶中,加入一定量的吸附剂,在一定温度下振荡一段时间后,取样,离心(转速2 500 r/ min),得上清液,测定X-3B质量浓度。
1.4 分析方法
1.4.1 XRD表征
采用D/max-2500/PC型X射线衍射仪对LDH以及吸附前后的LMO进行结构表征。室温,新型Cu靶专用单色器,2θ/θ连动,扫描速率10(°)/min ,2θ=5°~65°。
1.4.2 BET表征
采用全自动比表面积及孔隙分析仪,N2-BET法测定LDH和LMO的比表面积,分析温度为-195.86 ℃。
1.4.3 X-3B质量浓度的测定
采用分光光度计在X-3B特征波长(540 nm)下测定模拟X-3B废水的吸光度,通过吸附标准曲线(y=0.010 59x–0.000 744,R2=0.999 7,x为质量浓度,y为吸光度)计算X-3B的质量浓度,进而得出X-3B的吸附量和去除率。
2 结果与讨论
2.1 XRD表征
LDH、LMO和吸附后LMO的XRD谱图见图1。由图1可见:LDH在2θ为11°,23°,32°,39°,61°附近均出现LDH结构的特征衍射峰,对应于(003)、(006)、(009)、(015)、(110),证明该试样具有典型的LDH结构,这也说明以FA为原料,通过共沉淀法可以成功合成LDH[16-17];LMO在2θ为43°和62°附近明显出现MgO的特征衍射峰,但没有出现LDH的特征衍射峰,这是由于LDH经500 ℃焙烧后,失去层间水、层间阴离子和羟基官能团,导致LDH结构坍塌[11];吸附X-3B后的LMO在2θ为11°,23°,30°,61°附近均出现LDH结构的特征衍射峰,对应于(003)、(006)、(009)、(110),这是由于LMO在含有某种阴离子的溶液介质中,其结构可以部分恢复到LDH的有序层状结构,即LMO具有结构“记忆效应”[18-19]。

图1 试样的XRD谱图
2.2 BET表征
LDH和LMO的BET等温吸附方程相关参数见表1。由表1可见,R2分别为0.999 9、0.999 7,说明LDH和LMO对N2的吸附过程符合BET型等温吸附方程[20]。经计算,LDH和LMO的比表面积分别为22.25 m2/g和58.66 m2/g,说明LDH经过高温焙烧后,比表面积增加,对N2的吸附能力增强。

表1 LDH和LMO的BET等温吸附方程相关参数
2.3 X-3B吸附效果的比较
在初始X-3B质量浓度为50 mg/L、室温(20℃)、吸附pH为7(不调pH)、吸附时间为120 min的条件下,不同吸附剂及投加量对X-3B的吸附效果见图2。由图2可见,在吸附剂投加量为1.6~16.0 g/L范围内,FA,LDH,LMO对X-3B的最大去除率分别为72.9%,98.4%,98.7%;三者吸附X-3B效果的优劣顺序为LMO>LDH>FA;当投加量大于2.0 g/L时,LMO对X-3B的去除率均接近100%。LMO对X-3B的吸附主要基于其较大的比表面积以及结构“记忆效应”,可容纳大量的活性红X-3B染料分子。综合考虑吸附效果及投加量,后续实验均采用LMO为吸附剂,并确定最佳投加量为2.0 g/L。

图2 不同吸附剂及投加量对X-3B的吸附效果
2.4 LMO吸附X-3B的影响因素
2.4.1 吸附温度
在初始X-3B质量浓度为50 mg/L、LMO投加量为2.0 g/L、吸附pH为7、吸附时间为120 min的条件下,吸附温度对X-3B去除率的影响见图3。由图3可见:当吸附温度低于25 ℃时,X-3B去除率随着吸附温度的升高而逐渐增加;当吸附温度为25 ℃时, X-3B去除率高达98.7%;当吸附温度高于25 ℃时, X-3B去除率随着吸附温度的升高反而下降。究其原因是由于15~25 ℃时温度较低,LMO对X-3B的吸附主要是物理吸附,吸附热相对较小。随着温度的升高,吸附效果逐渐变好;但温度超过25 ℃以后,LMO对X-3B的吸附则以化学吸附为主,吸附热相对较大。LMO在水溶液中会吸附X-3B形成共价键,生成类水滑石的结构即结构“记忆效应”。由于键的形成是一个放热过程,升高温度不利于化学吸附的进行,所以使LMO对X-3B的吸附效果变差。因此,确定最佳吸附温度为25 ℃。
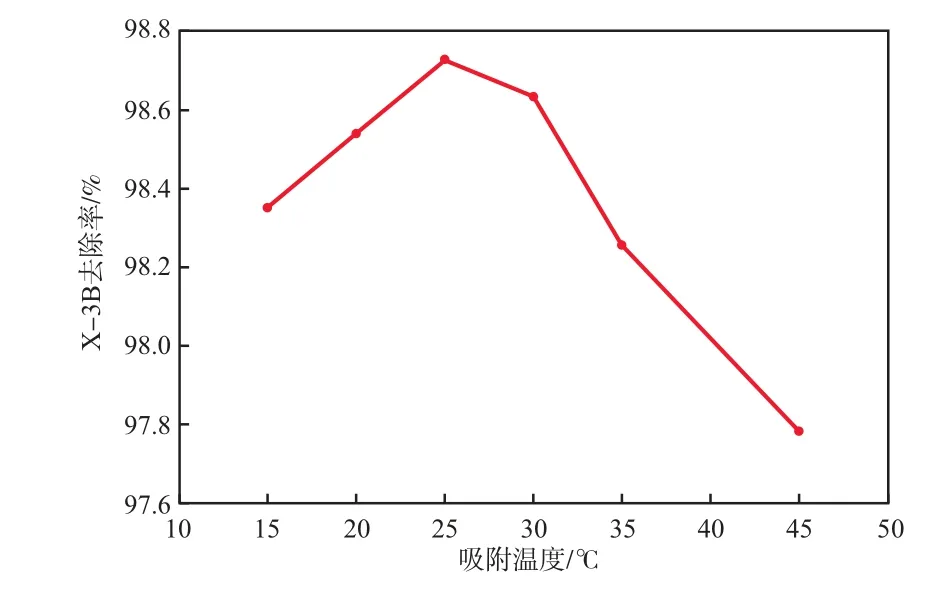
图3 吸附温度对X-3B去除率的影响
2.4.2 吸附pH
在初始X-3B质量浓度为50 mg/L、LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附时间为120 min的条件下,吸附pH对X-3B去除率的影响见图4。由图4可见:当吸附pH小于3时,X-3B去除率随着吸附pH的增加而急剧增加。这可能由于在强酸条件下LMO与H+发生反应,失去吸附能力;当吸附pH大于3时, X-3B去除率随着吸附pH的增加而缓慢增加。综合考虑吸附效果及经济成本,确定最佳吸附pH为7(即不调pH)。

图4 吸附pH对X-3B去除率的影响
2.4.3 吸附时间
在初始X-3B质量浓度为50 mg/L、LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附pH为7的条件下,吸附时间对X-3B去除率的影响见图5。由图5可见:LMO对X-3B的吸附可以分为快速阶段(0~30 min)和慢速阶段(30~120 min);在快速阶段,LMO对X-3B的吸附速率较大, X-3B去除率随吸附时间迅速增加。这是由于吸附初期LMO表面的吸附位点较多,液相与LMO表面的染料浓度差较大,X-3B容易扩散到LMO表面被吸附[21];随着吸附的进行,LMO表面的吸附点位趋于饱和,吸附进入慢速阶段,吸附速率逐渐降低,直至吸附达到平衡。因此,确定最佳吸附时间为30 min。此时X-3B去除率可达98.1%。

图5 吸附时间对X-3B去除率的影响
2.5 等温吸附方程
在LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附时间为120 min、吸附pH为7的条件下,对不同浓度的模拟X-3B废水进行吸附实验。利用Langmuir 和Freundlich等温吸附模型[14-15,21]对数据进行拟合,LMO对X-3B等温吸附方程的相关参数见表2。 由表2可见,Langmuir方程的R2高达0.999 1,而Freundlich方程的R2为0.947 6,说明Langmuir方程可以更好地描述LMO对X-3B的吸附行为。基于Langmuir方程计算出的饱和吸附量为129.53 mg/g,与实验得出的平衡吸附量120.79 mg/ g基本一致,这也证明了LMO对X-3B的吸附符合Langmuir式。此外,由Freundlich方程计算出的1/n介于0~1,说明X-3B容易被LMO吸附[22]。由kL=0.254 8可以推算出分离系数(RL)介于0~1,表明LMO对X-3B的吸附属于优惠吸附[23]。

表2 LMO对X-3B的等温吸附方程相关参数
2.6 吸附动力学
在LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附时间为5~120 min、吸附pH为7的条件下,对初始X-3B质量浓度分别为50 mg/L和100 mg/L的模拟X-3B废水进行吸附实验。利用准二级动力学方程对实验数据进行拟合[15,19,21],LMO对X-3B的吸附动力学参数见表3。

表3 LMO对X-3B的吸附动力学参数
由表3可见,准二级动力学方程的R2均为0.999 9,说明初始X-3B质量浓度分别为50 mg/L和100 mg/L时,LMO对X-3B的吸附过程均符合准二级动力学方程。由动力学方程计算出的平衡吸附量分别为24.88 mg/L和49.60 mg/L,与实验得到的平衡吸附量24.68 mg/L和49.12 mg/L基本一致,这也说明准二级动力学方程可以很好地描述LMO对X-3B的吸附过程。因此,可以推测出LMO表面发生了化学吸附[21]。
3 结论
a) 以FA为原料,采用共沉淀法制备LDH和LMO。XRD表征结果证实LMO在吸附X-3B过程中存在结构“记忆效应”;BET表征结果证实LDH经焙烧后比表面积增大。
b) 3种吸附剂对X-3B吸附效果的优劣顺序为:LMO>LDH>FA。在初始X-3B质量浓度为50 mg/L、LMO投加量为2.0 g/L、吸附温度为25 ℃、吸附pH为7、吸附时间为30 min的条件下,X-3B去除率可达98.1%。
c) LMO对X-3B的吸附符合Langmuir等温吸附方程,饱和吸附量为129.53 mg/g,且吸附过程可用准二级动力学方程描述。
d) 采用FA为原料制备LMO,利用其吸附水中的X-3B,可以为粉煤灰的综合利用提供一种新途径,同时为染料废水的治理提供一种新方法。
[1] Zeng Shixin,Wang Jialai. Characterization of mechanical and electric properties of geopolymers synthesized using four locally available fl y ashes[J]. Constr Build Mater,2016,121:386 - 399.
[2] Pavithra P,Reddy M S,Dinakar P,et al. A mix design procedure for geopolymer concrete with fl y ash[J]. J Clean Prod,2016,133:117 - 125.
[3] 邱素芬,王源,蔡觅,等. 粉煤灰及其制备沸石对高浓度氨氮的去除比较[J]. 化工环保,2015,35(6):583 - 587.
[4] 路红霞. 利用粉煤灰制备聚合氯化铝铁絮凝剂的实验研究[D]. 呼和浩特:内蒙古工业大学,2010.
[5] 朱静,吴丰昌. 改性粉煤灰在处理锑矿选矿废水中的应用[J]. 环境科学学报,2010,30(2):361 - 367.
[6] 欧阳平,范洪勇. 基于吸附的粉煤灰改性利用研究进展[J]. 现代化工,2014,34(3):25 - 28.
[7] 张钱,吴平霄. 煅烧阴离子粘土(LDO)对低浓度活性艳橙X-GN的吸附研究[J]. 环境科学学报,2011,31(4):770 - 776.
[8] Theiss F L,Ayoko G A,Frost R L. Synthesis of layered double hydroxides containing Mg2+,Zn2+,Ca2+and Al3+layer cations by co-precipitation methods:A review[J]. Appl Surf Sci,2016,383:200 - 213.
[9] Sajid M,Basheer C. Layered double hydroxides:Emerging sorbent materials for analytical extractions[J]. TrAC Trend Anal Chem,2016,75:174 - 182.
[10] Reinholdt M X,Babu P K,Kirkpatrick R J. Preferential adsorption of lower-charge glutamate ions on layered double hydroxides:An NMR investigation[J]. J Phys Chem C,2009,113:3378 - 3381.
[11] 徐淑芬,倪哲明,夏盛杰,等. Mg/Al双金属氧化物吸附Cr(Ⅵ)的动力学和热力学机理[J]. 硅酸盐学报,2009,37(5):773 - 777.
[12] 闫春燕,伊文涛,裘娜,等. 丙烯酸柱撑类水滑石的制备及其对Cu2+的吸附性能[J]. 化工环保,2012,32(6):557 - 560.
[13] Lafi R,Charradi K,Djebbi M A,et al. Adsorption study of Congo red dye from aqueous solution to Mg–Al-layered double hydroxide[J]. Adv Powder Technol,2015,27:232 - 237.
[14] 程珺煜,岳秀萍,曹岳,等. Zn/Al双金属氧化物对水中硫酸根离子的吸附性能[J]. 环境工程学报,2014,8(1):131 - 137.
[15] 孔垂鹏,聂玉伦,胡春. Mg/Al/Fe 复合氧化物吸附去除水体中氟化物的研究[J]. 环境工程学报,2010,4(1):110 - 114.
[16] Qian Yi,Li Shanshan,Chen Xilei. Synthesis and characterization of LDHs using Bayer red mud and its flame-retardant properties in EVA/LDHs composites[J]. J Mater Cycle Waste Manag,2015,17(4):646 - 654.
[17] Song Hua,Ren Quanming,Li Feng,et al. Preparation of a highly dispersed Ni2P/Al2O3catalyst using Ni-Al-CO32-layered double hydroxide as a nickel precursor[J]. Catal Commun,2016,73:50 - 53.
[18] Mascolo G,Mascolo M C. On the synthesis of layered double hydroxides(LDHs)by reconstruction method based on the “memory effect”[J]. Microporous Mesoporous Mater,2015,214:246 - 248.
[19] 郭宇,岳秀萍,刘吉明. Mg/Al/Fe水滑石的焙烧产物对F-的吸附[J]. 环境工程学报,2015,9(12):5921 - 5926.
[20] 梁薇. 微孔材料BET比表面积计算中相对压力应用范围的研究[J]. 工业催化,2006,14(11):66 - 70.
[21] 李海宁,陈静,李秋梅,等. 铁锰复合氧化物包覆海砂的吸附除磷研究[J]. 环境科学学报,2016,36(3):880 - 886.
[22] 张秀蓉,龚继来,曾光明,等. 磁性氧化石墨烯制备及去除水中刚果红的研究[J]. 中国环境科学,2013,33(8):1379 - 1385.
[23] 姜德彬,余 静,叶芝祥,等. 磁性纳米复合物对水中亚甲基蓝的吸附及其机理[J]. 中国环境科学,2016,36(6):1763 - 1772.
(编辑 叶晶菁)
Adsorption of reactive red X-3B from water by layered metal oxides based on fly ash
Layered double hydroxide(LDH)and layered metal oxides(LMO,or LDO)were prepared using fl y ash(FA)as the raw material by co-precipitation method,and characterized using XRD and BET. The adsorption effects of reactive red X-3B dye(X-3B)on FA,LDH and LMO were compared. The factors affecting adsorption of X-3B on LMO were investigated,and the adsorption mechanism was discussed. The XRD results demonstrated that LMO could restore the layered structure of LDH after adsorption of X-3B. The BET results showed that the specifi c surface area of LMO was larger than that of LDH. The X-3B adsorption effects of the 3 adsorbents decreased in the order of LMO>LDH>FA. The optimal adsorption conditions were as follows:LMO dosage of 2.0 g/L,adsorption temperature of 25 ℃,adsorption time of 30 min,adsorption pH of 7,with the highest X-3B removal rate as 98.1%. The adsorption of X-3B on LMO fitted the Langmuir isothermal adsorption equation well and the saturated adsorption capacity was 129.53 mg/g. The adsorption process could be best described by the pseudo-second-order kinetic model.
fl y ash;layered double hydroxide;layered metal oxide;adsorption;reactive red X-3B
X703
A
1006-1878(2017)02-0183-06
10.3969/j.issn.1006-1878.2017.02.010
Zhou Shaojie1,Liu Mingzhao2,Qian Yi1
(1. College of Environment and Safety Engineering,Qingdao University of Science & Technology,Qingdao Shandong 266042,China; 2. Laoshan Branch of Qingdao Environmental Protection Bureau,Qingdao Shandong 266061,China)
2016 - 08 - 11;
2017 - 01 - 18。
周绍杰(1990—),男,山东省临沂市人,硕士生,电话 18765272850,电邮 zhoushaojie316@163.com。联系人:钱翌,电话 0532 - 84022016,电邮 qianyi1962@126.com。
国家自然科学基金项目(51372129,51572138);青岛市科技局成果转化计划-科技惠民专项(城市发展)(16-6-2-54-nsh)。
