《金属的化学性质》教学设计
2017-06-08潘笛郑明花
潘笛 郑明花

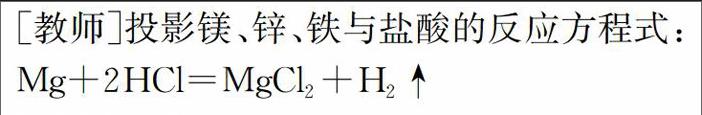

[摘要]物质的性质决定物质的用途,金属的用途不仅与它们的物理性质有联系,而且与它们的化学性质也密切相关,充分了解它们的性质,才能使学生学而有用,学而能用。
[关键词]金属化学性质教学设计
[中图分类号]G633.8
[文献标识码]A
[文章编号]1674-6058(2016)32-0107
一、设计理念
从学生现有的知识水平着手,依据义务教育阶段课程标准要求,构建三维一体的教学目标。在明确教学目标的基础上,以学生身心发展为起点,从生活实际出发,制订以培养学生社会责任感、树立自信心为目的的教学方法及策略。从化学课程的特点出发,在实验中联系生活,在生活中提出教学内容,制订人教版九年级化学上册《金属的化学性质》一节的教学设计,将知识点与社会生活生产紧密结合,体会科学与技术的内涵,充实教学内容,坚持“STS”的教育理念。
二、教学背景分析
1.课标分析
课程标准就本节课内容明确要求:能说明、会表示金属与氧气的反应和金属与酸的反应,并会判断置换反应,学会运用金属活动性顺序。
2.教材分析
《金屬的化学性质》是人教版九年级化学第八单元课题2的内容,在通过课题1了解了金属的物理性质和合金概念的基础上,本课题侧重金属的化学性质:回顾金属与氧气的反应,重点介绍金属与酸的反应、金属与金属化合物溶液的反应,以及常见金属活动性顺序。
3.学生分析
知识水平分析:学生已有九年级化学上册知识的基础,了解常见酸的概念,已掌握金属与氧气的反应,这些为本节课的学习奠定了知识基础,有利于在教育教学活动中总结判断金属活动性的方法。
认知水平分析:本课题安排在九年级下册第八单元的第2课题,学生处于对化学知识的初步探索阶段,虽已有上册知识打下的基础,但学生的逻辑思维能力还没有系统化,教师应在教授学生知识点的基础上,偏重于帮助其建立正确的唯物主义价值观。
三、教学目标
1.知识与技能
(1)通过回顾已学的知识,充分回忆和掌握铁、镁、铜等常见金属与氧气的反应;
(2)通过实验初步认识常见金属与酸的置换反应,能利用置换反应解释与日常生活有关的化学问题;
(3)联系相关的生产生活实际,学会运用金属活动性顺序表解决实际问题。
2.过程与方法
(1)能进行探究金属活动性强弱的实验设计,掌握探究金属活动性顺序的方法及其反应原理;
(2)通过观察演示实验,了解常见金属与酸的反应实验操作及注意事项;
(3)学习和体验对实验现象进行比较、分析、概括并获取结论的方法。
3.情感态度与价值观
(1)通过对实验的探究、分析,培养学生严谨、认真、实事求是的科学态度;
(2)学生在实验探究中学会与他人交流、合作,增强协作精神;
(3)通过联系生产生活实际问题,培养学生的社会责任感和唯物主义价值观。
四、教学重难点
教学重点:探究金属活动性顺序,归纳得出置换反应的特点。
教学难点:对金属活动性顺序和置换反应的理解和应用。
五、教学过程
1.导课
[教师]展示漫画故事:《真金与黄铜》。
[学生]听漫画故事,产生疑问:为什么黄铜害怕遇见盐酸?
设计意图:设置悬念,激发学生好奇心,引出课题——《金属的化学性质》
2.复习
[教师]投影A组:金属与氧气的反应。
[教师]提示学生按操作规范进行实验,且进行指导纠正。同时引导学生根据金属与氧气的反应现象与反应难易程度,比较金属的活动性强弱。
[学生]以小组的形式进行相关实验,比较出镁、铁、铜的活动强弱:镁比铁强,镁比铜强。并完成表格(参见表1),回忆、记录、巩固知识点。
设计意图:复习、巩固相关知识,加深印象,培养学生独立自主的学习能力,初步掌握判断金属活动性差异的方法,并引出新课程的学习内容。
3.活动与探究
[教师]投影B组:金属与稀盐酸的反应。
[教师]演示镁、锌、铁、铜与稀盐酸的反应,并要求学生完成表格(参见表2)。
[学生]观察到镁、锌、铁都能与稀盐酸反应,且反应剧烈程度不同,但铜不能与稀盐酸发生反应。同时完成表格的填写。
[教师]根据镁、锌、铁、铜与稀盐酸的反应现象,让学生试猜想金属与稀硫酸的反应现象。
[教师]投影C组:金属与稀硫酸的反应,并要求学生完成与B组实验相同的表格。
[教师]提示学生按操作规范进行实验,观察现象。巡视、指导实验,引导学生讨论、交流和展示探究结果。
[学生]小组实验,完成表格。讨论、交流,小组代表描述实验现象及结论,书写化学方程式。
设计意图:让学生在合作与交流中自主探究,在操作与思考的活动中实现三维目标。
[教师与学生]欣赏课本图8-12:金属与盐酸反应的比较。
[学生]观察图片,探究出镁、锌、铁、铜的金属活动性由强到弱依次为:镁>锌>铁>铜,思考、讨论得出结论:金属可分成能与酸发生反应和不能与酸发生反应两类。
设计意图:营造轻松、和谐的探究氛围,发展学生的想象力。
[教师]引导学生总结相关结论。
[学生]概括出第二种判断金属活动性强弱的方法:根据金属是否与稀盐酸、稀硫酸反应或反应的剧烈程度判断金属的活动性强弱。
设计意图:让学生在交流中实现思维的提升。
[教师]提问:这些反应有什么特点?
[学生]归纳得出:(单质)+(化合物)=(化合物)+(单质),即由一种单质跟一种化合物反应生成另一种单质和另一种化合物。
[教师]引出置换反应的概念。
[教师]提问:置换反应的通式如何书写?
[学生]思考,回答:A+BC=B+AC。
设计意图:培养学生独立思考的能力和实事求是的科学态度。
[教师]演示播放铝与硝酸铜、铜與硝酸银、铝与硫酸亚铁反应的实验视频。提出问题:通过实验,观察有哪些现象产生?要求学生试写出反应方程式。
[学生]认真观察实验,根据实验现象回答问题,书写方程式。
[教师]引导学生归纳总结。
[学生]总结判断金属活动性强弱的第三种方法:根据金属是否能把另一种金属从其金属化合物的溶液中置换出来,判断金属活动性的强弱。
[教师]操作铝与氧气反应的实验,并准确描述实验现象。
[教师]为什么置换反应中铝可以置换铁与铜,但与氧气的反应却不是燃烧,只是熔化,且又不滴落呢?
[学生]观察实验并思考问题。
设计意图:为引出“悬而未滴”现象做铺垫。
[教师]铝性质活泼,常温下易与氧气反应生成一种致密氧化膜,能够保护内部金属。若想观察到明显的实验现象,则需要将铝箔打磨后再进行实验。
设计意图:既为金属活动性顺序表中铝排在前面做说明,又强调铝的特殊之处,加强学生记忆。
4.总结归纳
[教师]讲述科学发展史,从而引出常见金属在溶液中的活动性顺序,即金属活动性顺序表。
设计意图:易于学生识记金属活动性顺序表。
5.课堂练习
[教师]家用铁锅生锈时,我们是否可以利用醋酸来除锈呢?我们应该怎样防止铁锅生锈?
[学生]思考并回答教师所提问题。
设计意图:使学生能够学以致用,体会“生活处处有化学”的意义;强化学生识记,便于学生所学知识系统化。
六、教学反思
本节课教师通过创设合理的教学情境,将铝与氧气反应的教学内容放在金属与金属盐溶液反应之后,有利于学生比较几种金属的活动性强弱,便于学生识记金属活动性顺序表。学生通过自主探究的方式掌握实验相关操作及注意事项,运用类比归纳置换反应的特点,学会运用金属活动性顺序表解答实际生活问题。真正做到了从学生出发,坚持“以学生为本”的教学理念。
