草苁蓉的质量标准研究
2017-06-05樊红军杨树东
樊红军 王 辉* 谷 杰 张 航 杨树东
(长春市食品药品检验中心,吉林 长春 130012)
草苁蓉的质量标准研究
樊红军 王 辉* 谷 杰 张 航 杨树东
(长春市食品药品检验中心,吉林 长春 130012)
目的建立草苁蓉的质量标准。方法用薄层色谱(TLC)法鉴别草苁蓉药材;以高效液相色谱(HPLC)法测定药材中齐墩果酸的含量。结果通过TLC,能有效的进行区别,易于识别。齐墩果酸进样量在0.1~2.5 μg 范围内与峰面积积分值呈良好线性关系(r=1.000);平均回收率为99.0%,RSD=1.8%(n=6)。结论所建标准可有效控制草苁蓉的质量。
草苁蓉;齐墩果酸;薄层色谱法;高效液相色谱法
草苁蓉为列当科草苁蓉属多年生草苁蓉的干燥全草[1],寄生于桦木科赤杨属Alnus植物的根上草本植物。 长白山地区的“地道药材”和民间药材,东北三宝之一。别名东北不老草,为国家二级保护植物[2]。近年在草苁蓉中发现含有多糖、草苁蓉苷、草苁蓉环烯醚萜苷等化学成分。具有补肾壮阳、腰膝冷痛、肾虚阳萎、滋阴补阳、膀胱炎和润肠通便等[3]。现代药理学研究证明在提高人体免疫、抗肿瘤[4-5]、抗炎、保护肝脏[6-10]等方面有疗效。目前未对其质量标准进行收载,本文通过TLC及高效液相色谱法,对草苁蓉及其相似品锁阳、肉苁蓉进行同步考察,建立草苁蓉的质量标准,对其质量控制有重要意义。
1 仪器、试药及对照药材
1.1 仪器:LC-1100 HPLC高效液相色谱仪;D101-1A干燥箱;GR-202电子分析天平;色谱柱Dima C18(250 mm×4.6 mm,5 μm);硅胶GF254(生产厂家:青岛海洋化工厂,规格200×200 mm批号:20140108 )。
1.2 试药:甲苯 (天津市北联精细化学品开发有限公司,批号20151120,分析纯);乙酸乙酯(生产厂家:北京化工厂,批号:20160107,分析纯);醋酸(生产厂家:天津市北联精细化学品开发有限公司,批号20130520,分析纯);甲醇(生产厂家:北京化工厂,批号:20150514,分析纯);乙腈(生产厂家Bioreacs,LOT:908765,CAS:75-05-8,色谱醇);磷酸(生产厂家北京化工厂,批号:20140625,分析纯);水(超纯水)。
1.3 对照品:肉苁蓉(提供:中国食品药品检定研究院,批号:121101-200402);锁阳(提供:中国食品药品检定研究院,批号:121393-200401);齐墩果酸(提供:中国药品生物制品检定所 批号:110705-200306,纯度为94.9%)。
2 样品的来源
采集和购买,共收集10批样品,经吉林农业大学韩梅教授鉴定,具体来源见表1。
3 草苁蓉的TLC鉴别
取样品粉末1 g,加入甲醇100 mL,超声提取1 h,过滤,滤液浓缩至约2 mL,作为供试品溶液。另取草苁蓉自采7号样品、肉苁蓉、锁阳各1 g作为对照药材,同法制成对照药材溶液。照薄层色谱法(中国药典2015年版通则0502)试验,吸取供试品溶液5~10 μL、对照药材溶液各5 μL,分别点于同一硅胶GF254薄层板上,以甲苯-乙酸乙酯-甲酸(20∶4∶0.5)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。此方法能区别草苁蓉及其类似品锁阳肉苁蓉[11]的鉴别。同时10样品薄层色谱图一致,10批样品紫外检视后,喷以10%硫酸乙醇试液,加热至斑点显色清晰,薄层色谱图一致。薄层色谱图见图1。结果此方法能作为草苁蓉薄层鉴别方法。

表1 10份样品来源
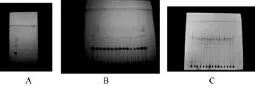
图1 TLC色谱图[A紫外光灯(254 nm)(1为草苁蓉样品;2为肉苁蓉;3为锁阳);B紫外光灯(254 nm)。(1~10为1-10号样品点样10 μL;11为1号样点样5 μL;12为1号样点样10 μL;13~15为1号样的3次重复);C 10%硫酸乙醇试液日光(1~10为1~10号样品点样10 μL;11为1号样点样5μL;12为1号样点样10 μL;13~15为1号样的3次重复)]
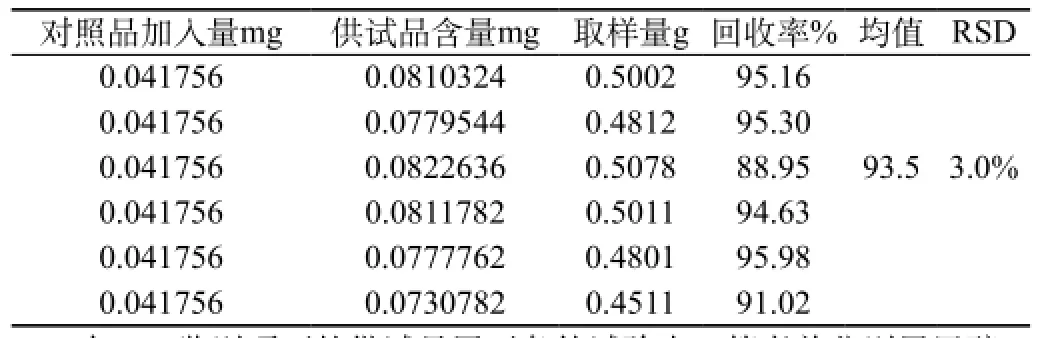
表2 样品回收率
4 含量测定
4.1 标准品溶液的制备:精密称取齐墩果酸对照品适量,置100 mL量瓶中,加甲醇适量使溶解并稀释至刻度,摇匀,即得。(每1 mL中含齐墩果酸0.0996 mg)。
4.2 供试品溶液的制备:取本品粉末(过二号筛)约0.5 g,精密称定,加入甲醇100 mL,超声(功率250 W,频率40 kHz)1 h,冷却至室温,摇匀,滤过,用甲醇洗涤提取器,每次20 mL,分3次洗涤,滤过,合并滤液,蒸干,残渣用甲醇溶解后,转移至10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得。
4.3 色谱条件。色谱柱:Dima C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.5% 磷酸溶液(85∶15);流速:1.0 mL/min;检测波长:210 nm;柱温:室温 ℃;进样量:10 μL。理论板数按齐墩果酸峰计算应不低于3000。色谱图见图2。

图2 高效液相色谱图(A.溶剂空白;B.齐墩果酸标准品;C.草苁蓉药材)
4.4 线性关系考察:分别精密吸取1.0 µL、5.0 µL、10 µL、15 µL、25 µL,分别注入液相色谱仪,记录色谱图。以峰面积为纵坐标,进样量(µg)为横坐标,测得回归方程为Y=426.33X+28.531,相关系数r=1.000(n=6)。结果表明,齐墩果酸进样量在0.1~2. µg,具有良好的线性关系。
4.5 精密度试验:精密吸取同一标准品溶液,注入液相色谱仪,连续测定6次,RSD为0.1%,实验结果表明仪器精密度良好。
4.6 最低检测限测定:按信噪比等于3(S/N=3),作为最低检测限,测得该方法中齐墩果酸的检测限为12.5 ng/mL。
4.7 重复性试验:取同一批号的样品,精密称定6份,分别依法提取制成供试液。按正文方法测定其含量。RSD为2.2%,重复性试验结果表明,本法重复性良好。
4.8 稳定性考察:精密吸取供试品溶液10 μL,每隔2 h进样测定一次,共测定24 h,计算含量,RSD为0.2%,稳定性试验结果,供试品溶液在24 h内基本稳定。
4.9 加样回收率试验:称取已知含量0.14 mg/g)的样品6份,每份约0.5 g,分别精密加入对照品贮备液(约0.1 mg/mL)3.0 mL按正文方法制备及测定,计算加样回收率,测得6次平均回收率为99.0%,RSD为1.8%,试验结果表明:供试品回收率较高,RSD在规定范围内,结果见表2。
4.10 样品含量测定:按照上述色谱条件及方法,测定10个不同产地草苁蓉药材的含量,产地见表1,结果见表3。

表3 样品含量测定结果
5 讨 论
在TLC鉴别项下的供试品展开条件试验中,笔者曾分别用甲醇∶醋酸∶水(2∶1∶7)和甲苯∶乙酸乙酯∶甲酸(20∶4∶0.5)展开剂分别在硅胶G板和硅胶GF254板展开,结果发现甲苯∶乙酸乙酯∶甲酸(20∶4∶0.5)分离点多,分离效果好。硅胶G板展开发现,草苁蓉与伪品鉴别不明显,而在硅胶GF254展开能有效鉴别草苁蓉及其相似品鉴别明显,同时斑点稳定,不同产地斑点一致,可作为草苁蓉薄层色谱质量控制方法,同时能有效区别真伪。
在HPLC含量测定项下笔者曾考察不同提取溶剂甲醇、60%乙醇和80%乙醇,不同提取方法回流和超声,通过实验结果选着上述提取方法。考察不同流动相分别为甲醇-0.5% 磷酸溶液(90∶10)、甲醇-0.5% 磷酸溶液(80∶20)、甲醇-水(85∶15)和乙腈-0.5% 磷酸溶液(85∶15),发现乙腈-0.5% 磷酸溶液(85∶15)没有干扰,分离效果好。可作为草苁蓉质量标准含量控制方法。草苁蓉不良反应小[12],同时为鹿鞭回春胶囊的原药材,通过对质量标准研究发现草苁蓉同锁阳及肉苁蓉的成分有差别,能够真伪鉴别。草苁蓉有不可替代的功效。
[1] 楚玉南,戴续红,吴华新.草苁蓉生物学特性初探[J].中国林副特产, 2009(3):104.
[2] 陈庆红,张睿,冯秀春,等.长白山区草苁蓉研究现状与病危机制[J].现代农业科技,2015(14):80-81.
[3] 冉先德.中华药海[M].哈尔滨:哈尔滨出版,1995:1281.
[4] 尹宗柱,金海玲,李天侏.草从蓉甲醉提取物对二乙基亚硝胶诱发大鼠肝脏癌前病变抑制作用[J].中国中药杂志,1998,23(7):424-426.
[5] 沈明花,尹宗柱.草苁蓉提取物对二乙基亚硝胺诱发的肝脏癌前病变大鼠抗氧化活力的影响[J].中国中药杂志,1999,24(12):746-749.
[6] 潘理会,李春辉,孙嘉斌.草苁蓉及氧化苦参碱治疗肝纤维化的实验研究[J].承德医学院学报,2005,22(3):195-198.
[7] 黄媛,金永日,朴熙绪,等.草苁蓉乙醇提取物对大鼠肝星状细胞增殖与调亡的影响[J].中国医院药学杂志,2012,32(1):1-5.
[8] 张炜煜,朴熙绪,金海燕,等.草苁蓉乙醇提取物对大鼠非酒精性脂肪性肝病的保护作用及机制[J].世界华人消化杂志,2012,20(32):3087.
[9] 周丽莎,朱书秀,望庐山.草苁蓉提取物对阿尔茨海默病大鼠乙酰胆碱及学习记忆能力的影响[J].中国医院药学杂,2009,29(23):1980.
[10] 李勇,金明,尹学哲.草苁蓉抗脂质过氧化活性研究[J].中国实验方剂学杂志,2010,16(15):203-205.
[11] 孙仓,常桂英,矫延春,等.肉苁蓉与草苁蓉的比较[J].吉林农业大学学报,1996,15(增 刊):118-121.
[12] 张航,王辉,杨树东.草苁蓉的本草考证及药理研究进展[J].长春中医药大学学报,2016,32(2):40-42.
Study on Quality Standard of Bosehniakia rossica
FAN Hong-jun, WANG Hui, GU Jie, ZHANG hang, YANG Shu-dong
(Changchun Institute for Food and Drug Control, Changchun,130012, China)
ObjectiveTo establish the quality standard of Bosehniakia rossica.MethodsIt was identified by TLC, at the same time the content of oleanolic acid in Bosehniakia rossica was determined by HPLC.ResultsThe TLC spots of syringin and echinocystic acid were clear and easy to identify. The linear range of ginsenoside in Bosehniakia rossica were 0.1-2.5 μg(r=1.000)with an average recovery of 99.0%(RSD=1.8%, n=6).ConclusionEstablished quality standard can be used for the quality control of Bosehniakia rossica.
Bosehniakia rossica.; Oleanolic acid; TLC; HPLC
R282.710.3
B
1671-8194(2017)12-0004-02
吉林省中药材地方标准[吉食药监科[2015]304号]
*通讯作者:E-mail: wanghui20141111@163.com
