基于合作探究的理论性知识的教学
2017-05-24王振魏斌胡志刚
王振+魏斌+胡志刚
摘要:理论性知识的教学是学科教学的重要内容。以“质量守恒定律”的教学为例,阐述基于合作探究的理论性知识的教学模式,并阐述了基于合作探究的教学反思和教学建议。
关键词:质量守恒定律;理论性知识;合作探究
文章编号:1005–6629(2017)4–0052–04 中图分类号:G633.8 文献标识码:B
化学理论性知识是指反映物质及其变化的本质属性的基本概念和基本原理[1]。在中学阶段,主要包括物质的组成、性质、变化等基本概念,以及质量守恒定律、元素周期律等基本理论,是化学教学中最关键的内容。
理论性知识的学习主要是学习者从大量的具体例证中概括得出事物特征。以质量守恒定律为例,课程标准明确指出“要引导学生通过实验探究认识化学变化的规律,初步了解研究化学变化的科学方法”[2]。现有教材中,质量守恒定律实验有白磷燃烧、铁钉与硫酸铜、碳酸钠固体与盐酸、镁条燃烧、氢氧化钠与硫酸铜、蜡烛燃烧等体系,通过实验探究认识化学变化的规律和构建质量守恒观。然而实际教学中很难在有限的一节课内做多个实验,教师疲于赶着一个个实验,教学效果往往不尽如人意。笔者在实践中总结一套可以节约课堂时间,且行之有效的分组合作探究教学模式,详见图1。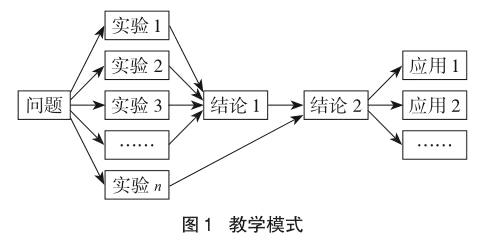
把全班分成不同的实验组,同时在做实验1、实验2、实验3、……,经过一系列实验得出粗略的结论1。通过实验n的反常现象,进一步升华得出完整的结论2,也就是我们想要学的理论性知识。最后通过理论性知识回归生活中的不同实践应用。我们以质量守恒定律为例,将不适合学生做的课本实验进行改进和取舍,改成适合学生分组探究的实验进行教学。
1 教学设计
1.1 導入新课——提出问题
[家庭实验]教师提供自制汽水的配料表,见表1,以及小苏打和柠檬酸的反应文字表达式:小苏打+柠檬酸→柠檬酸钠+水+二氧化碳。学生自由组团在家制汽水。
[影像展示]学生自制汽水的过程中,所有原料加一起后质量是多少?
学生A说:制好的汽水质量就是原料的加和:400g+10g+20g+1.5g+1.5g=433g。
学生B说:小苏打和柠檬酸会发生化学反应,不是简单的混合。反应后质量还会是433g吗?
[提出问题]以这一问题为契机趁机提出问题:化学反应前后,反应物的总质量是否等于生成物的总质量?
学生猜想:反应前后质量相等;反应前后质量不相等。
1.2 合作探究——得出结论
[提供方案]既然有争议,我们就该通过实验去证明。为了更好地得出结论,我们用四种不同的实验方案来看看反应前后质量到底相不相等。方案详见表1。
[分工详细]为了更好地验证,学生四人一组,互相配合完成实验。每组选择一位同学记录实验现象并汇报实验结果。全班十二组,每三组做同一种实验方案,以确保实验结论的可靠。
[分组实验]教师巡视并适当指导。
[汇报结果]前九组同学代表依次汇报各组的实验现象和结论,详见表2。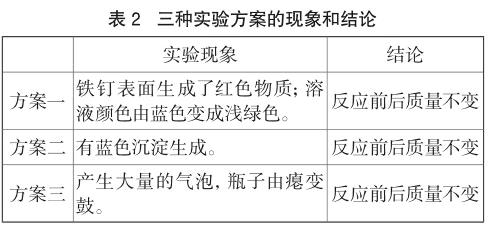
[得出结论]经过大家不同的实验得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律就叫质量守恒定律。
1.3 拓展提升——精炼理论
[汇报结果]剩下的三组同学代表依次汇报各自组的实验结论。小心地把盛有盐酸的小试管从烧杯中取出,并将其倾斜,使小试管中的盐酸进入小烧杯中,发现产生大量的无色无味的气体,反应后物质的质量变小。
教师:为什么实验三和实验四用同样的反应物,得出的结论却不同呢?
(提示教师投影展示方案三和方案四不同的实验装置图,详见图3。)
学生:因为方案四产生的气体逸散到空气中了。
教师:非常棒!因为参与化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。所以当有气体生成时,我们要选择什么样的装置?
学生:密闭的实验装置。
[追问]能不能从微观角度去解释质量守恒定律呢?
提示给学生演示水分子电解的动画,水通电后变成氢气和氧气,见图4。在这个化学反应过程中,反应后元素种类有没有改变、原子数目有没有改变、原子质量有没有改变?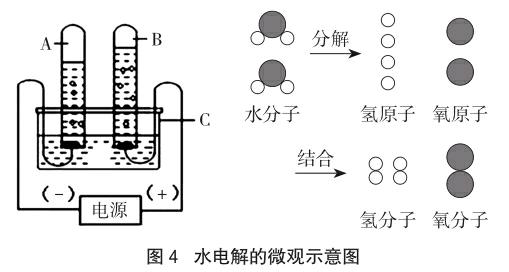
学生:化学反应前后,原子种类不变,数目没有增减,原子的质量也没有改变,所以化学反应前后物质的质量不会改变。
1.4 结束新课——实践应用
[实践应用1]学生用教师备好的材料(400g水,10g白糖,20g果汁,1.5g小苏打,1.5g柠檬酸)现场制汽水,质量会是433g吗?
教师:为什么他们制得汽水质量会少于433g?
学生:因为制汽水过程中,产生很多气体,没有及时盖上瓶盖,有一部分气体跑到瓶外了,所以汽水的质量会变小。
教师:非常好!当有气体生成,我们要考虑产生气体的质量。
[实践应用2]已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有 元素,可能含有 元素。
学生:石蜡中一定含有C和H元素,可能含有O元素。
2 教学反思
2.1 分组合作——课堂效率高
本节课通过不同组同时做四个不同的实验方案(实验1,实验2,实验3,实验4,详见图5),所以大大减少了课堂实验的时间,提高了课堂的效率,而且四人一组分工明确,培养了学生合作学习的经历。经过全班同学的不同实验验证了质量守恒定律,在教师的引导和启发下,层层深入,加深对质量守恒定律的理解。通过合作探究学习,不仅强化了班级体的团体观念,培养了学生合作学习的意识,而且顺利高效地完成了课堂教学目标。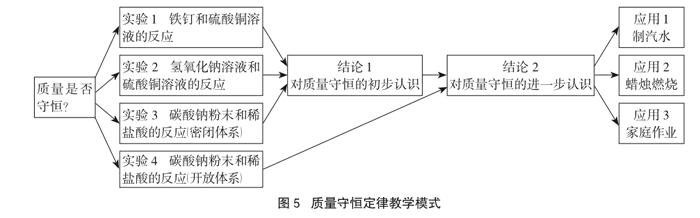
2.2 理论源于实践——理论指导生活
通过具体、生动的自制汽水实验,提出的问题更容易激发学生的学习兴趣和探究欲望。理论性知识的学习的实质是新知识与学生原有概念相互作用,建立其内在的逻辑联系,其结果是新知识纳入原有认知结构中,使原有认知结构得以丰富。学生在学习完质量守恒定律这一理论知识后,通过一系列的实践应用,让学生体会理论指导生活,逐步培养学生的物质变化观。如应用1现场制汽水后质量变少了,学生就比较轻松地知道生成物有气體,要采用密闭的装置图;应用2蜡烛燃烧,不仅从宏观认识物质变化,而且从微观和元素角度去分析推理蜡烛成分,强化了理论源于生活又高于生活。
2.3 培养思维——搭建思维“脚手架”
理论知识的学习,往往都是通过大量的实验验证得出具有一定的概括性结论,这些结论对以形象思维为主的初三学生来说比较难以理解。所以在理论知识的学习过程中,要注意在学生思维障碍处搭建“脚手架”,帮助学生顺利地达成教学目标。如质量守恒定律从宏观向微观过渡,学生在理解上就存在障碍,此时借助水电解的动画示意图,把微观的水分子呈现给学生,学生就容易想到化学反应前后原子的种类、数目、质量都不变,所以质量守恒。
2.4 勤于动手——从实践中发现问题
化学是一门以实验为基础的科学,教学要紧密联系生产、生活实际,使学生真切地感受到发生的化学变化。而实际的教学中,碍于课时的原因很多实验没时间做,可以鼓励学生从家庭实验中发现问题,让化学知识的学习回归到生活和生产中。鼓励学生勤于动手,在社会实践中发现问题,从化学课本中找到解析,在利用所学知识解决生活问题,更好地享受生活中化学带来的乐趣。
3 教学建议
3.1 铁钉和硫酸铜溶液的反应的改进
铁钉和硫酸铜溶液反应比较慢。丁吉念老师通过探究实验得出[3]:铁钉伸入质量分数为6.02%~1.88%的硫酸铜溶液,铁钉很快析出红色物质,而溶液的颜色大概需要60min才变为浅绿色,时间仍然较长。根据“氯离子效应”[4]在硫酸铜溶液中,稍加一些氯化钠能加快铁和硫酸铜溶液的反应,在两三分钟后即可看到铁钉表面变黑随后变红,原因是刚置换生成的铜颗粒比较小,发生了光学上的漫反射,把铁钉从溶液中取出即可看到铁钉表面生成的是红色的铜。
3.2 借助学生的错误操作拓展应用
优秀的教师往往善于利用学生的实际情况临时改变自己的教学,借助学生的动态生成,增加师生的活动。在教学前,没有预料到会有很多学生不会正确使用砝码,学生虽然已在八年级物理课上学过托盘天平的使用,但还是有小部分学生错误地用手捏砝码。在讲过质量守恒定律后,发现这一状况教师可以趁机提问学生,用手抓砝码会对称量的重量有什么影响?教师提示铁在潮湿的情况下,容易和空气中的氧气反应,生成铁锈,并写出文字表达式:铁+氧气+水→铁锈。巧借学生的错误操作,进一步拓展质量守恒定律到有气体参与反应的体系。
3.3 实验注意安全性
碳酸钠粉末和盐酸反应,在密闭体系状态下反应,最好装入药品时,把矿泉水瓶稍微捏瘪,有利于验证学生观察到产生大量的气泡后,瓶子变鼓,也避免了瓶中产生气体过多,压强变大,防止瓶盖喷出的安全隐患。氢氧化钠和硫酸铜溶液的反应,最好是把小试管里放入氢氧化钠溶液,以防学生倾倒液体时,手接触到氢氧化钠溶液。鼓励学生在条件允许的情况下,做一些社会实践活动,如家庭小实验,以弥补课堂教学的不足。
参考文献:
[1]胡志刚.化学课程与教学论[M].北京:科学出版社,2014:99~100.
[2]中华人民共和国教育部制定.义务教育化学课程标准(2011年版)[S].北京:北京师范大学出版社,2011.
[3]丁吉念.一则质量守恒定律实验最佳效果研究[J].化学教育,2012,(11):75~78.
[4]王程杰.关注氯离子效应在中学化学实验中的应用[J].化学教学,2015,(11):53~55.
