手性二茂铁双膦配体的研究进展
2017-05-18曹龙海
于 振,杨 杰,张 雪,曹龙海
(黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040)
YU Zhen,YANG Jie,ZHANG Xue and CAO Long-hai
(Institute of Petrochemistry,Heilongjiang Academy of Sciences,Harbin 150040,China)
手性二茂铁双膦配体的研究进展
于 振,杨 杰,张 雪,曹龙海
(黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040)
手性二茂铁双膦配体在不对称合成应中是一类非常优秀的配体,它们与有机金属元素配合能够获得很好的不对称催化活性。简略的列举了一些手性二茂铁双膦配体,及其对某些潜手性底物的对映体选择性。
手性;二茂铁;双膦;不对称催化;对映体选择性
前言
手性是一种自然界的基本属性。手性化合物的对映异构体虽然在结构上很相似,物理性质也基本相同,但对生物体而言,许多手性化合物的对映异构体具有截然不同的表现。所以在医药行业中,如果药物分子是手性分子就必须确定发挥药理作用的是哪种构型的分子,因为发挥药理作用的都是其单一构型,另一构型没有或很少有药理活性,甚至有毒副作用。要获得单一手性化合物的最有效的方法是催化不对称合成,而其关键是手性催化剂的研究,在不对称催化剂的研究中,手性膦配体是发展较快研究较广的,在不对称催化氢化反应中使用的大多数膦配体都是双膦配体,这是因为单膦配体制成催化剂后,构型易变,多数光学选择性不高[1~3]。但双膦配体制备难度大并且难以长期保存,之后人们发现二茂铁具有刚性骨架、容易转化为衍生物、化学性质稳定,这些特点使得二茂铁能够作为双膦配体的刚性骨架合成更稳定的双膦配体。人们对二茂铁双膦配体进行了大量的研究报道,合成了许多高效的二茂铁双膦配体,它们在与钌、铑、铱等过渡金属有机溶液配合后,对特定底物都具有良好的对映体选择性。
1 同侧取代的二茂铁双膦配体
Togni等人在1994年合成了一类配体Josiphos 1,这一类型配体实用性高,具有较高的立体选择性而应用广泛,它们与铑离子络合不对称氢化和硼氢化反应取得了99%的ee值[4]。
Kagan等人在1998年合成配体2,应用于不对称催化氢化反应,其对映体选择性很好[5],之后Kagan等人在2000年合成了双膦配体3,它与铑离子络合,不对称催化氢化衣康酸二甲酯能获得98%的ee值[6]。此外,同年他们还合成了配体4,它同样与铑离子络合,不对称催化氢化衣康酸和衣康酸二甲酯均能获得95%的ee值[7]。

Knochel等人1999年合成了一类配体Taniaphos 5,这类配体与铑离子络合,对不同的烯烃和β-羰基具有优异的不对称催化氢化的对映体选择性[8]。
Bophoz 6由Boaz等人在2002年合成[9],它与铑离子的络合催化剂,能够有效地对α脱氢氨基酸,衣康酸和α酮酸酯进行不对称催化氢化,Boaz等人将Bophoz6放于空气中储存,发现它具有极强的空气稳定性,放置三年后与铑离子络合催化氢化α脱氢氨基酸和衣康酸衍生物,依然能够获得高于95%的ee值[10]。其类似配体7和8是官能团化烯烃不对称氢化的有效催化剂,对脱氢氨基酸衍生物和α芳酰胺不对称氢化的ee值达到99.6%以上[11]。

配体Walphos 9它与铑离子络合不对称催化氢化烯烃具有很好的效果,能够获得95%的ee值[12]。

2 异侧取代的二茂铁双膦配体
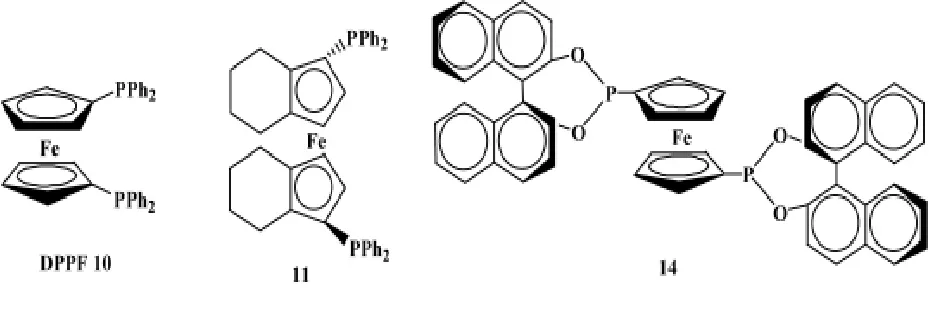
Dppf 10作为非手性的二茂铁双膦配体,自在20世纪中期被人们发现以来,衍生出了很多优秀的手性双膦配体[13],如有研究者在Dppf 10上引入较强刚性的环己烷,合成具有环戊烯并环己烷的二茂铁手性膦配11,它与钌离子络合后,在不对称催化氢化脱氢氨基酸的反应中具有较好的对映体选择性,能够有97%的ee值;与铑离子络合不对称催化氢化能够达到97%的ee值以上;与铱离子络合不对称催化氢化亚胺类潜手性底物能够获得79%以上的ee值[14,15]。
Reetz等人在1998年将联萘酚(BINOL)引入到二茂铁双膦配体中,合成配体14,它与铑离子络合后,对衣康酸二甲酯和2-乙酰氨基丙烯酸甲酯进行不对称催化氢化,均能获得99.5%的ee值[16]。
Knochel等人合成具有C2轴对称的二茂铁双膦配体Ferriphos 12[17],它与铑离子的络合物对甲基丙烯酸的不对称催化氢化反应获得的ee值高于97%;它的四乙基取代衍生物Ferrophos 13,与铑离子络合,不对称催化氢化α-(酰基)丙烯酸能够获得高于99%的ee值[18]。
BPPFA15是一类优秀的双膦配体[19],它具有面手性和碳手性,它是由N,N-二甲基-1-二茂铁基乙胺(Ugi’s胺16)与丁基锂在乙醚中发生取代反应后,再与二苯基氯化膦反应合成的。

BPPFA15经过不同的合成步骤,又能合成其它双膦配体,如合成带硫脲基团的双膦配体17,它和过渡金属络合催化氢化潜手性的烯烃,能够取得99%的ee值[20]。它的衍生配体18,与铑离子络合后对丙烯酸衍生物不对称催化氢化,能够获得93%的ee值[21]。之后Hayashi等人又合成了类似配体BPPFOH 19,它与铑离子络合,不对称催化氢化烯烃磷酸酯类化合物,能过获得大于78%的ee值[22]。

Ito研究的反位螯合的双膦配体TRAPS 20,在不对称氢化中效果同样较好。其衍生的EtTRAP和BuTRAP在催化氢化丙烯酸酯衍生物为底物时,其ee值均在88%以上[23]。
Piet等人合成的配体BPNF 21,它对丙烯基不对称加氢反应具有良好的对映体选择性,能够达到73%的ee值[24]。
还有配体22,它具有C2轴对称的二茂铁双膦配体,它与钯离子络合,催化氢化丙烯基,能够获得92%以上的ee值[25]。
配体23,它属于FerroTANE的一类配体,它与铑离子络合能够有效地对烯烃进行不对称催化氢化反应,例如它的苯基取代配体对衣康酸的不对称催化氢化反应能够得到98%的ee值[26]。

3 多二茂铁基的的双膦配体
Lutz等人又合成了多二茂铁配体24和25,配体25应用于丙烯基的不对称催化氢化反应能够获得88%的ee值[27]。

配体26具有两个手性二茂铁基团,它们通过Cp-Cp键连接在一起,每一个二茂铁基团的烷基膦侧链上都有一个手性碳,这类配体与铑离子络合对乙酰氨基丙烯酸酯的不对称催化氢化反应,能够获96%以上的ee值[28]。
陈卫平[29]等人合成的多二茂铁双膦配体27,它与铑离子的络合物,对α-取代肉桂酸的不对称催化氢化能够获得高于99%的ee值。
4 结论与期望
手性二茂铁类双膦配体,具有良好的化学稳定性,在不对称催化氢化反应中已经有了广泛的应用,并取得了不错的效果。绝大多数的二茂铁手性双膦配体,都要配合过渡金属,钌、铑、铱等才能更好的进行催化氢化反应,这就增加了催化剂的成本及应用难度,虽然对二茂铁基双膦配体的研究已经广泛的开展,但由于其对贵金属的依赖等原因,在工业上的应用就相对缺乏,绝大部分都停留在实验室应用阶段,需要人们进一步的应用研究早日应用到工业生产当中。
[1] GREBER G,KRICHELDORF H R.Preparation of Silyl Esters of Isocyanato Carboxylic Acids[J].Angewandte Chemie International Edition,1986,7:942.
[2] VINEYARD B D,KNOWLES W S,SABACKY M J,et al.Asymmetric hydrogenation.Rhodium Chiral Bisphosphine Catalyst[J].Journal of The American Chemical Society,1977,99:5946~5952.
[3] CHAUHAN P,CHIMNI S S.Organocatalytic Asymmetric Synthesis of 3-amino-2-oxindole Derivatives Bearing a Tetra-substituted Stereocenter[J].Tetrahedron:Asymmetry,2013,24:343~356.
[4] TOGNI A,BREUTEL C,SCHNYDER A,et al.A Novel Easily Accessible Chiral Ferrocenyldiphosphine for Highly Enantioselective Hydrogenation,Allylic Alkylation,and Hydroboration Reactions[J].Journal of The American Chemical Society,1994, 116(9):4062~4066.
[5] ARGOUARCH G,RIANT O,KAGAN H B A.Straightforward Asymmetric Synthesis of Enantiopure 1,2-Disubstituted Ferrocenes[J].The Journal of Organic Chemistry,1998,63(10): 3511~3514.
[6] SAMUEL O,ARGOUARCH G,KAGAN H B.Synthesis of Some Ferrocene-Based 1,3-Bis(phosphanes)with Planar Chirality as the Sole Source of Chirality[J].European Journal of Organic Chemistry,2000(16):2885~2891.
[7] ARGOUARCH G,SAMUEL O,KAGAN H B A.New Class of Ferrocene-Based l,2-Bis(phosphanes)Possessing only Planar Chirality[J].European Journal of Organic chemistry,2000(16): 2893~2899.
[8] GROSSHEIMANN G,IRELAND T,KNOCHEL P.et al.Ferrocenyl Ligands with Two Phosphanyl Substituents in the α,ε Positions for the Transition Metal Catalyzed Asymmetric Hydrogenation of Functionalized Double Bonds[J].Angewandte Chemie International Edition,1999,38(21):3212~3215.
[9] BOAZ N W,DEBENHAM S D,MACKENZIE E B,et al.Phosphinoferrocenyl-aminohposphines as Novel and Practical Ligands for Asymmetric Catalysis[J].Organic Letters,2002,4(14): 2421~2424.
[10] BOAZ N W,MACKENZIE E B,DEBENHAM S D,et al.Synthesis and Application of Phosphinoferrocenylaminophosphine Ligands for Asymmetric Catalysis[J].The Journal of Organic Chemistry,2005,70(5):1872~1880.
[11] JIA XIAN,LAM W S,KOK S H L,et al.The Synthesis of New Chiral Phosphine-phosphinites,Phosphine-phosphoramidite, and Phosphine-phosphite Ligands and Their Applications in Asymmetric Hydrogenation[J].Tetrahedron:Asymmetry,2004, 15(14):2273~2278.
[12] PETER H,STEFAN S.Preparation of(R)-2-Alkyl-3-Phenylpropionic Acids:WO,0202500(A1)[P].2003-04-20.
[13] AUDI FONG S.-W.,ANDY HOR T S.Clusters and Aggregates of 1,1′-Bis(diphenylphosphino)ferrocene(Dppf)[J].Journal of Cluster Science,1998,9(4):351~392.
[14] BURCKHARDT U,DROMMI D,TOGNI A.Synthesis,Structure,and Reactivity of New Chiral Ferrocenyl Pyrazole Ligands[J].Inorganica Chimica Acta,1999,296(1):183~194.
[15] MANFRED T R,ECKART W B,RICHARD G,et al.A New Class of Chiral Diphoshines Having Planar Chirality[J].Tetrahedron Letters,1999,40(27):4977~4980.
[16] REETZ M T,GOSBERG A,GODDARD R,et al.Diphosphonites as Highly Efficient Ligands for Enantioselective Rhodium-catalyzed Hydrogenation[J].Chemical Communications,1998(19): 2077~2078.
[17] LOTZ M,PEREA J J A,KNOCHEL P.Synthesis and Application of C2-Symmetric Diamino FERRIPHOS as Ligands for Enantioselective Rh-catalyzed Preparation of Chiral α-Amino Acids[J].Tetrahedron:Asymmetry,1999,10(2):375~384.
[18] KANG J,LEE J H,AHN S H,et al.Asymmetric Synthesis of A New Cylindrically Chiral and Air-stable Ferrocenyldiphosphine and Its Application to Rhodium-catalyzed Asymmetric Hydrogenation[J].Tetrahedron Letters,1998,39(31):5523~5526.
[19] HAYASHI T,YAMAMOTO K,KUMADA M.Asymmetric Catalytic Hydrosilylation of Ketones Preparation of Chiral Ferrocenylphosphines as Chiral Ligands[J].Tetrahedron Letters,1974,15(49~50):4405~4408.
[20] ZHAO Q,LI S,HUANG K,et al.A Novel Chiral Bisphosphine-Thiourea Ligand for Asymmetric Hydrogenation of β,β-Disubstituted Nitroalkenes[J].Organic Letters,2013,15(15):4014~4017.
[21] HAYASHI T,MISE T,MITACHI S,et al.Asymmetric Hydrogenation Catalyzed by a Chiral Ferrocenylphosphine-rhodium Complex[J].Tetrahedron Letters,1976,17(14):1133~1134.
[22] HAYASHI T,KANEHIRA K,KUMADA M.Asymmetric Hydrogenation of Enol Phosphinates Catalyzed by a Chiral Ferrocenylphosphine-rhodium Complex Asymmetric Synthesis of Optically Active Secondary Alkyl Alcohols[J].Tetrahedron Letters,1981, 22(44):4417~4420.
[23] 赵双琪,杨定乔.手性膦配体的兴起与进展[J].广州化工, 2005,33(3):43~46.
[24] WIDHALM M,NETTEKOVEN U,PIET W N M.Novel P-chiral Bidentate Phosphine Lligands:Synthesis and Use in Asymmetric Catalysis[J].Tetrahedron:Asymmetry,1997,8(19):3185.
[25] ZHANG WANBIN,KIDA T,NAKATSUJI Y,et al.Novel C2-symmetric Diphosphine Ligand with Only the Planar Chirality of Ferrocene[J].Tetrahedron Letters,1996,37(44):7995~7998.
[26] BERENS U,BURK M J,GERLACH A.Chiral 1,1′-Diphosphetanylferrocenes:New Ligands for Asymmetric Catalytic Hydrogenation of Itaconate Derivatives[J].Angewandte Chemie International Edition,2000,39(11):1981~1984.
[27] WIDHALM M,NETTEKOVEN U,LUTZ M,et al.Steric and Electronic Ligand Perturbations in Catalysis:Asymmetric Allylic Substitution Reactions Using C2-Symmetrical Phosphorus-Chiral(Bi)ferrocenyl Donors[J].The Journal of Organic Chemistry, 2001,66(3):759~770.
[28] BARBARO P,BIANCHINI C,GIAMBASTIANI G,et al.Progress in Stereoselective Catalysis by Metal Complexes with Chiral Ferrocenyl Phosphines[J].Coordination Chemistry Reviews,2004, 248(21~24):2131~2150.
[29] 陈卫平,张生勇,姚伟.一种手性二茂铁双膦配体及其制备方法:CN,103804431A[P],2014-05-21.
中国胶黏剂和胶黏带工业协会2017年主要活动安排
Research Progress in Chiral Ferrocenyl Diphosphine Ligand
The chiral ferrocenyl diphosphine ligand was very excellent in asymmetric synthesis.The high asymmetric catalytic activity was obtained by the combination of ligands and organometallic.In this paper,a few chiral ferrocenyl diphosphine ligand and the enantioselective of certain prochiral substrate were enumerated.
Chiral;ferrocene;disphosphine;asymmetric catalytic;enantioselective

2017年3月28-30日 常州 2017年中国热熔胶专业高峰论坛2017年4月24-26日 无锡 第五届工程用胶技术与信息交流会2017年6月13-15日 宜兴 第六届全国丙烯酸(酯)市场与应用高峰论坛2017年8月20-22日 上海 第二十届中国胶黏剂和胶粘带行业年会2017年8月23-25日 上海 第二十届中国国际胶黏剂及密封剂展览会2017年10月16-18日 黄山 第六届建筑胶黏剂专业技术与信息研讨会2017年11月6-8日 常州 第二届中国不干胶标签高峰论坛2017年12月19-22日 宁波 第五届胶黏剂基础知识与粘接技术培训班
TQ426.99
A
1001-0017(2017)02-0140-04
YU Zhen,YANG Jie,ZHANG Xue and CAO Long-hai
(Institute of Petrochemistry,Heilongjiang Academy of Sciences,Harbin 150040,China)
2016-12-07
于振(1986-),男,黑龙江哈尔滨人,助理研究员,主要研究方向为有机合成。
