二氧化钛光催化剂及其在环境中的应用研究进展
2017-05-18李淑辉张广鑫赵毅磊王洁莹孙东洲
张 智,张 娟,李淑辉,张广鑫,赵毅磊,王洁莹,孙东洲*
(1.黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 高技术研究院,黑龙江 哈尔滨 150020)
二氧化钛光催化剂及其在环境中的应用研究进展
张 智1,2,张 娟1,2,李淑辉1,张广鑫2,赵毅磊1,王洁莹1,孙东洲1,2*
(1.黑龙江省科学院 石油化学研究院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 高技术研究院,黑龙江 哈尔滨 150020)
二氧化钛光催化技术具有低耗能、操作简单、无毒性、降解无选择性、能够彻底降解有机污染物的特点,且因二氧化钛无二次污染并可回收循环利用而备受青睐。介绍了二氧化钛的结构、性能、光催化机理及几种提高二氧化钛光催化性能的改性方法。阐述了二氧化钛在净化空气、污水处理等环境保护领域中的应用和在应用中尚存的一些问题。对二氧化钛在环境领域中的应用前景进行了展望。
二氧化钛;光催化;环境;应用
前言
自20世纪70年代初Fujishima和Honda[1]发现TiO2在光照条件下具有分解水中有机物的功能以来,其在能源、半导体材料、光催化材料、陶瓷工业等领域被广泛应用。TiO2具有反应条件温和,无毒,无二次污染等优点,且能够降解难降解的有机污染物[2],在处理水污染等其他环境污染方面比传统的工艺有明显的优势。TiO2也可以循环利用,极大降低了成本。所以TiO2成为处理环境污染问题中的新兴材料,对环境保护有重要的意义。本文综述了TiO2机理,TiO2光催化性能的改性方法以及在环境领域中的应用研究。
1 半导体TiO2
1.1 TiO2的结构和性能
TiO2有三种晶体结构即锐钛矿、金红石及少量的板钛矿。当TiO2的晶体结构为锐钛矿时,其钛原子在整个几何结构八面体中心位置,其余的六个氧原子分别位于各个八面体的棱角,几何空间结构疏松。金红石晶型的TiO2中氧离子作为6方最紧密堆积。因此锐钛矿晶型的TiO2缺陷程度较大,易捕捉氧[3]。实验室比较容易制得的是经高温焙烧得到催化活性较高的锐钛矿晶型的TiO2。当焙烧温度过高,TiO2将发生相转变,得到锐钛矿的TiO2和金红石TiO2的混合相,且金红石晶型的TiO2存在的含量比在较低温度焙烧后的金红石晶型的TiO2的含量相对较高。由于锐钛矿和金红石两种晶体的空间几何结构不同,使得两种晶型的光催化性能有所差异,在应用方面也各有所长。金红石型TiO2晶体构造比锐钛矿型TiO2的晶体构造更紧密和稳定,折射率高,散射能力强,因此金红石型的TiO2常作为防晒剂。而锐钛矿的TiO2常作为光催化剂,这是由于金红石型的TiO2的比表面积小,晶格中的表面缺陷少,捕捉氧的能力低,容易发生空穴复合,光催化活性能力较弱。而锐钛矿晶型由于表面缺陷和位错多,比表面积相对较大,因此有较多氧空位来捕获电子,光催化活性较高[4~7]。
1.2 TiO2光催化机理
TiO2是n型半导体纳米粒子,由于TiO2的几何的空间结构,TiO2能带不能连续。TiO2的禁带宽度为3.2eV,半导体吸收能量被激发产生光生电子(e-)空穴(h+)对。由于有电场的存在,因此激发态的电子和空穴极易被束缚,重新合并以新的热量及其他方式散发,如图1所示。

图1 TiO2光催化机理Fig.1 Photocatalytic mechanism of TiO2
具体的反应如下:电子和空穴在库仑力的作用下迁移到粒子表面,当催化剂存在合适的表面缺陷时,在电子和空穴重新合并之前,就会与催化剂表面上所吸附的物质发生一系列氧化还原反应。这是由于电子具有强的还原作用,空穴具有很强的氧化作用。由于空穴具有很强的反应活性,在半导体中,催化剂表面所吸附的水分子和氢氧根离子发生一系列氧化还原反应,生成具有强氧化性的羟基自由基(·OH),具体反应如下[8~13]:
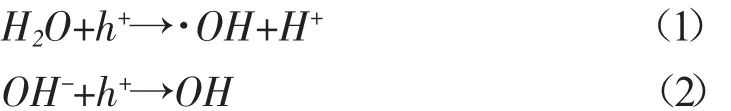
表面吸附的氧分子和溶液中的氧分子与电子发生反应,也是生成氧化能力极强的·OH的来源:
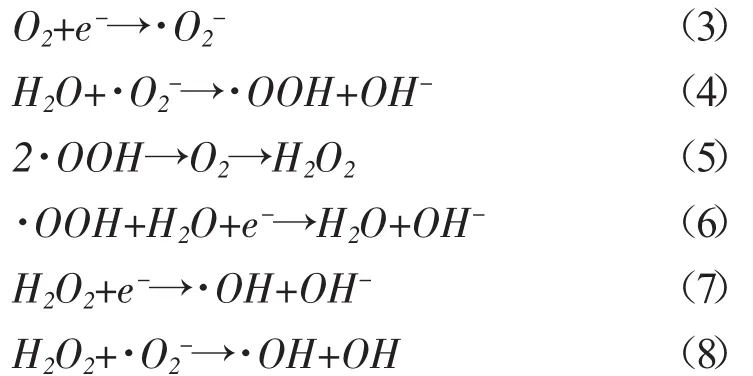
·OH自由基和·OOH自由基的氧化能力极强,可以彻底地降解有机物,使有机物彻底分解成CO2和H2O等无机物,对环境无二次污染。
TiO2光催化活性取决于TiO2的晶型结构,当TiO2的晶型结构为锐钛矿时,光催化性能相对较高,当TiO2的晶型结构为金红石时,光催化性能相对较低[14]。因此在制备经高温焙烧的TiO2过程中保持TiO2的晶型结构至关重要。当焙烧TiO2的温度在500℃时,TiO2的晶型结构为锐钛矿。当焙烧TiO2的温度为600℃时,TiO2开始发生相转变,此时TiO2的晶型结构为锐钛矿和金红石混合晶型且金红石相的TiO2的含量相对较多。当温度在700℃时,TiO2的晶型结构为金红石,因此实验焙烧一般在 500~600℃。TiO2光催化活性也与粒径大小有关,粒径小TiO2的光催化活性相对较高。
2 TiO2的改性
2.1 离子掺杂
适当的离子掺杂可以拓宽TiO2对可见光的吸收范围,并增加吸收强度,是目前可见光化研究中最为广泛的一种方法。掺杂光催化剂TiO2的离子一般包括过渡金属离子、稀土金属离子、贵金属离子和其他无机离子。由于掺杂引起能级位错变化,能很好地提高掺杂TiO2催化剂在可见光下的催化活性。目前研究者已经研究了将Fe(Ⅲ)掺杂到TiO2纳米晶中。纳米颗粒经500℃退火处理后,样品结构是锐钛矿结构,无杂相且粒径较小,从而使TiO2的光催化活性提高[15]。
吴奇[16]等用电化学阳极氧化法结合浸渍和退火后处理制备了Fe和N共掺杂的TiO2纳米管阵列光催化剂,表征结果表明,Fe、N共掺杂对TiO2纳米管阵列的形貌和结构影响不大,Fe和N均掺入了TiO2晶格中。紫外-可见(UV-Vis)漫反射光谱显示Fe和N共掺杂TiO2纳米管阵列的吸收带边较纯TiO2纳米管阵列和单一掺杂TiO2纳米管阵列可见光吸收增强。考察了降解罗丹明B(RhB)的光催化活性,Fe和N共掺杂TiO2纳米管阵列对RhB的降解速率较纯TiO2纳米管阵列和单一掺杂TiO2纳米管阵列明显提高,证明了Fe、N共掺杂具有协同效应。
Shamshi[17]等认为,稀土元素的f轨道能与被降解底物发生配位反应,从而提高TiO2的光催化活性。水淼等认为,稀土离子和Ti(Ⅳ)离子半径相差较大,若取代晶格Ti(Ⅳ)则引起TiO2晶格畸变、膨胀,有助于光生空穴-电子的分离,因而纳米TiO2掺杂适量La可提高其光催化活性。
2.2 表面光敏化
光敏化是通过添加适当的光活性敏化剂,使其吸附于TiO2表面,扩大了TiO2激发波长的范围,使之能充分利用可见光,是提高TiO2对可见光的利用的最有效的途径之一[18]。Lin[19]等认为PANI修饰后的TiO2在紫外光和可见光(420nm<λ<800nm)下,比单纯的TiO2和掺杂N后的TiO2的光催化活性和稳定更高。尤其在更长的波长(550nm<λ<800nm)下对甲基橙和对氯苯酚的催化强度更强。Wang[20]等认为铟离子掺杂到TiO2晶格中,形成了一种独特的化学物质O-In-Clx,存在于铟离子掺杂后的TiO2的表面。其禁带宽度为0.3eV,大大低于单纯的TiO2的禁带宽度。由于TiO2对可见光的利用与TiO2的禁带宽度有关,因此其光催化活性比单纯的TiO2的光催化活性高。
徐志兵[21]等,采用溶胶-凝胶法和水热法制备了Ag/TiO2催化剂,将其在叶绿素提取液中浸泡24 h,制成光敏化Ag/TiO2催化剂。以Cr6+溶液为研究对象,分别在紫外光和可见光下考察了纳米TiO2、纳米Ag/TiO2、光敏化TiO2和光敏化Ag/TiO2催化剂的光催化性能。结果表明,在四种催化剂相中,光敏化Ag/TiO2催化剂的性能最好,特别是在可见光下,光敏化Ag/TiO2催化剂光催化还原Cr6+,150min后脱除率达到100.0%。
杜雪岩[22]等采用曙红与叶绿素铜三钠对TiO2纳米颗粒进行了光敏化,研究了TiO2纳米颗粒在节能灯光源下的光催化活性。结果表明:光敏化可以保持TiO2的锐钛矿结构,对其形貌无明显影响。光敏化后的TiO2纳米颗粒在可见光区吸光程度有较大提高,两种光敏剂的协同作用可使光谱的响应波长向可见光方向移动,拓展了TiO2光谱响应范围。光催化降解实验表明:光敏化TiO2纳米颗粒具有优良的光催化性能,且在30℃,光敏化8h,曙红质量浓度30mg/L及叶绿素铜三钠质量浓度20mg/L时,光敏化的TiO2光催化效果最好,用节能灯作光源对甲基橙的降解率为61.33%。
2.3 分子筛负载
TiO2负载在分子筛上,由于分子筛特殊的结构,使其分布在分子筛表面和进入到分子筛孔径中去。Ugurlu[23]等认为海泡石具有纤维孔洞形状的含水硅酸镁,其在工业上的应用优势在于其多孔性结构和大的比表面积。TiO2负载在海泡石上增加其利用率,因此在同等用量上的TiO2其光催化活性更强。同时研究者也将TiO2负载在沸石上。这是由于沸石的特殊结构可以起到抑制电子—空穴复合的作用,使得沸石吸附的有机物可以很容易地获得活性基团,从而提高沸石负载TiO2光催化剂的活性。另一方面是当半导体表面和分子筛接触时,载流子能重新分布,光电子就从费米能级较高的n型半导体(即TiO2)转移到费米能级较低的分子筛上,重合形成统一的费米能级,从而形成肖特基势垒(Schottkybarrier)。即在TiO2半导体表面的分子筛中形成了电子捕获阱,促进了光生电子与空穴的分离,延长了空穴的寿命,从而提高了分子筛负载TiO2催化剂的光催化活性[24]。
韩阳[25]以在碱性水热条件下所制备的MCM-41分子筛作载体、用絮凝法制备TiO2/MCM-41分子筛,用同样方法制备了TiO2/ZSM-5/MCM-41分子筛,TiO2料子在两种分子筛上分散较均匀,两种样品均含有锐钛矿TiO2结构和部分金红石TiO2结构;其孔容积和比表面积均较原载体有所减小;用其光催化降解罗丹明B溶液,结果表明,负载率为40%,在500℃下焙烧4h,两种分子筛的光催化效果较好。催化剂加入0.04g时对罗丹明B溶液的光催化效果最佳,脱色率均达99%以上。
李慧芳[26]采用溶胶凝胶法制备了纯纳米TiO2及不同比例Zn、Cu、La离子单掺杂,La-Zn共掺杂的纳米TiO2光催化剂。用溶胶浸渍法制备了MCM-41分子筛负载纯纳米TiO2及La-Zn共掺杂纳米TiO2的复合光催化剂,并用其在紫外光下对甲基橙溶液和甲醛气体进行降解。用干燥器法测定了3A、5A、13X、MCM-41分子筛对甲醛的静态吸附量。结果表明:MCM-41介孔分子筛对甲醛的吸附性能最好,说明比表面积和孔径大有利于吸附甲醛气体。将MCM-41分子筛与纯纳米TiO2及0.05%Zn+0.1% La/TiO2的溶胶分别进行不同比例的浸渍负载,发现用分子筛负载能够抑制纳米TiO2的粒径生长,且粒径大小随负载量的增加而增大,复合材料的孔容和孔道直径都随负载量的增加而减小。
3 纳米TiO2光催化剂的应用
3.1 TiO2光催化剂在气体净化中的应用
近年来,空气中有害物质的去除引起了人们的关注。由于大部分空气污染物(如醛、酮、醇等)是可氧化的,因此用氧化法去除是可行的。去除空气中污染物常用的多相催化氧化法大都需要在较高温度下进行,而光催化能在室温下利用空气中的水蒸气和O2去除空气污染物。利用TiO2光催化剂在光照条件下可将空气中的有机物分解为CO2、H2O及相应的有机酸[27]。目前,国内外学者对烯烃、醇、酮、醛、芳香族化合物、有机酸、胺、有机复合物、三氯乙烯等气态有机物的TiO2光催化降解进行了研究,其量子效率(反应速率/入射光密度)是降解水溶液中同样有机物的10倍以上[28~29]。另外,在TiO2光催化反应中,一些芳香族化合物的光催化降解过程往往伴随着各种中间产物的生成,有些中间产物具有相当大的毒性,从而使芳香族化合物不适于液相光催化反应过程,如水的净化处理。但在气相光催化反应中,只要生成的中间产物挥发性不大,就不会从TiO2表面脱离进入气相,造成新的污染,而是进一步氧化分解,最终生成CO2和H2O。
3.2 TiO2光催化剂在污水净化中的应用
光催化反应的强氧化性能是其在水污染控制方面的技术优势所在。
3.2.1 废水处理
含卤衍生物如有机氯化物是水中最主要的一类污染物,毒性大,分布广,其治理是水污染处理的一个重要课题。光催化过程在处理有机氯化物方面显示出了较好的应用前景,目前关于这方面的研究已有许多报道,研究认为卤代烃、卤代脂肪酸等均可完全降解,氯酚、氯苯等经过一系列中间产物生成CO2和HCl[30]。印染废水进入水体会造成严重的环境污染,其中有的还含有苯环、胺基、偶氮基团等致癌物质。宋波[31]采用溶胶-凝胶和水热合成两种方法分别制备Fe元素和N元素掺杂改性的TiO2光催化剂,结果表明,样品在紫外光和太阳光下降解印染废水中目标降解物亚甲基蓝效率均能达到95%。
农药废水中含有机磷农药,三氯苯氧乙酸,DDVP,DTHP,DDT,三氮硝基甲烷等,毒性大,难降解,易生物积累。利用TiO2光催化去除农药虽然不能使所有的污染物最终达到完全矿化,但不会产生毒性更高的中间产物,这是其他方法无法相比的。孙宏伟[32]采用阳极氧化法制备TiO2纳米管薄膜光催化剂,并用Au-Pd对其进行共修饰,以有机磷农药马拉硫磷为探针考察Au-Pd沉积对光催化剂活性的影响。光催化实验结果表明,Au-Pd共修饰TiO2纳米管膜(Au-Pd-TiO2)光催化活性明显高于未经修饰的TiO2纳米管,反应速率常数提高1.72倍,单位级数能耗显著降低。
3.2.2 饮用水处理
目前地面水普遍受到污染,而常规的给水技术难以达到去除溶解性有机物的效果,由此造成饮用水中总是存在一定量的有机污染物。据报道,世界范围内饮用水中,已出现765种有机化合物,其中117种是属于致癌的或与致癌有关的物质。研究表明,TiO2光催化对这些微量有机污染物以及消毒副产物的前体物质如腐殖酸、酚类等的去除都有着显著的效果[33]。研究者用溶胶—凝胶法研制的TiO2光催化反应装置成功地去除了水中挥发性有机物,而且可以完全将其矿化成为H2O,CO2。最近研究者用合成的具有层状结构的TiO2纤维作为光催化剂,在O3/TiO2/UV体系处理含有腐殖质的饮用水,1h后腐殖质去除率达97.1%。染料废水、农药废水、表面活性剂、氟里昂、含油废水等都可以被纳米TiO2氧化降解。
3.3 灭活细菌
TiO2在光照下对环境中的微生物具有抑制或杀灭作用,从而达到抗菌效果。在人们的居住环境中存在着各种有害微生物,对人类生活产生不良影响。家居环境中的一些潮湿的场合如厨房、卫生间等,微生物容易繁殖,导致空气菌浓度和物品表面菌浓度增大,对人的健康产生威胁。利用纳米TiO2的光催化性可充分抑制或杀灭环境中的有害微生物,降低环境微生物对人的危害[34~35]。
3.4 除臭
空气中恶臭气体主要有五种:①含硫化合物,如硫化氢、二氧化硫、硫醇类、硫醚类等;②含氮化合物,如胺类、酰胺等;③卤素及其衍生物,如氯气、卤代烃等;④烃类,如烷烃、烯烃、炔烃、芳香烃等;⑤含氧的有机物,如醇、酚醛、酮、有机酸等。以前普遍采用活性炭去除这些臭气,随着气体在活性炭表面的富集,其吸附能力明显降低,使其应用受到限制。而TiO2光催化剂吸附这些气体,经紫外光照射气体分解后,又可恢复其新鲜表面,消除了吸附限制。近年来,采用TiO2光催化剂和气体吸附剂(沸石、活性炭、SiO2、Al2O3等)组成的混合型除臭吸附剂已得到实际应用。气体吸附剂吸附的臭气经表面扩散与TiO2光催化剂接触后,就会被氧化分解,既不会降低吸附剂的吸附活性,又解决了TiO2光催化剂对臭气吸附性较弱的特点,大大提高了臭气的光降解效率。
3.5 提供有效储氢方式
物理和化学方法储氢需要昂贵的设备,而TiO2纳米管可以提供一种有效而清洁的储氢方式[36]。用TiO2纳米管来制造燃料电池汽车中的氢容器,可有效避免空气污染或排放温室气体。
4 展望
光催化氧化技术具有高效、节能、清洁无毒等突出优点,是一项具有广泛应用前景的新型水污染处理技术。然而作为近30年发展起来的新的研究领域,光催化降解现在还基本上停留在实验室水平,实际应用很少。因此无论是在光催化机理的研究方面,还是在工业实际应用中都需要进一步的深入研究。以下为亟待解决的几个问题:(1)在处理污水过程中的回收问题;(2)制备出高热稳定性的TiO2;(3)光催化技术与其他技术耦合,利用技术的协同作用来获取最佳的处理效果。随着科学技术的发展,相信TiO2光催化技术会有更加广阔的应用前景。
[1] FUJISHIMA A,HONDA K.Electrochemical photolysis of water at asemiconductor electrode[J].Nature,1972,5358(238):37~38.
[2] LI F F,JIANG Y S,XIA M S,et al.Effect of the P/Ti ratio on the visible-light photocatalytic activity of P-doped TiO2[J].Journal of Physical Chemistry,2009,113:18143~18144.
[3] 刘立华,王璐,张勇,等.溶胶凝胶法制备Ti1-xFexO2纳米颗粒及磁性能研究[J].光散射学报,2011,23(1):42~44.
[4] LIU S W,YU J G,MIETEK JARONIEC.Anatase TiO2with dominant high-energy{001}facets:synthesis,properties,and applications[J].Chemistry of Materials,2011,23(18):4085~4093.
[5] PILLAI S C,PERIYAT P,GEORGE R,et al.Synthesis of hightemperature stable anatase TiO2photocatalyst[J].Journal of Physical Chemistry C,2007,11(4):1605~1611.
[6] CHANG S M,HOU C Y,LO P H,et al.Preparation of phosphated Zrdoped TiO2exhibiting high photocatalytic activity through calcination of ligand-capped nanocrystals[J].Applied Catalysis B, 2009,90:233.
[7] PERIYAT P,MCCORMACK D E,Hinder S J,et al.One-pot synthesis of anionic(nitrogen)and cationic(sulfur)codoped hightemperature stable,visible light active,anatase photocatalysts[J].Journal of Physical Chemistry C,2009,113(8):3246~3253.
[8] FUJISHIMA A,ZHANG X,TRYK D A.TiO2photocaltalysis and related surface phenomenon[J].Surface Science Spectra,2008,63(12):515~582.
[9] MIGUEL PELAEZ,NICHOLAS T,NOLAN,SURESH C.Pillai,et al.A review on the visible light active titanium dioxide photocatalysts for environmental applications[J].Applied Catalysis B:Environmental,2012,125:331~349.
[10] MO J H,ZHANG Y P,XU Q J,et al.Photocatalytic purification of volatile organic compounds in indoor air:A literature review[J].Atmospheric Environment,2009,43:2229~2246.
[11] 盛国栋,李家星,王所伟,等.提高TiO2可见光催化性能的改性方法[J].化学进展,2009,21(12):2492~2503.
[12] LU S Y,WU D,WANG Q L,et al.Photocatalytic decomposition on nano-TiO2:Destruction of chloroaromatic compounds[J].Chemosphere,2011,82:1215~1224.
[13] WU Y M,XING M Y,ZHANG J L.Gel-hydrothermal synthesis of carbon and boron CO-doped TiO2and evaluating its photocatalytic activity[J].Journal of Hazardous materials,2011,192:368~373.
[14] LI W,BAI Y,LIU C,et al.Highly thermal stable and highly crystalline anatase TiO2for photocatalysis[J].Environmetal Science Technoledge,2009,43:5423~5428.
[15] NURAZIMAH,AHMADZUHAIRIABDULAH.Reactivedyedegradation by combined Fe(III)/TiO2catalyst and ultrasonic irradiation:effect of Fe(III)loading and calcination temperature[J].Ultrasonics Sonochemistry,2011,18(2):669~678.
[16] 吴奇,苏钰丰,孙岚,等Fe、N共掺杂TiO2纳米管阵列的制备及可见光光催化活性[J].物理化学学报,2012,3:635~640.
[17] SHAMSHI HASSAN M,AMMA TOUSEEF,YANG O-BONG.TiO2nanofibersdoped with rareearthelements and their photocatalyticactivity[J].Ceramicsl International,2012,38(7):5925~5930.
[18] 张伟.TiO2光敏化研究进展[J].广东化工,2009,11:94~97.
[19] LIN Y M,LI D Z,HU J H,et al.Highly efficient photocatalytic degradation of organic pollutants by PANI-modified TiO2composite[J].Journal of Physical Chemistry C,2012,116:5764~5772.
[20] WANGEJ,YANGWS,CAOYA.Uniquesurfacechemicalspecies on indium doped TiO2and their effect on the vsible light photocatalytic activity[J].Journal of Physical Chemistry C,2009,113:20912~20917.
[21] 徐志兵,严家平,钮志远,等.光敏化Ag/TiO2催化剂的制备及其催化性能[J].石油化工,2013,3:330~333.
[22] 杜雪岩,王峭,续京,等.曙红,叶绿素铜三钠共敏化TiO2纳米颗粒的光催化性能[J].材料导报,2014,2:46~50.
[23] UGURLU M,KARAOGLU M H.TiO2supported on sepiolite: Preparation,structural and thermal characterization[J].Chemical Engineering Journal,2011,166:859~867.
[24] MASATO TAKEACHI,JUNICHI DEGUCHI,MANABA HIDAKA,et al.Enhancement of the photocatalyticreactivity of TiO2nanoparticles by asimplemechanicalblending with hydrophobicmordenite(MOR)zeolite[J].Applied Catalysis B:Environmental,2009,89(3~4):406~410.
[25] 韩阳.MCM-41分子筛和ZSM-5/MCM-41复合分子筛的合成与表征及其作为TiO2光催化剂载体的研究[D].燕山大学,2014.
[26] 李慧芳.分子筛负载改性纳米TiO2的制备及光催化活性研究[D].中南大学,2014.
[27] ZHANG LEXIN,HAGHIGHAT FARIBORZ,BLONDEAU PARTICE,et al.Modeling and physical interpretation of photocatalytic oxidation efficiency in indoor air applications[J].Building and Environment,2010,45(12):2689~2697.
[28] WANG S B,ANG H M,MOSES O.TADE.Volatile organic compounds in indoor environment and photocatalytic oxidation:State of the art[J].Environment International,2007,33(5):694~705.
[29] JIN M,ZHANG X T,Pu H T,et al.Photochromism-based detection of volatile organic compounds by W-doped TiO2nanofibers[J].Joural of Colloid and Interface Science,2011,362(1):188~193.
[30] CHONG M N,JIN B,CHRIS SAINT,et al.Recent developments in photocatalytic water treatmenttechnology:A review[J].Water Research.,2010,44:2997~3027.
[31] 宋波.改性纳米TiO2光催化剂的制备及其处理印染废水的试验研究[D].哈尔滨工程大学,2013.[32] 孙宏伟.纳米薄膜光催化剂的制备及光催化降解农药产物或其中间体的电化学检测研究[D].东北师范大学,2013.
[33] ZHAO J H.Research on UV/TiO2photocatalytic oxidation of organic matter in drinking water and its influencing factors[J].Procedia Environmental Sciences,2012,12:445~452.
[34] MA M Y,WANG X H,WANG X H,et al.Inactivated properties of activated carbon-supported TiO2nanoparticles for bacteria and kinetic study[J].Joural of Envionmental Science,2008,20(12): 1527~1533.
[35] PAL AMRITA,PEHKONEN SIMO,YU LIYA E,et al.Photocatalytic inactivation of Gram-positive and Gram-negative bacteria using fluorescent light[J].Journal of Photochemistry and PhotobiologyA:Chemistry,2007,186(2~30):335~341.
[36] 杨维虎,奚兴凤,方佳佳,等.二氧化钛纳米管储氢能力的分子动力学研究[J].化学研究与用,2012,24(2):309~313.
Research Progress of TiO2Photocatalyst and Its Application in Environment
ZHANG Zhi1,2,ZHANG Juan1,2,LI Shu-hui1,ZHANG Guang-xin2,ZHAO Yi-lei1,WANG Jie-ying1and SUN Dong-zhou1,2
(1.Institute of Petrochemistry,Heilongjiang Academy of Sciences,Harbin 150040,China;2.Institute of Advanced Technology,Heilongjiang Academy of Sciences,Harbin 150020,China)
The photocatalytic oxidation of TiO2has been paid more and more attention for the advantages of low-energy consumption,simple operation,non-toxic,non-selective reaction conditions,the complete degradation of organic pollutants,no secondary pollution,and recycling.The structure,property,photocatalytic mechanism of TiO2and several modification methods for improving TiO2photocatalytic properties were reviewed in this paper.The applications in air purification,waste water treatment,and other fields of environmental protection and the existing problems in these applications were introduced.At last,the application prospects of TiO2in environment were showed.
TiO2;photocatalytic;environment;application
TQ433.438
A
1001-0017(2017)02-0135-05
2016-12-30
张智(1971-),女,黑龙江哈尔滨人,副研究员,从事催化剂方面的研究。
*通讯联系人:孙东洲(1970-),男,副研究员,研究方向为高分子材料。E-mail:sundongzhou22@163.com。
