酮洛芬缓释微球的制备及其性能研究*
2017-05-18王小宁董雯丹张存劳
王小宁,董雯丹,张存劳
(西安医学院 药学院,陕西 西安 710021)
酮洛芬缓释微球的制备及其性能研究*
王小宁,董雯丹,张存劳
(西安医学院 药学院,陕西 西安 710021)
制备酮洛芬缓释微球并对其性能进行研究。采用乳化交联法制备微球,正交试验优化微球的工艺处方,对微球从形态、粒径分布、DSC方面进行表征;用透析法进行体外释药实验,并对释药曲线进行拟合。结果表明,微球的最优工艺处方为壳聚糖浓度为2%,搅拌速度为1000r/min,乳化温度30℃,交联剂用量2.5%。制得的微球平均粒径为(1.42±0.24)μm,包封率为(82.2±2.2)%,DSC分析表明药物以非结晶形式分散于微球骨架中,体外释药曲线符合Higuchi方程,与市售缓释制剂相比,微球显示了较好的缓释特性,值得进一步研究。
酮洛芬;微球;缓释;壳聚糖
前言
酮洛芬(Ketoprofen)属苯丙酸类非甾体抗炎药,临床主要用于治疗各种关节炎、术后疼痛及慢性癌痛等。然而,酮洛芬普通口服制剂存在生物半衰期短(1.6~1.9h)、有效血药浓度维持时间短等缺点,临床应用时需频繁给药(3~4/d),对胃肠道又具有刺激性,长期服用会导致消化道溃疡、出血等症状[1~2]。目前国内生产的酮洛芬制剂主要为普通片剂和肠溶胶囊,一日服药数次,患者顺应性不好,而且会对治疗效果和安全性造成影响,影响其临床应用前景,因此开展酮洛芬缓释制剂的研究具有重要意义。
微球(microspheres)是一种将药物分散或包埋在多聚物中,形成粒径为1~300μm的球状载体给药系统。微球除可实现药物的靶向给药外,还可控制释药,降低药物毒副作用,提高药物稳定性等[3]。常用的药物载体材料中合成高分子载体通常生物相容性差,有时还含有痕量引发剂等毒性杂质,而天然高分子由于安全无毒、可生物降解、生物相容性好而备受关注。壳聚糖是天然存在的惟一碱性多糖高分子材料,组织相容性好,毒副作用小。壳聚糖作为药物载体制备微球可以控制药物释放、延长药物疗效、降低药物毒副作用,并且可以降低药物对胃肠道的刺激性[4]。因此,自20世纪90年代以来,壳聚糖微球载体在药物缓释给药载体中的研究已成为热点[5~6]。
本论文的目的在于制备酮洛芬壳聚糖缓释微球,对微球的制备工艺、微球性能及体外释药过程进行研究,以解决酮洛芬生物利用低、毒副作用大的问题,为酮洛芬缓释制剂的研究提供理论基础。
1 实验部分
1.1 主要原料与试剂
酮洛芬原料药(医药级,湖北拓楚慷元医药化工有限公司),壳聚糖(相对分子质量507 kD,济南海得贝海洋生物工程有限公司),甲醇为色谱纯,司盘80、冰醋酸、液体石蜡、戊二醛、石油醚等均为分析纯。
1.2 仪器与设备
双头磁力加热搅拌器(HJ-2,北京九州空间科技有限公司),电子天平(ALC-210.4型,北京赛多利斯科技仪器有限公司),动态光散射激光粒度仪(ZEN3600型,Malvern),差示扫描量热仪(DSC1,梅特勒-托利多),高效液相色谱仪(Agilent1260型,美国安捷伦公司)。
1.3 酮洛芬微球的制备
1.3.1 微球的制备方法
采用乳化交联法制备微球[7]。用3%的冰醋酸溶液溶解壳聚糖,配置成一定浓度的壳聚糖溶液。将一定量的司盘80加入液体石蜡中,搅拌均匀后将备用的壳聚糖溶液缓慢加入其中,以一定搅拌速度恒温搅拌,以使体系乳化。在乳化体系中加入一定量的交联剂戊二醛,在常温下搅拌1h,交联反应结束后,静置30min待完全分层后除去上清液,下层物质分别用石油醚和异丙醇洗涤三次,然后在50℃下烘干,即得微球。
1.3.2 微球包封率和载药量的测定
精密称取微球10mg置于10mL容量瓶中,用混合溶剂适量使溶解,0.45μm微孔滤膜过滤后,取滤液用高效液相色谱法测定含量。根据下式计算包封率和载药量:载药量=(微球中药物的含量/微球的质量)×100%,包封率=(微球中药物的含量/所投药物的总量)×100%。
1.3.3 正交试验

表1 因素及水平Table 1 Factors and levels
以对微球包封率影响显著的4个因素:壳聚糖浓度(A)、搅拌速度(B)、乳化温度(C)、交联剂用量(D)作为考察因素,以包封率为指标,采用四因素三水平L9(34)正交表进行正交试验,因素水平表见表1。
1.4 微球的表征
用光学显微镜观察微球形态,动态光散射法(Dynamic Light Scattering,DLS)测定粒径分布,差示扫描量热法考察微球分散状态。
1.5 酮洛芬微球的体外释药
采用透析法测定微球的体外释药特性[8]。精密称取3份微球10mg(约含酮洛芬2mg),加入pH值为(6.8±0.05)的磷酸盐缓冲液5mL,置于透析袋中;将上述装有样品的透析袋置于含有60mL溶出介质的具塞三角瓶中,在(37±0.5)℃的恒温摇床中以75r/min速度振荡,分别于0.5,1,2,4,6,8,10,12,24,36,48h时从透析袋外释放介质中取样,取样量为3mL,并立即补加等量释放介质。用HPLC法测定释放的药量,计算累积释放度。
2 结果与讨论
2.1 酮洛芬含量的测定
色谱条件:AgilentHC-C18(2)(4.6×150mm,5μm),流动相:甲醇-0.05mol/L磷酸二氢钾(55∶45),柱温25℃,检测波长258nm,流速1.0mL/min,进样量20μL。以峰面积A为纵坐标,浓度C为横坐标,绘制标准曲线,曲线方程为:A=57.254 C+18.113,R2=0.9998。
2.2 酮洛芬微球的制备
(1)正交试验结果
正交试验表见表2,方差分析表见表3。
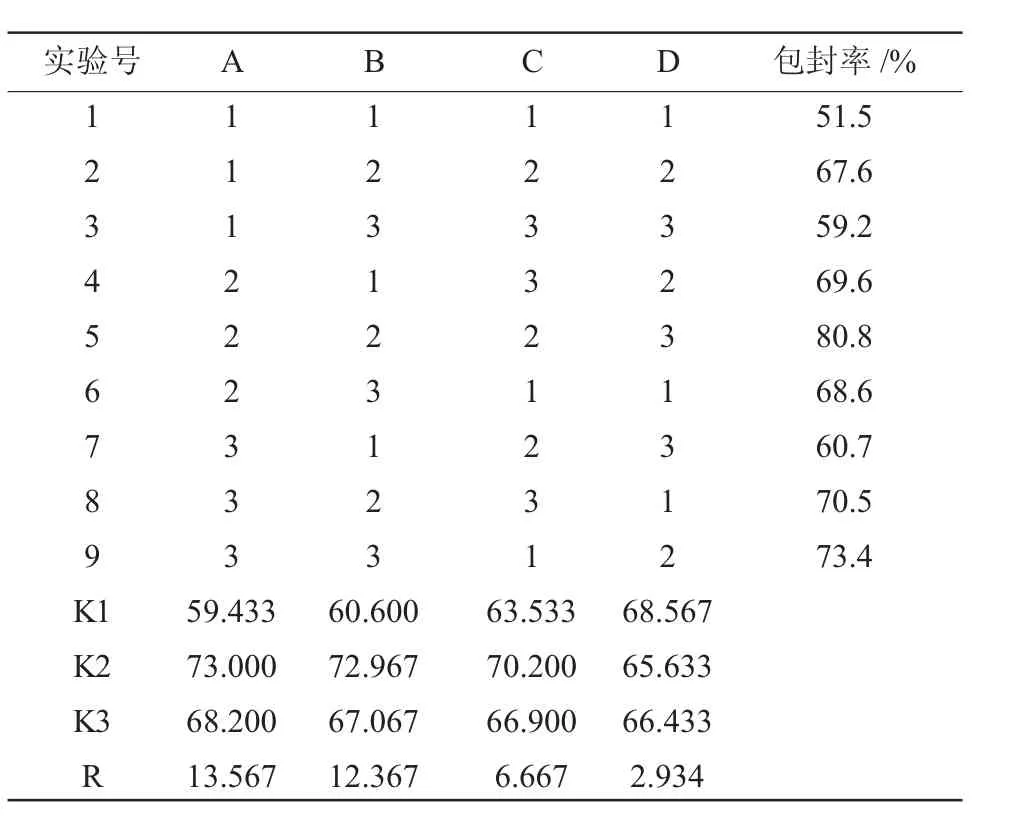
表2 L9(34)正交实验及结果Table 2 The L9(34)orthogonal test and data processing

表3 方差分析Table 3 The analysis of variance
实验结果的极差以及方差分析如表3、表4所示:各因素对微球包封率的影响程度依次为A(壳聚糖浓度)>B(搅拌速度)>C(乳化温度)>D(交联剂用量),且壳聚糖浓度(A)对包封率有显著影响(P<0.05)。这可能是由于随着壳聚糖浓度的增加,体系黏度增加,能有效阻止药物分子扩散,从而使包封率提高。从实验结果来看,壳聚糖微球的最佳制备工艺为A2B2C2D1,即壳聚糖浓度为2%,搅拌速度为1000r/min,乳化温度30℃,交联剂用量2.5%,进行验证试验确定工艺。
(2)验证试验
按A2B2C2D1工艺制备酮洛芬微球,各平行制备3份,测定包封率分别为81.9%、82.1%、82.5%,RSD为0.37%,表明优化的微球制备工艺稳定可行,包封率高。
2.3 酮洛芬微球的表征
2.3.1 微球的形态
通过光学显微镜观察微球形态,如图1所示。
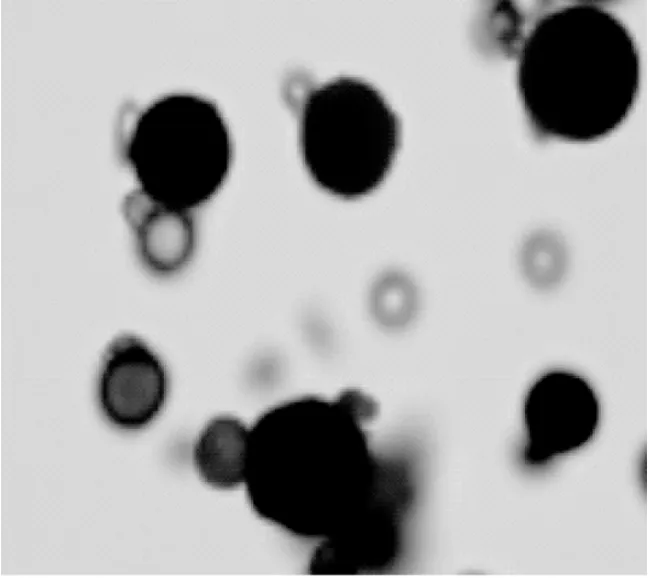
图1 微球形态图Fig.1 The morphology of microspheres
从光学显微镜下初步观察到微球外观形态,结果显示,微球的成球性较好,外观圆整。
2.3.2 微球粒径分布的测定
酮洛芬微球的粒径及Zeta电位值由激光散射粒径分析仪测得,粒径分布图见图2。
酮洛芬微球的平均粒径为(1.42±0.24)μm,PDI为0.292,表明所制备微球粒径分布集中。

图2 微球的粒径及粒径分布图Fig.2 The particle size and size distribution of microspheres
2.3.3 DSC分析
分别称取相同量的酮洛芬原料药、空白微球及载药微球适量,依次进行DSC分析,以验证药物是否包裹于微球中及药物的分散状态。分析条件如下:高纯氮气下,扫描范围10~250℃,升温速度10℃/min。分析结果见图3。

图3 DSC谱图A:酮洛芬原料药 B:空白微球 C:载药微球Fig.3 The DSC curves of A:crude drug,B:blank microspheres and C: drug-loaded microspheres
由图3可见,酮洛芬原料药在95℃左右存在吸热峰,空白微球不存在明显吸热峰,而载药微球中无酮洛芬原料药的特征吸收峰存在,说明药物是以非结晶形式分散于载体骨架中,未吸附在微球表面,即微球已形成。
2.4 酮洛芬微球的体外释药
采用透析法测定酮洛芬微球、市售酮洛芬缓释片、市售酮洛芬缓释胶囊的体外释药特性,用HPLC法测定释放的药量,计算累积释放度,释放曲线见图4。

图4 酮洛芬制剂的体外释药曲线Fig.4 The drug in-vitro release curve of different ketoprofen products
由释放曲线可以看出,与市售酮洛芬缓释片和缓释胶囊相比,酮洛芬微球表现出更明显的缓释特性。2h、4h、10h释放度分别为(21.42±4.11)%、(39.84± 3.40)%和(73.15±5.43)%,没有突释现象,随后药物的释放达到平台期。12h时,微球的释放度为(79.61± 7.12)%,市售酮洛芬缓释片和缓释胶囊的释放度分别为(97.30±4.62)%、(90.32±6.51)%,微球表现出更明显的缓释效果。24h时,微球的累积释放度为(85.87±5.53)%,而市售酮洛芬缓释片和缓释胶囊的释放度均高于95.0%,已基本释放完全。因此,壳聚糖微球具有较好的缓释效果,可能是因为壳聚糖发生交联后,聚合物骨架不易溶蚀,凝胶层厚度较大,同时,酮洛芬是难溶性药物,扩散较慢,因此缓释效果更好[9]。48h时,微球的释放度为(96.40± 5.22)%,释放基本完全,这是由于随着释放的进行,微球表面的亲水凝胶层逐渐增厚,微球释放的面积逐渐减小,所以缓释平稳,直至缓释完全。对酮洛芬微球的释放曲线分别进行零级、一级和Higuchi方程拟合,得出释药方程如表5所示。由拟合结果可以看出,酮洛芬微球的药物体外释放符合Higuchi方程。

表5 拟合结果Table 5 The fitting results
3 结论
(1)壳聚糖微球的最佳制备工艺为A2B2C2D1,即壳聚糖浓度为2%,搅拌速度为1000r/min,乳化温度30℃,交联剂用量2.5%,且壳聚糖浓度对包封率有显著影响。验证试验表明优化的微球制备工艺稳定可行,包封率高,平均包封率为(82.2±2.2)%。
(2)经表征,所制备的酮洛芬微球外观圆整,粒径分布集中,药物以非结晶形式分散于载体骨架中。
(3)与市售缓释制剂相比,微球表现出更明显的缓释特性,体外释药显示48h内药物释放完全,释放曲线符合Higuchi方程。
[1] 陈琰,胡晋红,范国荣,等.酮洛芬的制剂研究[J].药学进展, 2001,15(4):219~223.
[2] 王小宁,冯锁民,张存劳.酮洛芬醇质体的制备、表征及其体外经皮渗透研究[J].应用化工,2015,44(8):1461~1463,1467.
[3] 韩敏,苏秀霞,李仲谨.载药微球制剂的研究进展[J].应用化工, 2007,36(5):493~495.
[4] 车小琼,孙庆申,赵凯.甲壳素和壳聚糖作为天然生物高分子材料的研究进展[J].高分子通报,2008,2:45~49.
[5] JOSE S,FANGUEIRO J F,SMITHA J,et aI.Cross-linked chitosan microspheres for oral delivery of insulin:Taguehi design and in vivo testing[J].Colloids and Surfaces B:Biointerfaees,2012,92:175~179.
[6] 魏海霞,赵凯,纪鑫,等.壳聚糖微球的制备及其在药物载体中的应用进展[J].中国新药杂志,2008,17(13):1105~1108.
[7] PENG HAILONG,XIONG HUA,LI JIHUA,et a1.Vanillin crosslinked chitosan microspheres for controlled released of resveratrol[J].Food Chemistry,2010,121(1):23~28.
[8] 王钦,成艳,张玮,等.去甲斑蝥素壳聚糖微球的制备及其体外释放特性[J].中国新药杂志,2008,17(11):949~951.
[9] 金政,刘美华,刘振梅,等.壳聚糖缓释体系研究进展[J].化学与黏合,2015,37(1):65~71.
Preparation and Property of Ketoprofen Sustained-Release Microspheres
WANG Xiao-ning,DONG Wen-dan and ZHANG Cun-lao
(College of Pharmacy,Xi'an Medical University,Xi'an 710021,China)
The ketoprofen microspheres was prepared and characterized.The emulsification cross-linking method was used to prepare the microspheres,and the orthogonal experiment was used to optimize the process.The prepared microspheres were characterized by morphology,size distribution and DSC.The in-vitro release was investigated by dialysis method,and the release curve was fitted by models.The optimized preparation process was showed as follows:the 2%chitosan and 2.5%crosslinking agent was stirred at 1000r/min with an emulsifying temperature of 30℃.The average size of microspheres was(1.42±0.24)μm,and the average drug envelopment was(82.2±2.2)%.The DSC curves indicated that the drug dispersed in the bone structure of microsphere in amorphous form,the curve of drug release in vitro fitted with Higuchi equation.Compared with commercially available microspheres,the prepared ones showed obvious sustained-release property,so it was worthy of further study.
Ketoprofen;chitosan;microspheres;sustained release
TQ469;R 944.9
A
1001-0017(2017)02-0112-04
2016-11-24
西安医学院校级大学生创新基金项目(编号:2015DXS1-11);西安医学院校级科研青年基金项目
(编号:2015QN05)。
王小宁(1987-),女,陕西眉县人,讲师,主要从事制剂新技术与新剂型的研究。
