加速溶剂萃取-离子色谱法同时测定黄连上清片中9种常见无机阴离子的含量
2017-05-16胡恩泽黄正辉江汉大学附属医院武汉市第六医院西药剂科武汉430015武汉市医疗救治中心结核科武汉43003
胡恩泽,魏 明,黄正辉#(1.江汉大学附属医院/武汉市第六医院西药剂科,武汉 430015;.武汉市医疗救治中心结核科,武汉 43003)
加速溶剂萃取-离子色谱法同时测定黄连上清片中9种常见无机阴离子的含量
胡恩泽1*,魏 明2,黄正辉2#(1.江汉大学附属医院/武汉市第六医院西药剂科,武汉 430015;2.武汉市医疗救治中心结核科,武汉 430023)
目的:建立同时测定黄连上清片中9种常见无机阴离子含量的方法。方法:采用加速溶剂萃取-离子色谱法。阴离子交换分析柱为Ion Pac AS11-HC,保护柱为Ion Pac AG11-HC,淋洗液为氢氧化钾溶液(梯度洗脱),流速为1.2 mL/min,洗脱时间为18 min,柱温为30 ,进样体积为25 μL。结果:氟离子、甲酸根离子、氯离子、亚硝酸根离子、溴离子、硝酸根离子、硫酸根离子、草酸根离子和磷酸根离子检测质量浓度线性范围均为0.1~5 mg/L(r为0.999 0~0.999 9);定量限分别为0.020、0.078、0.030、0.058、0.052、0.068、0.084、0.064、0.074 mg/L,检测限分别为0.005、0.024、0.008、0.017、0.015、0.022、0.026、0.020、0.021 mg/L;精密度、稳定性、重复性试验的RSD<4.0%;加样回收率为80.00%~125.08%(RSD为0.97%~2.47%)。结论:该方法操作简便,精密度、稳定性、重复性好,可用于黄连上清片中9种常见无机阴离子含量的同时测定。
加速溶剂萃取;离子色谱法;黄连上清片;无机阴离子
黄连上清片收载于2015年版《中国药典》(一部),主要由大黄、黄连、黄柏、黄芩、白芷、栀子、桔梗等17味中药材组成[1],具有清热通便、散风止痛的作用,主要用于治疗风热上攻、头晕目眩、牙齿疼痛、口舌生疮、咽喉肿痛和大便秘结等症状[2-3]。根据现代药理研究表明,中药复方制剂中含多味中药,化学成分复杂,药效是其多种有效成分共同作用的结果,而有效成分不仅包括有机成分,还包括无机离子成分[4]。因此,中药复方制剂的质量控制应该包括有机成分和无机成分。目前,2015年版《中国药典》(一部)规定了应用薄层色谱法鉴定大黄素、小檗碱、栀子苷,以控制黄连上清片的质量[1]。再者,有不少文献报道了黄连上清片中的相关有机成分质量控制的研究[5-8]。但截止目前,尚未有文献报道控制黄连上清片中阴阳离子等无机成分的含量。氟(F)、氯(Cl)、磷(P)、氮(N)是人体必不可少的元素,对人体的骨骼、牙齿和机体酸碱平衡起着重要作用[9]。硝酸根离子(NO2-)、硫酸根离子(SO42-)和草酸根离子(C2O42-)等常见的阴离子含量过高对人体健康有一定的影响[10]。离子色谱法具有简便、快速、灵敏度高、干扰少等特点,能实现多组分同时定量分离,被广泛应用于环境、医药、生命科学和食品等领域[11-12]。再者,加速溶剂萃取法是在高温高压下通过溶剂提取样品成分,提高目标成分溶解度的方法,具有耗时少,溶剂用量少,提取效率高等优势。中药复方制剂机制复杂,各种离子含量差异比较大。为了更加全面的控制黄连上清片的质量,笔者采用加速溶剂萃取-离子色谱法测定了黄连上清片中9种常见无机阴离子的含量。
1 材料
1.1 仪器
ASE350型加速溶剂萃取仪、ICS-900 RFC30型离子色谱仪,包括ASRS 300(4 mm)抑制器,CD电导检测器(美国Dionex公司);BS224S型电子分析天平(北京赛多利斯仪器系统有限公司);TDZ4-WS型离心机(长沙市平凡仪器有限公司)。
1.2 药品与试剂
黄连上清片(江苏苏中药业集团股份有限公司,批号:20160305,规格:0.3 g/片);氟离子(F-)、甲酸根离子(COO-)、氯离子(Cl-)、亚硝酸根离子(NO2-)、溴离子(Br-)、NO3-、SO42-、C2O42-和磷酸根离子(PO43-)标准品溶液(中国计量科学研究院,批号分别为B1627013、B1627013、B1627015、B1627013、B1627030、B1622014、B1622015、B1622015、B1622015,质量浓度均为1 000 mg/L);氢氧化钾溶液为离子色谱仪自动产生,水为超纯水(电阻率>18.2 MΩ·cm)。
2 方法与结果
2.1 色谱条件
色谱柱:阴离子交换分析柱Ion Pac AS11-HC(250 mm×4 mm,4µm)、保护柱Ion Pac AG11-HC(50 mm×4 mm,4µm);淋洗液:氢氧化钾溶液,梯度洗脱(0~2.5 min,5 mmol/L;2.5~3 min,5→35 mmol/L;5~13 min,35 mmol/L;13~14 min,35→5 mmol/L;14~18 min,5 mmol/L);流速:1.2 mL/min;洗脱时间:18 min;柱温:30 ;进样量:25 μL。
2.2 溶液的制备
2.2.1 混合标准品溶液 分别准确量取各待测无机阴离子标准品溶液1 mL,置于同一10 mL量瓶中,加0.1%氢氧化钾溶液定容,得F-、COO-、Cl-、NO2-、Br-、NO3-、SO42-、C2O42-和PO43-质量浓度均为100 mg/L的混合标准品贮备液。分别准确量取上述混合标准品贮备液0.010、0.020、0.050、0.10、0.20、0.50 mL,置于同一10 mL量瓶中,加0.1%氢氧化钾溶液定容,制成系列混合标准品溶液(0.10、0.20、0.50、1.00、2.00、5.00 mg/L)。准确移取SO42-标准品溶液1 mL,置于10 mL量瓶中,加0.1%氢氧化钾溶液定容,得SO42-质量浓度为100 mg/L的标准品贮备液。准确量取上述SO42-标准品贮备液0.10、0.20、0.50、1.0、2.0、5.0 mL,分别置于10 mL量瓶中,加0.1%氢氧化钾溶液定容,制成系列SO42-标准品溶液(1.0、2.0、5.0、10.0、20.0、50.0 mg/L)。
2.2.2 供试品溶液 将样品研磨至粉末后混合均匀,准确称取样品粉末50 mg,置于萃取池中(萃取温度:40 ;萃取压力:1 600 psi;萃取溶剂:20 mL 0.1%氢氧化钾溶液,静态循环10 min,循环3次;冲洗体积:10 mL,冲洗时间:30 s)处理,萃取液转移至50 mL离心管中,充分摇匀,以半径为6 cm、3 500 r/min离心5 min,取上清液经0.22µm微孔滤膜滤过,即得。
2.3 系统适用性试验
取“2.2”项下混合标准品溶液、供试品溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。结果,9种无机阴离子成分分离度>1.5,各成分分离良好,不受杂质影响。
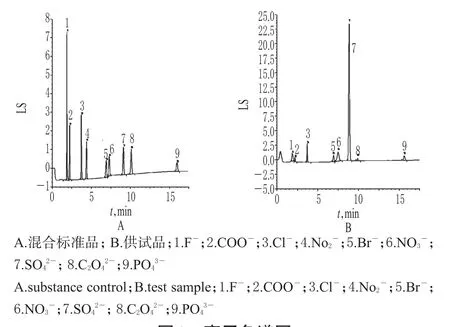
图1 离子色谱图Fig 1 Ion chromatography
2.4 线性关系考察
分别精密量取“2.2.1”项下系列混合标准品溶液各25 μL,按“2.1”项下色谱条件进样测定,记录峰面积。以待测无机阴离子质量浓度(x,mg/L)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程与线性范围,详见表1。
2.5 定量限与检测限考察
分别精密量取“2.2.1”项下系列混合标准品溶液各适量,倍比稀释,按“2.1”项下色谱条件进样测定,当信噪比为10∶1时,得定量限;当信噪比为3∶1时,得检测限,详见表1。
2.6 精密度试验
取“2.2.1”项下混合标准品溶液(1.00 mg/L)适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,F-、COO-、Cl-、NO2-、Br-、NO3-、SO42-、C2O42-和PO43-峰面积的RSD分别为1.1%、1.5%、1.2%、0.9%、0.5%、1.6%、1.9%、1.4%、1.6%(n=6),表明仪器精密度良好。

表1 回归方程、线性范围、定量限与检测限Tab 1 Regression equation,linear range,the limits of quantitation and detection
2.7 稳定性试验
取“2.2.2”项下供试品溶液(批号:20160305)适量,分别于室温下放置0、2、4、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,F-、COO-、Cl-、NO2-、Br-、NO3-、SO42-、C2O42-和PO43-峰面积的RSD分别为1.6%、1.8%、2.2%、1.4%、2.8%、3.5%、1.8%、2.4%、1.7%(n=5),表明供试品溶液室温放置12 h内基本稳定。
2.8 重复性试验
精密称取同一批样品(批号:20160305)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,F-、COO-、Cl-、NO2-、Br-、NO3-、SO42-、C2O42-和PO43-峰面积的RSD分别为1.8%、1.4%、2.1%、1.7%、1.3%、2.8%、
2.4 %、1.2%、1.6%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取已知含量样品(批号:20160305)适量,共6份,分别加入低、中、高质量浓度的各待测无机阴离子标准品溶液,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.10 样品中无机阴离子含量测定
取样品适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表3(表中“-”为未检出)。
3 讨论
3.1 色谱条件优化
Ion Pac AS11-HC阴离子交换分析柱是烷醇季铵基团的中高亲水性色谱柱,对水溶液中的阴离子分离能力良好,柱容量高,适合复杂基体中低质量浓度阴离子的分离。因此,本试验选择Ion Pac AS11-HC阴离子交换分析柱分离9种无机阴离子。由于中药复方制剂成分复杂,测定离子种类较多,采用等度洗脱无法实现每个阴离子的良好分离,同时不能较好地排除杂质峰的干扰,因此采用梯度洗脱。在离子色谱法中,用于分离水溶液中阴离子的淋洗液一般为氢氧化纳溶液或氢氧化钾溶液;考虑到仪器兼容性的问题,本试验采用氢氧化钾溶液作为淋洗液。梯度淋洗液是由仪器淋洗液自动发生系统产生,因此仪器的梯度淋洗基线平稳,重现性好。在优化梯度淋洗条件下,笔者分别考察了淋洗液强度、淋洗时间长度和淋洗速度。结果表明,淋洗强度和淋洗时间长度对阴离子的分离度影响最为显著,淋洗速度主要影响分析时间长短。试验过程发现,F-和COO-在Ion Pac AS11-HC阴离子交换分析柱的保留行为比较接近,同时相对其他的阴离子,保留能力较弱,在较强浓度的淋洗液下无法实现良好的分离,且较早出峰。因此,本研究选择较低的淋洗液强度。由于PO43-在Ion Pac AS11-HC阴离子交换分析柱中的保留较强,需要使用较强浓度的淋洗液缩短分析时间,因此综合考虑分离度情况和分析时间,最终确定了“2.1”项下的试验条件。结果表明,各无机阴离子能实现良好分离,每个阴离子的分离度均≥1.5。

表2 加样回收率试验结果(n=9)Tab 2 Results of recovery tests(n=9)

表3 样品中无机阴离子含量测定结果(n=3,mg/g)Tab 3 Results of inorganic anion content determination of samples(n=3,mg/g)
3.2 提取溶液的优化
由于需要提取样品中的COO-、NO2-、SO42-、C2O42-、PO43-等无机阴离子,而碱性溶液能够使样品更容易释放上述离子,因此采用碱性溶液提取样品。但若碱性溶液体积分数过高,会对仪器和色谱柱不利,而溶液体积分数过低,则不能有效释放样品中的阴离子,因此本试验分别考察了0.01%、0.05%、0.1%、0.2%、0.5%体积分数的氢氧化钾溶液对样品中各无机阴离子的提取效率。结果表明,各无机阴离子的总平均提取回收率分别为72.78%、89.38%、96.28%、96.42%、84.16%。综合考虑提取率和溶液体积分数对仪器的影响,最终选择0.1%氢氧化钾溶液作为提取溶液。
3.3 加速溶剂萃取的优化
根据温度(40、60、80、100 )、静态时间(5、10、15、20 min)、循环次数(1、2、3、4次)、冲洗体积(5、10、20、40 mL)和冲洗时间(10、30、60、90 s)5因素4水平设计单因素试验,考察不同因素对各无机阴离子提取率的影响。按单因素试验考察,结果表明提取温度和循环次数对提取率的影响较大。温度对某些无机阴离子如Cl-的提取率影响较小,对某些无机阴离子如NO2-和SO42-提取率的影响较明显。综合考虑,最终选择40 为提取温度。循环次数对提取率也有较明显的影响,这可能是因为循环次数越多,样品中无机阴阴离子释放越充分的缘故,当无机阴离子释放完全,循环次数增加,提取率将趋于稳定。为了缩短提取时间,本研究循环次数选择3次。静态时间、冲洗体积和冲洗时间对各无机阴离子的提取率的影响较小。为了节省资源和时间,静态时间最终选择10 min,冲洗体积为10 mL,冲洗时间为30 s。因此,最后确定加速溶剂萃取的条件为萃取温度40 ,静态循环10 min,循环3次,冲洗体积10 mL,冲洗时间30 s。
3.4 样品含量分析
研究结果表明,黄连上清片的样品中常见无机阴离子的含量差异明显,其中SO42-含量明显高于其他阴离子,而样品中均未检测出NO2-,其他阴离子的含量均在0.15~2.43 mg/g间,含量较低,根据对常见无机阴离子的认识,少量的氟化物能够预防龋齿;氯离子可以调节人体水分,渗透压和酸碱平衡;硝酸盐和亚硝酸盐是人体中典型的有害阴离子;过量摄入硫酸盐,会出现肠胃功能紊乱,腹胀腹泻等生理症状[13]。而该药中硫酸盐浓度如此之高,对人体的影响应该引起重视,有待进一步的药理研究。虽然,目前还没有药理学的证据证明这些无机阴离子在该药中具体的药理作用,但其理化指标的明显变化可说明生产或运输过程环节可能出现了问题,需要及时进行检查和质量监控,以保证药品的安全性,同时为进一步的研究提供依据。
[1] 中华人民共和国药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:1067-1068.
[2] 黄海燕,钟建理,薛漓.黄连上清片中黄连的鉴别及含量测定[J].中国医院药学杂志,2007,27(3):412-413.
[3] 师永清,师永花.双波长RP-HPLC同时测定黄连上清片中栀子苷和黄芩苷的含量[J].中国药事,2011,28(11):1041-1044.
[4] 周伟娥,杨立佼,谢巍,等.离子色谱法同时测定感冒清热颗粒中9种无机阴离子[J].中国药房,2015,26(18):2546-2549.
[5] 俞永梅,牟娜,张平,等.高效液相色谱法测定黄连上清片中3种生物碱[J].中成药,2012,34(5):861-864.
[6] 李洪亮,程齐来,张道英,等.RP-HPLC测定黄连上清片中盐酸小檗碱含量[J].光谱实验室,2010,27(4):1423-1426.
[7] 苏静华,张超,孙磊,等.RP-HPLC法同时测定黄连上清片的黄芩-黄连-黄柏药对中9个指标性成分的含量[J].药物分析杂志,2015,35(11):1940-1945.
[8] 陈娟.高效液相荧光色谱法测定黄连上清片中盐酸小檗碱含量[J].海峡药学,2015,27(11):53-55.
[9] Emsley J.Nature’s building blocks:an AZ guide to the elements[M].London:Oxford University Press,2011:128-130.
[10] J del Nozal M,Bernal JL,Diego JC,et al.Determination of oxalate,sulfate and nitrate in honey and honeydew by ion-chromatography[J].J Chromatogr A,2000,881(1):629-638.
[11] 杨绍美,陆建平,曹家兴,等.离子色谱同时测定中草药中磷硫含量[J].分析试验室,2011,30(7):119-120.
[12] Heitkemper DT,Vela NP,Stewart KR,et al.Determination of total and speciated arsenic in rice by ion chromatography and inductively coupled plasma mass spectrometry[J].J Anal Atom Spectrom,2001,16(4):299-306.
[13] 裴丹,赵梦蝶,张医翀,等.饮用水和茶水中无机阴离子含量调查[J].广东化工,2016,43(7):25-27.
(编辑:张 静)
Simultaneous Determination of 9 Common Inorganic Anions in Huanglian Shangqing Tables by Accelerat-ed Solvent Extraction-ion Chromatography
HU Enze1,WEI Ming2,HUANG Zhenghui2(1.Pharmacy Dept.of Western Medicine,the Affiliated Hospital of Jianghan University/Wuhan Sixth Hospital,Wuhan 430015,China;2.Dept.of Tuberculosis,Wuhan Medical Treatment Center,Wuhan 430023,China)
OBJECTIVE:To establish the method for simultaneous determination of 9 common inorganic anions in Huanglian shangqing tablet.METHODS:The accelerated solvent extraction-ion chromatography was adopted.Inorganic anions were determined by Ion Pac AS11-HC anion exchange column,protected by Ion Pac AG11-HC column and eluted by hydroxide potassium solution(gradient elution)at the flow rate of 1.2 mL/min.The column temperature was set at 30 ,elution time was 18 min,and sample volume was 25 mL.RESULTS:The linear ranges of fluorinion,formate ion,nitrite ion,bromide ion,nitrate ion,sulfate ion,oxalate ion and phosphate ion were 0.1-5 mg/L(r=0.999 0-0.999 9).The limits of quantitation were 0.020,0.078,0.030,0.058,0.052,0.068,0.084,0.064,0.074 mg/L,and the limits of detection were 0.005,0.024,0.008,0.017,0.015,0.022,0.026,0.020,0.021 mg/L,respectively.RSDs of precision,stability and repeatability were all lower than 4.0%;recoveries were 80.00%-125.08%(RSD ranged 0.97%-2.47%).CONCLUSIONS:The method is simple,precise,stable and repeatable,and can be used for 9 common inorganic anions in Huanglian shangqing tablet.
Accelerated solvent extraction;Ion chromatography;Huanglian shangqing tablet;Inorganic anion
R917
A
1001-0408(2017)12-1706-05
2016-09-26
2016-11-25)
*主管药师。研究方向:医院药学。E-mail:pharmacydong@163. com
#通信作者:主治医师。研究方向:临床医学。E-mail:13080668635@126.com
DOI10.6039/j.issn.1001-0408.2017.12.34
