愈酚维林片的溶出度测定方法研究
2017-05-16李筱玲李美芳李玉兰王铁杰深圳药品质量标准研究重点实验室深圳市药品检验研究院深圳518057
李筱玲,刘 敏,李美芳,李玉兰,王铁杰(深圳药品质量标准研究重点实验室/深圳市药品检验研究院,深圳518057)
愈酚维林片的溶出度测定方法研究
李筱玲*,刘 敏,李美芳,李玉兰#,王铁杰(深圳药品质量标准研究重点实验室/深圳市药品检验研究院,深圳518057)
目的:建立愈酚维林片溶出度的测定方法,并比较不同厂家制剂的差异。方法:采用浆法进行溶出,以水为溶出介质,体积为1 000 mL,转速为75 r/min,取样时间为45 min;采用高效液相色谱法测定制剂中枸橼酸喷托维林和愈创甘油醚的溶出度:色谱柱为CAPCELL PAK C18MGⅡS-5,流动相为乙腈-磷酸三乙胺缓冲溶液(pH 2.6±0.05)(33∶67,V/V),流速为1.0 mL/min,检测波长为215 nm(枸橼酸喷托维林)、275 nm(愈创甘油醚),柱温为35 ,进样量为20 μL。结果:枸橼酸喷托维林、愈创甘油醚检测质量浓度线性范围分别为5.091 6~50.915 5 μg/mL(r=0.999 9)、29.999 5~299.995 2 μg/mL(r=0.999 9);精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为97.90%~100.68%(RSD=0.95%,n=9)、97.09%~101.85%(RSD=1.32%,n=9)。6个厂家样品中枸橼酸喷托维林的平均累积溶出度分别为12%、98%、66%、97%、91%、32%(n=3),愈创甘油醚分别为8%、95%、68%、90%、93%、18%(n=3)。结论:该方法简便、准确、灵敏度高、专属性强,适于愈酚维林片的溶出度测定;不同厂家样品及同一厂家同批次样品间的溶出度均存在较大差异。
高效液相色谱法;愈酚维林片;溶出度;浆法;枸橼酸喷托维林;愈创甘油醚
愈酚维林片为复方止咳祛痰药,主要含有枸橼酸喷托维林和愈创甘油醚两种成分。其中,枸橼酸喷托维林具有中枢及外周性镇咳作用,其镇咳作用强度约为可待因的1/3,除对延髓的呼吸中枢有直接的抑制作用外,还有轻度的阿托品样作用,可使痉挛的支气管平滑肌松弛,降低气道阻力[1];愈创甘油醚为恶心性祛痰药[2],两药合用具有祛痰止咳作用。愈酚维林片为《国家药品标准·化学药品地方标准上升国家标准》(第十五册)收载的品种[3],国内外药典均未收载。现行国家标准未对愈酚维林片设置溶出度检查项,且目前国内也尚未见愈酚维林片溶出度测定方法的报道。为了更好地控制该制剂的内在质量,更加全面地评价其生产工艺,完善药品质量标准[4-7],以保障用药安全,笔者参照2015年版《中国药典》(四部)“溶出度与释放度测定法”(浆法)[8]和《普通口服固体制剂溶出度试验技术指导原则》[9]中的相关要求,对愈酚维林片进行了溶出度考察,建立了采用高效液相色谱法(HPLC)测定愈酚维林片中枸橼酸喷托维林和愈创甘油醚溶出度的检查方法。
1 材料
1.1 仪器
RCZ-8MD型智能溶出试验仪(天津天大天发科技有限公司);U-3000型HPLC仪,包括二级管阵列检测器(美国Dionex公司);XS205DU型电子天平(瑞士Mettler-Toledo公司)。
1.2 药品与试剂
愈酚维林片(厂家A,批号:20130901;厂家B,批号:20130801;厂家C,批号:130101;厂家D,批号:130201;厂家E,批号:120303;厂家F,批号:120501,规格均为:每片含愈创甘油醚0.15 g、枸橼酸喷托维林25 mg);枸橼酸喷托维林对照品(批号:100432-200702,纯度:98%)、愈创甘油醚对照品(批号:10058-201303,纯度:≥98%);乙腈、三乙胺为色谱纯,其余试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:CAPCELL PAK C18MGⅡS-5(250 mm× 4.6 mm,5 μm);流动相:乙腈-磷酸三乙胺缓冲溶液(pH 2.6±0.05)(33∶67,V/V);流速:1.0 mL/min;检测波长:215 nm(枸橼酸喷托维林)、275 nm(愈创甘油醚);柱温:35 ;进样量:20 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取枸橼酸喷托维林对照品0.012 78 g,置于50 mL量瓶中,加流动相溶解并定容,摇匀,作为枸橼酸喷托维林对照品贮备液;精密称取愈创甘油醚对照品0.015 06 g,置于50 mL量瓶中,加10 mL枸橼酸喷托维林对照品贮备液,加流动相定容,摇匀,作为混合对照品贮备液。取上述混合对照品贮备液10 mL,置于50 mL量瓶中,摇匀,即得。
2.2.2 供试品溶液 取样品适量,采用2015年版《中国药典》(四部)“溶出度与释放度测定”第二法(浆法),以水为溶出介质,体积为1 000 mL,转速为75 r/min,温度为(37±5 ),依法操作,于45 min时取溶出液10 mL,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3 系统适用性试验
取“2.2”项下混合对照品溶液、供试品溶液和溶出介质水各20 μL,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数以枸橼酸喷托维林峰计≥2 000,保留时间为14.436 min。结果表明,其他成分对测定无干扰。
2.4 线性关系考察

图1 高效液相色谱图Fig 1 HPLC chromatogram
精密称取“2.2.1”项下混合对照品溶液2.00、4.00、 6.00、8.00、10.00、20.00 mL,分别置于20 mL量瓶中,加流动相定容,摇匀,即得系列混合对照品溶液。取上述系列混合对照品溶液各适量,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/mL)为横纵标、峰面积(y)为纵坐标进行线性回归,得枸橼酸喷托维林、愈创甘油醚回归方程分别为y=11 906x-4 845.4(r=0.999 9)、y=13 809x-14 208(r=0.999 9)。结果表明,枸橼酸喷托维林、愈创甘油醚检测质量浓度线性范围分别为5.091 6~50.915 5、29.999 5~299.995 2 μg/mL。
2.5 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。结果,枸橼酸喷托维林、愈创甘油醚峰面积的RSD分别为0.1%、0.2%(n=6),表明仪器精密度良好。
2.6 稳定性试验
取“2.2.2”项下供试品溶液(批号:20130801)适量,分别于室温下放置0、4、8、12、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,枸橼酸喷托维林、愈创甘油醚峰面积的RSD均为0.1%(n=5),表明供试品溶液在室温放置24 h内稳定性良好。
2.7 重复性试验
取样品(批号:20130801)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,枸橼酸喷托维林、愈创甘油醚峰面积的RSD分别为1.8%、1.6%(n=6),表明本方法重复性良好。
2.8 加样回收率试验
取样品(批号:20130801)适量,共9份,分别置于100 mL量瓶中,加入低、中、高质量的枸橼酸喷托维林对照品和愈创甘油醚对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。

表1 加样回收率试验结果(n=9)Tab 1 Results of recovery tests(n=9)
2.9 溶出介质的选择
取6个厂家的样品各适量,按2015年版《中国药典》(四部)“通则0931”第二法(浆法),分别以水、0.1 mol/L盐酸溶液、pH 4.0醋酸盐缓冲溶液和pH 6.8磷酸盐缓冲溶液为溶出介质,体积为1 000 mL,转速为75 r/min,在5、10、15、20、30、45、60 min时取样,按“2.1”项下色谱条件进样测定,考察不同厂家样品在4种溶出介质中的累积溶出曲线,结果见图2。不同厂家样品在水中的累积溶出曲线见图3。
由图2可知,6个厂家的样品在4种溶出介质中的溶出行为均相似。考虑到枸橼酸喷托维林和愈创甘油醚两种主成分均为水溶性物质且均对pH不敏感,同时从图3中可以看出,不同厂家的样品在溶出介质水中溶出行为差异较大,一致性较差,综合考虑操作简便、经济环保等因素,选择水为溶出介质。
2.10 溶出转速的确定
取图2、图3中溶出行为较差厂家A的样品及溶出行为较好的厂家B的样品各1批。采用浆法,以水为溶出介质,体积为1 000 mL,转速分别为50、75 r/min,在5、10、15、20、30、45、60 min时取样,按“2.1”项下色谱条件进样测定,考察样品在不同转速、不同时间点的平均累积溶出度,结果见表2。由表2可知,不同厂家的溶出行为差异较大。综合考虑,选择参考浆法推荐的50~75 r/min的较高转速75 r/min作为拟定转速。

图2 不同厂家样品在4种溶出介质中的累积溶出曲线Fig 2 Accumulative dissolution curve of samples from different manufactures in 4 types of dissolution medium

图3 不同厂家样品在水中的累积溶出曲线Fig 3 Accumulative dissolution curve of samples from different manufactures in water
2.11 取样时间及溶出限度的确定
取6个厂家的样品适量,采用浆法,以水为溶出介质,体积为1 000 mL,转速为75 r/min,在5、10、15、20、30、45、60 min时取样,按“2.1”项下色谱条件进样测定,考察不同厂家样品不同时间点的平均累积溶出度,结果见表3、表4。

表2 厂家A、厂家B样品在不同转速及不同时间测定的平均累积溶出度(n=6,%)Tab 2 Average accumulative dissolution of samples fr-om manufacture A or B at different rotation speed and different time(n=6,%)

表3 6个厂家样品枸橼酸喷托维林不同时间点的平均累积溶出度(n=3,%)Tab 3 Average accumulative dissolution of pentoxyve rine citrate of samples from 6 manufactures at different time(n=3,%)
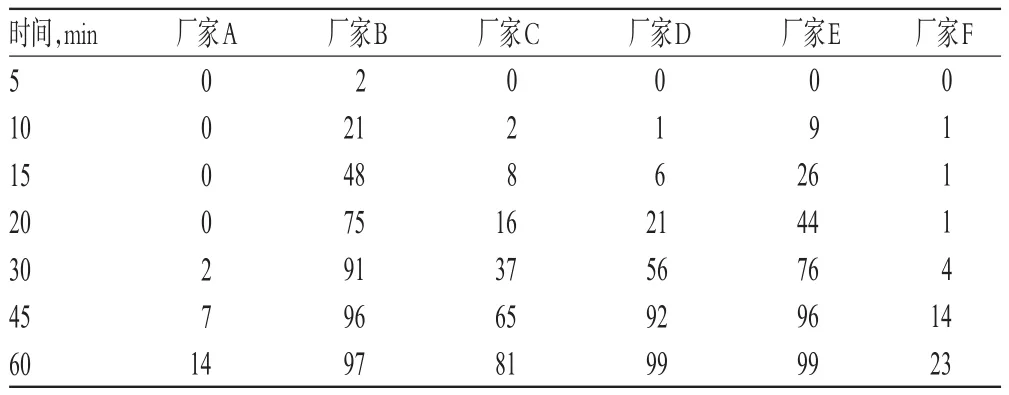
表4 6个厂家样品愈创甘油醚不同时间点的平均累积溶出度(n=3,%)Tab 4 Average accumulative dissolution of guaifenesin of samples from 6 manufactures at different time(n=3,%)
由表3、表4可知,厂家A、厂家C和厂家F的样品,在60 min时,两种主成分的平均累积溶出度均<85%,因此在设定标准时不考虑这3个厂家的产品情况。根据厂家B、厂家D和厂家E样品的试验结果,在45 min时,3个厂家样品的两种主成分的平均累积溶出度均>85%,厂家D和厂家E的样品为首次>85%。因此,拟定取样时间为45 min。同时,3个厂家样品的两种主成分在45 min时的平均累积溶出度在92%~96%之间,依据《普通口服制剂溶出度试验技术指导原则》,限度拟订为75%[9]。
2.12 滤膜吸附试验
取“2.2.1”项下混合对照品溶液适量,经0.45 μm微孔滤膜滤过,取续滤液1、2、3、5、6 mL,按“2.1”项下色谱条件进样测定。结果,0.45 μm微孔滤膜对枸橼酸喷托维林、愈创甘油醚的吸附量均<2.0%(n=5),符合规定[9]。
2.13 样品溶出度测定
取6批样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算枸橼酸喷托维林、愈创甘油醚的溶出度,结果见表5。

表5 样品溶出度试验结果(n=3,%)Tab 5 Results of dissolution tests of different samples (n=3,%)
3 讨论
对于口服固体制剂,溶出度作为一种控制药品质量的重要指标,已广泛应用于药品的研发、生产和监督检验中[10]。溶出度试验是评价口服固体制剂质量的一种重要手段,有望成为检测口服固体制剂质量的简易、有效、可行的方法。本试验结果显示,同一厂家同批次的样品差异较大,溶出度离散性大,溶出行为一致性差;不同厂家的样品,差异均较大,因此极其有必要增订溶出度检查项(注:拟定方法已上报国家药典委员会)。
[1] 田兆红,梁柱红.HPLC法测定枸橼酸喷托维林片的含量[J].西北药学杂志,2008,23(1):4-6.
[2] 李冰,刘汶,赵小冬,等.HPLC法测定氢溴酸右美沙芬愈创甘油醚干混悬剂的含量[J].中国药品标准,2006,7 (2):27-30.
[3] 国家药典委员会.国家药品标准:化学药品地方标准上升国家标准:第十五册[S].2003:179-181.
[4] 王茉莉,敦洁宁,郭毅,等.复方炔诺酮片的溶出度测定方法研究及质量评价[J].中国药房,2016,27(12):1695-1698.
[5] 谢沐风.溶出曲线相似性的评价方法[J].中国医药工业杂志,2009,40(4):308-311.
[6] 李芳,李瑛,刘建平,等.不同生产厂家常用口服避孕药体外溶出度考察[J].中国药房,2007,18(7):535-538.
[7] 陈丽姣,杨冬霞,赵艳霞.HPLC法测定他米巴罗汀片的溶出度[J].中国药房,2016,27(30):4304-4306.
[8] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:121-124.
[9] 国家食品药品监督管理局.普通口服固体制剂溶出度试验技术指导原则[S].2009.
[10] 国家药典委员会.国家药品标准:化学药品地方标准上升国家标准:第五册[S].2002:270-272.
(编辑:刘 柳)
Study on Determination Method for Dissolution of Pentoxyverine Citrate and Guaifenesin Tablets
LI Xiaoling,LIU Min,LI Meifang,LI Yulan,WANG Tiejie(Shenzhen Key Laboratory of Drug Quality Standard Research/Shenzhen Institute for Drug Control,Guangdong Shenzhen 518057,China)
OBJECTIVE:To establish a method for the dissolution determination of Pentoxyverine citrate and guaifenesin tablets,and to compare the difference of preparations from different manufactures.METHODS:The paddle method was used to determine the dissolution,using water as medium with medium volume of 1 000 mL and rotation speed of 75 r/min,sampling at 45 min. HPLC method was used to determine the accumulative dissolution of pentoxyverine citrate and guaifenesin:CAPCELL PAK C18MG ⅡS-5 column;mobile phase of acetonitrile-triethylamine phosphoric buffer solution(pH 2.6±0.05)(33∶67,V/V),flow rate of 1.0 mL/min,detection wavelength of 215 nm(pentoxyverine citrate)and 275 nm(guaifenesin),column temperature of 35 ,sample size of 20 μL.RESULTS:The linear range of pentoxyverine citrate and guaifenesin were 5.091 6-50.915 5 μg/mL(r=0.999 9)and 29.999 5-299.995 2 μg/mL(r=0.999 9),respectively.RSDs of precision,stability and reproducibility tests were all lower than 2.0%.Average recoveries were 97.90%-100.68%(RSD=0.95%,n=9)and 97.09%-101.85%(RSD=1.32%,n=9).Average accumulative dissolution of pentoxyverine citrate in 6 manufactures of samples were 12%,98%,66%,97%,91%,32%(n=3);those of guaifenesin were 8%,95%,68%,90%,93%,18%(n=3),respectively.CONCLUSIONS:The method is simple,accurate,sensitive,specific and suitable for the dissolution determination of Pentoxyverine citrate and guaifenesin tablets.The dissolution of samples between different manufactures and the same manufactures different batches are quite different.
HPLC;Pentoxyverine citrate and guaifenesin tablets;Dissolution;Paddle method;Pentoxyverine citrate;Guaifenesin
R927.2
A
1001-0408(2017)12-1702-05
2016-05-02
2017-01-11)
*主管药师,硕士。研究方向:药物分析。电话:0755-26031735。E-mail:20505695@qq.com
#通信作者:主任药师,博士。研究方向:药物分析。电话:0755-26031736。E-mail:liyulan@szda.gov.cn
DOI10.6039/j.issn.1001-0408.2017.12.33
