新制CuO与醛基反应的机理探究
2017-05-12雷素娟重庆市北碚区西南大学附属中学校重庆400700
雷素娟(重庆市北碚区西南大学附属中学校,重庆 400700)
新制CuO与醛基反应的机理探究
雷素娟(重庆市北碚区西南大学附属中学校,重庆 400700)
人教版高中化学教材有机化学部分讲到醛类的性质,其中,醛类的催化氧化性是醛类一个比较重要的性质,通常用来鉴定醛基的存在,所用到试剂为银氨溶液和新制的Cu(OH)2,这是因为醛在碱性环境中被弱氧化剂银氨溶液、新制的Cu(OH)2氧化生成羧酸盐,而氧化剂分别被还原成单质银和+1价铜的氧化物。选修5实验3-6中写道:“在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4~6滴Cu(OH)2,……”,分析数据不难发现相对于CuSO4溶液,NaOH溶液是过量的,Cu(OH)2是两性氧化物(既可以溶于酸,也可以溶于过量的浓碱),对于该反应为什么在碱性条件下进行已有很多学者对其进行了探讨。
杨淑梅[1]认为乙醛在碱性条件下失去一个H+生成碳负离子,生成的碳负离子可与Cu2+络合,进而产生H-,H-的强还原性可将Cu(OH)2还原为Cu2O。陈廷俊[2]在前者研究的基础上,认为在碱性环境中,乙醛能产生碳负离子,与[Cu(OH)4]2-电离产生的Cu2+生成络合物,进而产生产生H-还原Cu(OH)2还原为Cu2O。段昌平[3]提出醛基在碱性条件下的还原性比在酸性条件下强得多,这是因为
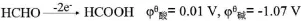
即从电极电势的角度分析了碱性条件对醛基还原性的影响。综上所述,醛基在碱性条件下能将新制Cu(OH)2还原为Cu2O[4-5],其机理得到了很好的解释,然而,并未发现有学者对新制CuO与醛基之间的氧化还原反应进行系统研究。
本文通过研究了新制CuO与醛基之间反应过程产生的现象,通过对比其产生沉淀的颜色和最终产物气味等因素来确定新制CuO与醛基之间反应的主产物和副产物,并在现有理论基础上探讨了该反应主反应和副反应进行的反应机理,很好的解释了新制CuO与醛基反应生成砖红色沉淀的原理。
实验部分
1 仪器与试剂
试剂:铜丝,乙醛
仪器:试管,砂纸,酒精灯,胶头滴管,试管夹,铁夹,表面皿等
2 实验过程
2.1 新制CuO的制备
取直径为1 mm左右的铜丝20 cm,用砂纸打磨铜丝表面至光滑有金属光泽,将铜丝绕成螺旋状,至于酒精灯外焰上灼烧,直到铜丝表面完全变成黑色时,停止加热。
2.2 新制CuO和醛基的反应
用量筒量取10 mL乙醛加入试管中,将2.1中制得的灼热氧化铜迅速插入装有10 mL乙醛的试管,待铜丝冷却至室温后取出,观察实验现象并记录。
结果与讨论
通过对新制CuO和醛基的反应的实验现象进行观察,并与新制Cu(OH)2和醛基反应的实验现象作对比发现:铜丝表面黑色的氧化铜逐渐消失,铜丝表面出现红色的固体,取出铜丝后,向试管中滴入几滴紫色石蕊试液,试管中溶液变红,反应过程中可以闻到有刺激性的气味。
实验过程中现象如下图1所示:

图1 新制CuO和醛基的反应的实验现象
通过对比反应中的实验现象不难发现,新制CuO和醛基的反应后CuO被醛基还原生成了Cu2O,而乙醛中的醛基本身被氧化为羧基,因而,新制CuO和乙醛反应的主反应方程式为:
CH3CHO+2CuO+NaOH CH3COONa+Cu2O↓+H2O
即在浓碱性条件下,新制的氧化铜会被还原为砖红色Cu2O固体,那么,该反应为什么需要在碱性条件下进行呢?这个反应能发生,其机理是如何进行的呢?本文对该反应的机理进行了探索,内容如图2所示:

图2 新制CuO与乙醛反应的机理图
分析图2可以看出:当乙醛中的醛基与新制CuO在浓碱条件下反应时,由于好浓度OH-存在会使得CuO分子中的C=O双键打开变为单键,两两结合为带有一个单位正电荷的O-Cu-OCu+离子,来进攻乙醛中醛基上的碳原子,导致乙醛中醛基上的C=O双键打开,与O-Cu-O-Cu+离子与之配位的氧原子相互作用形成羧基,而O-Cu-O-Cu+离子中剩余的原子结合为Cu2O,即产生砖红色的固体,而羧基在碱性条件下会形成相应的羧酸盐和水。经过分析可以看出,在浓碱条件下,醛基会被新制CuO氧化为羧基,而自身被还原为砖红色的Cu2O,其反应机理得到了合理的解释。
3 结语
本文通过实验探究发现:醛基在浓碱的环境中能够被弱氧化剂银氨溶液、新制的Cu(OH)2氧化生成羧酸盐,而氧化剂分别被还原成单质银和+1价铜的氧化物,而同样在浓碱条件下也能被新制的CuO氧化为羧基,而自身被还原为砖红色的Cu2O固体,主要是因为高浓度的OH-存在会使得醛基上的碳原子被活化,与氧化铜形成的O-Cu-O-Cu+离子形成配位键,从而自身的C=O被打开,与O-Cu-O-Cu+离子中的氧原子形成羧基,O-Cu-O-Cu+离子剩余原子结合为砖红色的Cu2O固体,文中从反应机理出发,证明了该反应进行的必然性,为后续关于醛基性质的探索提供了理论依据,具有较为广泛的应用价值。
[1]杨淑梅.对乙醛还原氢氧化铜实验的探讨.化学工程与装备,2007,7,33-34.
[2]陈廷俊.对乙醛还原氢氧化铜实验现象的探讨.化学教育,2013,3,68-69.
[3]段昌平.细说氢氧化铜与新制氢氧化铜.化学教育,
2013,12,76-77.
[4]朱和清.醛与新制Cu(OH)2反应的实验探讨.邵阳学院学报,2002,2(1),125-126.
[5]王志平.新制Cu(OH)2与醛基反应本质的认识.化学教学,1997,5,44-45.
Explore the mechanism of aldehyde with CuO reaction system
LEI Su-juan(High school Affiliated to Southwest University,Chongqing,400700)
本着完善醛基作为还原剂被弱氧化剂氧化的目的,本文研究了新制的CuO与乙醛反应过程的现象,通过与醛基和新制Cu(OH)2的反应作对比,确定了醛基在碱性条件下被新制的CuO氧化所得产物为羧基,并探讨了该反应进行的反应机理,很好的对该氧化还原反应进行了解释。
新制CuO;醛基氧化;羧基
With the purpose of improving the weak antioxi⁃dant oxidation reduction,this paper studies the new system of the phenomenon of newly-prepared CuO and acetaldehyde reaction process,with the aldehyde group and a new system of Cu(OH)2re⁃action,and determines the aldehyde group under alkaline condi⁃tions was newly-prepared CuO oxidation of the products of the new system of carboxyl,and discusses the reaction mechanism of the reaction,a good explanation for the REDOX reaction.
newly-prepared CuO;aldehyde group reaction; carboxyl
雷素娟(1989-),女,汉族,陕西咸阳人,重庆市北碚区西南大学附属中学校化学教师,中学二级教师
