埃克替尼联合放疗治疗EGFR突变型肺腺癌无症状脑转移疗效观察
2017-05-11罗鹏辉王湘萍莫敦昌刘艳萍黄昌杰
罗鹏辉,王湘萍,莫敦昌,刘艳萍,黄昌杰
(广西医科大学第三附属医院肿瘤科,广西南宁530031)
埃克替尼联合放疗治疗EGFR突变型肺腺癌无症状脑转移疗效观察
罗鹏辉,王湘萍,莫敦昌,刘艳萍,黄昌杰
(广西医科大学第三附属医院肿瘤科,广西南宁530031)
目的评价埃克替尼联合放疗在治疗EGFR突变型肺腺癌无症状脑转移患者中的作用。方法回顾性分析2012年1月至2015年6月广西医科大学第三附属医院61例EGFR突变型肺腺癌无症状脑转移患者的临床资料,其中埃克替尼联合放疗(联合组)23例,埃克替尼单药治疗(靶向治疗组)38例。靶向治疗第1、3、5个月及之后每3个月复查评价疗效。χ2检验评价两组客观缓解率、疾病控制率,Kaplan Meier法和Log-rank法进行生存分析。结果在靶向治疗第5个月,联合组的总客观缓解率和总疾病控制率分别为82.6%和95.7%,均明显高于靶向治疗组的55.3%和76.3%,差异均有统计学意义(P<0.05);联合组的脑转移瘤客观缓解率和疾病控制率分别为95.7%和100.0%,均明显高于靶向治疗组的55.3%和81.6%,差异均有统计学意义(P<0.05);中位无进展生存时间联合组14个月,靶向治疗组8个月,差异亦有统计学意义(P<0.05);Ⅲ~Ⅳ级毒副反应中,联合组疲乏、恶心、呕吐明显高于靶向治疗组,差异均有统计学意义(P<0.05),但可耐受,皮疹、腹泻、骨髓抑制差异均无统计学意义(P>0.05)。结论埃克替尼联合放疗明显提高EGFR突变型肺腺癌无症状脑转移患者的治疗效果,延长患者中位无进展生存时间,毒副反应可以耐受。
肺癌;肺腺癌;脑转移;埃克替尼;放疗;靶向治疗
肺癌是全世界发病率和死亡率最高的恶性肿瘤[1]。脑转移瘤的原发部位最常来源于肺癌,是肺癌患者主要死亡原因[2-3]。肺癌中最容易发生脑转移(brain metastases,BM)的病理类型是腺癌和小细胞肺癌,即使采用放疗、化疗、手术等积极的治疗方法,也难明显延长肺癌脑转移患者的生存时间[4-6],因此探索肺癌脑转移新的治疗方法十分必要。厄洛替尼等表皮生长因子受体酪氨酸激酶抑制剂能明显延长EGFR突变型晚期肺腺癌患者的生存时间,成为这类患者首选治疗方法[7-9]。Weber等[10]研究发现EGFR-TKIs对EGFR突变型肺腺癌脑转移病灶有明显治疗效果。Zeng等[11]和Fan等[12]在各自的研究中相继发现,EGFR-TKIs联合放疗治疗EGFR突变型肺癌脑转移瘤的疗效优于单存放疗或单存靶向治疗。Lee等[13]研究中发现放疗在EGFR突变型非小细胞肺癌脑转移病灶的效果明显优EGFR野生型患者。但关于靶向治疗、放疗在EGFR突变型肺腺癌无症状脑转移的疗效报道罕见。因此,笔者回顾三年多在我院接受埃克替尼靶向治疗联合放疗或单纯埃克替尼靶向治疗的EGFR突变型肺腺癌无症状脑转移患者的临床资料,现将两组的治疗效果及副反应情况比较分析如下:
1 资料与方法
1.1 一般资料回顾性分析2012年1月至2015年6月61例在广西医科大学第三附属医院住院治疗的EGFR突变型肺腺癌无症状脑转移患者的临床资料,将其中接受靶向治疗联合放疗的23例患者作为联合组,38例单纯靶向治疗者作为靶向治疗组。治疗前经病理确诊为肺腺癌,MRI检查明确存在脑转移瘤,基因检测确诊EGFR基因突变,两组患者的临床资料比较见表1。
1.2 治疗方法靶向治疗采用口服盐酸埃克替尼片,每次125 mg,3次/d,至疾病进展或出现无法耐受的副反应时停药;放疗采用全脑照射(两侧野对穿照射)30 Gy,局部病灶调强放疗加量至60 Gy,1次/d,每周5 d,每次剂量200 cGy。
1.3 疗效评价方法采用新版实体瘤疗效评价标准(RECIST 1.1版)[14],在靶向治疗第1、3、5个月及之后每3个月复查胸部CT、头颅MRI,及疗效评价。在靶向治疗第5个月进行总体疗效评价和脑转移病灶的局部疗效评价。客观有效率为(CR+PR)/(CR+PR+SD+ PD)×100%,疾病控制率为(CR+PR+SD)/(CR+PR+SD+ PD)×100%。统计分析两组患者无进展生存时间。
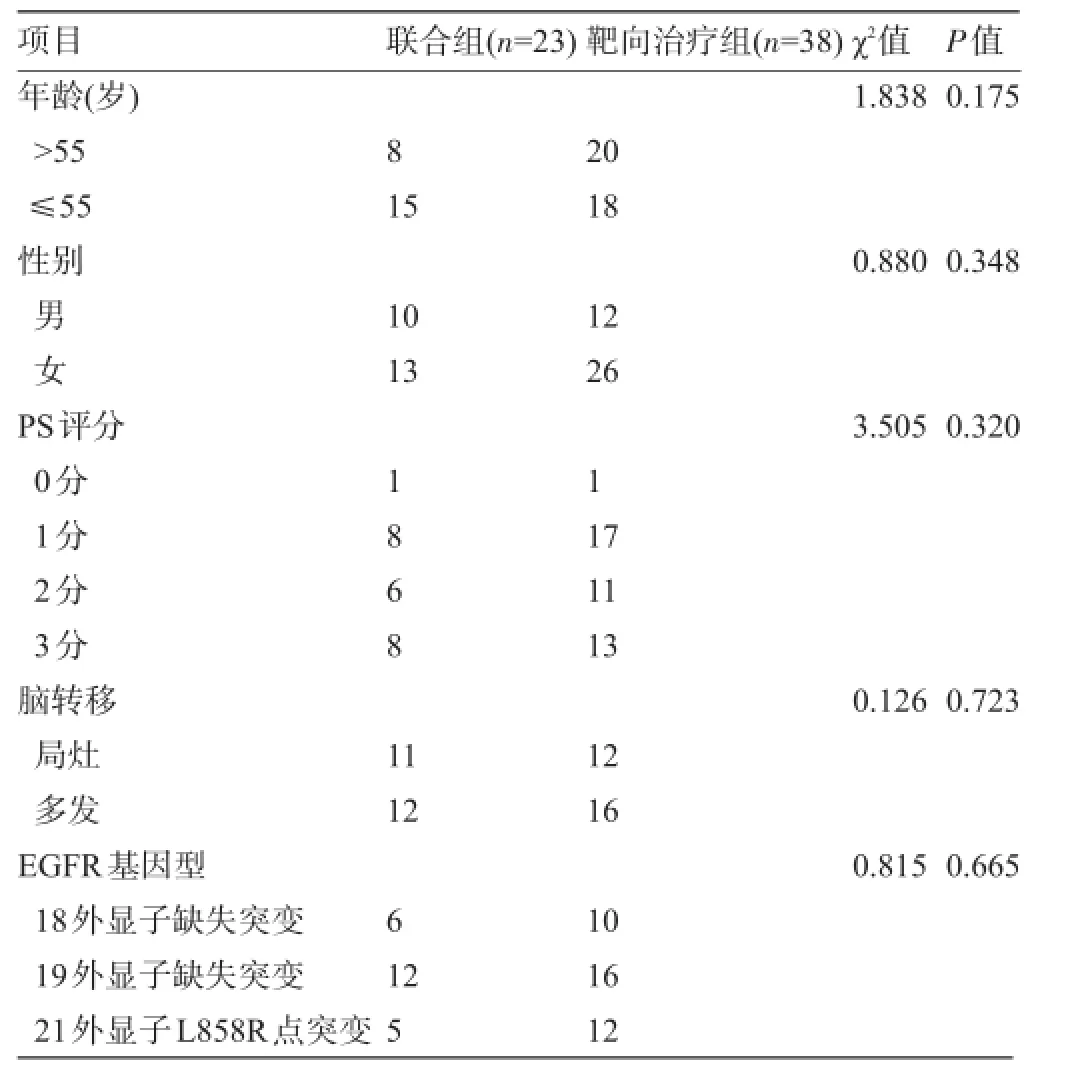
表1 两组患者的临床资料比较(例)
1.4 不良反应评估方法采用美国国家癌症研究所制定的毒副评价标准进行不良反应评估[15]。
1.5 统计学方法应用SPSS19.0统计软件进行数据分析,两组间计数资料比较采用Pearson χ2检验,采用Kaplan Meier法进行生存分析,并行Log-rank法检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的总体客观有效率和疾病控制率比较两组患者生存时间大于5个月,CR、PR、SD、PD在联合组中分别为8例、11例、3例、1例,靶向治疗组分别为3例、18例、8例、9例,差异均有统计学意义(χ2= 9.522,P=0.023)。联合组客观有效率和疾病控制率分别为82.6%、95.7%,靶向治疗组分别为55.3%、76.3%,经统计学分析,差异均有统计学意义(χ2=4.746,P= 0.029;χ2=3.909,P=0.048)。
2.2 两组患者脑转移病灶的客观有效率和疾病控制率比较两组患者脑转移病灶CR、PR、SD、PD在联合组中分别为17例、5例、1例、0例,靶向治疗组分别为6例、15例、10例、7例,差异均有统计学意义(χ2= 22.283,P=0.000)。联合组客观有效率和疾病控制率分别为95.7%、100%,靶向治疗组分别为55.3%、81.6%,差异均有统计学意义(χ2=11.236,P=0.001;χ2= 4.786,P=0.029)。
2.3 两组患者严重不良反应比较在严重不良反应表现中,联合组疲乏、恶心、呕吐发生率均高于靶向治疗组,差异均有统计学意义(P<0.05),而皮疹、腹泻、骨髓抑制发生率比较差异均无统计学意义(P>0.05),见表2。所有不良反应经对症处理后患者均能耐受。
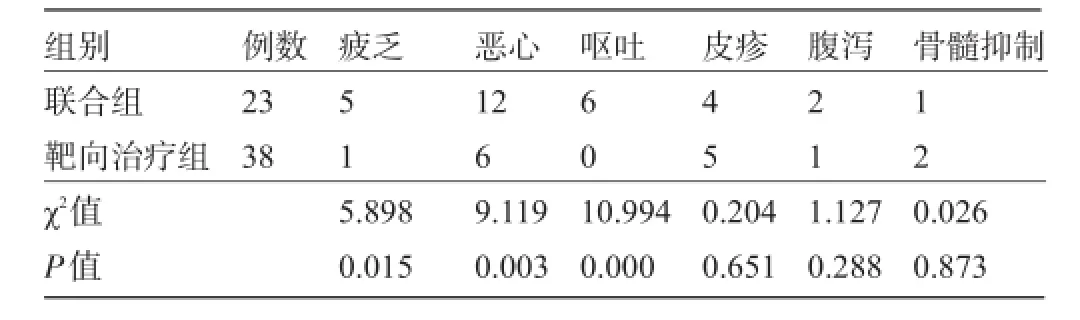
表2 严重不良反应发生率(例)
2.4 两组患者无进展生存时间比较随访5~29个月,联合组中位无进展生存时间14个月(95%CI:8.690~19.310),靶向治疗组中位无进展生存时间8个月(95%CI:5.738~10.262),差异具有统计学意义(χ2= 5.753,P=0.016)。见图1。
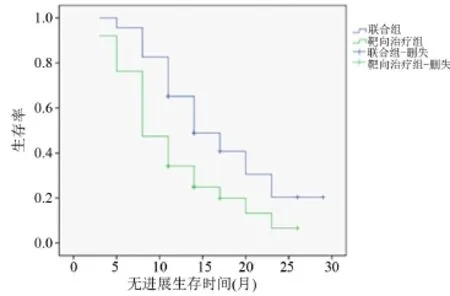
图1 两组无进展生存曲线
3 讨论
EGFR-TKIs是晚期EGFR突变型非小细胞肺癌一线治疗药物,在疾病控制率和总体生存率方面明显优于化疗[14-15]。由于血脑屏障的原因,化学药物等大分子、亲水性物质很难进入颅内,而EGFR-TKIs等小分子靶向药物能通过血脑屏障、进入颅内杀灭脑转移瘤。Miller等[16]用厄洛替尼联合放疗治疗脑胶质瘤,进行药代动力学研究发现7%的厄洛替尼可透过血脑屏障,作用于脑胶质瘤,最大稳态脑脊液浓度达130 ng/mL,证实EGFR-TKIs可通过血脑屏障、治疗颅内肿瘤。
目前也有研究证实EGFR-TKIs对非小细胞肺癌脑转移瘤治疗有效。Weber等[10]用[¹¹C]标记厄洛替尼,治疗EGFR基因突变型(19外显子缺失)非小细胞肺癌脑转移患者,用PET/CT检测颅内被[¹¹C]标记的厄洛替尼的聚集情况,发现厄洛替尼能渗透过血脑屏障,在脑转移病灶中浓聚,经厄洛替尼治疗后脑转移瘤明显缩小。Fan等[12]对20例已有脑转移的非小细胞肺癌患者采用埃克替尼靶向治疗联合全脑放疗(其中EGFR突变型18例,EGFR野生型2例),同时检测脑脊液和血浆中埃克替尼的浓度,中位随访20个月,结果总反应率为80%,中位无进展生存时间7个月,中位生存时间14.6个月,其中EGFR突变型患者中位生存时间22个月,野生型7.5个月,脑脊液中埃克替尼浓度为(11.6±9.1)ng/mL,埃克替尼通过血脑屏障的渗透率为(1.4±1.1)%。这两项研究均证实EGFR-TKIs药物厄洛替尼、埃克替尼能透过EGFR突变型非小细胞肺癌患者的血脑屏障,对肺癌患者的脑转移病灶有治疗作用。本组61例EGFR突变型肺腺癌无症状脑转移患者接受埃克替尼靶向治疗后颅内病灶均得到控制,联合组脑转移病灶疾病控制率为100%,靶向治疗组脑转移病灶疾病控制率为81.6%。
放射治疗是脑转移瘤的主要治疗模式。脑转移瘤的放疗方式包括全脑放疗(whole brain radiotherapy,WBRT)和立体定向放疗(stereotactic radiosurgery,SRS),脑转移瘤患者WBRT的中位生存期(median overall survival,mOS)3~6个月,SRS可延长至10个多月,但SRS主要适用于脑转移灶数目较少、体积较小的患者[4,17],因此靠单纯放疗明显延长脑转移瘤患者的生存时间可能性不大。EGFR-TKIs问世以后,研究者们不断尝试用EGFR-TKIs联合放疗治疗脑转移瘤,来提高脑转移瘤患者的生存时间。如Olmez等[18]采用全脑放疗联合厄洛替尼治疗8例非小细胞肺癌脑转移患者,结果所有患者颅内转移病灶得到有效控制,但出现明显的Ⅲ~Ⅳ级毒副反应;Welsh等[19]用厄洛替尼联合全脑放疗治疗40例出现脑转移的非小细胞肺癌患者,结果发现总反应率为86%,无神经毒性及Ⅳ级毒副反应发生,中位随访28.5个月,中位生存时间11.8个月。其中17例进行了EGFR基因检测,EGFR野生型患者中位生存时间9.3个月,EGFR突变患者中位生存时间19.1个月。提示EGFR-TKIs联合放疗可协同放射线作用,增加放疗对EGFR突变型非小细胞肺癌患者脑转移病灶治疗效果,使非小细胞肺癌脑转移患者获得更长的生存时间。本研究回顾性分析61例EGFR突变型肺腺癌无症状脑转移患者的临床资料,其中埃克替尼联合放疗(联合组)23例、单纯埃克替尼靶向治疗(靶向治疗组)38例,随访时间大约5个月,经统计分析发现联合组比靶向治疗组有效,联合组总客观缓解率、总疾病控制率、脑转移病灶客观缓解率、脑转移病灶疾病控制率比靶向治疗组均高,联合组的中位无进展生存时间比靶向治疗组长,联合组Ⅲ~Ⅳ毒副反应如疲乏、恶心、呕吐等发生率高于靶向治疗组,但可耐受。
综上所述,EGFR突变型肺腺癌无症状脑转移患者能从EGFR-TKIs靶向治疗联合放疗的治疗方案中获益,副反应能耐受。但是放疗后脑转移瘤进展时如何选择治疗方案,是否可以继续放疗,还是换用新的靶向治疗药物,及治疗时机如何确定,值得我们进一步探讨。本研究为回顾性研究,入组病例较少,未能将化疗联合放疗进行对比,未将EGFR基因不同突变类型进行分层分析,随访时间较短,且未对比患者的总生存时间,值得在今后的研究中不断深入分析。
[1]Jang SH.Long term therapeutic plan for patients with non-small cell lung cancer harboring EGFR mutation[J].Tuberc Respir Dis (Seoul),2014,76(1):8-14.
[2]Tang WH,Alip A,Saad M,et al.Prognostic factors in patients with non-small cell lung carcinoma and brain metastases:a Malaysian perspective[J].Asian Pac J Cancer Prev,2015,16(5):1901-1906.
[3]Nayak L,Lee EQ,Wen PY.Epidemiology of brain metastases[J]. Curr Oncol Rep,2012,14(1):48-54.
[4]Yamamoto M,Serizawa T,Shuto T,et al.Stereotactic radiosurgery for patients with multiple brain metastases(JLGK0901):a multi-institutional prospective observational study[J].Lancet Oncol,2014,15 (4):387-395.
[5]Barlesi F,Gervais R,Lena H,et al.Pemetrexed and cisplatin as first-line chemotherapy for advanced non-small-cell lung cancer (NSCLC)with asymptomatic inoperable brain metastases:a multicenter phaseⅡtrial(GFPC 07-01)[J].Ann Oncol,2011,22(11): 2466-2470.
[6]Kocher M,Soffietti R,Abacioglu U,et al.Adjuvant whole-brain radiotherapy versus observation after radiosurgery or surgical resection ofonetothreecerebralmetastases:resultsoftheEORTC 22952-26001 study[J].J Clin Oncol,2011,29(2):134-141.
[7]Rosell R,Carcereny E,Gervais R,et al.Erlotinib versus standard chemotherapy as first-line treatment for European patients with advancedEGFRmutation-positivenon-small-celllungcancer (EURTAC):a multicentre,open-label,randomised phase 3 trial[J]. Lancet Oncol,2012,13(3):239-346.
[8]Sequist LV,Yang JC,Yamamoto N,et al.Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations[J].J Clin Oncol,2013,31(27): 3327-3334.
[9]Khozin S,Blumenthal GM,Jiang X,et al.U.S.Food and Drug Administrationapprovalsummary:Erlotinibforthefirst-line treatment of metastatic non-small cell lung cancer with epidermal growth factor receptor exon 19 deletions or exon 21(L858R) substitution mutations[J].Oncologist,2014,19(7):774-779.
[10]Weber B,Winterdahl M,Memon A,et al.Erlotinib accumulation in brain metastases from non-small cell lung cancer:visualization by positron emission tomography in a patient harboring a mutation in the epidermal growth factor receptor[J].J Thorac Oncol,2011,6(7): 1287-1289.
[11]Zeng YD,Zhang L,Liao H,et al.Gefitinib alone or with concomitant whole brain radiotherapy for patients with brain metastasis from non-small-cell lung cancer:a retrospective study[J].Asian Pac J Cancer Prev,2012,13(3):909-914.
[12]Fan Y,Huang Z,Fang L,et al.A phaseⅡstudy of icotinib and whole-brain radiotherapy in Chinese patients with brain metastases from non-small cell lung cancer[J].Cancer Chemother Pharmacol, 2015,76(3):517-523.
[13]Lee HL,Chung TS,Ting LL,et al.EGFR mutations are associated with favorable intracranial response and progression-free survival following brain irradiation in non-small cell lung cancer patients with brain metastases[J].Radiat Oncol,2012,7:181.
[14]Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1) [J].Eur J Cancer,2009,45(2):228-247.
[15]Trotti A,Bentzen SM.The need for adverse effects reporting standards in oncology clinical trials[J].J Clin Oncol,2004,22(1):19-22.
[16]Miller VA,Riely GJ,Zakowski MF,et al.Molecular characteristics of bronchioloalveolar carcinoma and adenocarcinoma,bronchioloalveolar carcinoma subtype,predict response to erlotinib[J].J Clin Oncol,2008,26(9):1472-1478.
[17]Maemondo M,Inoue A,Kobayashi K,et al.Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR[J].N Engl J Med,2010,362(25):2380-2388.
[18]Olmez I,Donahue BR,Butler JS,et al.Clinical outcomes in extracranial tumor sites and unusual toxicities with concurrent whole brain radiation(WBRT)and Erlotinib treatment in patients with non-small cell lung cancer(NSCLC)with brain metastasis[J].Lung Cancer, 2010,70(2):174-179.
[19]Welsh JW,Komaki R,Amini A,et al.Phase II trial of erlotinib plus concurrent whole-brain radiation therapy for patients with brain metastases from non-small-cell lung cancer[J].J Clin Oncol,2013,31 (7):895-902.
Clinical effect of icotinib combined with radiotherapy for asymptomatic brain metastasis in patients with epidermal growth factor receptor mutant non-small cell lung cancer.
LUO Peng-hui,WANG Xiang-ping,MO Dun-chang,LIU Yan-ping,HUANG Chang-jie.Department of Oncology,the Third Affiliated Hospital of Guangxi Medical University,Nanning 530031,Guangxi,CHINA
ObjectiveTo assess the efficacy of icotinib combined with radiotherapy for asymptomatic brain metastasis(BM)in patients with epidermal growth factor receptor(EGFR)mutant non-small cell lung cancer(NSCLC). MethodsSixty-one patients diagnosed as EGFR mutant NSCLC with asymptomatic BM treated in the Third Affiliated Hospital of Guangxi Medical University from January 2012 to June 2015 were retrospectively reviewed.Twenty-three of them were treated with icotinib and brain radiotherapy(joint therapy group).Thirty-eight of them were treated with Icotinib only(targeting treatment group).The curative effect in target therapy after 1,3,5 months and every 3 months(including cranial MRI examination),and at the end of radiotherapy were evaluated.χ2test between two groups was carried out to evaluate the objective response rate(ORR),disease control rate(DCR),and the Kaplan Meier method and the Log-rank method were used for survival analysis.ResultsIn the fifth month of targeted therapy,the overall ORR and DCR in the joint therapy group were 82.6%and 95.7%,which in the targeting treatment group were 55.3%and 76.3%,showing the differences were statistically significant(P<0.05).The levels of ORR and DCR about brain metastasis in the joint therapy group were 95.7%and 100.0%,which were significantly higher than those in the targeting treatment group(55.3%and 81.6%),showing the differences were statistically significant(P<0.05).The median progression-free survival time in the joint therapy group was 14 months,but which in the targeting therapy group was 8 months,showing the differences were statistically significant(P<0.05).Regarding theⅢ~Ⅳdegree of toxicity,the incidence of fatigue, nausea and vomiting in the joint therapy group were significantly higher than those in the targeting treatment group, which could be tolerated(P<0.05).But no difference existed in the occurrence of erythra,diarrhea and myelosuppression(P>0.05).ConclusionIcotinib combined with radiotherapy could obviously improve the outcome and the median progression-free survival time of the asymptomatic BM in patients with EGFR mutant NSCLC,and side effects are tolerable.
Lung carcinoma;Adenocarcinoma of lung;Brain metastasis;Icotinib;Radiotherapy;Targeted therapy
10.3969/j.issn.1003-6350.2017.08.005
R734.2
A
1003—6350(2017)08—1219—04
2016-11-13)
广西科学研究与技术开发计划(编号:桂科攻14124004-1-21)
黄昌杰。E-mail:youyougu23@sina.com
