935例银杏叶制剂药品不良反应分析
2017-05-10刘雅楠尹先国
刘雅楠,雷 凯,尹先国,赵 丽,刘 东
(1.华中科技大学同济医学院附属同济医院药学部,湖北 武汉 430030;2.湖北省药品不良反应监测中心,湖北 武汉 430071)
935例银杏叶制剂药品不良反应分析
刘雅楠1,雷 凯1,尹先国2,赵 丽2,刘 东1
(1.华中科技大学同济医学院附属同济医院药学部,湖北 武汉 430030;2.湖北省药品不良反应监测中心,湖北 武汉 430071)
目的:分析银杏叶制剂导致不良反应(ADR)的规律及特点,为临床合理应用该药提供理论参考。方法:采用回顾性分析的方法,对2012年1月– 2014年12月期间湖北省药品不良反应监测中心数据库中收集到的935例银杏叶制剂导致的ADR报告进行分析。分别从患者的年龄与性别、用药方法与剂量、ADR发生时间、ADR累及系统/器官和临床表现等方面进行统计分析。结果:935例银杏叶制剂导致的ADR中,男女发生比例为1 : 1.35,且在各个年龄段均有分布,中老年患者中例数较多;所导致的不良反应以中枢及外周神经系统损害(23.30%)、胃肠系统损害(19.90%)、皮肤及其附件损害(17.52%)、心血管系统损害(17.01%)和全身性损害(12.92%)为主;存在超说明书规定剂量用药的现象;严重ADR 21例。结论:银杏叶制剂所致ADR的原因包括不合理的使用剂量、给药速率等,同时也与患者自身身体状况相关。建议临床在使用该药时应参考患者的不良反应史,控制使用剂量和给药速率,及时治疗已发生的不良反应,确保临床用药的安全有效。
银杏叶制剂;药品不良反应;临床应用
银杏叶制剂具有抑制血小板聚集,清除氧自由基,扩张冠脉血管、脑血管,改善脑缺血症状,保护血管内皮和提升记忆力等功能,在临床上广泛应用于冠状动脉缺血、高血压、糖尿病、冠心病、脑部及周围血流循环障碍等疾病[1]。其中银杏达莫注射液是应用最多的一类,该药是将银杏叶的有效成分加以分离、富聚后与适量的双嘧达莫精制而成的第四代银杏叶提取物复合制剂[2]。笔者对2012 – 2014年期间湖北省药品不良反应监测中心数据库中收集到的935例ADR/ADE报告进行回顾性分析,旨为促进银杏叶制剂的安全合理用药提供参考。
1 资料与方法
采用回顾性分析方法,收集2012年1月 – 2014年12月期间湖北省药品不良反应监测中心数据库中收集到的银杏叶制剂所致ADR/ADE报告,共计935例。银杏叶制剂包含银杏达莫注射剂液、银杏酮酯滴丸、银杏酮酯分散片和银杏叶片等常见制剂。对935例银杏叶制剂所致ADR/ADE报告从患者年龄与性别、家族过敏史和既往不良反应情况、ADR/ADE发生时间、ADR/ ADE累及系统/器官及临床表现等方面进行统计分析。
2 结果
2.1 患者年龄与性别分布
935例银杏叶制剂引起的ADR/ADE报告中,详细记录患者年龄和性别的共计931例,男性患者396例,女性患者535例。男女发生比为1 : 1.35,其中年龄最大的患者为91岁,最小的为8岁。本研究中,银杏叶制剂导致的ADR/ADE在各年龄段均有发生,其中50岁以上人群病例数最高,占总人数的73.90%,详见表1。
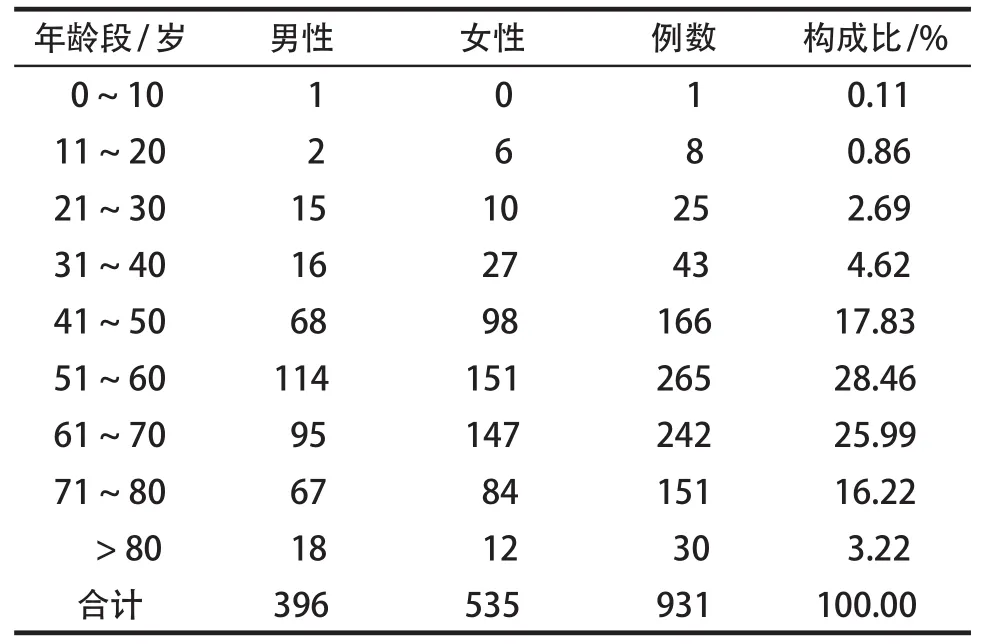
表1 ADR/ADE患者年龄和性别分布Tab 1 Distribution of patients' age and gender in ADR/ADE cases
2.2 患者既往不良反应情况和家族药品不良反应史
935例银杏叶制剂所致ADR/ADE报告中,提及了既往药品不良反应情况的439例(46.95%),提及家族药品不良反应情况的312例(33.37%),超过半数的患者既往不良反应情况不明确。
2.3 给药方法与剂量
在935例银杏叶制剂引起的ADR/ADE报告中,静脉滴注给药方式所致ADR/ADE 880例(94.12%),口服给药方式所致ADR/ADE 55例(5.88%)。其中静脉滴注药物均为银杏达莫注射液,银杏达莫注射液说明书中的用法用量为成人一次10 ~ 25 mL[3]。共208例注射给药剂量超出说明书中规定的最高剂量,占注射给药总数的23.64%。
2.4 ADR/ADE发生时间分布
在935例银杏叶制剂引起的ADR/ADE报告中,ADR/ADE发生时间在给药后2 min ~ 24 d。其中静脉滴注给药方式所致ADR/ADE多发生在30 min内(589例,66.93%),口服给药方式所致ADR/ADE主要发生在1 ~ 7 d之间(33例,60.00%),详见表2。
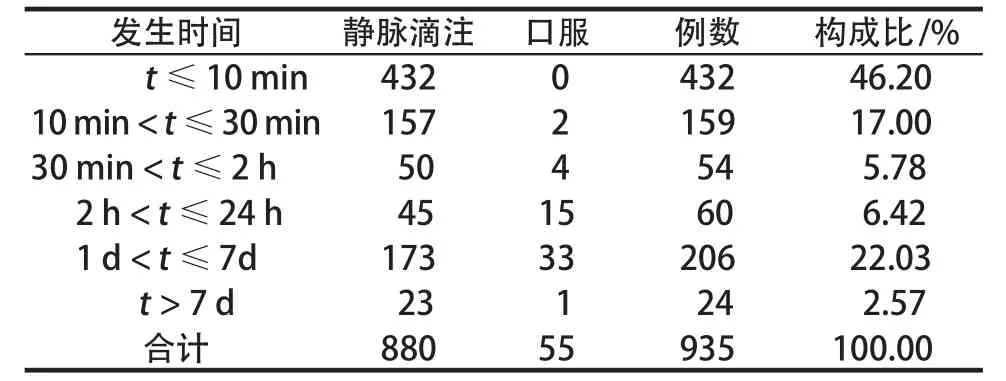
表2 ADR/ADE发生时间分布Tab 2 Distribution of occurrence time in ADR/ADE cases
2.5 ADR/ADE累及系统/器官和临床表现
按照《WHO药品不良反应术语集》将报告中涉及的ADR/ADE名称进行分类,银杏叶制剂主要引起的不良反应以中枢及外周神经系统损害(23.30%)、胃肠系统损害(19.90%)、皮肤及其附件损害(17.52%)、心血管系统损害(17.01%)和全身性损害(12.92%)为主。其中严重ADR/ADE主要表现为过敏性反应、呼吸困难、胸闷心悸等。由于部分ADR/ADE病例累及多个系统,故例次大于例数,总例次为1176例。详见表3。

表3 ADR/ADE累及系统/器官及临床表现Tab 3 Systems/organs involved in ADR/ADE and clinical manifestations
2.6 ADR/ADE的严重程度及严重不良反应
根据药品不良反应上报监测中心的评估标准,将935例银杏叶制剂引起的ADR/ADE报告进行分级,其中严重12例(1.28%),新的严重9例(0.96%),一般774例(82.78%),新的一般140例(14.98%)。
报告为严重的病例共有21例,其中7例ADR/ADE危及生命,经过停药或治疗后不良反应症状均痊愈或好转。严重的ADR/ADE报告中21例患者均使用银杏达莫注射液,其中5例超剂量使用。患者的原患疾病包括高血压、冠心病、脑梗塞、慢性胃炎、突发性耳聋等疾病,用药原因主要为扩血管和改善微循环。
2.7 关联性评价及转归
参考国内外的文献报道情况并综合分析报告表资料对药品及不良反应关联性进行评价,结果如下:肯定20例(2.14%)、很可能309例(33.05%)、可能501例(53.58%)、可能无关1例(0.11%)、无法评价2例(0.21%)、待评价102例(10.91%)。转归结果为:920例好转或痊愈,2例未好转,另有13例转归情况不明。
3 讨论
本研究结果显示50岁以上的中老年人发生ADR/ ADE的例数最多,这与银杏叶制剂主要适应证为中老年人常见病症,中老年人使用银杏叶制剂较多,同时中老年人的身体器官功能开始减退,吸收、分布、代谢和排泄功能均有改变有关,且中老年人可能由于多种疾病并存使药物在体内的过程复杂,增加了不良反应发生的风险[4-6]。银杏叶制剂说明书中指出过敏体质者、心力衰竭患者、严重心脏疾病、肝肾功能异常患者、凝血机制或血小板功能障碍患者以及有出血倾向者应慎用,故临床用药之前应详细询问并记录患者的病史、用药史以及不良反应史[7]。
从给药剂量的数据结果显示,23.64%的静脉注射给药剂量超过说明书推荐剂量,据文献[8]报道在临床上银杏达莫注射液普遍存在超说明书用药现象,最普遍的使用剂量为30 mL[9]。这样的使用方法与说明书中剂量相比,单次给药剂量过高,可能超过患者的耐受范围而诱发不良反应[10]。目前对于超说明书剂量使用银杏达莫注射液对患者是否会产生不良影响的研究并不完善,仅有小样本总量的基础研究[8]表明30 mL剂量的银杏达莫注射液在用于治疗糖尿病周围神经病变时具有良好的用药安全性,但这一结论还需要更多的研究加以证实。
银杏叶制剂所致的ADR/ADE发生时间分布较广,由表2可知,本研究中静脉注射导致的ADR/ADE在30 min内的发生率最高(66.93%)。静脉滴注给药,药物直接进入血液,血药浓度增加较快,ADR/ADE发生迅速。在本文收集的数据中,只有极少病例记录了滴注速率,但关于滴注速率和不良反应的发生已有相关报道,滴注速率过快或过慢会导致心力衰竭、肺水肿、胃肠道反应、静脉炎和中枢神经系统症状[11-12]。较高的血药浓度和不合适的滴注速率是导致静脉注射ADR/ADE发生迅速的原因之一。因此在静脉滴注初期需注意滴注速率,0 ~ 30 min内需密切监护患者的状况,并做好记录,发现不良反应后及时处理,为今后静脉滴注给药留下参考数据。口服银杏制剂导致的ADR/ADE主要发生在第一次给药后1 ~ 7 d,更需要观察长期给药后患者的用药后反应,如有不良反应症状出现及时治疗。
注射给药途径中均使用的是银杏达莫注射液,银杏达莫注射液有关说明书中指出其不良反应可为:偶有恶心、呕吐、头晕、皮肤过敏反应发生,罕见心绞痛加重[5]。本次报告中除说明书中指出的症状以外还有过敏性休克、呼吸困难、发热、寒战、心悸、多汗以及眼异常等。对于较轻的不良反应,停药后可自愈。但严重的胸闷、呼吸困难、过敏性休克等症状出现时,应立即停药,使患者半卧位并予以吸氧,再酌情选用糖皮质激素、抗组胺药进行治疗[13-14]。
银杏叶制剂作为中药制剂,成分复杂,容易引发不良反应,医护人员应重视患者的不良反应史和过敏史[15-16],采用合理的剂量和给药速率,用药过程中应密切监护患者的情况,发生不良反应后应及时采取停药或治疗措施。各级不良反应监测中心、医疗单位以及有关企业应联手对银杏叶制剂进行上市后安全性再评价,为该药的合理使用提供更多的参考。
[1] 张红梅.天然药物银杏的化学成分和药理作用[J].首都师范大学学报(自然科学版),2014,35(3):41-46,66.
[2] 周群,侯东彬.银杏达莫注射液的药理作用及不良反应研究进展[J].中国药房, 2013,24(28):2686-2688.
[3] 谢海丽.71例银杏达莫注射液不良反应分析[J].海峡药学,2011,23(4):225-226.
[4] 谢海丽,方崇波.银杏达莫注射液安全性评价分析[J].药物流行病学杂志,2010,19(6):359-360.
[5] 陆逸雁.66例银杏达莫注射液不良反应分析[J].上海食品药品监管情报研究,2011,110:43-46.
[6] 张敏红.38例银杏达莫注射液不良反应报告分析[J].中国医药导报,2013,10(2):109-110,113.
[7] 张玉萌,栗晓东,牛晓芳.银杏达莫注射剂致过敏性休克文献分析[J].中国药物应用与监测,2012,9(5):291-293.
[8] 陈清光,章丽琼,徐隽斐,等.不同剂量银杏达莫注射液治疗糖尿病周围神经病变的安全性评价[J].中医药导报,2016,22(5):66-68.
[9] 丁月霞,张雷,刘飞宇,等.38例银杏达莫注射液不良反应报告分析[J].药物流行病学杂志,2015,24(2):114-116.
[10] 李文杰,尹晓飞,范雪亮.超剂量使用中药注射剂应引起高度重视[J].中国药业,2011,20(15):65-66.
[11] 李娜.静脉输液不良事件原因分析及防范对策[J].中国医院用药评价与分析,2014,14(6):570-573.
[12] 马艳丽.静脉输液速度与药物不良反应的关系[J].中国现代药物应用,2011,5(17):119.
[13] 卢兰芳.1994 ~ 2009年银杏达莫注射液不良反应文献分析[J].中国实用医药,2010,5(12):167-168.
[14] 黄瑾,徐慧欣,蔡和平.银杏达莫注射液新的严重不良反应一例[J].药学服务与研究,2009,9(1):57-64,68.
[15] 陈伟,喻微,姚鹏,等.银杏达莫注射液主要成分指纹图谱研究[J].贵阳中医学院学报,2015,37(3):13-21.
Analysis of 935 cases of ADR/ADE reports of ginkgo biloba preparation
LIU Ya-nan1, LEI Kai1, YIN Xian-guo2, ZHAO Li2, LIU Dong1
(1. Department of Pharmacy, Tongji Hospital, Tongji Medical College, Huazhong University of Science and Technology, Wuhan 430030, China; 2. Hubei Center for ADR Monitoring, Wuhan 430071, China)
Objective:To analyze the rule and characteristics of ginkgo biloba preparation, to provide references for clinical use.Methods:Using retrospective studies, 935 cases of ADR/ADE reports collected by Hubei Center for ADR Monitoring from January 2012 to December 2014 were analyzed according to patients' age and gender, dosage and administration, occurrence time, the involvement system and manifestation, nature and causality evaluation and so on.Results:From the analysis of 935 cases of ADR/ ADE reports of ginkgo biloba preparation, the ratio of male to female was 1 : 1.35, female were more than male, and the ADR/ADE reports appeared in all age groups, especially old people; the mainly involvement system contained central and peripheral nervous system damage (23.30%), gastrointestinal system damage (19.90%), skin and appendages damage (17.52%), cardiovascular damage (17.01%), systemic damage (12.92%); off-label drug use existed in some cases. A total of 21 severe ADR/ADE cases were reported.Conclusion:The ADR/ADE reports of ginkgo biloba preparation were mainly caused by incorrect dosage, administration rate and so on. The health condition of patients also must be taken into account. To reduce the occurrence of ADR/ADE and ensure the safety of clinical use, it is necessary to refer to patients' ADR/ADE history, control the dosage of utilize and provide timely treatment for ADR in clinical use.
Ginkgo biloba preparation; ADR/ADE reports; Clinical application
R969.3
A
1672 – 8157(2017)02 – 0107 – 04
2016-10-06
2017-01-12)
刘东,男,博士生导师,主任药师,研究方向:临床药学。E-mail:ld2069@outlook.com
刘雅楠,女,硕士研究生,研究方向:临床药学。E-mail:liuyanan1037@163.com
