复方野菊花降压颗粒提取工艺及制剂工艺研究
2017-05-10齐芳芳颜美秋鲁文杰唐静月戴明珠吕圭源陈素红
齐芳芳颜美秋鲁文杰唐静月戴明珠吕圭源,陈素红,3
1.温州医科大学 浙江,温州 325035 2.浙江中医药大学 3.浙江工业大学
复方野菊花降压颗粒提取工艺及制剂工艺研究
齐芳芳1颜美秋2鲁文杰1唐静月1戴明珠1吕圭源1,2陈素红1,3
1.温州医科大学 浙江,温州 325035 2.浙江中医药大学 3.浙江工业大学
[目的]优选复方野菊花降压颗粒提取工艺和制剂工艺。[方法]以总多糖、总黄酮和浸膏收率为综合指标,采用多指标正交试验法,得出复方野菊花降压颗粒的最佳提取工艺。以成型率、吸湿率和溶化率的综合评分为评价指标,采用单因素试验优选制剂工艺。[结果]药液比(P<0.01)和提取次数(P<0.05)对提取得率有显著影响,提取时间对提取得率的影响不显著;复方野菊花降压颗粒最优提取工艺为药液比1:15,提取3次,每次加热回流提取1.5h;制剂工艺采用湿法制粒,以95%乙醇作润湿剂,干浸膏粉与糊精的配比为1:0.5,矫味剂用量为干浸膏粉的1.0%。[结论]按照合适的工艺参数,可以最大限度地提取复方野菊花中的主要成分,表明该颗粒的提取和制剂工艺合理可行,可为工业化生产提供依据。
复方野菊花降压颗粒;提取工艺;制剂工艺;正交试验;总多糖;总黄酮
复方野菊花由野菊花和黄芪等中药组成,野菊花性微寒,味苦、辛,具有清热解毒、平肝功效,是常用的降压中药[1];黄芪性微温,味甘,具有补气升阳、益卫固表等功效,具有降压作用[1]。前期实验对初步药效研究发现,复方野菊花水提物对自发性高血压大鼠(spontaneously hypertensive rats,SHR)具有良好的降压效果。现代研究表明,野菊花总黄酮能扩张外周血管[2],降低SHR的收缩压和舒张压,其降压的主要药效物质基础为黄酮类化合物[3];而黄芪多糖可舒张血管,保护血管内皮细胞[4],可能为黄芪降压的主要有效成分。故本文拟通过以总多糖、总黄酮为考察指标对复方野菊花提取工艺进行多指标综合优化,并对颗粒剂制备工艺进行研究,为后期进一步开发成辅助降血压功能的保健食品及药品提供基础。
1 仪器、药材与试剂
Mili-QAcademic超纯水仪(美国Millipore公司);AR2130 OHAUS电子天平(美国奥豪斯,万分之一);AG135 METTLER ToleDo电子天平(瑞士梅特勒,十万分之一);美国Lambda45紫外分光光度计(Perkin-Elmer);LXJ-IIB低速大容量多管离心机(上海安亭科学仪器厂);KQ500DE型超声波清洗器(昆山市超声仪器有限公司)。野菊花(150401,安徽);黄芪(生)(150402,甘肃);甲醇、乙腈色谱纯;D-无水葡萄糖(110833-200904,中国药品生物制品检定所);芦丁(100080-200707,中国药品生物制品检定所)。其余试剂均为分析纯。
2 方法与结果
2.1 提取工艺的优化设计 本文设计在粉碎度相同的条件下,考虑水料比(A)、煎煮次数(B)、煎煮时间(C)为因素,选择L9(34)正交试验表,采用总多糖、总黄酮和干浸膏收率的综合评分为考察指标,优选复方野菊花最佳提取工艺。因素水平见表1。

表1 实验因素水平表Tab.1 The factor and level of experiment
2.2 紫外-可见分光光度法测定复方野菊花供试品溶液中多糖含量
2.2.1 葡萄糖对照品溶液的制备 取干燥至恒重的葡萄糖粉末,精密称定,加水溶解后,定容至刻度,摇匀即得葡萄糖对照品溶液(0.1mg·mL-1)。
2.2.2 供试品溶液的制备 称取复方野菊花中各味药材共24g,加入15倍水回流提取1.5h,提取3次,滤过,合并提取液,提取完成后将药液经过减压浓缩,定容到200mL。精密量取2mL,置15mL离心管中,精密加入80%乙醇10mL,摇匀,冷藏1h,取出,离心(4000r/min)20min,弃去上清液(必要时滤过)。沉淀加热水溶解,转移至50mL量瓶中,放冷,加水至刻度,摇匀,即得。
2.2.3 标准曲线的制备 精密量取标准溶液0.4mL、0.6mL、1.0mL、1.2mL、1.4mL共6份,分别置于具塞试管中,加蒸馏水至2mL,再加5%苯酚溶液1.0mL,摇匀,迅速加浓硫酸5mL,迅速摇匀,放置5min;置沸水浴加热20min,取出,冰水浴中冷却10min,迅速冷却至室温。另取2mL蒸馏水做同上平行操作,作为空白对照。用可见-紫外分光光度计在波长为200~700nm处扫描,在488nm处有最大吸收峰,见图1。故于488nm波长处测定吸收度,绘制标准曲线,所得标准曲线为:Y=0.05X-0.0559(R2=0.9993)[其中Y为吸光度,X为葡萄糖浓度(μg·mL-1)]。
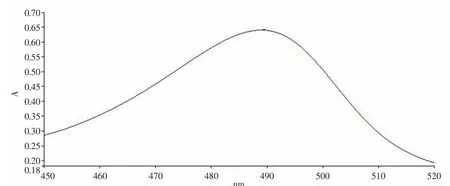
图1 葡萄糖标准品溶液波长扫描图Fig.1 The spectrum of glucose standards solution
2.2.4 含量测定 称取复方野菊花中各味药材,依照正交试验设计因素水平表进行试验。加入水回流提取,滤过,合并提取液,提取完成后将每份药液经过减压浓缩,定容到200mL。精密量取2mL,置15mL离心管中,精密加入80%乙醇10mL,摇匀,冷藏1h,取出,离心(4000r/min)20min,弃去上清液(必要时滤过)。沉淀加热水溶解,转移至50mL量瓶中,放冷,加水至刻度,摇匀,即得。吸取供试品溶液0.5mL,按“2.2.3标准曲线的制备”项下自“加蒸馏水至2.0mL”依次操作,测定吸收度。根据标准曲线计算出药材中粗多糖的量。见表2。
2.2.5 精密度测定 精密吸取对照品溶液0.8mL,置于10mL试管中,其余按“标准曲线的制备”项下自“加蒸馏水至2.0mL”依次操作,测定吸收度,平行测定6次。RSD为0.08%,表明实验精密度良好。
2.2.6 稳定性测定 精密吸取供试品溶液1mL,置于10mL试管中,按“标准曲线的制备”项下自“加蒸馏水至2.0mL”依次操作,分别于0、10、20、30、40、50、60min后测定吸光度。RSD为1.32%,表明显色后样品在60min内稳定。
2.2.7 重现性测定 同份样品平行处理5份,按“标准曲线的制备”项下自“加蒸馏水至2.0mL”依次操作,测定吸收度。RSD为2.77%,说明本方法重现性良好。
2.2.8 加样回收率 精密量取已知多糖含量的供试品溶液10mL,分别精密加入葡萄糖对照品溶液4.5mL,精密移取1mL置10mL试管中,平行处理6份,按“标准曲线的制备”项下自“加蒸馏水至2.0mL”依次操作,测定吸收度。回收率(%)=(实验测值-样品所含被测成分量)/加入纯品量×100%。平均回收率为104.79%,RSD为2.37%。
2.3 采用紫外-可见分光光度法测定复方野菊花供试品中总黄酮含量
2.3.1 芦丁对照品溶液的配制 取干燥至恒重的芦丁对照品,精密称定,加70%乙醇溶解后,定容至刻度,摇匀即得芦丁对照品溶液(0.2mg·mL-1)。
2.3.2 供试品溶液的配制 称取复方野菊花中各味药材共24g,加入15倍水回流提取1.5h,提取3次,滤过,合并提取液,提取完成后将药液经过减压浓缩,定容到200mL。分别稀释5倍后作为供试品溶液。
2.3.3 标准曲线的制备 精密吸取芦丁对照品溶液0mL、1.0mL、1.5mL、2.0mL、3.0mL、3.5mL、4.0mL共7份,分别置于具塞试管中,加5%亚硝酸钠溶液0.4mL,摇匀后放置6min,加10%硝酸铝溶液0.4mL摇匀,放置6min,加4%氢氧化钠溶液4mL,振摇,加70%乙醇至10mL,摇匀后放置15min,即得。用可见-紫外分光光度计在波长为200~700nm处扫描,两者均在500nm处有最大吸收峰,见图2。故于500nm波长处测定吸收度,绘制标准曲线,所得标准曲线为:Y=0.0129X-0.0592(R2=0.9992)[其中Y为吸光度,X为芦丁浓度(μg·mL-1)]。
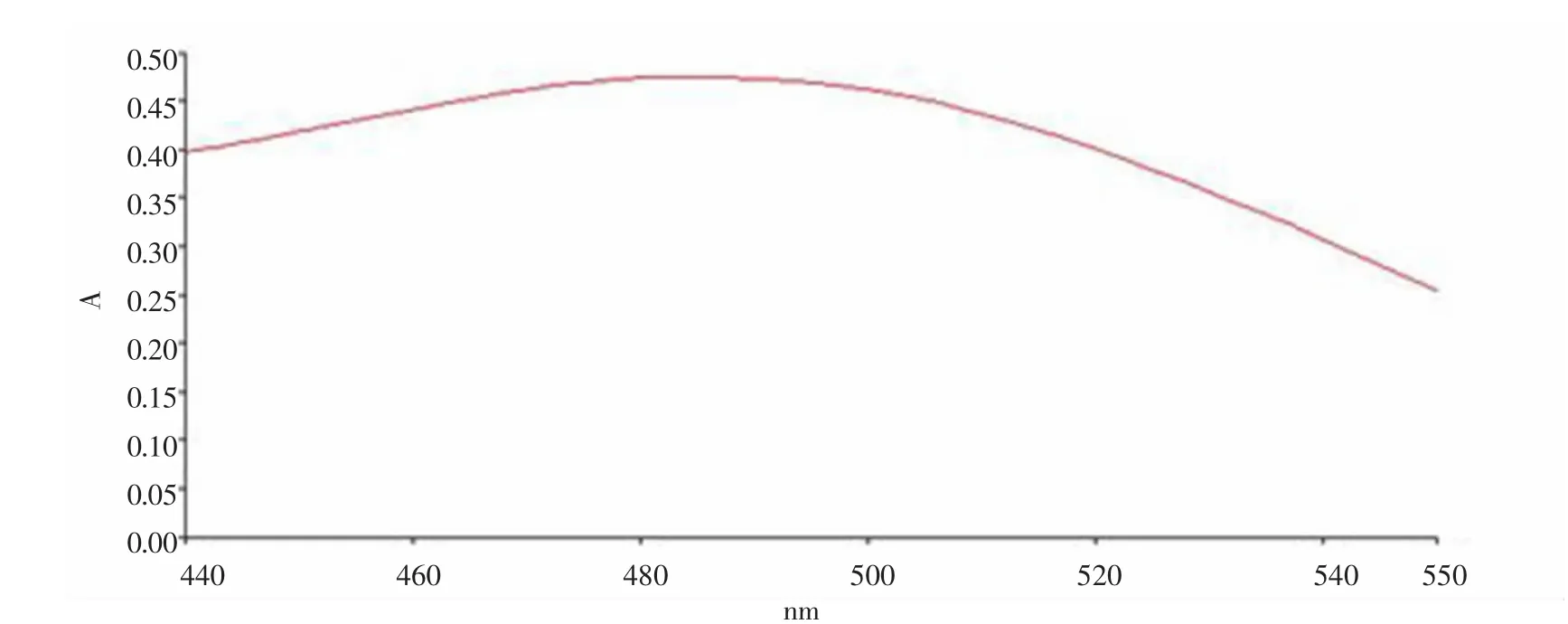
图2 芦丁标准品溶液波长扫描图Fig.2 The spectrum of Rutin standard solution
2.3.4 含量测定 称取药材,依照正交试验设计因素水平表进行试验。加入水回流提取,滤过,合并提取液,提取完成后将每份药液经过减压浓缩,定容到200mL。分别稀释5倍后作为供试品溶液。精密吸取样品液1mL,按“2.3.3标准曲线的制备”操作,测定吸收度。根据标准曲线计算出药材中黄酮的量。见表2。
2.3.5 精密度测定 精密吸取芦丁对照品溶液2mL,置于10mL试管中,其余操作按标准曲线制备操作,测定吸光度,平行测定6次。结果表明,RSD为0.088%,表明实验精密度良好。
2.3.6 稳定性测定 精密吸取供试品溶液1mL,置于10mL试管中,其余操作按“2.3.3标准曲线的制备”操作,分别于0、10、20、30min后测定吸光度。RSD为0.60%,表明实验在30min内测定稳定。
2.3.7 重现性测定 同份样品平行处理6份,其余操作按“2.3.3标准曲线的制备”操作,测定吸光度。RSD 为2.16%,说明本方法重现性良好。
2.3.8 加样回收率 精密量取已知黄酮含量的供试品溶液4mL,精密加入芦丁对照品溶液5mL,精密移取1mL置10mL试管中,平行处理5份,按“2.3.3标准曲线的制备”操作,测定吸光度。平均回收率为103.74%,RSD为2.82%。
2.4 干浸膏收率测定 精密吸取定容后供试品溶液10mL,置已干燥至恒重的蒸发皿中,水浴蒸干,于105℃干燥3h,置干燥器中冷却30min,迅速称定重量,计算干浸膏收率,以药材干重计。干浸膏得率=[(M2-M1)×V]/K×10×100%。其中M1为干燥至恒重的蒸发皿重量,M2为干浸膏与蒸发皿总重量,V为正交试验各样品溶液定容体积,K为投料药材重量。见表2。
2.5 正交试验结果 按照L9(34)正交设计表的条件进行试验,分别测定总多糖、总黄酮的含量和浸膏得率。采用信息熵权重分析法[5]确定多糖含量(X)(%)、总黄酮含量(Y)(%)和浸膏得率(Z)(%)的权重系数分别为0.5904,0.261,0.1486。根据各指标的权重,计算多属性综合评价指标,对正交试验数据进行综合分析。综合评分=0.5904X/5.0487+0.261Y/2.2762+ 0.1486Z/35.71。见表2、表3。
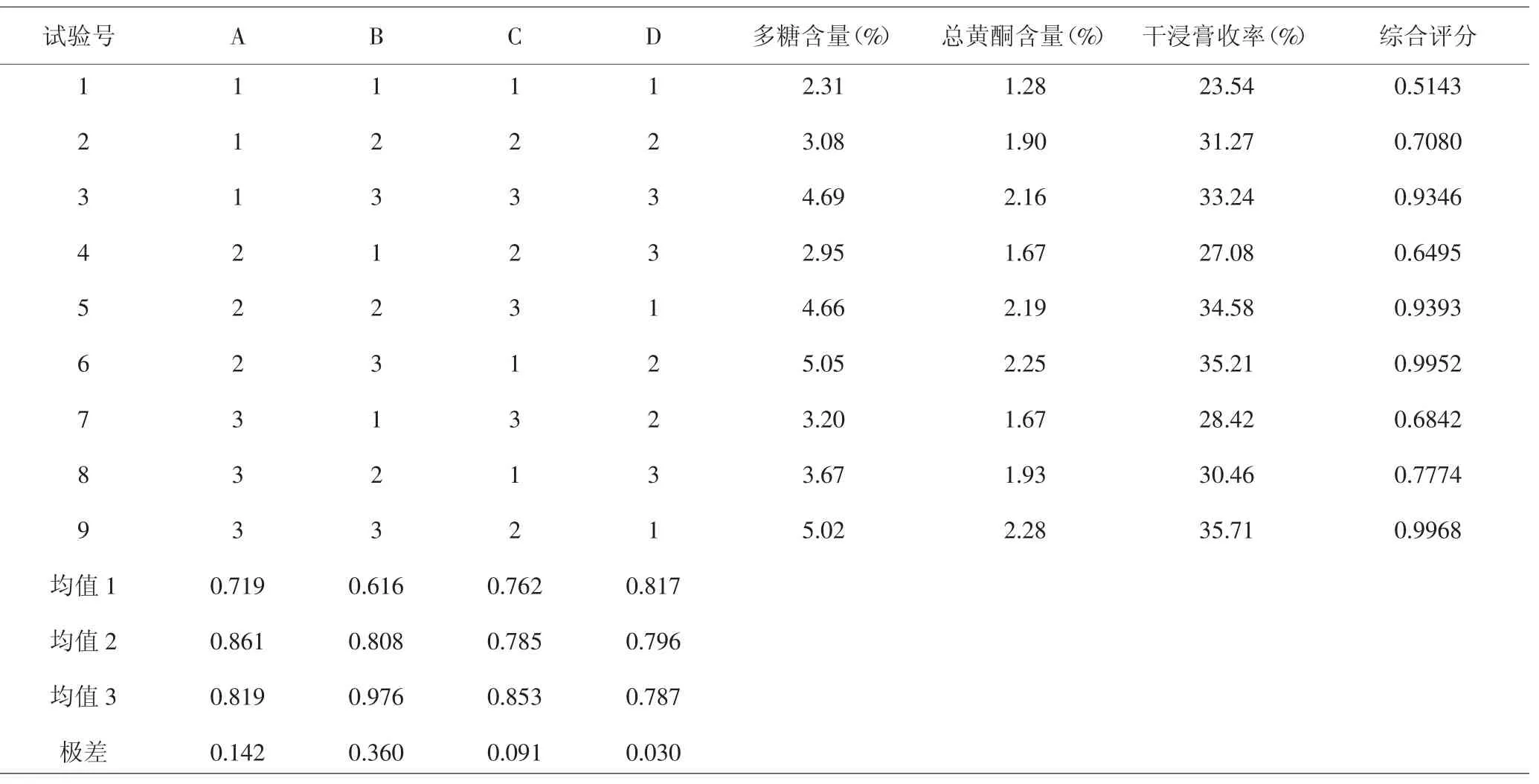
表2 水提工艺正交试验设计表及结果Tab.2 Design and result of orthogonal test for water extraction
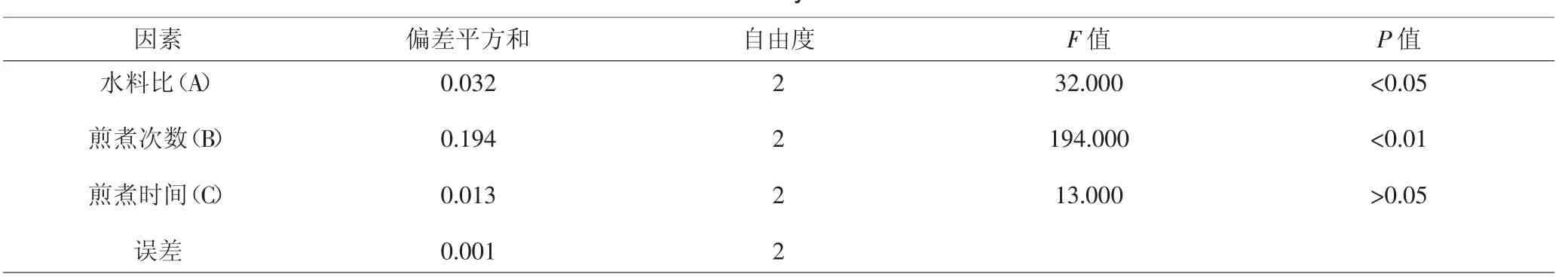
表3 有效成分提取量方差分析表Tab.3 Variance analysis of the content
直观分析表明,以综合评分为标准,在所选因素水平范围内,各因素作用主次顺序为 B>A>C。方差分析表明,A(水料比)和B(煎煮次数)为主要影响因素,具有显著性(P<0.05),最终确定最佳提取工艺为A2B3C3,即水料比为1:15,煎煮次数为3次,每次为1.5h。
2.6 验证实验 按确定的提取工艺进行平行5次验证实验。测得总多糖含量为4.93%,总黄酮含量为2.05%,干浸膏收率为34.50%;RSD分别为2.57%、2.08%、2.77%。验证实验结果表明该优选工艺稳定、可靠。
2.7 复方野菊花降压颗粒制备工艺考察
2.7.1 颗粒的制备 将干浸膏粉过80目筛,分别和不同辅料按1:1比例混匀并研细,加入润湿剂制软材,使用18目筛制粒,55℃烘干通风干燥1h,过18目筛整粒,即得。
2.7.2 辅料的筛选 选择可溶性淀粉、糊精和微晶纤维素这三种辅料,以制得颗粒的成型率、吸湿率和溶化率为评价指标,设定总分为100分,溶解性、成型率各占25分,吸湿性占50分,进行综合评分,筛选最优的辅料。
2.7.3 成型率的测定 将制备得到的颗粒称重后,依次通过一号筛和五号筛,收集能通过一号筛而不能通过五号筛的颗粒并称重,计算制得颗粒的成型率。成型率=(过筛后能通过一号筛而不能通过五号筛的颗粒总重量/过筛前颗粒重量)×100%。成型率分值=(成型率值/最大成型率值)×25。
2.7.4 吸湿百分率的测定 取2.7.2中制得的已干燥至恒重的三种颗粒,置于扁形称量瓶中(颗粒的平铺厚度约为2mm),精密称定,将其放入底部盛有NaCl过饱和溶液的干燥器中(干燥器已提前放置于25℃的恒温培养箱中恒温24h,此时其内部的相对湿度为75%)并于25℃保存,24h后称定,计算颗粒的吸湿百分率,以吸湿率0%为50分,对各处方进行扣分,计算各处方分值。吸湿百分率=(颗粒吸湿后的重量-颗粒重量)/颗粒重量×100%。
2.7.5 溶化率的测定 精密称量颗粒0.5g加入干燥至恒重的15mL离心管中,精密加入沸水10mL,搅拌振荡5min,5000r/min离心10min,弃去上清液,在80℃将残渣烘干至恒重,精密称定,计算溶化率。溶化率=溶化颗粒重/总颗粒重×100%。
2.7.6 综合评价 对各处方成型率、吸湿百分率、溶化率三个指标的得分加和汇总进行综合评价,结果见表4。由综合评分结果可知,干浸膏粉与糊精混匀后制得颗粒的的分值最高,故选择糊精作为辅料。

表4 各处方成型率、吸湿百分率、溶化率综合评价Tab.4 The comprehensive evaluation of forming rate,moisture rate and melting rate of all prescriptions
2.7.7 辅料用量的考察 通过单因素试验,对药粉与糊精以不同配比所制得颗粒的成型率、吸湿率和溶化率(24h)进行考察,确定最优的药辅比。见表5。
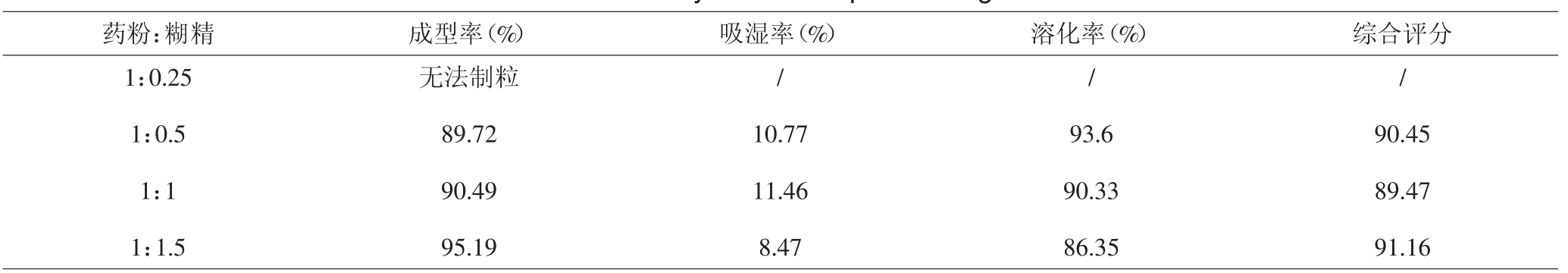
表5 辅料用量考察Tab.5 Study on the excipient dosage
从上表中结果可知,当药粉与糊精的比例在1: 0.25无法制粒,其他配比所制颗粒的成型率、吸湿率和溶化率的结果均较好,考虑每日用量不宜过大,故选择药粉与加入的糊精用量比为1:0.5。
2.7.8 润湿剂的筛选 分别对不同浓度乙醇的制粒情况进行考察,结果见表6。从制粒情况、颗粒性状以及成型率这三个方面综合考虑,宜选用95%的乙醇作为润湿剂来进行制粒。
2.7.9 矫味剂的筛选 阿斯巴甜的用量分别为干浸膏粉的0.5%、1.0%、1.5%、2.0%,实验结果表明当加入阿斯巴甜1.0%时已能起到较好的矫味作用。
3 讨论
3.1 提取工艺评价指标的确定 复方野菊花以野菊花、黄芪为主药,功能清泻肝火,用于防治高血压。文献报道野菊花总黄酮能扩张通过皮下注射丙酸睾酮建立的高血压模型大鼠的外周血管[2],能显著降低SHR的收缩压和舒张压[3];黄芪多糖可升高NO含量和降低ET含量对高血压病患者血清导致的血管内皮细胞损伤有保护作用[4];提示野菊花总黄酮、黄芪多糖是其降压的主要成分。

表6 乙醇浓度的考察Tab.6 Study on the ethanol concentration
中药传统最常用的提取方法是水煎煮法。复方野菊花降压的主要成分为多糖和黄酮类化合物,水是一种强的极性溶剂,多糖和天然黄酮苷类是亲水性成分,易溶于水。结合实验前期初步药效研究发现,复方野菊花水提物对SHR具有良好的降压效果,故本实验拟采用总多糖和总黄酮为指标优选其水提工艺,充分提取其有效成分,确保其降压效果。
本实验根据各药所含主要活性成分的理化性质,筛选符合工艺实际的多个指标进行实验,较用某种单一成分的含量进行提取工艺控制更为科学合理[6]。采用多指标信息熵权重分析法,结合正交设计优化制备工艺,兼顾了评价指标的全面性及各指标间的差异性,使确定的提取工艺参数更客观、合理。
3.2 制粒工艺及辅料的选择 颗粒剂一般采用湿法制粒、干法制粒和喷雾制粒等方法。湿法制粒的产物具有外形美观、流动性好、耐磨性较强、压缩成形性好等优点,在医药工业中的应用最为广泛。干浸膏本身吸湿性较强,粘度较大,制粒较困难,需加入辅料来改善其吸湿率和成型率。本实验采用湿法制粒进行颗粒剂的制备工艺。结合文献及预实验结果,选择可溶性淀粉、糊精和微晶纤维素这三种辅料,以制得颗粒的成型率、吸湿率和溶化率为评价指标,进行综合评分,结果表明糊精吸湿性小,溶化率高,成型率好,故选取糊精为辅料。最佳制剂工艺为将干浸膏粉和糊精按1:0.5比例混匀并研细,加入95%乙醇制软材,使用18目筛制粒,55℃烘干通风干燥1h,过18目筛整粒,即得。参考文献
[1] 国家药典委员会.中国人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:302-303,314-315. National Pharmacopoeia Commission.Pharmacopoeia of the People's Republic of China(a)[M].Beijing:China Medical Science and Technology Press,2015:302-303,314-315.
[2] 刘伟,张倩,何宏媛,等.益母草,野菊花单方与复方水煎液对高血压模型大鼠降压作用的比较[J].山东中医药大学学报,2015,39(6):555-556. LIU Wei,ZHANG Qian,HE Hongyuan,et al.Comparison of Antihypertensive Effect of LeonurusJaponicus Decoction,Wild Chrysanthemum Decoction and Compound Decoction of Them on Hypertensive Rats[J].Journal of Shandong University of Traditional Chinese Medicine,2015,39 (6):555-556.
[3]LV G Y,ZHANG Y P,GAO J L,et al.Combined antihypertensive effect of luteolin and buddleoside enriched extracts in spontaneously hypertensive rats[J].Journal of ethnopharmacology,2013,150(2):507-513.
[4] 李眺,陈利国,李权,等.川芎嗪配伍黄芪多糖对血管内皮细胞的保护作用[J].中华中医药杂志,2011,26(11):2672-2675. LI Tiao,CHEN Ligun,LI Quan,et al.The protective effects of Tetramethylpyrazine(TMP)combined with Astragalus Polysaccharides(APS)on vascular endothelial cells (VECs)[J].Chinese Archives ofTraditionalChinese Medicine,2011,26(11):2672-2675.
[5] 吴静,吴晓燕,高忠长.客观多因素权重分配方法及其应用[J].上海航天,2011,28(3):60-63. WU Jing,WU Xiaoyan,GAO Zhongchang.Objective Multi-Factor Weight Allocation Method and Its Application[J].Aerospace Shanghai,2011,28(3):60-63.
[6] 单丽芳,杨红梅,曹蕾,等.多指标综合评分法优选参芪复方颗粒提取工艺及其热稳定性考察[J].中国实验方剂学杂志, 2016,22(7):24-27. SHAN Lifang,YANG Hongmei,CAO Lei,et al.Optimization of Extraction Process of Shenqi Compound Granules with Multi-index Comprehensive Evaluation Method and Investigation of Its Thermal Stability[J].Chinese Journal of Experimental Traditional Medical Formulae,2016,22(7): 24-27.
Optimization of the Extraction Technology and Preparation Process of Flos Chrysanthemi Indicigranules for Antihypertension
QI Fangfang1,YAN Meiqiu2,LU Wenjie1,et al 1.Wenzhou Medical College,Zhejiang(325035),China;2.Zhejiang Chinese Medical University
[Objective]To optimize extraction technology and preparation process of Compound Flos Chrysanthemi Indici granuls.[Method]L9(34)orthogonal test was adopted to achieve the best extraction technology of Compound Flos Chrysanthemi Indici granules with the content of polysaccharides,flavonoids and extract yield as the index.Furthermore granulating conditions were studied and optimizd with the indexes of the molding rate,the water absorption rate and the melting rate.[Result]The liquid ratio(P<0.01)and the extraction times(P<0.01)had a significant effect on the extraction yield,the extraction time had little effect on the extraction yield.The optimized extraction technology was to extract 3 times for 1.5h each times with 15 fold water;preparation process as follows:extraction powder:adjuvant was mixed with the portion of 1:0.5 with 95%alcohol as wetting agent and 1.0%sweeting agent was added.[Conclusion] According to the process parameters,the main components of Compound Flos Chrysanthemi can be fully extracted,it shows the extraction technology and granulation process are reasonable and feasible,this research can provide the basis for industrial production.
Compound Flos Chrysanthemi Indici granules;extraction technology;preparation process;orthogonal test;polysaccharides;flavonoids
R282.71
A
1005-5509(2017)04-0323-06
10.16466/j.issn1005-5509.2017.04.017
2016-11-17)
国家重大新药创制专项(2011ZX09102-011-07);浙江省卫生高层次创新人才培养工程项目(浙卫[2010]190 号);浙江省重点实验室(2012E10002)
Fund projects:National major new drug creation special(2011ZX09102-011-07);Zhejiang Province high-level health innovation talent training project(Zhejiang Wei[2010]190);The Key Laboratory of Zhejiang Province(2012E10002)
陈素红,E-mail:chensuhong@aliyun.com
