两种曼尼希碱缓蚀剂的缓蚀性能
2017-05-09唐甜甜李克华胡琳莉石东坡
唐甜甜,李克华,胡琳莉,石东坡
(长江大学 化学与环境工程学院,荆州 434023)
两种曼尼希碱缓蚀剂的缓蚀性能
唐甜甜,李克华,胡琳莉,石东坡
(长江大学 化学与环境工程学院,荆州 434023)
采用甲醛/苯甲醛、苯乙酮和水合肼为原料分别合成了AJ和BJ两种曼尼希碱缓蚀剂。通过静态挂片失重法、电化学测试法等方法研究了在15% HCl(质量分数)溶液中,这两种缓蚀剂对N80钢的缓蚀性能。结果表明:在15%的HCl溶液中,AJ和BJ缓蚀剂对N80钢具有良好的缓蚀作用,且BJ缓蚀剂的缓蚀效果要优于AJ缓蚀剂的;两种缓蚀剂均为阳极型缓蚀剂,都能自发吸附在N80钢表面,其行为均符合Langmuir吸附等温式。
缓蚀剂;曼尼希碱;吸附;缓蚀机理
酸化是油田提高油井采收率的一种常用方法,但酸液的注入会造成金属管线的严重腐蚀,且溶蚀Fe3+进入地层会产生永久损害[1]。为了减缓酸液对金属的腐蚀,在油井酸化作业时,通常采用向酸液中添加缓蚀剂,这种方法既简单且有效[2]。使用最为普遍的酸化缓蚀剂均是有机化合物,其中含氮化合物占据着较大的比例,如曼尼希碱缓蚀剂。水合肼中含有两个N原子,N原子能够提供孤对电子,故N原子上的氢极易被其他基团所取代,引入非极性基团后,缓蚀剂会在金属表面生成一层疏水性保护层,即与金属表面配位形成金属表面配合物[3],从而起到隔离作用[4]。本工作以甲醛/苯甲醛、苯乙酮和水合肼为原料分别合成了AJ、BJ两种曼尼希碱缓蚀剂,并采用静态挂片失重法、电化学法、分子动力学模拟法深入研究了所合成缓蚀剂的缓蚀特性及其吸附机理。
1 试验
1.1 试验材料、试剂和仪器
试验材料为N80钢,其主要化学成分(质量分数)为0.35% C,0.33% Si,1.65% Mn,0.02% P,0.015% S,0.14% V,余量Fe。腐蚀浸泡试样尺寸为40 mm×13 mm×2 mm(表面积12.52 cm2)。电化学试样的工作面为13 mm×2 mm,其非工作面用环氧树脂封装。所有试样用100~1 000号砂纸逐级打磨至表面光亮,然后依次用丙酮、无水乙醇清洗,冷风吹干,放入干燥器备用。
主要试剂:甲醛、苯甲醛、苯乙酮、水合肼、浓盐酸、无水乙醇和丙酮等,均为分析纯。
主要仪器:恒温水浴锅、CHI600E型电化学工作站、分析天平(精度0.1 mg)、移液管、游标卡尺(精度0.02 mm)、镊子、脱脂棉、滤纸等。
1.2 缓蚀剂合成
在装有电动搅拌器、回流冷凝管和温度计的三口烧瓶中依次加入一定计量的甲醛/苯甲醛、苯乙酮、水合肼,其中醛/胺物质的量比为3.1、酮/胺物质的量比为3.0,再加入少量乙醇做溶剂,缓慢滴加浓盐酸将pH调为2,在给定温度下加热搅拌,反应一定时间后所得液体即为曼尼希碱缓蚀剂,其产率分别为76%和78%。AJ、BJ缓蚀剂的合成反应方程式见式(1)和式(2)。
1.3 缓蚀性能测试
1.3.1 静态挂片失重法
腐蚀浸泡试验采用静态挂片失重法并参照AJ缓蚀剂:
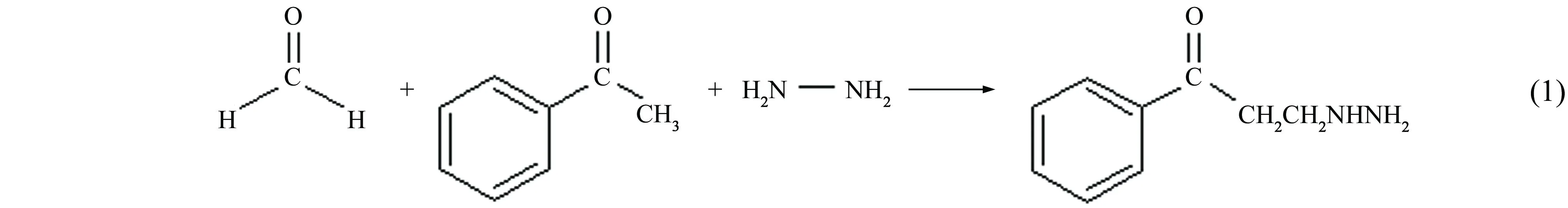
BJ缓蚀剂:
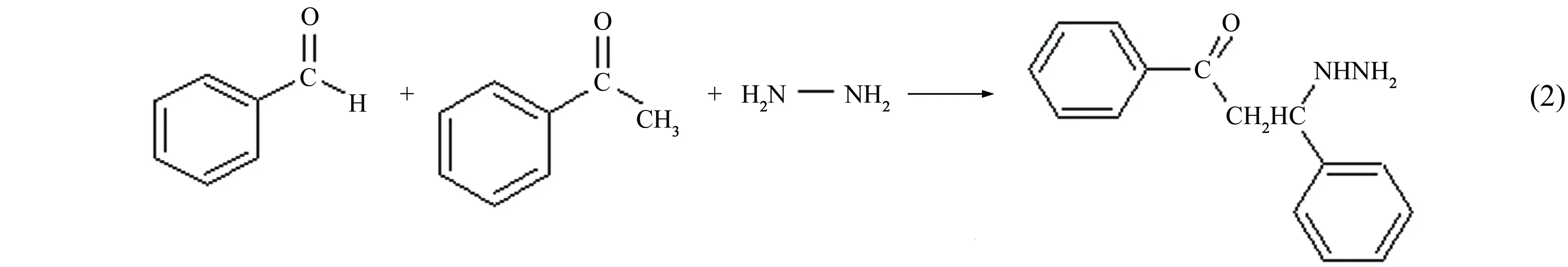
SY/T 5405-1996《酸化用缓蚀剂性能试验方法及评价指标》标准进行。腐蚀介质为15% HCl(质量分数,下同)溶液,向溶液中分别加入AJ、BJ两种缓蚀剂使其质量分数分别为0.3%,0.5%,0.7%,1%。试验在常压,60 ℃下进行,试验时间为4 h。试验后,按式(3)计算腐蚀速率,按式(4)计算缓蚀率。
(3)
式中:v为腐蚀速率,g·m-2·h-1;w1为钢片腐蚀前的质量,g;w2为钢片腐蚀并除去腐蚀产物后的质量,g;A为钢片在腐蚀介质中的总面积,mm2;t为腐蚀时间,h。
(4)
式中:η为缓蚀率,%;v0,v分别为未加缓蚀剂和添加缓蚀剂时钢片的腐蚀速率,g·m-2·h-1。
1.3.2 电化学测试法
电化学测试在辰华CHI660E电化学工作站上进行。测试采用三电极体系[5]:工作电极为N80钢,辅助电极为铂电极,参比电极为饱和甘汞电极。腐蚀介质为含缓蚀剂的15% HCl溶液,试验温度为25 ℃。极化曲线扫描范围为-300~-600 mV(相对开路电位),电位扫描速率为5 mV·s-1。电化学阻抗谱测量频率为0.1~100 kHz,交流激励信号幅值为5 mV。
1.3.3 动力学吸附模拟法
选取晶体Fe(001)晶面为吸附表面,表面体系厚度为6层共计792个Fe原子。模拟时使用Materials Studio 7.0软件包中COMPASS力场对体系进行优化,正则系统(NVT)的分子动力学(MD)模拟通过Discover模块完成[6]。根据式(5)计算缓蚀剂分子在钢铁表面上的吸附能。
(5)
式中:Einteration为相互作用能;Eabsorption为吸附能;Esurface为未吸附分子的金属表面能量;Emolecule为自由分子总能量;Etotal为金属表面体系和分子的总能量。
2 结果与讨论
2.1 失重法测试结果
由图1可知,随着酸性腐蚀介质中缓蚀剂含量的增加,N80钢的腐蚀速率逐渐减小,当AJ、BJ缓蚀剂的质量分数达到1%时,腐蚀速率分别减小到0.686 2 g·m-2·h-1和0.293 8 g·m-2·h-1,相应的缓蚀率分别为93.58%和97.25%,均优于SY/T 5405-1996《酸化用缓蚀剂性能试验方法及评价指标》中的一级标准,且BJ缓蚀剂的缓蚀效果要优于AJ缓蚀剂的。
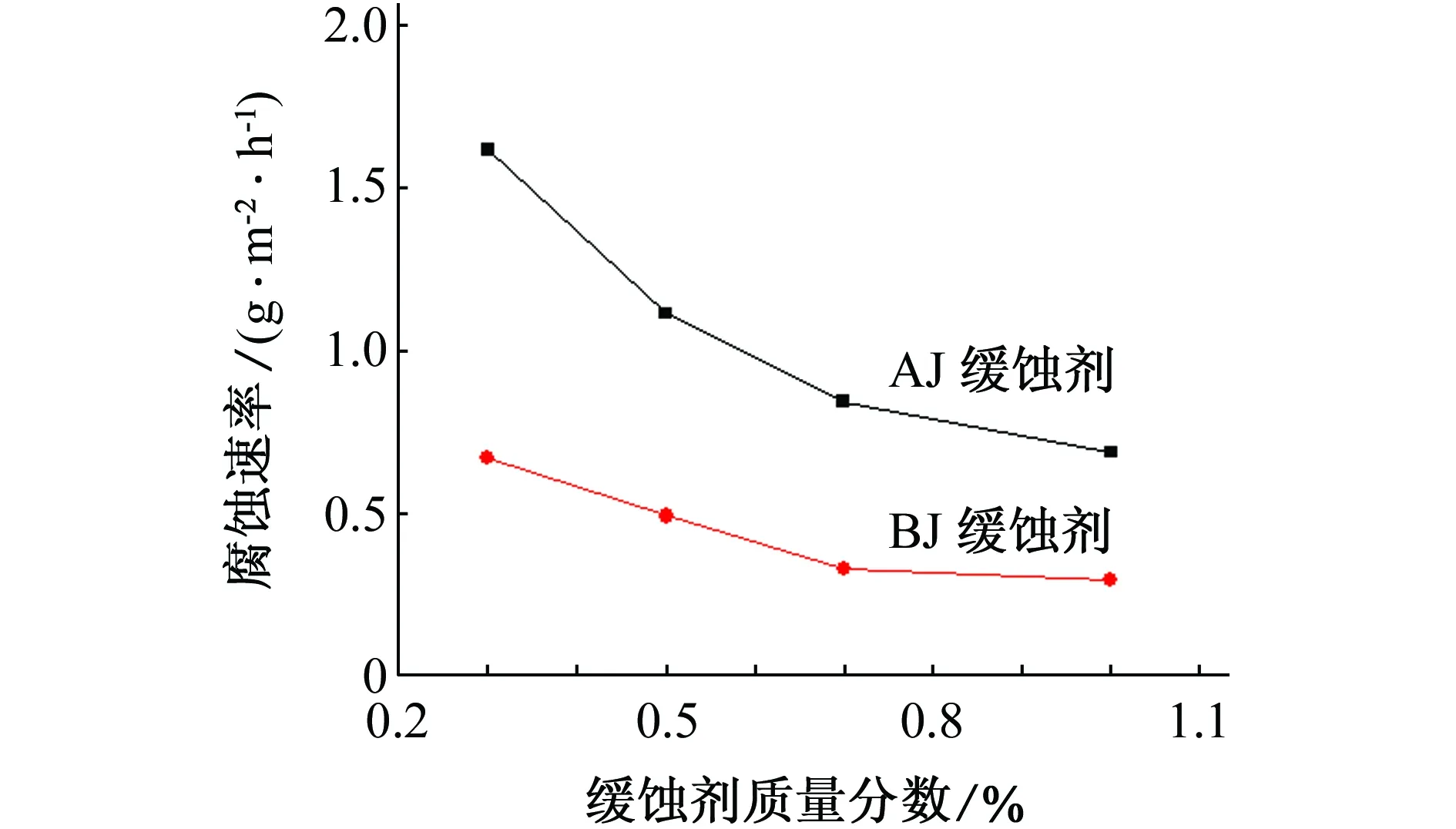
图1 N80钢在缓蚀剂含量不同的15% HCl 溶液中的腐蚀速率Fig. 1 Corrosion rates of N80 steel in 15% HCl solution with different concentrations of inhibitors
2.2 电化学测试结果
2.2.1 极化曲线
图2为N80钢在缓蚀剂含量不同的15% HCl溶液中的极化曲线。对极化曲线进行拟合,得到的相关电化学参数见表1。
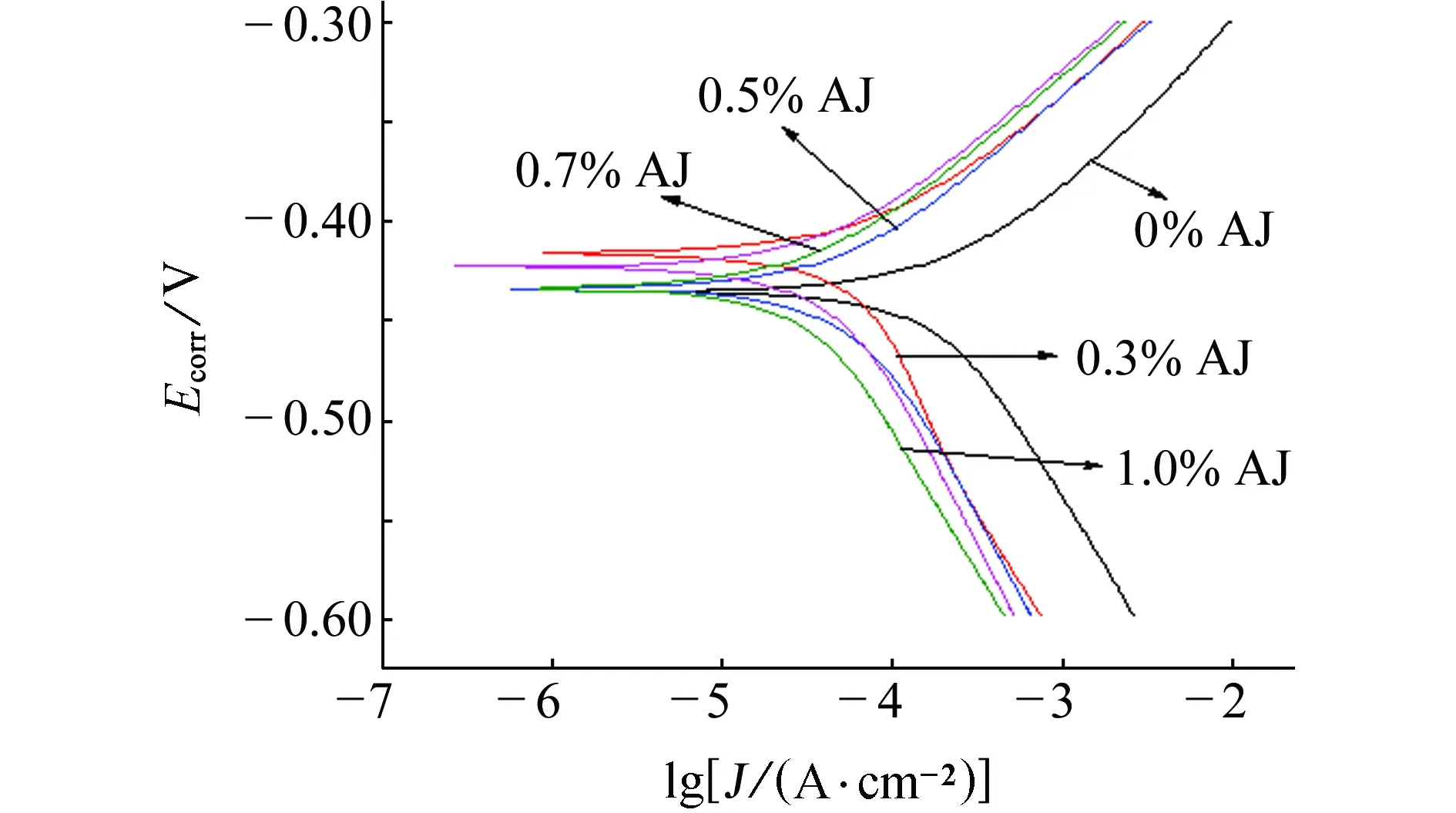
(a) AJ
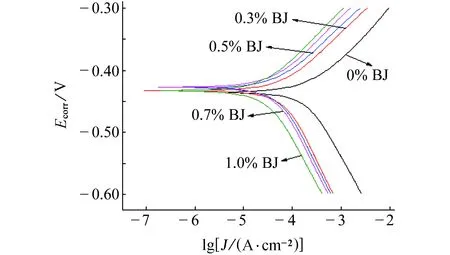
(b) BJ图2 N80钢在缓蚀剂含量不同的15% HCl溶液中 的极化曲线Fig. 2 Polarization curves of N80 steel in 15% HCl solution with different concentrations of inhibitors AJ (a) and BJ (b)表1 图2中极化曲线的拟合结果Tab. 1 Fitted results of polarization curves in figure 2
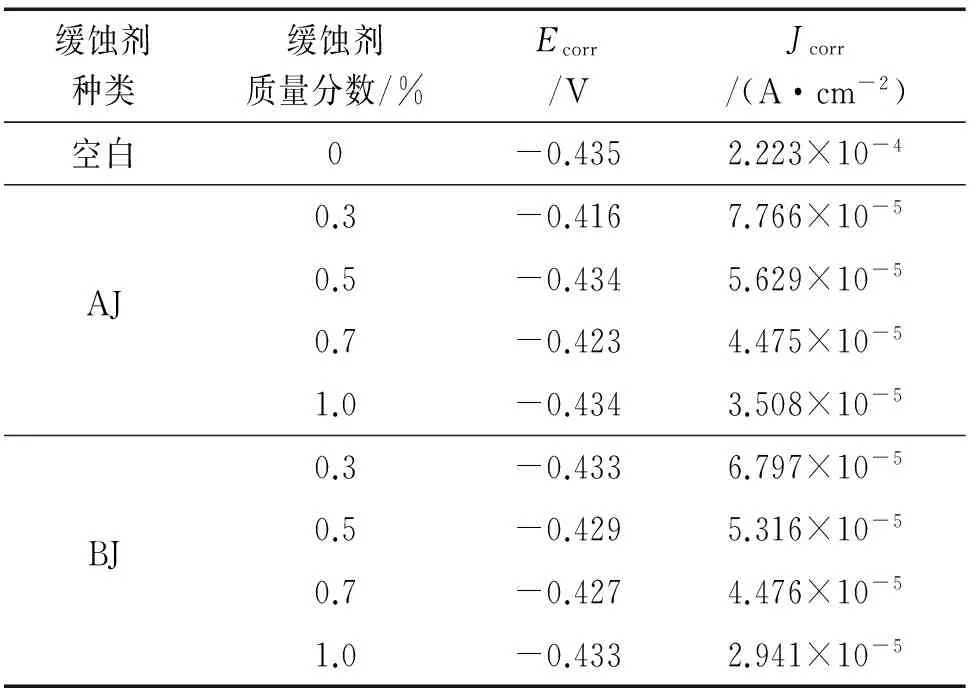
缓蚀剂种类缓蚀剂质量分数/%Ecorr/VJcorr/(A·cm-2)空白0-0.4352.223×10-40.3-0.4167.766×10-5AJ0.5-0.4345.629×10-50.7-0.4234.475×10-51.0-0.4343.508×10-50.3-0.4336.797×10-5BJ0.5-0.4295.316×10-50.7-0.4274.476×10-51.0-0.4332.941×10-5
由图2和表1可知,在15%的HCl中分别加入AJ和BJ缓蚀剂后,N80钢的自腐蚀电流密度减小,这说明腐蚀反应的速率减缓,两种缓蚀剂的加入均抑制了腐蚀反应的进行;加入AJ和BJ缓蚀剂后自腐蚀电位均正移,说明阳极过程受阻,这两种缓蚀剂都是阳极抑制型缓蚀剂;相同条件下,加入BJ缓蚀剂的自腐蚀电流密度比加入AJ缓蚀剂的更小一些,说明BJ缓蚀剂的缓蚀效果要优于AJ缓蚀剂的。
2.2.2 电化学阻抗谱
图3为N80钢在缓蚀剂含量不同的15% HCl溶液中的电化学阻抗谱。其拟合等效电路如图4所示。其中,Rs为溶液电阻,Rp为极化电阻,CPE为吸附的常相位角元件。用Zveiw软件对阻抗谱进行拟合,结果见表2。
N80钢表面的腐蚀电化学信息可以通过电化学阻抗谱来反映[9],图中半圆直径越大,表明对应的极化电阻越大,缓蚀剂成膜越致密[10]。由图4可知,随缓蚀剂含量的增大,半圆容抗弧直径变大,这表明缓蚀剂的缓蚀效率也随之增大。相同条件下,加入BJ缓蚀剂的半圆容抗弧直径大于加入AJ缓蚀剂的,说明BJ的缓蚀效果要优于AJ的。由表2可知,随着AJ、BJ缓蚀剂含量的增大,溶液电阻和极化电阻都增大,这表明N80钢片表面的腐蚀反应受到抑制,腐蚀速率减小;CCPE-T减小,表明电极界面的双电层电容减小,原因是缓蚀剂分子在N80钢表面形成了吸附膜。相同条件下,加入BJ缓蚀剂的溶液电阻和极化电阻均大于加入AJ缓蚀剂的,这说明BJ缓蚀剂在N80钢表面产生的缓蚀效果优于AJ缓蚀剂的。
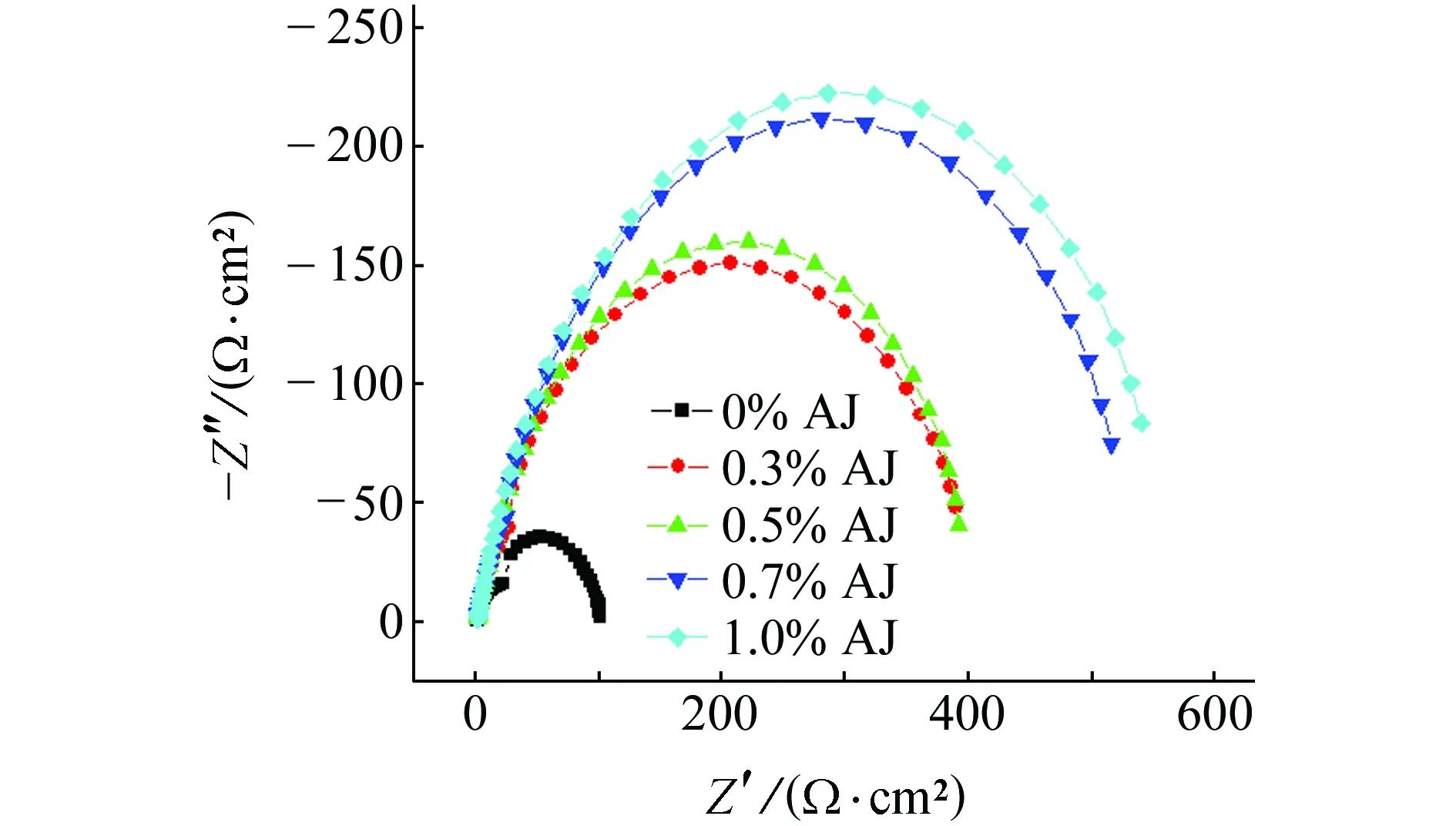
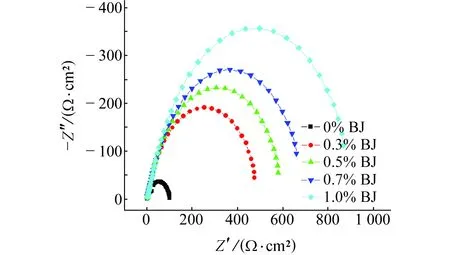
图3 N80钢在缓蚀剂含量不同的15% HCl溶液中 的电化学阻抗谱Fig. 3 EIS of N80 steel in 15% HCl solution with different concentrations of inhibitors AJ (a) and BJ (b)
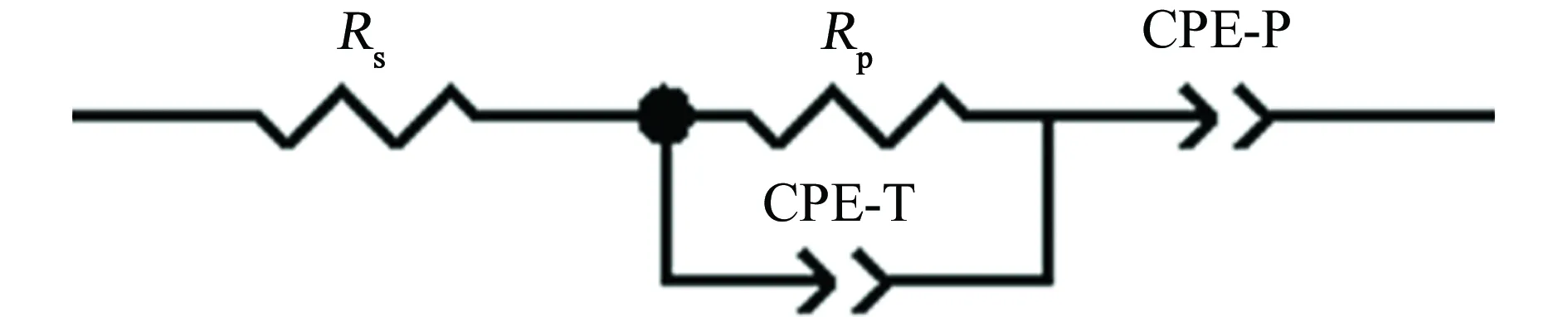
图4 电化学阻抗谱的等效电路Fig. 4 Equivalent circuit of EIS表2 图3中电化学阻抗谱的拟合结果Tab. 2 Fitted results of EIS in fig. 3
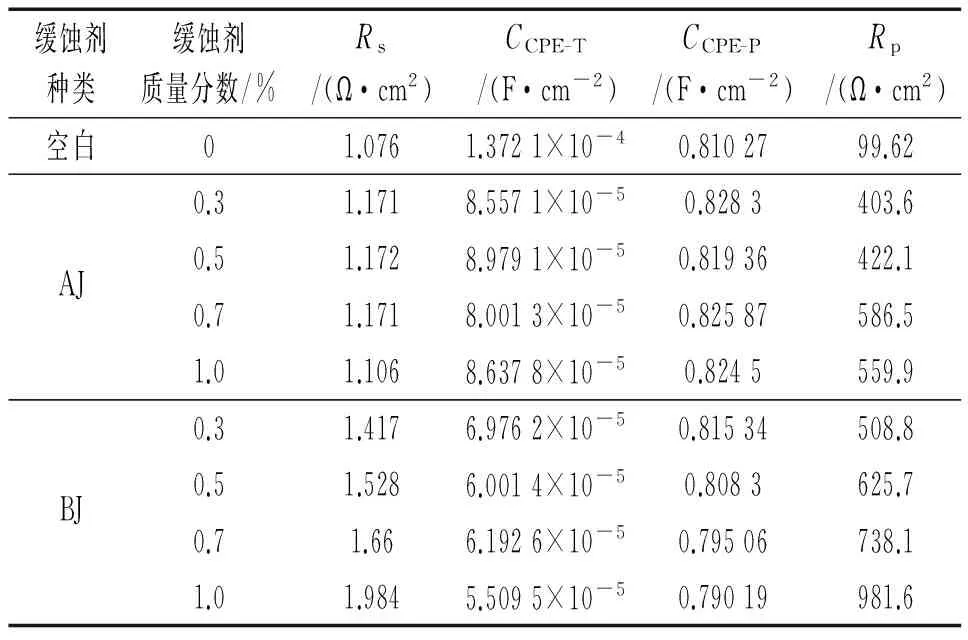
缓蚀剂种类缓蚀剂质量分数/%Rs/(Ω·cm2)CCPE-T/(F·cm-2)CCPE-P/(F·cm-2)Rp/(Ω·cm2)空白01.0761.3721×10-40.8102799.620.31.1718.5571×10-50.8283403.6AJ0.51.1728.9791×10-50.81936422.10.71.1718.0013×10-50.82587586.51.01.1068.6378×10-50.8245559.90.31.4176.9762×10-50.81534508.8BJ0.51.5286.0014×10-50.8083625.70.71.666.1926×10-50.79506738.11.01.9845.5095×10-50.79019981.6
2.3 吸附机理分析
2.3.1 缓蚀剂对N80钢的吸附行为的影响
用静态挂片失重法测得缓蚀剂的缓蚀率如图5所示。一般情况下,缓蚀剂分子在钢片表面的覆盖度θ无法直接测得,当缓蚀剂作用为几何覆盖效应时[9],可认为覆盖度θ近似等于缓蚀率η。将覆盖度分别代入Langmuir[10],Frumkin[11],Bockris-Swinkels[12]等吸附等温式中进行拟合。结果表明,在试验条件下AJ和BJ缓蚀剂在N80钢表面的吸附符合Langmuir吸附等温模型,其吸附等温式如式(6)所示。
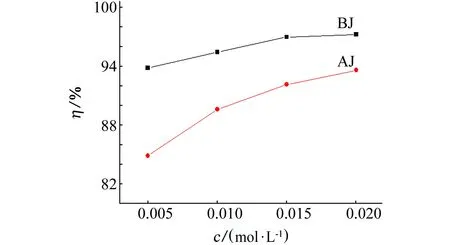
图5 缓蚀剂浓度对缓蚀率的影响Fig. 5 Effect of concentration of inhibitor on inhibition rate
(6)
式中:K为Langmuir吸附平衡常数;c为缓蚀剂的浓度,mol/L;θ为覆盖度。
将式(6)变形,以c/θ对c作图,如图6所示,拟合得到一条斜率近似为1的直线;根据该拟合直线方程的截距可求出吸附平衡常数,再由式(7)计算吸附作用的吉布斯自由能(ΔG),结果如表3所示。
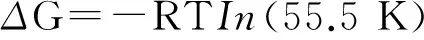
(7)
式中:R为理想气体常数,8.314 J·mol-1·K-1;T为热力学温度,K。
由表3可知,AJ和BJ缓蚀剂在N80钢表面吸附的吉布斯自由能均为负值,这表明两种缓蚀剂均能自发吸附于N80钢表面,BJ缓蚀剂的吉布斯自由能的绝对值大于AJ缓蚀剂的,表明BJ缓蚀剂在N80钢表面吸附的自发性优于AJ缓蚀剂的。
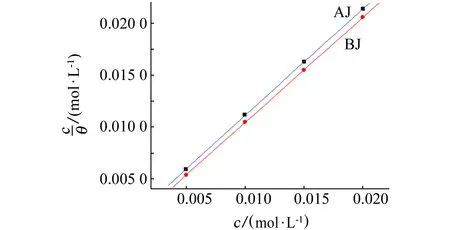
图6 缓蚀剂在N80钢表面的吸附等温线Fig. 6 Adsorption isotherm of inhibitors on the surface of N80 steel表3 吸附过程的热力学参数Tab. 3 The thermodynamic parameters of the adsorption process
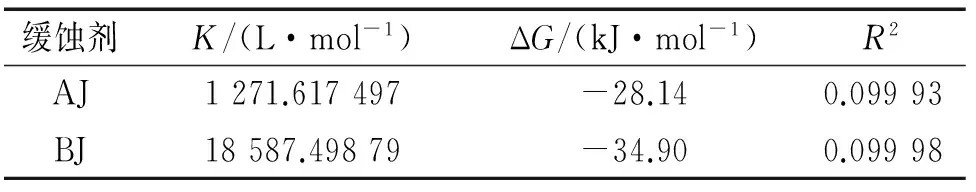
缓蚀剂K/(L·mol-1)ΔG/(kJ·mol-1)R2AJ1271.617497-28.140.09993BJ18587.49879-34.900.09998
2.3.2 缓蚀剂对腐蚀体系活化能的影响
测N80钢在303~343 K温度范围内的腐蚀速率,以1/T为横坐标,lnvcorr为纵坐标,作图得Arrhenius曲线,如图7所示。然后,根据Arrhenius公式[17]计算腐蚀体系的表观活化能,如式(8)所示。腐蚀前后的活化能参数见表4。
(8)
式中:vcorr腐蚀速率;Ea为表观活化能;R为理想气体常量;T为热力学温度;A为指前因子,可由截距得到[18]。
由图7和表4可知,腐蚀反应的活化能随缓蚀剂含量的增大而增大,较高的活化能意味着N80钢发生腐蚀需要克服的能量障碍也较高,这使得N80钢的腐蚀速率得到了降低,有效地抑制了腐蚀反应的进行。
2.3.3 分子动力学吸附模拟
分子动力学模拟方法是从微观角度上来解释缓蚀剂分子与金属表面之间的作用机理。它克服了普通试验方法只能从宏观上来研究缓蚀剂的缓蚀效果,而无法从微观上分析缓蚀剂作用机理的缺点,是一种非常有效的研究手段。试验采用Materials Studio 7.0软件模拟AJ、BJ缓蚀剂分子在N80钢表面的吸附过程。由于Fe的(111)、(110)、(001)等晶面中,(001)晶面的密度最大,能量最小,晶面最稳定,出现的几率最大[15-16],故选用(001)晶面作为吸附表面进行模拟。
缓蚀剂分子之所以能在N80钢表面上吸附从而起到防护效果,主要是因为其含有N、O、S等活性较强的部分,这些杂原子上有未共用的孤对电子,能与金属表面Fe原子空d轨道配位而形成共价键[17]。AJ和BJ两种缓蚀剂中均含有N、O原子,故能在金属表面上较强吸附。
AJ和BJ缓蚀剂在Fe(001)晶面的吸附构型如图8所示。
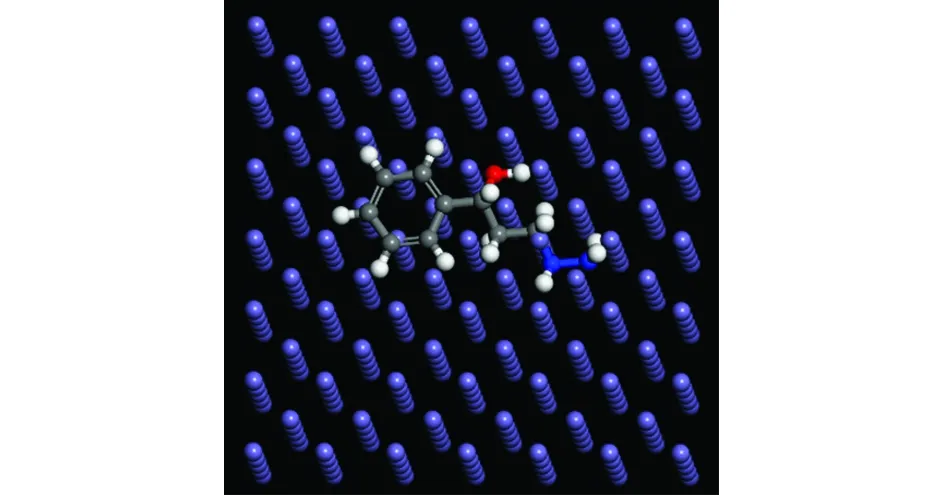
(a) AJ
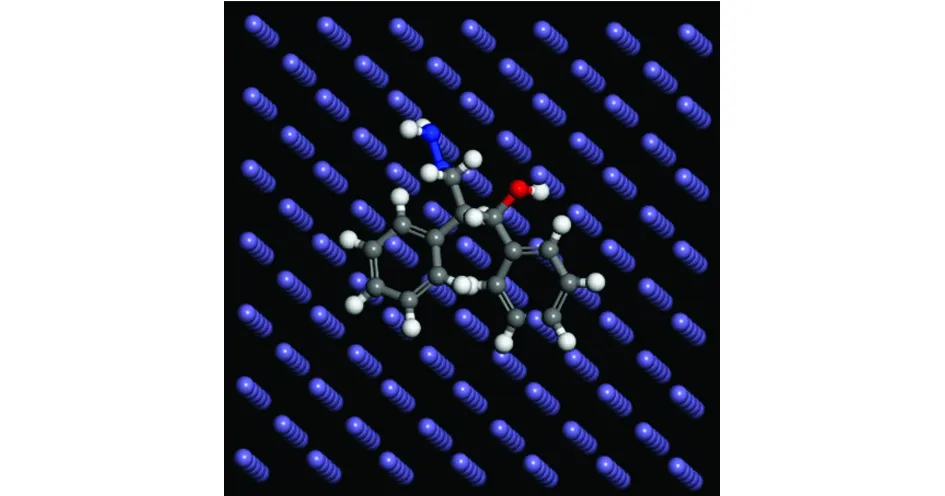
(b) BJ图8 缓蚀剂分子在Fe(001)晶面的平衡吸附构型Fig. 8 Equilibrium adsorption configurations of inhibitors AJ (a) and BJ (b) on Fe(001) plane
由图8可知,AJ和BJ两种缓蚀剂分子均以平行的方式吸附于Fe(001)晶面,这是由于缓蚀剂分子与Fe(001)表面形成了多个吸附中心的结果[18]。这种平行吸附有利于缓蚀剂分子与金属表面形成覆盖更高、致密性更好的分子膜[19]。表5为AJ、BJ和H2O分子与Fe(001)晶面的吸附能。缓蚀剂分子与金属表面的吸附能越大,表明缓蚀性能越好。从表5中可知,两种缓蚀剂分子与Fe(001)晶面间的吸附能均大于H2O分子与Fe(001)晶面间的吸附能,说明AJ和BJ分子均能挤走吸附于Fe(001)表面的H2O分子[20],从而达到对N80钢的保护作用;而且BJ分子与Fe(001)面的吸附能大于AJ的,说明BJ分子与Fe(001)晶面的相互作用更强,缓蚀效果更好。

表5 缓蚀剂分子与Fe(001)晶面的吸附能Tab. 5 Adsorption Energy of Fe(001) plane to inhibitor moleculars kJ·mol-1
BJ在分子结构上比AJ多出一个苯环,其分子的空间体积更大,这就使得其在钢片表面的覆盖面积增大,在金属表面形成更完整且致密的保护膜。苯环上的大π键能与金属络合,使其能以化学吸附的方式在金属表面上形成吸附,N、O原子与N80钢表面的铁原子通过配位键的形式形成络合物,故含有两个苯环的BJ缓蚀剂比仅有一个苯环的AJ缓蚀剂的缓蚀效果更好。
3 结论
(1) 在15%的HCl溶液中,AJ和BJ缓蚀剂对N80钢具有良好的缓蚀作用,且BJ缓蚀剂的缓蚀效果要优于AJ缓蚀剂的。
(2) AJ和BJ缓蚀剂均为阳极型缓蚀剂,腐蚀反应过程中的自腐蚀电流随着缓蚀剂在酸液介质中浓度的增加而变小。
(3) AJ和BJ缓蚀剂在N80钢表面的吸附符合Langmuir吸附等温式,缓蚀剂分子能自发吸附于N80钢表面。
(4) 分子动力学模拟结果表明,两种缓蚀剂分子都以一种平行的方式吸附在Fe(001)晶面上,且能够自发的吸附在N80钢表面并能挤走吸附在Fe(001)表面的水分子。
[1] 赵福麟. 油田化学[M]. 东营:中国石油大学出版社,2000.
[2] 张天胜,张浩,高红,等. 缓蚀剂[M]. 北京:化学工业出版社,2008.
[3] 何新快,陈白珍,张钦发. 缓蚀剂的研究现状与展望[J]. 材料保护,2003,26(8):2-2.
[4] 吴兰兰. 肼改性为酸化缓蚀剂的研究[D]. 荆州:长江大学,2013.
[5] 曹楚南. 腐蚀电化学原理[M]. 3版. 北京:化学工业出版社,2008:211-212.
[6] 王翠苹,王宝琳,刘婧婷,等. 新型材料电气石对酸性溶液中镉离子的吸附[J]. 科学通报,2012,57(21):1992-1999.
[7] 郑家燊. 缓蚀剂的研究现状及其应用[J]. 腐蚀与防护,1997,18(3):36-40.
[8] PASSINIEMI P,VAKIPAETA K. Characterization of polyaniline blends with AC impedance measurements[J]. Synthetic Metals,1995,69(1/3):237-238.
[9] 曹楚南. 腐蚀电化学[M]. 北京:化学工业出版社,1994:134.
[10] ALBERTY R A. Thermodynamics of reactions of nicotinamide adenine dinucleotide and nicotinamide adenine dinucleotide phosphate[J]. Biochemistry and Biophysics,1993,307(1):8-14.
[11] GILEADI E,KIROWA-EISNER E. Some observations concerning the Tafel equation and its relevance to charge transfer in corrosion[J]. Corrosion Science,2005,47(12):3068-3085.
[12] JOHNSON W,WROBLOWA H,BOCKRIS J O M. The mechanism of the electrochemical oxidation of oxalic acid[J]. Electroehem Soc,1994,9(5):639-651.
[13] 段世泽,谭逸玲. 界面化学[M]. 北京:高等教育出版社,1990:124.
[14] 李克华,陈洁,王任芳,等. 曼尼希碱缓蚀剂CJ的合成及其性能[J]. 腐蚀与防护,2014,35(11):1113-1115.
[15] ZHANG S,LI G,GONG H,et al. Molecular dynamics simulation of energetic Cu55 clusters deposition on a Fe(001) surface[J]. Computational Materials Science,2015,97:136-147.
[16] NAYAK S K,NOOIJEN M,BERNASEK S L,et al. Electronic structure study of CO adsorption on the Fe(001) surface[J]. Journal of Phycical Chemistry:B,2001,105(1):164-172.
[17] 李克华,吴兰兰. 曼尼希碱缓蚀剂XJ合成及其对N80钢的缓蚀性能[J]. 油田化学,2013,30(3):434-437.
[18] 苏铁军,罗运柏,李克华,等. 苯并咪唑-N-曼尼希碱对盐酸中N80的缓蚀性能[J]. 中国腐蚀与防护学报,2015:35(5):415-421.
[19] SHI W Y,DING C,YAN J L,et al. Molecular dynamics simulation for interaction of PESA and acrylic copolymers with calcite crystal surfaces[J]. Desalination,2012,291:8.
[20] 刘洁,刘峥,刘进,等. 3,5-二溴水杨醛-2-噻吩甲酰肼席夫碱缓蚀剂在油田水中对碳钢的缓蚀性能及分子动力学模拟[J]. 中国腐蚀与防护学报,2014,34(2):101-111.
Corrosion Inhibition of Two Kinds of Mannich Base Inhibitors
TANG Tian-tian, LI Ke-hua, HU Lin-li, SHI Dong-po
(School of Chemistry and Environmental Engineering, Yangtze University, Jingzhou 434023, China)
Two kinds of mannich base inhibitors AJ and BJ were synthesized using formaldehyde/ benzaldehyde, acetophenone and hydrazine hydrateas as raw materials. The corrosion inhibition of these two kinds of inhibitors to N80 steel in 15 wt.% HCl solution was investigated by means of static weight loss method and electrochemical testing. The results show that both AJ and BJ had good corrosion inhibition to N80 steel in HCl solution, and the later was better than the former. These two kinds of inhibitors were all belong to anodic corrosion inhibitor, and were able to adsorb on the surface of N80 steel spontaneously. And the adsorption of both AJ and BJ follows Langmuir isotherm law.
corrosion inhibitor; mannich base; adsorption; inhibition mechanism
10.11973/fsyfh-201704004
2016-06-07
国家自然科学基金(41202111); 国家大学生创新实验计划项目(111048910)
胡琳莉(1980-),讲师,硕士,从事油气田环境保护和功能材料合成方面研究,15927788875,hulinli@yangtzeu.edu.cn
TG174
A
1005-748X(2017)04-0262-06
