高纯3,3′-二氨基-4,4′-氧化偶氮呋咱(DAOAF)的合成工艺
2017-05-07王小旭陈明龙孟俞富索志荣杨海君李鸿波
王小旭, 张 勇, 黄 明, 陈明龙, 孟俞富, 索志荣, 杨海君, 李鸿波
(1. 西南科技大学材料科学与工程学院, 四川 绵阳 621010; 2. 中国工程物理研究院化工材料研究所, 四川 绵阳 621999)
1 引 言
呋咱环是氮氧五元杂环,又称噁二唑环,含有较多的碳氮键和氮氧键,具有高的正生成焓,含有活性氧;因其芳香性,具有较高的热稳定性和安定性及较低的感度[1]。在呋咱环上引入不同基团如氨基、硝基、偶氮基等可能会提高物质的能量密度和爆炸性能。
自1968年Coburn[2]首次合成3,4-二氨基呋咱(DAF)以来,已衍生出众多呋咱含能化合物[3-6],成为含能材料研究的热点之一。DAF可经多种氧化剂氧化制得3,3′-二氨基-4,4′-氧化偶氮呋咱(DAOAF)。DAOAF是一种含能化合物,其能量密度大(密度为1.685 g·cm-3,爆速7930 m·s-1,爆压30.6 GPa),正生成焓高(+443 kJ·mol-1),热稳定性好(热分解温度260 ℃),不仅具有耐热炸药六硝基茋优良的耐热性,而且爆轰性能优于六硝基茋;特性落高大于320 cm(2.5 kg落锤),对静电火花和摩擦的刺激不敏感[7-8],有望成为新型冲击片雷管用始发药。目前,国内外对DAOAF的研究主要集中在新合成方法、配方研制、性能测试上,尚无用于制备标准物质的高纯DAOAF的合成工艺报道。
DAOAF的合成工艺主要有两种: (1)以适宜的氧化剂,如Oxone[9]、H2O2/H2SO4[10]、H2O2/HNO3-H2SO4[11]等氧化DAF合成DAOAF,其中以H2O2/HNO3-H2SO4为氧化剂时,DAOAF产率为96.8%,纯度为99.2%,但反应时间较长(20 h),且易产生大量酸性废液,不适于工艺放大。(2)以DAF为原料,先在甲酸溶液中甲酰化得到中间体3-氨基- 4-甲酰氨基呋咱和3,4-二甲酰氨基呋咱,再经H2O2氧化得DAOAF[12],工艺存在反应步骤多、时间长和成本高等问题。前期本课题组以H2O2/浓H2SO4[10]为氧化体系所得DAOAF粗品,纯度低(92%),反应时间长(22 h),效果并不理想。黄明等[13]以乙二醛和盐酸羟胺为原料合成关键中间体DAF ,一步法收率最高为43%,本研究在此基础上进一步优化DAF的合成工艺,获得较佳的工艺条件;同时还着重优化了过硫酸氢钾氧化DAF制备DAOAF的工艺条件,并利用HPLC法测定产品中杂质的种类与含量,粗品经简单后处理可成功制得高纯DAOAF。
2 实验部分
2.1 试剂与仪器
3-氨基-4-硝基呋咱(ANF)、3,3′-二氨基-4,4′-偶氮呋咱(DAAF)等标准品(自制,纯度大于99%,满足色谱分析要求);乙二醛(40%)、盐酸羟胺、尿素、氢氧化钠、碳酸氢钠、N,N-二甲基甲酰胺(DMF)等试剂均为分析纯,购于成都市科龙化工试剂厂;过硫酸氢钾(42%~46%)为分析纯,购于上海麦克林生化科技有限公司。
WRS-2微机熔点仪,上海申光仪器仪表有限公司;AV 600型(600 MHz)超导核磁共振波谱仪,瑞士Bruker公司;Nexus 870型傅里叶变换红外光谱仪,美国Nicolet公司;Varian 325-LC-MS质谱仪,美国Agilent公司;Zorbax SB-C18柱,美国Agilent公司;Ultimate3000DGLC 双三元、二维液相色谱仪,美国Thermo Fisher Scientific公司。
2.2 实验过程
2.2.1 合成路线
以乙二醛和盐酸羟胺为原料,一步法合成中间体DAF。DAF在NaHCO3溶液缓冲体系中经过硫酸氢钾氧化,最终生成DAOAF。合成路线见Scheme 1。
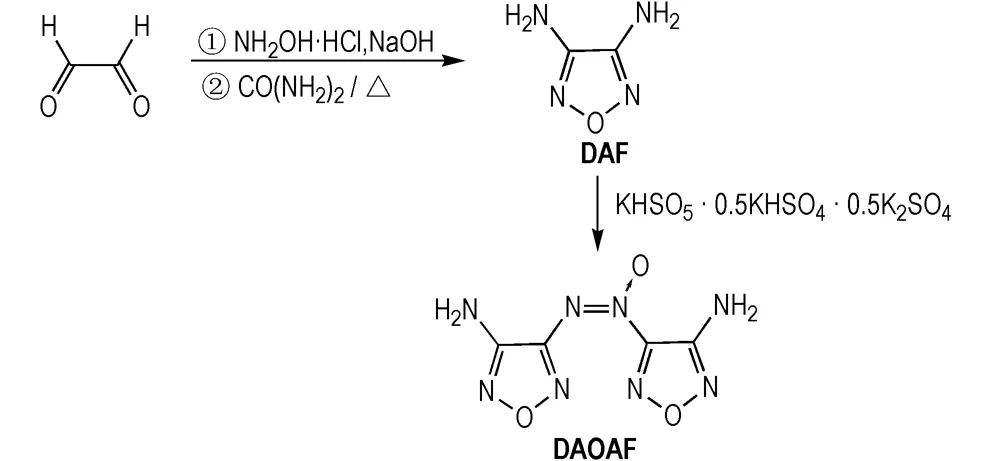
Scheme 1
2.2.2 DAF的合成
将装有搅拌和温度计的2 L三口烧瓶置于冰浴中。取115 mL(1.0 mol)乙二醛(40%)加入到三口烧瓶中,开启搅拌,加入500 mL水,再加入450 g(6.5 mol)固体盐酸羟胺,搅拌溶解。冰浴搅拌下,将280 g(7.0 mol)氢氧化钠溶于600 mL水的溶液于6 h内缓慢滴加至三口烧瓶中(T<15 ℃)。滴毕,缓慢升温至102~108 ℃,回流反应6 h。80 ℃下减压蒸馏出约350 mL溶剂,反应液中加入350 g(5.8 mol)尿素,升温至105 ℃进行回流反应22 h。冷却后置于冰箱中冷藏,析出白色针状结晶。抽滤、水洗、真空干燥得白色针状晶体48.0 g,收率48.0%。纯度99.8%(HPLC归一化法)。m.p. 181.7~183.0 ℃。

2.2.3 高纯DAOAF的合成
将100 g(1.0 mol)新制得的DAF,252 g(3.0 mol)碳酸氢钠,6 L水加入10 L反应瓶中,搅拌并将体系温度稳定在20~25 ℃。待DAF溶解后,于1 h内分三批次加入615 g(2.0 mol)过硫酸氢钾,体系变黄。加毕恒温继续搅拌反应2 h。反应液中再加入252 g碳酸氢钠,于1 h内分三批次加入615 g 过硫酸氢钾,控制温度20~25 ℃搅拌反应3 h。静置、抽滤、水洗、真空干燥得橙黄色粉末89.1 g,收率84.1%,纯度98.22%(HPLC归一化法)。

3 结果与讨论
3.1 DAOAF中杂质表征及纯度分析
采用HPLC(面积归一化法)测定产品纯度[14],并分析产品中杂质。DAF、ANF、DAAF、DAOAF在同一液相色谱条件下分析,结果见图1。
液相色谱条件: Zorbax SB-C18(250 mm×4.6 mm,5.0 μm)柱;流动相为乙腈/水(体积比为40/60);流速为0.8 mL·min-1;柱温25 ℃;检测波长230 nm;进样体积10 μL。
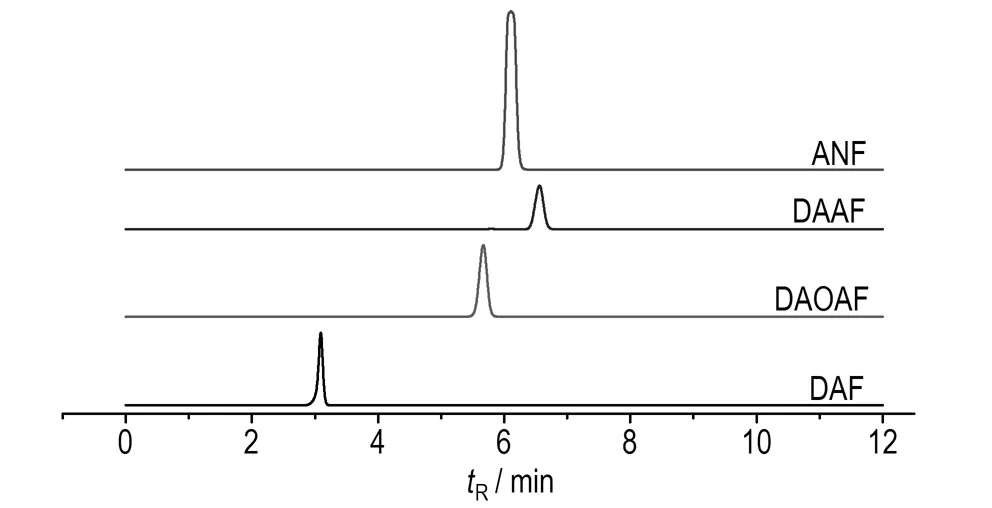
图1DAOAF及杂质的HPLC谱图
Fig.1HPLC spectra of DAOAF and impurities
粗品DAOAF及其重结晶后的HPLC谱见图2。从图1和图2可知,粗品DAOAF中主要杂质为原料DAF、副产物ANF和DAAF。通过高效液相色谱的面积归一化法测定DAOAF纯度及杂质含量,粗品和高纯DAOAF及其所含杂质的相对含量分别见表1、表2。
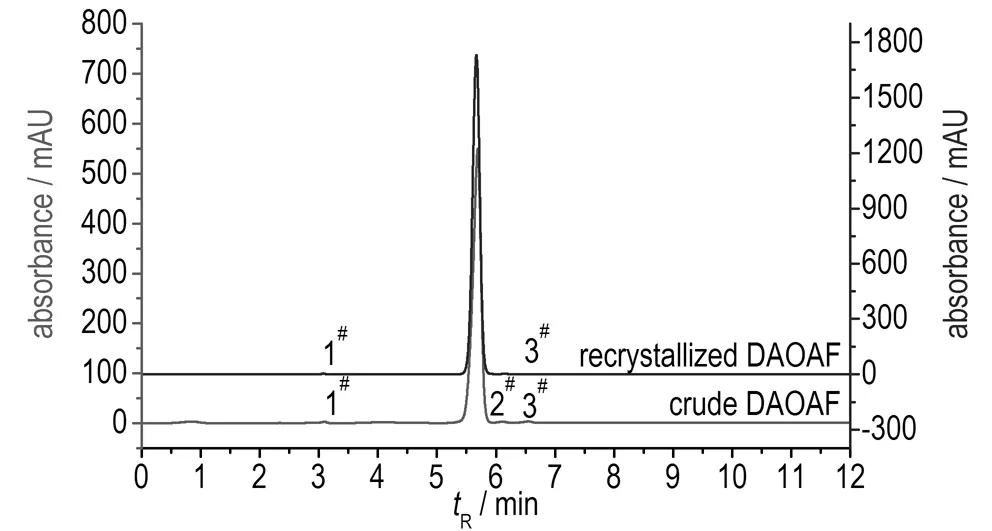
图2粗品和重结晶后DAOAF的HPLC谱图
Fig.2HPLC specta of crude DAOAF and recrystallized DAOAF
表1粗品DAOAF及其杂质相对含量
Table1Relative content of crude DAOAF and its impurities
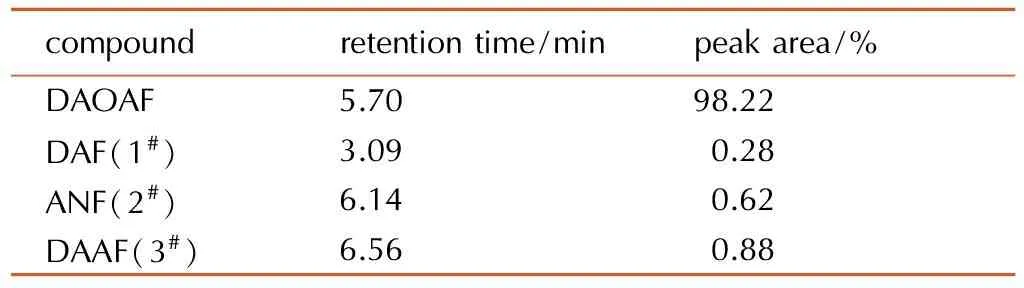
compoundretentiontime/minpeakarea/%DAOAF5.7098.22DAF(1#)3.090.28ANF(2#)6.140.62DAAF(3#)6.560.88
表2高纯DAOAF及其杂质相对含量
Table2Relative content of high-purity DAOAF and its impurities

compoundretentiontime/minpeakarea/%DAOAF5.7099.6DAF(1#)3.090.1DAAF(3#)6.560.3
从图2和表2中看出,粗品DAOAF于95 ℃经DMF重结晶后,可完全除尽杂质ANF,同时有效减少杂质DAF和DAAF的含量,从而制得高纯DAOAF(纯度99.6%)。
3.2 DAOAF收率的影响因素
过硫酸氢钾氧化DAF生成DAOAF的过程中,NaHCO3和过硫酸氢钾的投量都会对反应收率造成影响,同时反应时间和温度对收率也有较大的影响。本实验着重考查了反应物投料比、反应时间和温度对DAOAF收率的影响。
3.2.1 反应物投料比的影响
室温,反应时间为5 h,反应物DAF、NaHCO3与过硫酸氢钾的投料比对DAOAF收率的影响见表3。由表3可知,当反应物摩尔比n(DAF)∶n(NaHCO3)∶n(KHSO5·0.5KHSO4·0.5K2SO4)=1∶6∶5时,DAOAF收率最佳(84.8%),考虑到过硫酸氢钾使用成本因素,选用n(DAF)∶n(NaHCO3)∶n(KHSO5·0.5KHSO4·0.5K2SO4)=1∶6∶4为宜(收率84.1%)。
表3反应物摩尔比对 DAOAF 收率的影响
Table3Effect of reactant molar ratio on the yield of DAOAF

n(DAF)∶n(NaHCO3)∶n(KHSO5·0.5KHSO4·0.5K2SO4)yield/%1∶6∶270.41∶6∶376.71∶6∶484.11∶6∶584.81∶6∶681.31∶4∶468.71∶8∶475.4
3.2.2 反应时间的影响
由于DAF制备DAOAF为氧化反应,氧化剂过硫酸氢钾应分批分量于一定时间内加入,避免副产物生成,故氧化剂加毕后的总反应时间对产品收率的影响需进一步考察。室温,反应物投料比n(DAF) :n(NaHCO3) :n(KHSO5·0.5KHSO4·0.5K2SO4)=1∶6∶4时,反应时间对DAOAF收率的影响见图3。由图3可知,当反应时间5 h时,DAOAF收率最佳(84.1%),若继续延长反应时间,DAOAF的收率并无明显提升。薄层色谱检测同时表明反应5 h后,原料DAF反应较完全且副产物少。故反应时间确定为5 h。
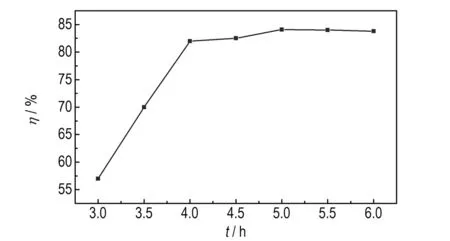
图3反应时间对DAOAF收率的影响
Fig.3Effect of reaction time on the yield of DAOAF
3.2.3 反应温度的影响
反应物摩尔比n(DAF) :n(NaHCO3) :n(KHSO5·0.5KHSO4·0.5K2SO4)=1∶6∶4,反应时间为5 h时,反应温度对DAOAF收率的影响见图4。由图4可知,温度低于17 ℃时,反应速率较慢,原料反应不充分,DAOAF收率较低(不足78%);当温度高于30 ℃时,易产生副产物ANF和DAAF,导致DAOAF收率明显下降。因反应过程中体系温度会有轻微变化,故将反应温度控制在20~25 ℃为宜。
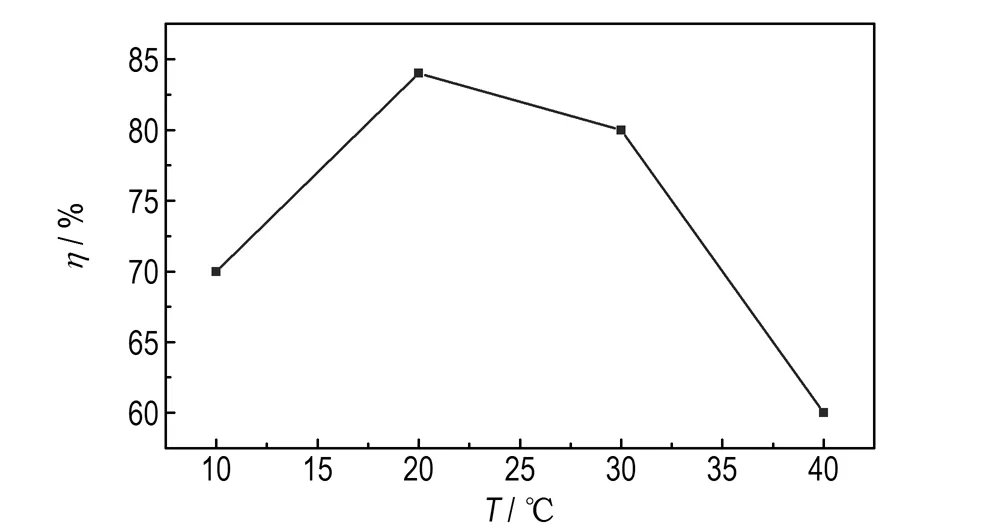
图4反应温度对DAOAF收率的影响
Fig.4Effect of reaction temperature on the yield of DAOAF
4 结 论
(1) 以乙二醛和盐酸羟胺为原料经一步法合成中间体DAF,收率为48.0%,纯度99.8%。
(2) 在NaHCO3溶液缓冲体系中,DAF经过硫酸氢钾氧化可制得DAOAF。优化后的最佳合成工艺为:n(DAF)∶n(NaHCO3)∶n(KHSO5·0.5KHSO4·0.5K2SO4)=1∶6∶4,反应时间5 h,反应温度20~25 ℃。产品收率为84.1%,纯度98.22%。
(3) HPLC法测定出粗品DAOAF主要杂质为原料DAF、副产物DAAF与ANF。粗品DAOAF于95 ℃经DMF重结晶可实现高纯DAOAF的制备,回收率86.6%,纯度99.6%。
参考文献:
[1]Olofson R A, Michelman J S. Furazan[J].JournalofOrganicChemistry, 1965, 30(6): 1854-1859.
[2]Coburn M D. Picrylamino-substituted heterocycles Ⅱ Furazans[J].JournalofHeterocyclicChemistry, 1968, 5(1): 83-87.
[3]Sheremetev A B. Chemistry of furazans fused to five-membered rings[J].JournalofHeterocyclicChemistry, 1995, 32(2): 371-385.
[4]Pivina T S, Sukhachev D V, Evtushenko A V, et al. Comparative characteristic of energy content calculating methods for the furazan series as an example of energetic materials[J].Propellants,Explosives,Pyrotechnics, 1995, 20(1): 5-10.
[5]张寿忠, 冯晓晶, 朱天兵, 等. 新型含能材料呋咱类化合物的研究进展[J]. 化学推进剂与高分子材料, 2013, 11(2): 1-5.
ZHANG Shou-zhong, FENG Xiao-jing, ZHU Tian-bing, et al. Research progress in novel energetic materials—furazan-based compounds [J].ChemicalPropellants&PolymericMaterials, 2013, 11(2): 1-5.
[6]And A B S, Kulagina V O, Ivanova E A. Zero-hydrogen furazan macrocycles with oxy and azo bridges[J].JournalofOrganicChemistry, 1996, 61(4): 1510-1511.
[7]Cannizzo L F, Hamilton R S, Highsmith T K, et al. Furazan-based energetic ingredients[R]. ADA405840/XAB, 1999.
[8]Sinditskh V, Manh V U, Shelaputina V, et al. Study on thermal decomposition and combustion of insensitive explosives 3,3′-diamino-4,4′-azofurazan and 3,3′-diamino-4,4′-azoxyfurazan[C]∥Proceedings-2007 International Autumn Seminar on Propellants, Explosives and Pyrotechnics, Xi′an, 2007, 422-428.
[9]Francois E G, Chavez D E, Sandstrom M M. The development of a new synthesis process for 3,3′-diamino-4,4′-azoxyfurazan (DAAF)[J].Propellants,Explosives,Pyrotechnics, 2010, 35(6): 529-534.
[10]周群, 王伯周, 张叶高, 等. 3,3′-二氨基-4,4′-偶氮呋咱合成工艺的改进及性能[J]. 火炸药学报, 2013, 36(2): 16-19.
ZHOU Qun, WANG Bo-zhou, ZHANG Ye-gao, et al. Improvement on synthesis process and properties of 3,3′-diamino-4,4′-azofurazan[J].ChineseJournalofExplosivesandProprllants, 2013, 36(2): 16-19.
[11]刘燕, 安崇伟, 王晶禹. 3,3′-二氨基-4,4′-氧化偶氮呋咱的合成[J]. 合成化学, 2016, 24(10): 899-902.
LIU Yan, AN Chong-wei, WANG Jing-yu. Synthesis of 3,3′-diamino-4,4′-azofurazan[J].ChineseJournalofSyntheticChemistry, 2016, 24(10): 899-902.
[12]吴敏杰, 陈树森, 金韶华, 等. 一种合成3,3′-二氨基-4,4′-氧化偶氮呋咱的新方法[J]. 含能材料, 2013, 21(2): 273-275.
WU Min-jie, CHEN Shu-sen, JIN Shao-hua, et al. A new method to synthesize 3,3′-diamino-4,4′-azoxyfurazan[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2013, 21(2): 273-275.
[13]黄明, 李洪珍, 李金山. 3,4-二氨基呋咱的三种简便合成方法[J]. 含能材料, 2006, 14(2): 114-115.
HUANG Ming, LI Hong-zhen, LI Jin-shan.Three methods of synthesizing 3,4-diaminofurazan[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2006, 14(2): 114-115.
[14]何乃珍, 索志荣, 张勇, 等. 3,3′-二氨基-4,4′-氧化偶氮呋咱的纯度测定及杂质表征[J]. 含能材料, 2016, 24(8): 793-797.
HE Nai-zhen, SUO Zhi-rong, ZHANG Yong,et al. Determination of 3,3′-diamino-4,4′-azoxyfurazan characterization of impurities[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2016, 24(8): 793-797.
