芳香耐热含能化合物合成研究进展
2017-05-07张俊林毕福强胡怀明王伯周
张俊林, 周 静, 毕福强, 霍 欢, 胡怀明, 王伯周
(1. 西安近代化学研究所, 陕西 西安 710065; 2.西北大学化学与材料科学学院, 陕西 西安 710127)
1 引 言
含能化合物是实现高能毁伤和高强推进作用的能量源泉[1-3]。在核武器、空间探测及深井爆破等领域,含能化合物需要面对高温使用环境,因此要求化合物必须具有较高的熔点、较低的蒸汽压和良好的耐热性能,在经历长时间加热后依然能够可靠完成爆轰反应[4]。芳基稳定性高,耐热含能化合物骨架多为芳环结构,在此基础上通过分子设计利用不同的稳定化效应可有效实现化合物耐热性能的提升。目前芳香耐热含能化合物设计采用的稳定化效应主要有两类: 一是在硝基芳环中引入氨基结构,利用分子间及分子内的氢键作用,提升分子晶格能与热稳定性[5-6]; 二是利用共轭体系进行稳定,通过离域能及π-π堆积作用的增强来提升化合物的热稳定性[7]。此外,将含能化合物转化为对应的盐类,也能够在一定程度上提升化合物的耐热性能[8]。
为了推动耐热含能化合物研究,以单环、并环及偶联多芳环结构进行分类,总结了芳香耐热含能化合物的研究进展,对不同结构耐热含能化合物的合成研究进行梳理,重点介绍近年来部分耐热性能突出的共轭型含能化合物的合成,为新型耐热含能化合物的设计制备提供借鉴。
2 单环耐热含能化合物
单环体系含能化合物的共轭稳定化效应有限,故多通过在硝基芳环中引入氨基[9],利用氨基与硝基间氢键作用来增强化合物的整体热稳定性。三氨基三硝基苯(TATB)和2,6-二氨基-3,5-二硝基-1-氧吡嗪(LLM-105)是目前最为重要的单环耐热含能化合物。
TATB含三组以交错方式排列的氨基和硝基,充分利用了氢键的稳定化效应,常温下为黄色粉状晶体,熔点330 ℃,爆速为7970 m·s-1。由于氢键拉近了分子间的距离,晶体密度达到了1.94 g·cm-3[10]。TATB早期合成方法较多[11-12],多利用含有易离去基团(主要是卤素)的芳环进行硝化,所得产物中易离去基团在氨的亲核进攻下被取代生成TATB。Pagoria等[13-14]利用硝基芳环与氨基亲核试剂(VNS试剂)直接进行VNS反应改进了TATB的合成,实现了无卤素的TATB合成(Scheme1)。
LLM-105是目前能量性能最为优异的单环耐热含能化合物,密度1.91 g·cm-3,爆速8590 m·s-1,能量水平较TATB高出近15%,加之其热分解峰温接近350℃,可作为高性能耐热炸药[15]。LLM-105的分子中1-氧吡嗪的结构有效的提升了分子密度及能量水平[16],但同时也增加了合成难度。合成LLM-105的方法主要分为两种,一是首先合成2,6-二氨基-3,5-二硝基吡嗪(ANPZ)[17],之后进行氮氧化反应[18]; 二是直接利用缩合反应构建1-氧吡嗪骨架。Shreeve等[19]报道了采用三氟乙酸与过氧化氢体系实现吡嗪骨架氮氧化的研究; Liu等[20]则报道了通过盐酸羟胺与双氰基的缩合环化实现1-氧吡嗪骨架直接构建的研究(Scheme2)。
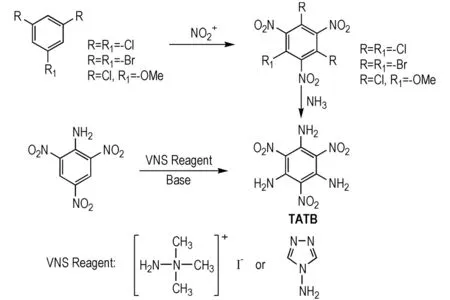
Scheme 1 Synthesis of TATB[11-14]
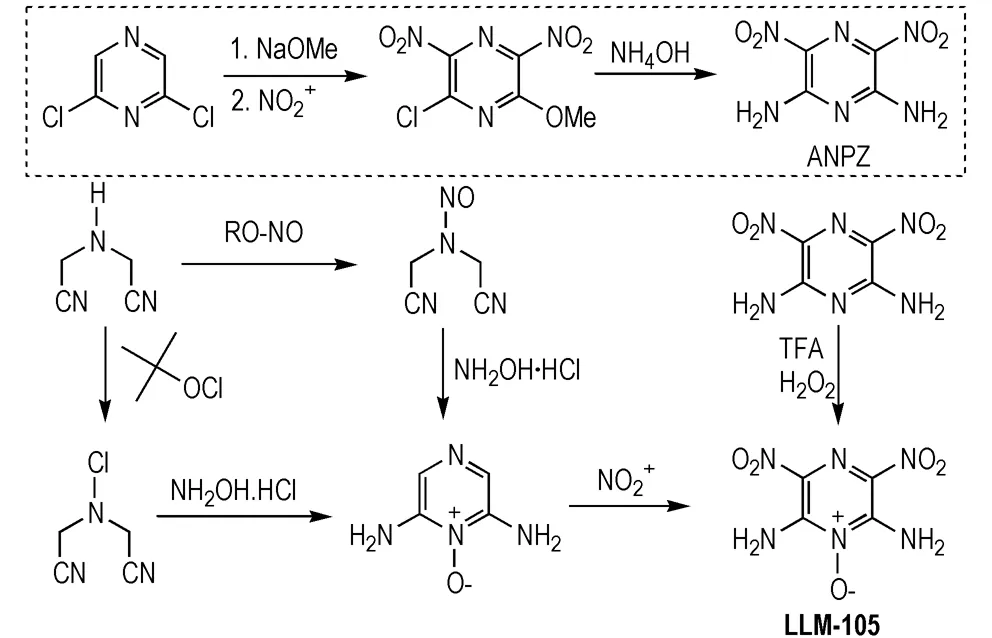
Scheme 2 Synthesis of LLM-105[17-20]
Ritter等[21]通过硝化2,6-二氨基吡啶获得2,6-二氨基-3,5-二硝基吡啶(ANPY),Wilson等[22]利用过氧乙酸对吡啶氮原子进行氮氧化获得了类似LLM-105结构的单环耐热炸药2,6-二氨基-3,5-二硝基-1-氧吡啶(ANPYO),其密度1.88 g·cm-3,爆速7840 m·s-1,初始分解温度290 ℃,低于LLM-105的能量水平。在ANPYO基础上,Wilson等[23]利用C-胺化反应进一步制备了2,4,6-三氨基-3,5-二硝基-1-氧吡啶,但其初始分解温度为252.7 ℃,较胺化前有所下降(Scheme3)。
单环耐热含能化合物中氢键作用的强弱直接影响着化合物的热稳定性,以TATB体系为例,随着氨基数目的增加,化合物中氢键强度不断增加,热稳定性也不断提升[2](图1)。对比TATB,LLM-105、ANPYO及其衍生物的结构特点与性能可见,环系骨架中杂原子及N—O键的引入提升了化合物的爆轰性能,但并未显著改进化合物的耐热性能,表明除氢键作用外,环系骨架本身的稳定性对化合物耐热性能更具决定性影响。
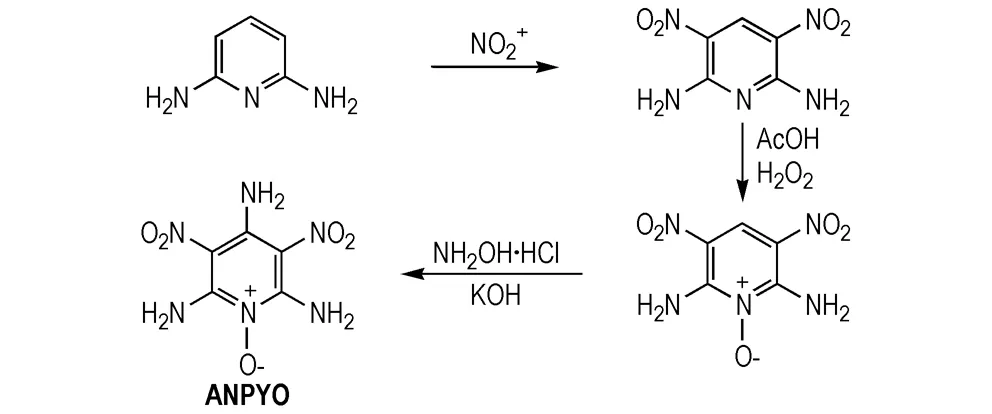
Scheme 3 Synthesis of ANPYO and its derivative[21-23]
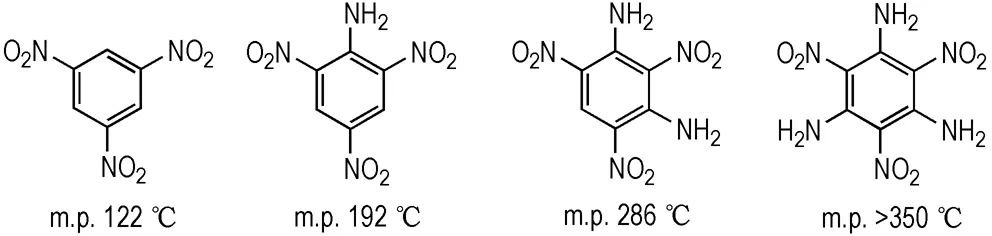
图1TATB及其类似物热分解温度[2]
Fig.1Thermal decomposition temperature of TATB and its analogues[2]
3 并环耐热含能化合物
并环体系含能化合物较单环体系共轭结构增大,有利于利用离域能提升化合物的热稳定性。此外,硝基并环体系中引入氨基将进一步增强分子间氢键的稳定化效应。
四硝基二苯并-1,3a,4,6a-四氮杂戊搭烯(TACOT)是一类结构独特的内盐型含能化合物,二苯并四氮杂戊搭烯骨架中四个氮原子均位于桥头位置,组成了四环共轭的平面环系结构,高度的芳香共轭体系赋予了分子高度的热稳定性,其中z-TACOT分解温度达到378 ℃[24],γ-TACOT分解温度达到400 ℃[25]。Hatchard 等[26]报道了通过热环化反应完成TACOT并环骨架构建的研究,反应过程中释放两分子氮气,最终形成内盐结构(Scheme4)。
以TACOT合成为基础,Trudell等[27]一方面将其中苯环片段替换为吡啶片段,另一方面则在四环基础上引入两组氧化呋咱,扩大了共轭体系,增强了化合物的耐热性能[28]。但相比TACOT,这两类新型内盐结构的热稳定性均低于TACOT,其中aza-TACOT分解温度为342 ℃[27],而γ-DBBD的分解温度降则降至274 ℃[25],原因可能在于多硝基氮杂环及多硝基苯并氧化呋咱结构片段的热稳定性均低于多硝基苯环结构片段(Scheme5)。
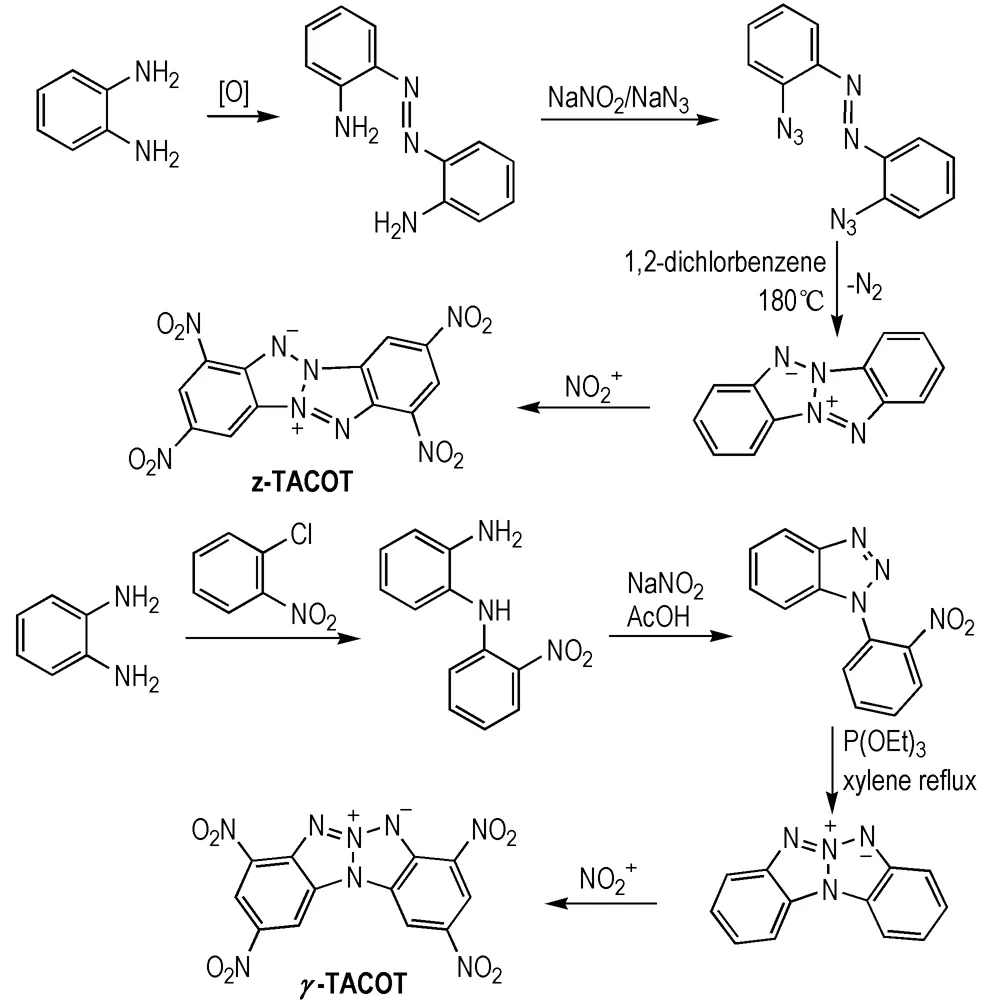
Scheme 4 Synthesis of TACOT[24-26]
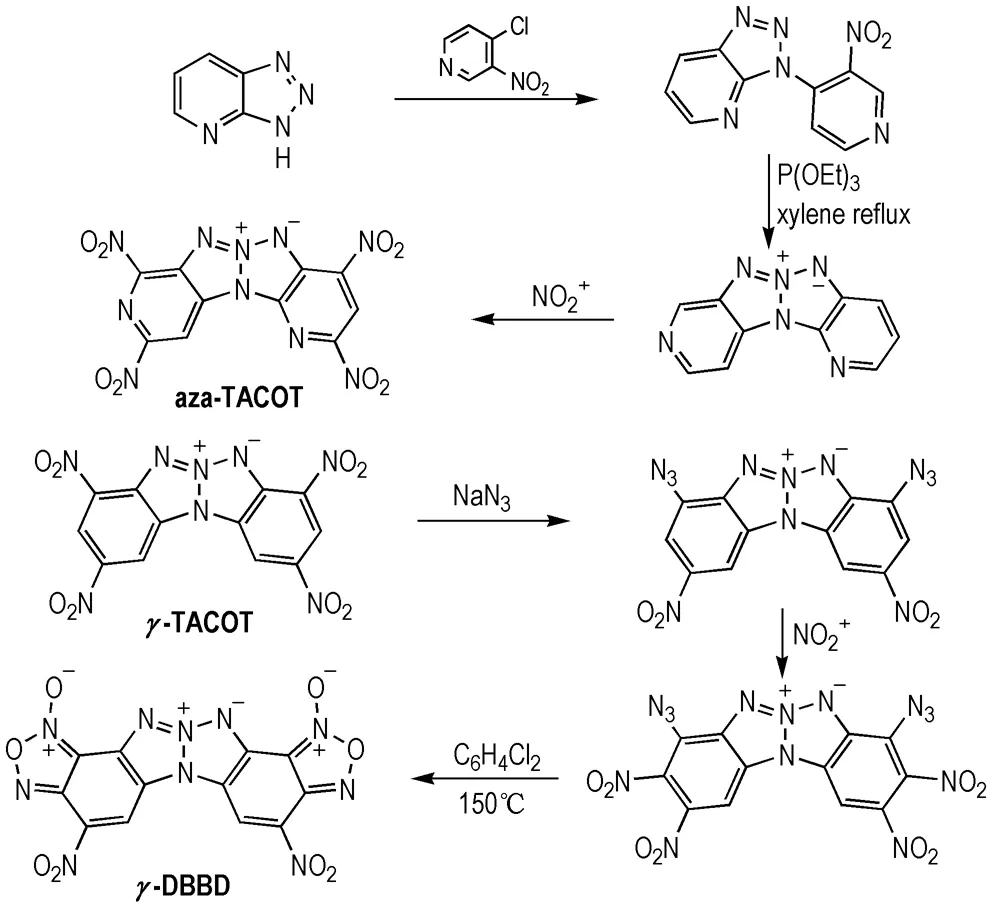
Scheme 5 Synthesis of γ-DBBD[27]
DNPP为双吡唑并环骨架[28],通过吡唑氮的胺化反应可构建1,4-二氨基-3,6-二硝基吡唑[4,3-c]并吡唑(LLM-119)(Scheme6),Wang等[29]发现LLM-119的分解温度为232 ℃,具有一定的耐热性能。
Norris等[30]利用2-硝基苯胺合成7-氨基-4,6-二硝基苯并呋咱(ADNBF),Wang等[31]通过2,4,6-三硝基氯苯合成5,7-二氨基-4,6-二硝基苯并呋咱(DADNBF)(Scheme7),ADNBF和DADNBF在多硝基苯环上引入氨基结构形成分子间氢键实现了较好的热稳定性,两化合物的热分解温度分别为270 ℃及292 ℃[32]。

Scheme 6 Synthesis of LLM-119[28-29]
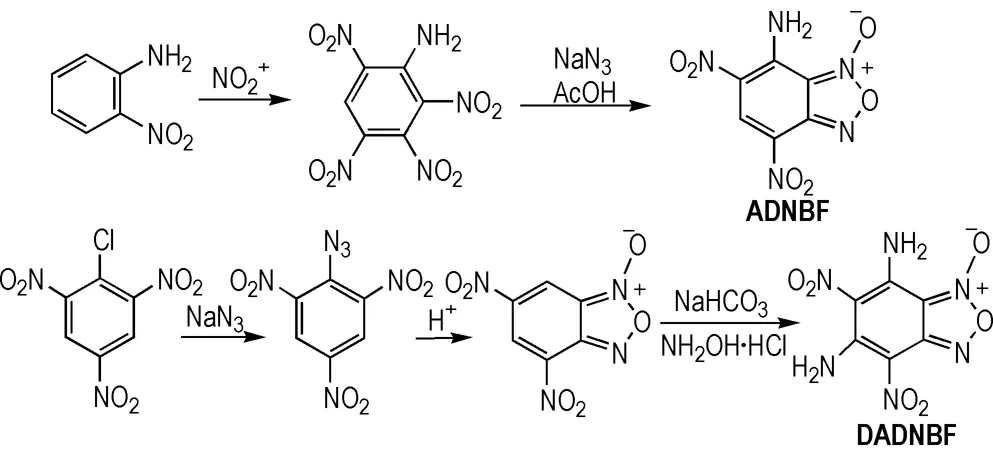
Scheme 7 Synthesis of ADNBF and DADNBF[30-32]
并环体系较之单环体系,其化合物热稳定性的提升呈现两方面特点: (1)化合物可以形成独特的内盐结构,如TACOT及其衍生物,此类有机内盐结构一方面充分发挥成盐效应对化合物热稳定性的显著提升作用,同时避免了普通酸碱成盐法所带来的吸湿性等问题; (2)并环化合物结构紧凑,既通过共轭体系增大提升了热稳定性,同时避免了骨架过于松散对化合物爆轰性能的不利影响。
4 偶联多芳环耐热含能化合物
偶联芳环体系结构多样,通过芳基之间的偶联扩展共轭环系提升离域能,可有效增强化合物稳定性。偶联芳环化合物研究是目前耐热含能化合物研究的主要方向,通过不同共轭结构的结合可有效设计并获得具有高度耐热性能的化合物结构。
六硝基茋(HNS)广泛应用于航空航天及石油开采领域,曾被制成柔性导爆索用于阿波罗计划中的月震探测[33]。Gilbert[34]等及Lu[35]等分别通过2,2,4,4,6,6-六硝基联苄(HBNN)在氧气、卤素及高价金属的氧化作用下合成了HNS,Shipp等[36]采用2-(氯甲基)-1,3,5-三硝基苯直接偶联实现HNS的合成(Scheme8)。HNS熔点317 ℃,分子本身通过烯烃将两个苦基进行偶联形成14电子的共轭平面结构,有效提升了分子的热稳定性[37]。2,2,4,4,6,6-六硝基偶氮苯(HNAB)以偶氮实现两组苦基的偶联,形成了与HNS相似的14电子的共轭平面结构,但其熔点仅为221 ℃[38],明显低于HNS,表明偶氮基团用于芳环链接的稳定性低于烯烃基团。

Scheme 8 Synthesis of HNS and HNAB[34-38]
化合物在熔融状态下分解速率大大高于普通固体状态,多硝基苯直接通过单键偶联使分子量大幅增加,显著提升了化合物熔点的同时提升了化合物的热稳定性; 同时,多组芳环体系直接相连所形成的共轭体系离域能大幅增加,使化合物热稳定性进一步增强。2,2′,2″,4,4′,4″,6,6′,6″-九硝基-间三联苯 (NONA)是典型的多硝基芳环直接偶联形成的耐热含能化合物,Dacons等[39]通过Ullman偶联[40]反应高效构建NONA,Redecker等[41]报道了类似的环系合成应用于更大的共轭体系合成甚至聚合物的合成(Scheme9)。NONA分子热稳定性突出,分解温度达到440 ℃,表明共轭效应提升化合物耐热性能的高效性[39]。

Scheme 9 Coupling of polynitrobenzene[39-41]
Pagoria 等[42]以3,5-二氨基-1,2,4-三唑为原料,通过氨基氧化反应合成3,5-二硝基-1,2,4-三唑,5-硝基在肼的选择性还原作用下可生成产物3-氨基-5-硝基-1,2,4-三唑(ANTA)。ANTA熔点238 ℃,具备一定耐热性。Charrue等[43]和Coburn等[44]分别通过芳环亲核取代反应将ANTA与不同芳环体系进行偶联,获得了一系列多芳环耐热含能基化合物。ANTA与吡嗪偶联产物热分解温度达到330 ℃,与四嗪偶联后化合物热分解温度为260 ℃,与三嗪偶联后化合物热分解温度为300 ℃。Zhou等[45]利用ANTA与3,4,5-三硝基吡唑偶联并成盐,获得了新型耐热含能盐(Scheme10)。

Scheme 10 Synthesis of ANTA and its derivatives[42-45]
Sitzman等[46]最早实现了噁二唑偶联的多硝基苯结构: 通过噁二唑将两组多硝基苯偶联,分子通过三硝基苯甲酰氯与水合肼缩合后发生脱水环化反应构建了2,5-二苦基-1,3,4-噁二唑(DPO)。DPO热分解温度为342℃,表明共轭作用有效提升了化合物的热稳定性。Klapötke等[47]报道了与DPO相似结构的新型耐热含能化合物5,5′-双(2,4,6-三硝基苯基)-2,2′-双(1,3,4-噁二唑) (TKX-55),通过三硝基苯甲酰氯与草酰肼缩合后脱水环化形成两组噁二唑环系(Scheme11)。TKX-55的共轭体系较之DPO更大,但其热分解温度为335 ℃,与DPO相当,原因可能在于两组噁二唑环系直接相连在一定程度上降低了化合物的热稳定性,抵消了共轭体系提升所带来的稳定化效应。
Wang等[48]将4H,8H-双呋咱并[3,4-b:3′,4′-e]吡嗪(DFP)与苦基氯及1-氯-2,4-二硝基苯偶联,获得三类耐热含能化合物,其中与苦基氯偶联产物热分解温度达到415 ℃,而与1-氯-2,4-二硝基苯偶联产物分解温度有所降低,为405 ℃,与苦基氯偶联后再进行氮胺化反应所得产物热分解温度仅为283 ℃,表明该化合物中氨基较少,氢键稳定化作用较弱。Coburn等[49]利用三唑与苦基氯偶联获得具有高耐热性能的含能化合物2,6-二苦基[1,2-d][4,5-d′]双三唑-4,8-二酮,热分解温度达到430 ℃。Klapötke等[50]将2,6-二氨基吡啶与苦基氯偶联,对偶联产物进行硝化得到了具有良好耐热性能的含能化合物(2,6-双-(三硝基苯氨基)-3,5-二硝基吡啶(PYX)及其衍生盐,PYX的热分解温度可达460 ℃(Scheme12)。
Agrawal等[51]通过3,5-二氯苯胺与2,4,6-三氯三嗪偶联后硝化及胺化获得了2,4,6-三(3′,5′-二氨基-2′,4′,6′-三硝基苯胺)-1,3,5-三嗪(PL-1)分子(Scheme13)。分子中大量的氢键起到了较强的稳定化作用,因此较为钝感,同时具有较好的热稳定性,分解温度为335 ℃。
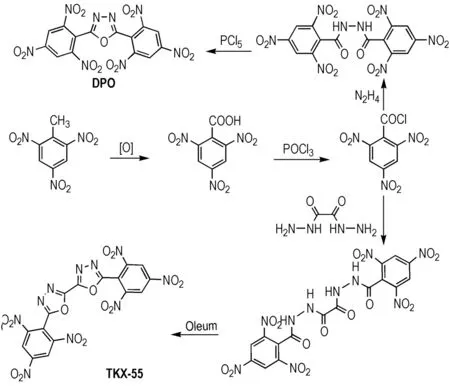
Scheme 11 Synthesis of DPO and TKX-55[46-47]
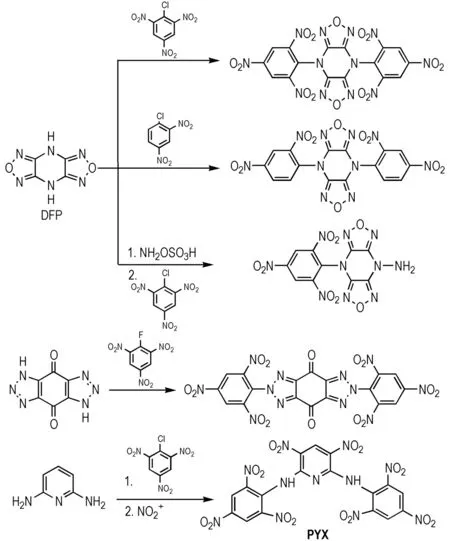
Scheme 12 Synthesis of polynitroaromatic compounds[48-50]
Agrawal 等[52]通过4-氯-3,5-二硝基苯胺在硝硫混酸的作用下发生一步原位的氧化及硝化反应,获得偶氮基偶联的多硝基氯苯结构,之后氯原子在氨基三唑的进攻性下被取代,获得N,N′-双(1,2,4-三唑-3-基)-4,4′-二氨基-2,2′,3,3′,5,5′,6,6′-八硝基偶氮苯(BTDAONAB),该化合物是目前已报道的耐热性能最高的含能化合物,其热分解温度达到550 ℃,分子中包含较大的共轭体系,有效地发挥了热稳定化效应(Scheme14)。

Scheme 13 Synthesis of PL-1[51]
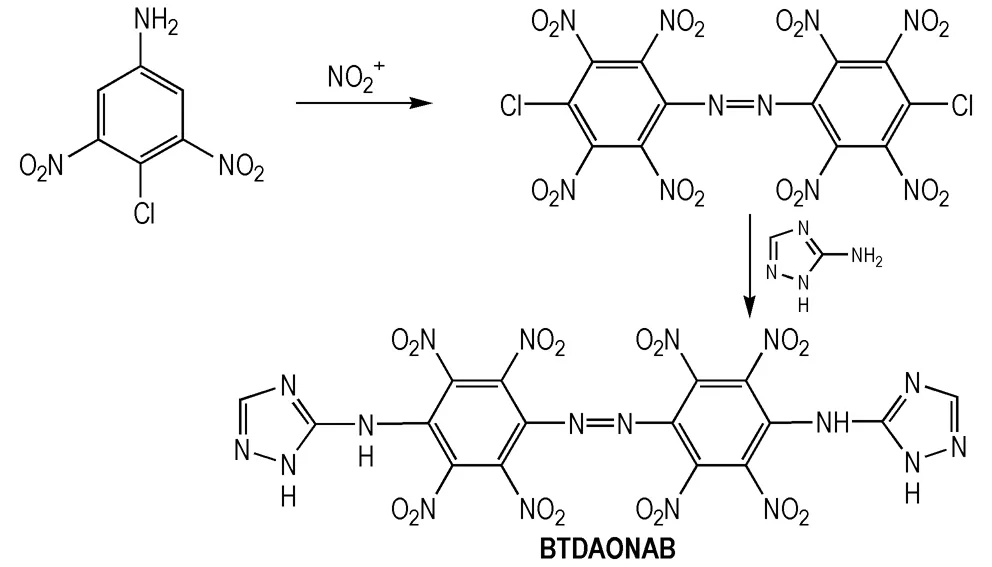
Scheme 14 Synthesis of polynitroaromatic substituted DFP and PYX[52]
5 结 论
耐热含能化合物骨架多为芳环结构,根据环系的不同可划分为单环、并环和偶联多芳环三类体系。单芳环含能化合物合成一般对硝基芳环结构进行官能团引入,其中通过芳环氨基化反应等实现氨基引入是最主要的模式; 并芳环含能化合物通常采用不同环化反应,将已有的芳环体系进一步扩展,在此过程中有利于形成独特的内盐结构; 偶联多芳环含能化合物则利用亲核取代等方式将多个芳环体系进行链接,共轭体系的大小直接取决于偶联芳环的数目。
作为特种用途含能材料,不断提升化合物的耐热性能始终是耐热含能化合物发展的主要方向。
(1)单环体系的耐热含能化合物基本依靠氢键的稳定化作用来提升耐热性能,在目前的结构设计及性能研究基础上进一步实现耐热性能大幅提升的空间较为有限。
(2)并环体系结构紧凑,具有比单环体系更强的共轭稳定化效应,尤其是并环体系可以形成有机内盐结构,利用成盐效应大幅改进化合物的热稳定性,是芳香耐热含能化合物应着重发展的研究方向。
(3)偶联多芳环体系对化合物耐热性能的提升主要依靠共轭体系的扩展,其偶联单元中稳定性最差的单元通常会直接降低化合物整体的热稳定性,如何将高度热稳定性的含能单元有效进行链接是该体系化合物设计及合成的主要研究方向。
除此之外,大分子及聚合物分子通常热稳定性较高,设计并发展具有类似石墨体系的大共轭含能芳环体系及发展具有强分子间作用力的立体网状含能聚合物结构,也将是有效提升化合物热稳定性的有效研究思路。
参考文献:
[1]Zhang Q H, Shreeve J M. Energetic ionic liquids as explosives and propellant fuels: a new journey of ionic liquid chemistry [J].ChemicalReviews, 2014, 114(20): 10527-10574.
[2]Agrawal J P, Hodgson R D. Organic chemistry of explosives[M]. John Wiley & Sons, UK, 2007.
[3]Badgujar D M, Talawar M B, Asthana S N, et al. Advances in science and technology of modern energetic materials: an overview[J].JournalofHazardousMaterials, 2008, 151(23): 289-305.
[4]Yan Q L, Zeman S. Theoretical evaluation of sensitivity and thermal stability for high explosives based on quantum chemistry methods: A brief review[J].InternationalJournalofQuantumChemistry, 2013, 113(8): 1049-1061.
[5]Yin P, Parrish D A, Shreeve J M. Energetic multifunctionalized nitraminopyrazoles and their ionic derivatives: ternary hydrogen-bond induced high energy density materials[J].JournaloftheAmericanChemicalSociety, 2015, 137(14): 4778-4786.
[6]Zhang J H, Zhang Q H, Vo T T, et al. Energetic salts with π-stacking and hydrogen-bonding interactions lead the way to future energetic materials[J].JournaloftheAmericanChemicalSociety, 2015, 137(4): 1697-1704.
[7]Agrawal J P. Past, present & future of thermally stable explosives[J].CentralEuropeanJournalofEnergeticMaterials, 2012, 9(3): 273-290.
[8]Coburn M D, Jackson T E. Picrylamino-substituted heterocycles. III. 1,2,4-triazoles[J].JournalofHeterocyclicChemistry, 1968, 5(2): 199-203.
[9]Chhaly L, Pritzkow W. 4-Nitro benzylchloride as a nucleophile in VNS reactions[J].JournalFürPraktischeChemie, 1994, 336(6): 558-560.
[10]Nandi A K. Assay of the thermally stable, insensitive, high explosive 1,3,5-triamino-2,4,6-trinitrobenzene (TATB)[J].CentralEuropeanJournalofEnergeticMaterials, 2014, 11(2): 3-13.
[11]Agrawal J. Some new high energy materials and their formulations for specialized applications[J].Propellants,Explosives,Pyrotechnics, 2005, 30(5): 316-328.
[12]Nandi A K, Kasar S M, Thanigaivelan U, et al. Formation of the sensitive impurity 1,3,5-triamino-2-chloro-4,6-dinitrobenzene in pilot plant TATB production[J].OrganicProcessResearch&Development, 2012, 16(12): 2036-2042.
[13]Pagoria P F, Mitchell A R, Schmidt R D. 1,1,1-Trimethylhydrazinium iodide: a novel, highly reactive reagent for aromatic amination via vicarious nucleophilic substitution of hydrogen [J].JournalofOrganicChemistry, 1996, 61(9): 2934-2935.
[14]王友兵, 王伯周, 叶志虎, 等. VNS法合成TATB[J]. 含能材料, 2011, 19(2): 142-146.
WANG You-bing, WANG Bou-zhou, YE Zhi-hu, et al. Synthesis of TATB by VNS method[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2011, 19(2):142-146.
[15]Li J S, Huang Y G, Dong H S. Theoretical calculation and molecular design for high explosives: theoretical study on polynitropyrazines and theirN-oxides[J].Propellants,Explosives,Pyrotechnics, 2004, 29(4): 231-235.
[16]He W D, Zhou G, Wong N B, et al. Intramolecular H-bonds in LLM-105 and its derivatives: a DFT study[J].JournalofMolecularStructure:Theochem, 2005, 723(1-3): 217-222.
[17]Philbin S P, Millar R W, Coombes R G. Preparation of 2,5-diamino-3,6-dinitropyrazine (ANPZ-i): a novel candidate high energy insensitive explosive[J].Propellants,Explosives,Pyrotechnics, 2000, 25(6): 302-306.
[18]Zuckerman N B, Shusteff M, Pagoria P F, et al. Microreactor flow synthesis of the secondary high explosive 2, 6-diamino-3, 5-dinitropyrazine-1-oxide (LLM-105)[J].JournalofFlowChemistry, 2015, 5(3): 178-182.
[19]Wei H, Gao H X, Shreeve J M.Chemistry-AEuropeanJournal, 2014, 20(51): 16943-16952.
[20]Jing S M, Liu Y C, Liu D C, et al. Research on a new synthesis of LLM-105 usingN-nitroso-bis(cyanomethyl)amine,CentralEuropeanJournalofEnergeticMaterials, 2016, 13(1): 21-32.
[21]Ritter H, Licht H H. Synthesis and reactions of dinitrated amino and diaminopyridines[J].JournalofHeterocyclicChemistry, 1995, 32(2): 585-590.
[22]Hollins R A, Merwin L H, Nissan R A, et al. Aminonitropyridines and theirN-oxides [J].JournalofHeterocyclicChemistry, 1996, 3(3): 895-904.
[23]Hollins R A, Merwin L H, Nissan R A, et al. AminonitroheterocyclicN-oxides-a new class of insensitive energetic materials[J].MaterialsResearchSocietySymposiumProceeding, 1996, 418: 31.
[24]Nair U R, Gore G M, Sivabalan R, et al. Preparation and thermal studies on tetranitrodibenzo tetraazapentalene (TACOT): A thermally stable high explosive[J].JournalofHazardousMaterials, 2007, 143(1-2): 500-505.
[25]Subramanian G, Eck G, Boyer J H, et al. Synthesis of benzotriazolo[1,2-a]benzotriazole derivatives as new high density, insensitive energetic materials[J].JournalofOrganicChemistry, 1996, 61(17): 5801-5803.
[26]Carboni R A, Kauer J C, Hatchard W R, et al. Aromatic azapentalenes. Ⅱ. reactions of monobenzo- and dibenzo-1,3a,4,6a-tetraazapentalenes[J].JournaloftheAmericanChemicalSociety, 1967, 89(11): 2626-2633.
[27]Balachari D, Trudell M L. Synthesis of new dipyridotetraazapentalenes[J].TetrahedronLetters, 1997, 38(50): 8607-8610.
[28]Li Y N, Shu Y J, Wang B Z, et al. Synthesis, structure and properties of neutral energetic materials based onN-functionalization of 3,6-dinitropyrazolo[4,3-c]pyrazole[J].RSCAdvances, 2016, 6(88): 84760-84768.
[29]李亚南, 唐婷, 廉鹏,等. 1,4-二氨基-3,6-二硝基吡唑[4,3-]并吡唑的合成、热性能及量子化学研究[J]. 有机化学, 2012, 32(3): 580-588.
LI YAN-nan, TANG Ting, LIAN Peng, et al. Synthesis, thermal performance and quantum chemistry study on 1,4-diamino-3,6-dinitropyrazolo[4,3-c]pyrazole[J].ChineseJournalofOrganicChemistry, 2012, 32(3): 580-588.
[30]Norris W P. US 000476[P], 1988.
[31]王伯周, 霍欢, 李吉祯,等. 4,6-二硝基-5,7-二氨基苯并氧化呋咱(CL-14)的合成与表征[J]. 有机化学, 2011, 31(1):132-135.
WANG Bo-zhou, HUO Huan, LI Ji-zhen, et al. Synthesis and characterization of 4,6-dinitro-5,7-diamino benzenfuroxan (CL-14)[J].ChineseJournalofOrganicChemistry, 2011, 31(1):132-135.
[32]董岩.多氨基多硝基苯并氧化呋咱及其金属配合物的合成与性能研究[D]. 南京: 南京理工大学, 2014.
DONG Yan. Research on synthesis and performance of polyamino and poly niro benzofuroxan and their metal complex[D]. Nanjing: Nanjing University of Science and Technology, 2014.
[33]Nair U R, Asthana S N, Rao A S, et al. Advances in high energy materials [J].DefenceScienceJournal, 2010, 60(2):137-151.
[34]Gilbert E E. The preparation of hexanitrostilbene from hexanitrobibenzyl[J].Propellants,Explosives,Pyrotechnics, 1980, 5(6): 168-172.
[35]Lu T T, Yao K, Mao Y, et al. A novel and efficient synthesis of hexanitrostilbene byN-hydroxyphthalimide/FeCl2-catalyzed aerobic dehydrogenation of hexanitrobibenzyl[J].JournalofEnergeticMaterials, 2013, 31(3): 217-223.
[36]Sollott G P. Conversion of 2,4,6-trinitrobenzyl chloride to 2,2′,4,4′,6,6′-hexanitrostilbene by nitrogen bases[J].JournalofOrganicChemistry, 1982, 47(12): 2471-2474.
[37]Rieckmann T, Völker S, Lichtblau L, et al. Investigation on the thermal stability of hexanitrostilbene by thermal analysis and multivariate regression[J].ChemicalEngineeringScience, 2001, 56(4): 1327-1335.
[38]张静, 王娟, 徐海凤,等. HNAB的制备及其热分解动力学[J]. 含能材料, 2013, 21(1): 7-11.
ZHANG Jing, WANG Juan, XU Hai-feng. Synthesis and thermal decomposition kinetics of hexanitroazobenzene[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2013, 21(1): 7-11.
[39]Dacons J C. Nonanitro terphenyi: US, US 3755471[P], 1973.[40]Hassan J, Sévignon M, Gozzi C, et al. Aryl-aryl bond formation one Century after the discovery of the Ullmann reaction[J].ChemicalReviews, 2002, 102(5): 1359-1470.[41]Hagel R, Redecker K H. Polynitropolyphenylene, a high-temperature resistant, non-crystalline explosive[J].Propellants,Explosives,Pyrotechnics, 1987, 12(6): 196-201.
[42]Simpson R L, Pagoria P F, Mitchell A R, et al. Synthesis, properties and performance of the high explosive ANTA[J].Propellants,Explosives,Pyrotechnics, 1994, 19(4): 174-179.
[43]Charrue P, Laval F, Wartenberg C. Conception, synthèse et caractérisation d′un nouvel explosif insensible et énergétique : Le DANTNP[J].Propellants,Explosives,Pyrotechnics, 1995, 20(1): 23-26.
[44]Coburn M D, Hiskey M A, Lee K Y, et al. An improved synthesis of 5-amino-3-nitro-1H-1,2,4-triazole (ANTA), a useful intermediate for the preparation of insensitive high explosives[J].JournalofEnergeticMaterials, 1991, 9(5): 415-428.
[45]Li C, Zhang M, Chen Q, et al. Three-dimensional metal-organic framework as super heat-resistant explosive: potassium 4-(5-amino-3-nitro-1H-1,2,4-triazol-1-yl)-3,5-dinitropyrazole[J].Chemistry-AEuropeanJournal, 2017, 23(7): 1490-1493.
[46]Sitzman M E. 2,5-Dipicryl-1,3,4-oxadiazole: a shock-sensitive explosive with high thermal stability (thermally-stable substitute for petn)[J].JournalofEnergeticMaterials, 1988, 6(1-2):129-144.
[47]Klapötke T M, Witkowski T G. 5,5′-Bis(2,4,6-trinitrophenyl)-2,2′-bi(1,3,4-oxadiazole) (TKX-55): Thermally stable explosive with outstanding properties[J].ChemPlusChem, 2016, 81(4): 357-360.
[48]Liu N, Shu Y J, Li H, et al. Synthesis, characterization and properties of heat-resistant explosive materials: polynitroaromatic substituted difurazano[3,4-b:3′,4′-e]pyrazines[J].RSCAdvances, 2015, 5(54): 43780-43785.
[49]Berlin J K, Coburn M D. Picryl derivatives of benzo[1,2-d:4,5-d′]bistriazole and benzo[1,2-d:4,5-d′]bistriazole-4,8-dione[J].JournalofHeterocyclicChemistry, 1975, 12(2): 235-237.[50]Klapötke T M, Stierstorfer J, Weyrauther M, et al. Synthesis and investigation of 2,6-bis(picrylamino)-3,5-dinitro-pyridine (PYX) and its salts[J].Chemistry, 2016, 22(25): 8619.
[51]Agrawal J P, Bapat V K, Mehilal, et al. Synthesis and characterization of 2,4,6-tris (3′, 5′-diamino-2′,4′,6′-trinitrophenylamino)-1,3,5-triazine (PL-1): a new thermally stable insensitive high explosive[J].JournalofEnergeticMaterials, 2000, 18(4): 299-309.
[52]Agrawal, J P, Sikder A K, Sikder N.N,N′-bis(1,2,4-triazol-3-yl-)-4,4′-diamino-2,2′,3,3′,5,5′,6,6′-octanitroazobenzene (BTDAONAB): a new thermally stable insensitive high explosive[J].IndianJournalofEngineeringandMaterialsSciences, 2004, 11(6): 516.
