酸对过氧化氢异丙苯热稳定性的影响研究
2017-05-02臧晓勇陈萌萌
王 昊 , 臧晓勇 , 陈萌萌
(1.青岛科技大学 环境与安全工程学院 , 山东 青岛 266042 ; 2.青岛海湾集团有限公司 , 山东 青岛 266000 ; 3.青岛海晶化工集团有限公司 , 山东 青岛 266000)
•开发与研究•
酸对过氧化氢异丙苯热稳定性的影响研究
王 昊1,2, 臧晓勇3, 陈萌萌1
(1.青岛科技大学 环境与安全工程学院 , 山东 青岛 266042 ; 2.青岛海湾集团有限公司 , 山东 青岛 266000 ; 3.青岛海晶化工集团有限公司 , 山东 青岛 266000)
为研究酸对过氧化氢异丙苯(CHP)热稳定性的影响,利用C600微量量热仪研究了CHP及CHP与不同含量硫酸、乙酸的混合物在空气中受热分解的反应和放热特性,利用Semenov热爆炸模型计算出了自加速分解温度(SADT)。结果表明,与酸以一定比例混合后能够使CHP的起始放热温度、最大放热温度降低,乙酸对其热稳定性的影响更加明显;计算得到25%CHP的SADT为140 ℃,通过对CHP与不同含量硫酸、乙酸混合物SADT进行比较,发现少量的硫酸和乙酸均能降低CHP的SADT,而CHP与乙酸混合物的SADT更小。
C600微型量热仪 ; 过氧化氢异丙苯 ; 热稳定性 ; 自加速分解温度
过氧化氢异丙苯(CHP)作为生产苯酚、丙酮和苯乙烯以及许多聚合反应的重要原料,在化工生产中有着极其广泛的应用,这主要归结为其相对较弱的过氧键(键分解能为83.717~209.292 kJ/mol)[1]。然而,由于不稳定过氧基的存在,使得CHP在生产和储运过程中极易分解,如果接触到热源、酸催化剂、碱催化剂、金属化合物或机械冲击,有可能导致火灾爆炸及反应失控事故[2-5]。CHP作为一种重要的有机过氧化物类化工原料,在实际存储及使用中难免会与酸性物质接触,因此探讨酸对CHP热稳定性的影响对于降低其在存储使用过程中发生热失控事故的危险性具有重要意义。
国内外一些学者通过应用多种量热仪,例如微差扫描量热仪(DSC)、热活性检测仪(TAM)、加速量热仪(ARC)、紧急排放安全处理仪(VSP2)和C80微量量热仪,研究了在各种过程条件下有机过氧化物的热危害性和分解动力学[6-9]。然而,很长一段时间里酸催化分解特征并没有给出较详细的分析。
本文利用C600微量量热仪对25%CHP和不同浓度硫酸、乙酸以不同比例混合后在空气气氛下的热分解反应进行研究,讨论了两种酸对CHP热稳定性的影响,根据实验得出数据,并利用Semenov热爆炸模型计算出了SADT。
1 实验试剂和方法
1.1 试剂
样品组成及配比如表1所示。其中,25%CHP根据国药集团化学试剂有限公司生产的CHP(纯度≥70%)配制而成;硫酸(纯度95.0%~98.0%)由烟台三和化学试剂有限公司生产,乙酸(纯度≥99.5%)由国药集团化学试剂有限公司生产。
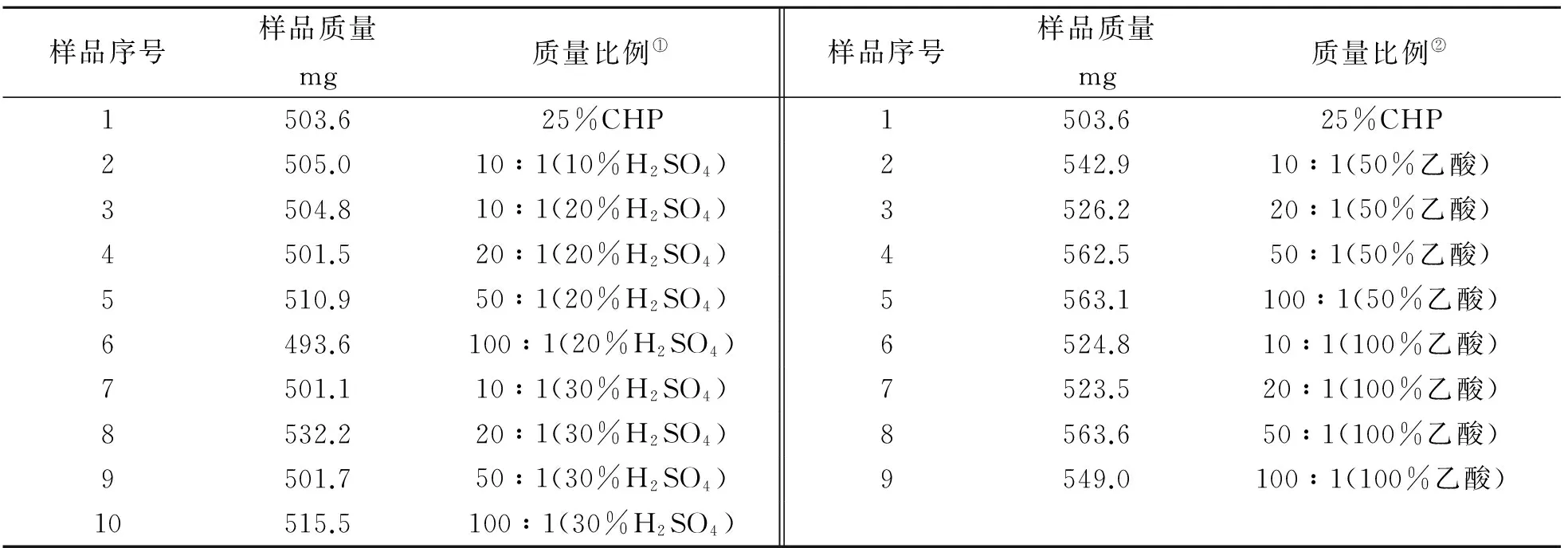
表1 实验样品的组成及配比
注:①为25%CHP与不同浓度H2SO4的质量比;②为25%CHP与不同浓度乙酸的质量比。
1.2 分析测试仪器
C600微量量热仪能够在程序温度控制下,测量处于同一温度条件下的样品和参比物(参比物为Al2O3,稳定,不易发生反应)在单位时间内的能量差随温度的变化规律,其优点是热敏感度高、精确度好,另外对热通量的信号采集效率比同步热分析仪(DSC)大3~4个数量级,能够更准确地反映物质本质属性。
1.3 测试方法
称取适量待测样品并添加到样品池,向参比池内放入同等质量的惰性物质(Al2O3),将参比池和样品池装入C600微量量热仪。设定升温速率为1.0 ℃/min,通过C600控制软件实时观察实际反应进程,直至试验结束。
2 酸对过氧化氢异丙苯稳定性的影响
CHP在常温和正常条件下是稳定的,但是在高温酸性条件下却会分解,因此这里着重研究一定升温速率下不同浓度的硫酸、乙酸溶液对25%CHP热稳定性的影响,得出的实验数据可以为CHP法环氧丙烷工艺提供最基本的技术支持。
2.1 无机酸对过氧化氢异丙苯稳定性的影响
25%CHP及25%CHP与不同浓度的硫酸溶液以不同比例混合的热流—温度曲线见图1,这是微量量热法得到的各样品热分解过程的典型曲线。
对图1中各样品的放热曲线进行数据处理,得到T0、Tp和ΔH等热特性参数,见表2。
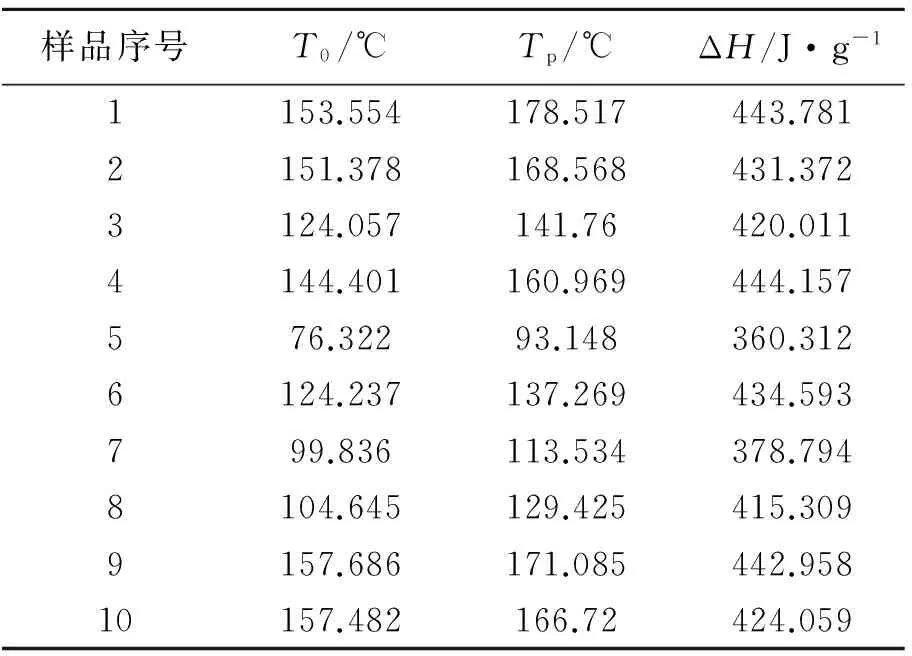
表2 各实验样品的热特性参数
注:T0,初始放热温度;Tp,最高放热温度;ΔH,放热量。
从图1中可以得出,25%CHP及25%CHP与不同浓度硫酸以不同比例混合后在50~220 ℃出现一个很明显的放热峰,而且与不同浓度硫酸以不同比例混合后的放热峰较纯25%CHP有着不同程度的提前,说明25%CHP遇硫酸后分解反应提前发生,25%CHP中混入硫酸后能够促进其分解反应的发生。
下面结合表2的数据,分别作各实验样品的T0和Tp关系曲线图,如图2所示。

图1 各实验样品的放热曲线
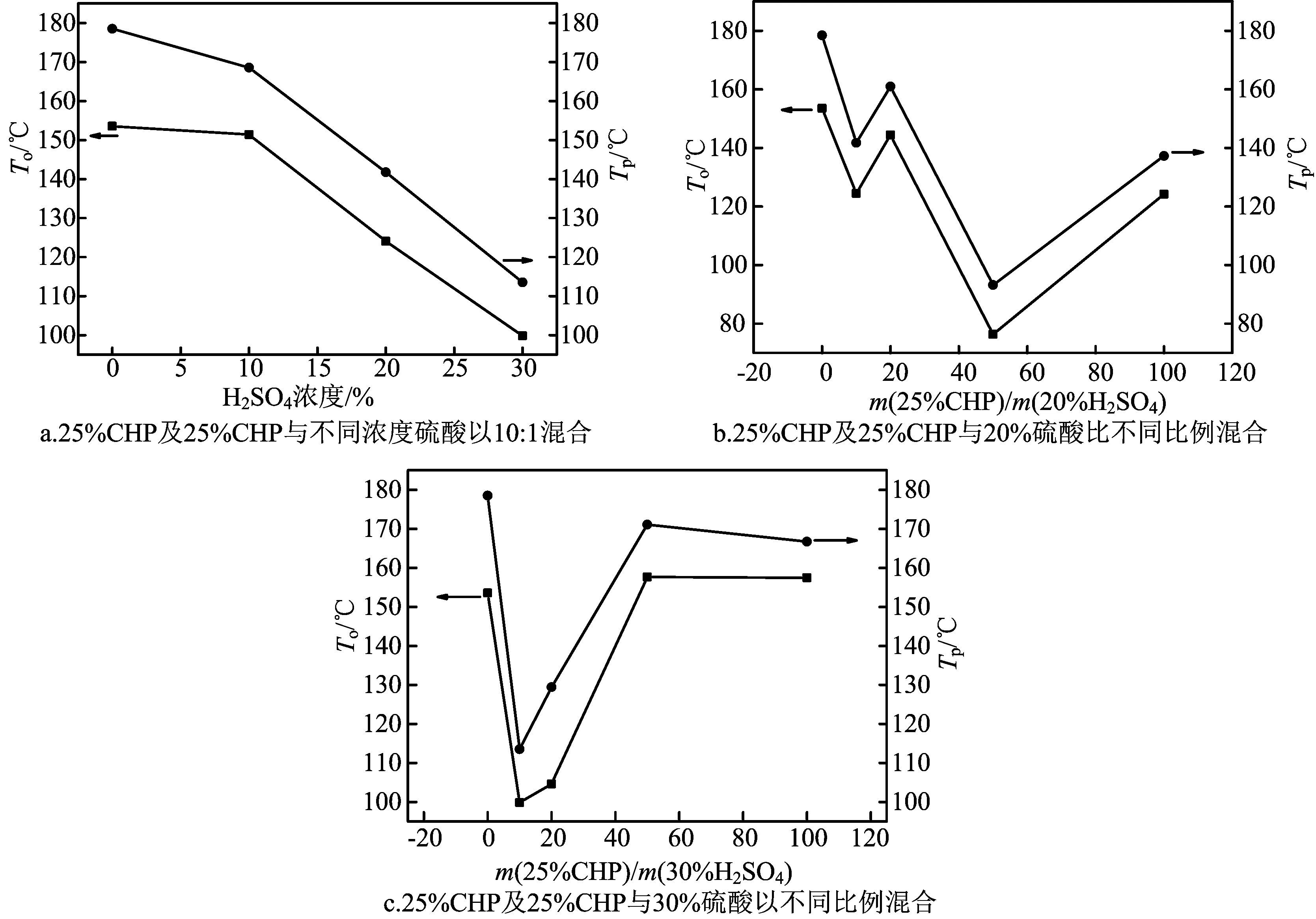
图2 不同硫酸含量与T0和Tp关系曲线图
由图2a可以看出,25%CHP与不同浓度的硫酸以质量比10∶1混合后T0和Tp随硫酸浓度的增大呈现明显的减小趋势。样品7的T0和Tp最小,说明混入高浓度的硫酸对25%CHP的分解反应促进作用最强。然而对比图2b和2c得出,同一浓度的酸以不同比例与25%CHP混合,对其分解反应的影响也比较明显,样品5的T0和Tp最小,即25%CHP和20%H2SO4以质量比50∶1混合时,T0和Tp达到最低值,分别为76.322 ℃和93.148 ℃,较25%CHP的T0和Tp分别降低了77.232 ℃和85.369 ℃,说明该比例混合时对25%CHP的分解促进作用是最强的,其次是与30%的H2SO4以质量比10∶1和20∶1混合。但是少量的高浓度的酸对25%CHP的分解没有影响。
2.2 有机酸对过氧化氢异丙苯稳定性的影响
25%CHP及25%CHP与不同浓度的乙酸溶液以不同比例混合的热流—温度曲线见图3,这是微量量热法得到的各样品热分解过程的典型曲线。
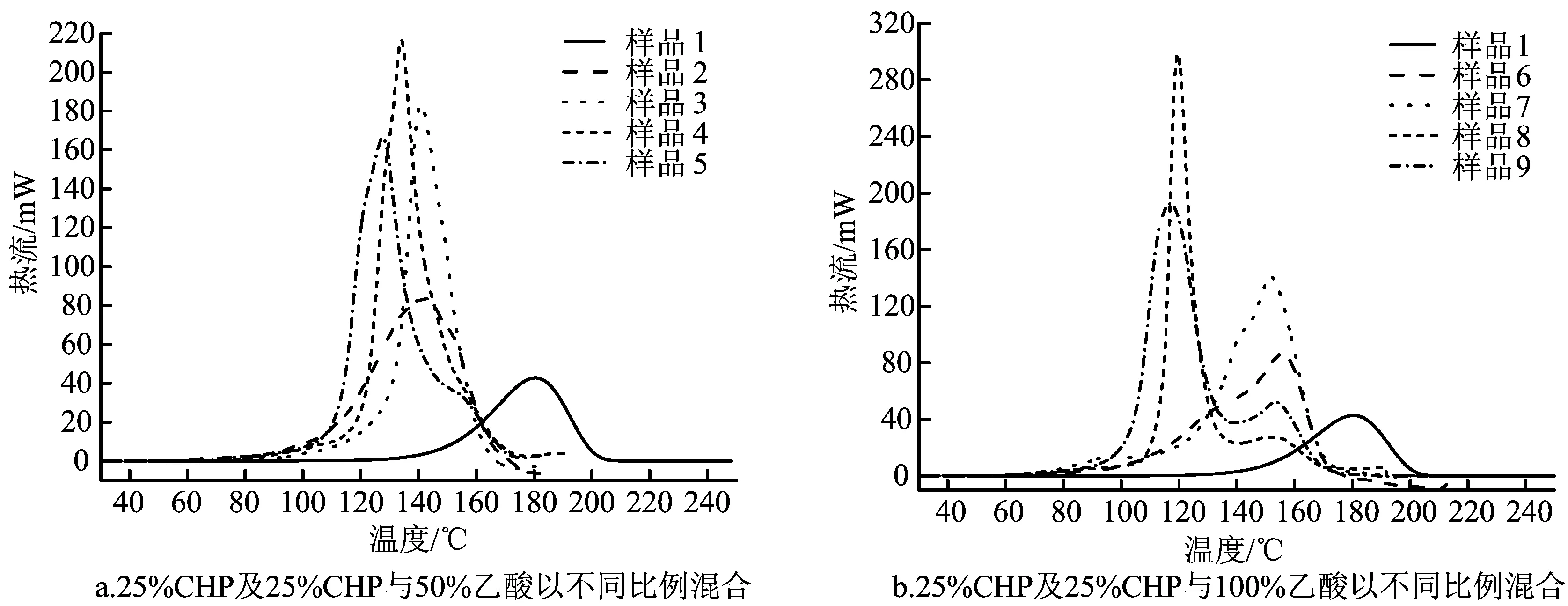
图3 各实验样品的放热曲线
对图3中各样品的放热曲线进行数据处理,得到T0、Tp和ΔH等热特性参数,见表3。
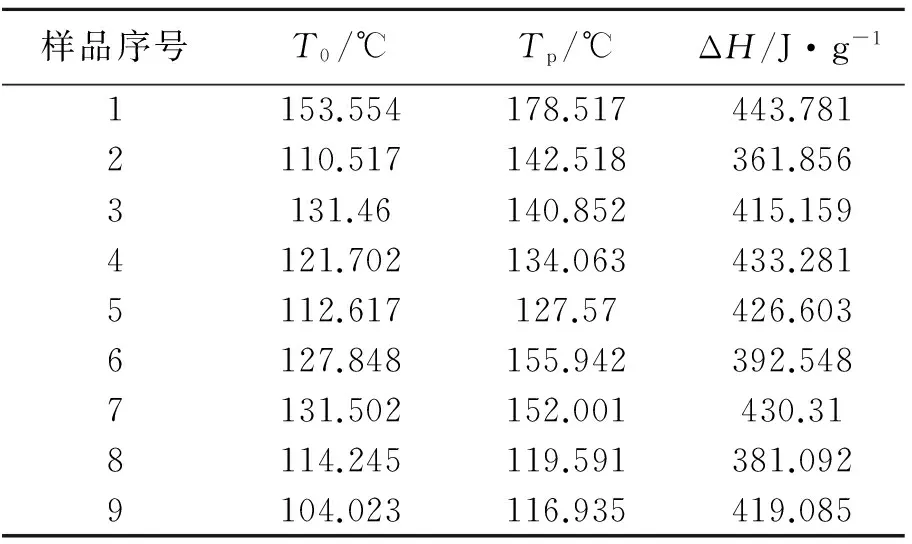
表3 各实验样品的热特性参数
注:T0,初始放热温度;Tp,最高放热温度;ΔH,放热量。
从图3中可以得出,25%CHP及25%CHP与不同浓度乙酸以不同比例混合后在80~220 ℃出现一个很明显的放热峰,而且25%CHP与不同浓度乙酸以不同比例混合后的放热峰较纯25%CHP有着不同程度的明显提前,说明25%CHP遇乙酸后分解反应提前发生,25%CHP中混入乙酸后能够促进其分解反应的发生。下面结合表3的数据,分别作各实验样品的T0和Tp关系曲线图,如图4所示。
由图4a和4b可看出,25%CHP与不同浓度的乙酸以不同质量比混合后T0和Tp随质量比的增大呈现明显的减小趋势。样品9的T0和Tp最小,即25%CHP和100%乙酸以质量比100∶1混合时,T0和Tp达到最低值,分别为104.023 ℃和116.935 ℃,较25%CHP的T0和Tp分别降低了49.531 ℃和61.582 ℃,说明少量的高浓度乙酸混入25%CHP中对其的分解反应促进作用最强,与50%的乙酸以质量比10∶1和100∶1混合的促进作用次之。而大量乙酸的存在对25%CHP分解反应的影响相对较小,说明在25%CHP受热分解的过程中,过量H+的存在对CHP的分解有抑制作用,使得CHP分解反应速率减慢,这个可以从样品6、7的放热峰比较宽可以看出。
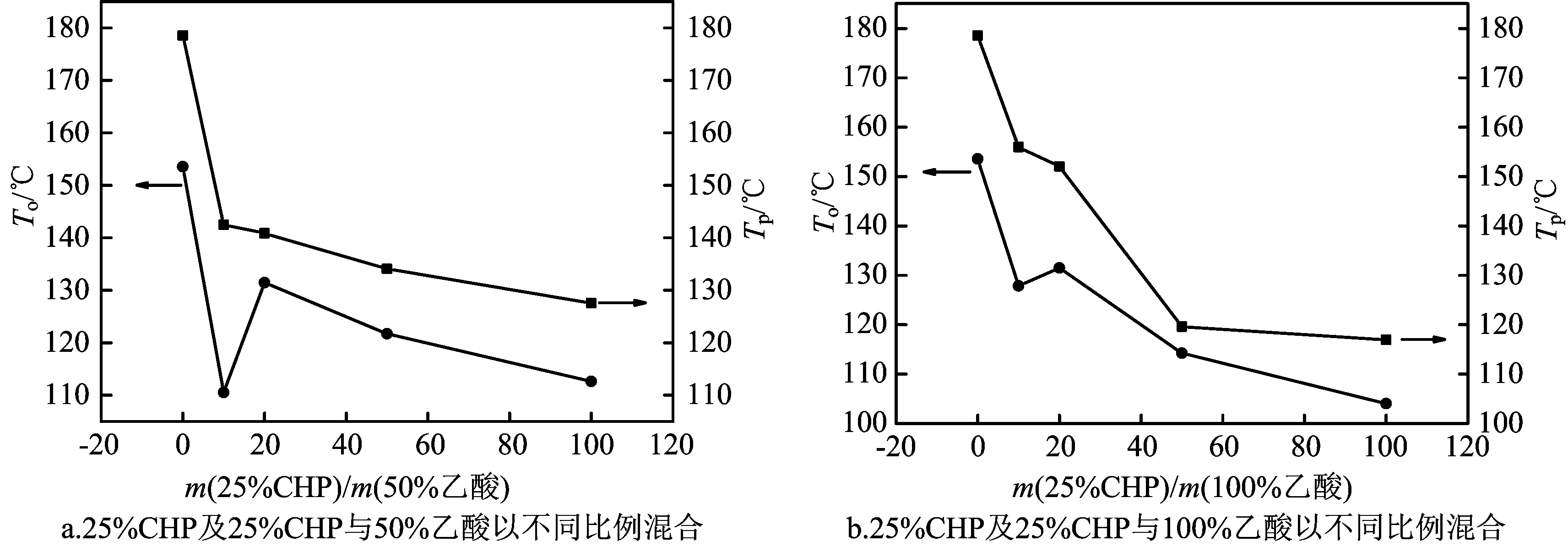
图4 不同乙酸含量与T0和Tp关系曲线图
3 SADT推算
Semenov模型下,反应初期反应体系热平衡方程式为[10]:
(1)
(2)
在反应物发生热爆炸的临界温度 ,满足条件:
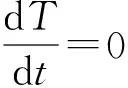
(3)
此时的环境温度Tα即为Semenov模型下的SADT:
(4)
根据以上公式,计算得到2.1和2.2中各实验样品25 kg标准包装的SADT结果见表4,包装参数为系统与环境的接触面积S=4812.4 cm2,表面换热系数U=2.838 6×10-4J/(cm2·K·s)[11]。

表4 各实验样品SADT计算结果
从表4的计算结果可知,少量无机酸和有机酸的存在使25%CHP的SADT降低,尤其是硫酸的影响最明显,SADT最大降低值达到77 ℃,增加了CHP的危险性。因此,在存储、运输和使用CHP的过程中,应尽量避免酸碱性物质与CHP的接触,并控制好CHP储运及使用环境温度。在环氧丙烷工艺及其它涉及CHP的工艺中,严密监测混入的酸性物质,避免酸性物质给工艺带来不可控危险性。
4 结论
25%CHP与硫酸和乙酸混合后,其起始放热温度和最大放热温度都有不同程度的降低,危险性增大,这就要求存储和使用CHP的过程中应尽量避免与酸性物质接触,并控制好CHP的储运及使用环境温度,以免危害事故的发生。SADT计算结果表明,少量硫酸和乙酸的存在均能降低CHP的SADT,增加CHP的热危险性,尤其应注意避免与强酸性物质的接触,同时控制温度,避免发生不可控事故。
[1] Hou H Y,Shu C M,Tsai T L.Reactions of cumene hydroperoxide mixed with sodium hydroxide[J].Journal of Hazardous Materials,2008,152:1214-1219.
[2] Levin M E,Gonzales N O,Zimmerman L W,et al.Kinetics of acidcatalyzed cleavage of cumene hydroperoxide[J].Hazard Mater,2005,130:88-106.
[3] Wu K W,Hou H Y,Shu C M.Thermal phenomena studies for dicumyl peroxide at various concentrations by DSC[J].Journal of Thermal Analysis and Calorimetry,2006,83(1):41-44.
[4] Hou H Y,Liao T S,Du H Y S,et al.Thermal hazard studies for dicumyl peroxide by DSC and TAM[J].Journal of Thermal Analysis and Calorimetry,2006, 83(1): 167~171.
[5] Wu S H,Wang G Y W,Wu T C,et al.Evaluation of thermal hazards for dicumyl peroxide by DSC and VSP2[J].Journal of Thermal Analysis and Calorimetry,2008,93(1):189-194.
[6] Hou H Y,Liao T S,Duh Y S,et al.Thermal hazard studies for dicumyl peroxide by DSC and TAM[J].Therm Anal Calorim.2006,83(1):167-171.
[7] 金满平,孙 峰,石 宁,等.水和弱酸对过氧化氢异丙苯热危险性的影响[J].化工学报,2012,63(12):4096-4102.
[8] Hou H Y,Duh Y S,Lin W H,et al.Reactive incompatibility of cumene hydroperoxide mixed with alkaline solutions[J].Therm Anal Calorim,2006,85(1):145-150.
[9] Li X R,Koseki H.Thermal decomposition kinetic of liquid organic peroxides[J].Journal of Loss Prev Process Ind.2005,18(4-6):460-464.
[10] Semenov N N.Some Problems in chemical kinetics and neactivity[M].U S A:Princeton University Press,1959.
[11] Yu Yuhua,Hasegawa Kazutoshi.Derivation of the self-accelerating decomposition temperature for self-reactive substances using isothermal calorimetry[J].Journal of Hazardous Materials,1996,45(2-3):193-205.
Study on the Influence of Acid on the Thermal Stability of Cumene Hydroperoxide
WANG Hao1,2, ZANG Xiaoyong3, CHEN Mengmeng1
(1.College of Environment and Safety Engineering , Qingdao University of Science and Technology , Qingdao 266042 , China ; 2.Qingdao Hiwin Group Ltd , Qingdao 266000 , China ; 3.Qingdao Hygain Chemical Group Ltd, Qingdao 266000 , China)
In order to study the influence of acid on the thermal stability of cumene hydroperoxide (CHP),the thermal decomposition of CHP and CHP mixtures with different content of sulfuric acid and acetic acid in the air is studied by C600 calorimeter.The corresponding kinetic and thermodynamic parameters based on experimental data obtained,makes use of Semenov model to calculate the SADT.The results show that mixed with acertain proportion of acid can reduce the initial exothermic temperature,peak exothermic temperature,it is more obvious that the effect of acetic acid on its thermal stability.Calculated SADT of CHP is 140℃, by comparing the SADT calculation results of samples, can know that small amount of strong acid and weak acid can reduce SADT of CHP, and have lower SADT when mixture with acetic acid.
C600 calorimeter ; CHP ; thermal stability ; SADT
2016-12-15
王 昊(1979-),男,中级经济师,从事生产管理工作,E-mail:wh@qdhw.com。
TQ241
A
1003-3467(2017)03-0018-05
