六堡茶急性和亚急性毒性安全性评价研究
2017-04-22吴文亮林勇刘仲华黄建安龙志荣滕翠琴马士成邱瑞瑾曹中环
吴文亮,林勇,刘仲华,黄建安,龙志荣,滕翠琴,马士成,邱瑞瑾,曹中环
1. 湖南农业大学茶学教育部重点实验室,湖南 长沙 410128;2. 国家植物功能成分利用工程技术研究中心,湖南 长沙 410128;3. 植物功能成分利用协同创新中心,湖南 长沙 410128;4. 梧州市六堡茶研究院,广西 梧州 543003;5. 梧州市农业科学研究所,广西 梧州543003;6. 湖南省农业科学院茶叶研究所,湖南 长沙 410125
六堡茶急性和亚急性毒性安全性评价研究
吴文亮1,2,3,6,林勇1,2,3*,刘仲华1,2,3,黄建安1,2,3,龙志荣4,5,滕翠琴4,5,马士成4,5,邱瑞瑾4,5,曹中环4,5
1. 湖南农业大学茶学教育部重点实验室,湖南 长沙 410128;2. 国家植物功能成分利用工程技术研究中心,湖南 长沙 410128;3. 植物功能成分利用协同创新中心,湖南 长沙 410128;4. 梧州市六堡茶研究院,广西 梧州 543003;5. 梧州市农业科学研究所,广西 梧州543003;6. 湖南省农业科学院茶叶研究所,湖南 长沙 410125
六堡茶产制历史悠久,是广西特色名优农产品,但其安全性研究不够。为了探明六堡茶饮用的安全性,本实验以广西梧州六堡茶为原料,采用国家标准方法分析六堡茶常规理化成分;并按照食品安全性毒理学评价程序,进行较系统的六堡茶急性毒性和亚急性毒性实验。结果表明:六堡茶理化指标符合广西地方标准,且3个批次有较好的重复性;在小鼠急性毒性试验中,采用bliss法计算得出六堡茶半数致死剂量(LD50)为9.38 g·kg-1,95%的可信限为8.43~10.44 g·kg-1,大于5 g·kg-1的经口急性毒性标准;采用大鼠30 d喂养实验发现,期间动物的生长发育良好,六堡茶 3个剂量组(0.47 g·kg-1·d-1、0.94 g·kg-1·d-1、1.88 g·kg-1·d-1)的动物体质量、血常规指标、血生化指标、脏器指数与对照组比较,均无显著性差异(P>0.05)。因此从食品毒理学的标准来看,六堡茶属于无毒级食品,符合食品安全性要求。
六堡茶;急性毒性;亚急性毒性;半致死剂量
六堡茶作为黑茶家族的重要成员,是广西特色名优农产品,因原产于广西梧州市苍梧县六堡镇而得名,至今已有一千五百多年的历史,远销日本、东南亚各国及粤港澳地区,是广西传统的出口产品[1]。近年来,随着黑茶的热销,使得同属黑茶类的六堡茶倍受消费者青睐,六堡茶消费市场不断升温,现在也日渐为内地其他地方消费者认可;品牌价值不断提升,目前年产量已超1万t,产值达10亿元以上,2016年6月《2016中国茶叶区域公用品牌价值排行榜》发布,六堡茶品牌价值 15.79亿元,居中国茶叶区域品牌价值第28位、黑茶类第3位、广西茶类第1位。
根据世界贸易组织(WTO)的有关协定要求和食品法典委员会(CAC)的有关准则,食品安全性评价是食品卫生标准制定的重要依据[2]。同时,应用食品毒理学的方法对食品进行安全性评价,可为我们正确认识和开发食品新资源提供可靠的技术保障。六堡茶作为我国传统饮品,已有较久的安全饮用历史,从某种意义上讲,可基本认为饮用六堡茶的主导产品是安全的,但六堡茶生产中存在一系列微生物参与的渥堆工序,增加了成品茶代谢产物及生化成分的复杂性和鉴定难度。因此对六堡茶进行有效的安全性毒理学评价是保证六堡茶质量安全,保障出口(卫生标准与国际接轨),促进茶叶消费和产业健康持续发展的必由之路。
从目前的黑茶安全性研究来看,仅见对云南普洱茶和湖南安化黑茶进行过较为系统的安全性毒理学评价[2-6]。而作为黑茶大家族中的一个很重要成员——广西六堡茶的安全性评价研究涉及较少,尤其是特别重要的六堡茶急性及亚急性毒性安全性评价研究缺乏相关确切的试验数据[7]。这样必然会影响到六堡茶及整个黑茶产业的健康可持续发展。基于此,本研究以六堡茶质量安全特性为出发点,参照食品安全性毒理学评价程序[8-9],开展六堡茶的急性及亚急性毒理学试验并对质量安全问题进行理论分析,为促进六堡茶及黑茶消费热的兴起提供科学依据。
1 材料与方法
1.1 试验材料
1.1.1 茶叶原料
六堡茶(三鹤牌,批号:0128、0211、0401)由广西壮族自治区梧州茶厂提供。
1.1.2 试验动物
昆明种(KM)小鼠,SPF级,雌雄各半,体质量 18~22 g,购自湖南斯莱克景达实验动物有限公司,试验动物生产许可证号:SCXK(湘)2011-003。
SD大鼠,SPF级,雌雄各半,体质量60~80g,购自湖南斯莱克景达实验动物有限公司,试验动物生产许可证号:SCXK(湘)2013-004。
基础饲料主要营养成分:粗蛋白24.3%,粗脂肪7.5%,粗纤维3.5%,粗灰粉8.6%,钙1.16%,磷0.7%,含水量7.5%。
1.1.3 试验仪器
LC10AT-VP Plus高效液相色谱系统(日本岛津公司),UV-2550型紫外分光光度计(日本 Shimadzu公司),TBA-40FR型全自动生化分析仪(日本东芝公司),血液细胞分析仪(美国贝克曼公司),MODULYOD-230冷冻干燥机(广州三元科技有限公司),EASYpureⅡ纯水仪(杭州普瑞科技有限公司),SK3300LH超声波清洗器(上海科导超声仪器有限公司),电热恒温水浴锅(江苏金坛市荣华仪器制造有限公司),ABl04-N电子分析天平(梅特勒-托利多仪器有限公司),灌胃器等。1.1.4 试验试剂
血清谷丙转氨酶(Alanine transaminase,ALT)、谷草转氨酶(Aspartate transaminase,AST)、血糖(Glucose,Glu)、总胆固醇(Total cholesterol,TC)、甘油三酯(Triglyceride,TG)、高密度脂蛋白胆固醇(High density lipoprotein cholesterol,HDL-C)试剂盒均购自上海科华生物工程股份有限公司(批号:20160622)。
1.2 试验方法
1.2.1 茶样干粉制备
取六堡茶样品100 g,用沸水3次浸提(每次的料液比为 1∶10,浸提时间分别为 20 min),纱布过滤,合并3次浸提茶汤,减压浓缩至 100 mL,再将浓缩的茶汤于-20℃预冻12 h,放入冷冻干燥机进行干燥后收集、称重、密封包装,-20℃保存。
1.2.2 茶样常规成分测定
水浸出物的测定按GB/T 8302—2002《茶水浸出物测定》方法,水分的测定按 GB/T 8304—2002《茶 水分测定》方法,茶多酚的测定按GB/T 8313—2008《茶叶中茶多酚和儿茶素类含量的检测方法》,咖啡碱的测定按GB/T 8312—2002《茶 咖啡碱测定》方法,氨基酸的测定按GB/T 8314—2002《茶 游离氨基酸总量测定》方法。
1.2.3 动物实验
急性毒性试验:①预测试动物全死和不死剂量:参照文献[2]的方法,取体质量18~22 g健康昆明小鼠,适应性喂养4 d后,用蒸馏水溶解茶样干粉配置1个高浓度的茶样剂量(0.3 g·mL-1),再稀释设置组距3~10倍的多个剂量组,以4只小鼠为1组,对各组试验小鼠采用经口灌胃,每次灌胃剂量20 mL·kg-1;对高剂量组采取1日内2或3次灌胃,每次间隔4 h。常规观察饲养 7 d,记录各组动物死亡和中毒症状,测试出茶样的全死和不死剂量。②茶样LD50的测定:根据上述预测试结果,参照文献方法[3,10]对茶样分别在全死与无死剂量间按 0.8等比设 4~6个剂量组,每个剂量组用18~22 g小鼠10只,雌雄各半,另设纯水对照组。试验时,小鼠禁食给水 12 h后,以 20 mL·kg-1的灌胃剂量对每只小鼠灌胃一定浓度的茶汤。对于高剂量组,可以采取1日内多次灌胃,每次间隔4 h。对灌胃后小鼠活动状况、死亡时间、体质量及取食状况进行观察记录,并对死亡动物进行剖检。检查各组织和脏器的体积、颜色、质地等有无异常,如有异常及时取材,进行组织病理学检查。观察 14 d后用Bliss法对各茶样剂量组的动物死亡情况进行统计分析。实验期间动物饲养环境:室内气温20~25℃,湿度70%~90%,光照12 h·d-1。
亚急性毒性试验:①大鼠30 d喂养实验:取4周龄健康SD大鼠80只,适应性喂养 1周后,随机分4个组(空白对照组、六堡茶低剂量组、中剂量组、高剂量组),每组20只,雌雄各半,分笼喂养。按照《保健食品检验与评价技术规范》的毒理学检验方法的要求[8],茶 汤剂量分 别为 470 mg·kg-1·d-1、 940 mg·kg-1·d-1、1 880 mg·kg-1·d-1(1/20 LD50、1/10 LD50、1/5 LD50),每天灌服1次,连续30 d,每周称体质量一次,同时设对照组,灌胃蒸馏水。②指标观察与检测:每天观察大鼠的行为、活动、饮食、睡眠、毛色、粪便等的变化。实验末期,大鼠禁食过夜后,称体质量,腹腔注射2%戊巴比妥钠麻醉大鼠,眼眶取血2份,一份血样抗凝处理用动物血液细胞分析仪检测白细胞数目(WBC)、红细胞数目(RBC)、红细胞压积(HCT)、平均红细胞体积(MCV)、平均红细胞血红蛋白浓度(MCHC)、红细胞分布宽度(RDW)、平均血小板体积(MPV)、淋巴细胞比值(Lymph)、单核细胞比例(Mon)、粒细胞比例(Gran)、等;另一份血样分离血清用全自动生化分析仪检测谷丙转氨酶(ALT)、谷草转氨酶(AST)、甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白(HDL-C)、血糖(Glu)。然后处死和解剖大鼠,进行大体观察,取肝、心、脾、肺、肾、睾丸称重,并计算脏器指数。
1.2.4 数据处理与分析
数据分析用SPSS 10.0 for Windows统计学软件,数据以均数±标准差表示,组间比较采用单因素方差分析。P<0.05为差异有统计学意义。
2 结果与分析
2.1 常规化学成分测定结果
食品毒理学为开发食品新资源提供可靠的技术保障,化学分析法是食品毒理学评价的重要手段,为正确认识和安全使用食品及添加剂提供有效的技术支持。六堡茶生化成分的分析研究已有报道,茶叶的常规成分测定是对实验茶样的情况作简要判断。本试验选检几个主要测试项目,以对所试茶样的情况作简要界定。结果如表1所示,3个批次六堡茶样品的常规成分中水浸出物、水分、茶多酚、咖啡碱和氨基酸总量平均含量分别 为 (36.79±1.56)% 、 (10.13±0.78)% 、(11.54±1.06)%、(3.21±0.24)%和(1.63±0.12)%,符合六堡茶的广西地方标准,表明所选茶样的常规成分具有较好的代表性。

表1 六堡茶常规成分测定结果Table 1 Measured results of conventional composition in Liupao tea %
2.2 急性毒性试验结果
2.2.1 经口灌胃后一般观察及急性毒性结果
由预试得出小鼠灌胃给予不同剂量茶样后产生 0~100%死亡率的剂量大致是:6~15 g·kg-1,故以15 g·kg-1作为本试验的最高剂量,按 0.8等比设置 6个茶汤剂量进行六堡茶急性毒性试验。实验数据及结果如表 2所示,在灌胃茶汤剂量为6.1 g·kg-1及以下时,小鼠全部存活无死亡现象,且表现较为活跃,活动增加,对刺激较为敏感,均未见有明显毒性反应现象。从7.7 g·kg-1剂量开始,小鼠出现死亡,大多数死亡时间都是在灌胃后 4 h以后,中毒反应基本于灌胃后20 min左右出现,主要表现为活动减少、震颤、竖尾、呼吸减慢、惊厥等,且其程度随着剂量增加而增加,深度中毒者于灌胃后30 min开始死亡;在茶汤剂量为 12 g·kg-1的实验组中只有 1只小鼠存活,且存活小鼠灌胃后10 min即表现活动减少、闭眼、强直震颤、取食减少等,次日才开始恢复睁眼取食、活动增加;而在剂量为 15 g·kg-1的实验组中小鼠全部死亡。对死亡小鼠进行剖检发现,没有发现器官异常现象;对照急性毒性试验观察的动物反应指标[11]表明,中毒部位可能与中枢神经系统有关。
2.2.2 急性毒性统计结果分析
六堡茶的急性毒性统计分析结果如表 3所示。急性毒性试验中半致死剂量(LD50)的计算有多种方法[12],本试验采用Bliss法对茶样的急性毒性实验结果进行统计分析,其结果如下:计算得出六堡茶的半致死剂量 LD50为9.38 g·kg-1,由于试验误差的不确定性,其LD50有95%的可能性在8.43~10.44 g·kg-1之间,回归方程为y=-6.845+12.182Log(x)。根据1977年 WHO颁布的毒性分级标准[12]以及国家颁布分级标准,六堡茶的经口急性毒性的 LD50大于 5 g·kg-1,因此,六堡茶样可以判定为 2级(实际无毒)。

表2 急性毒性实验动物死亡情况Table 2 The animal death of acute toxicity experiment
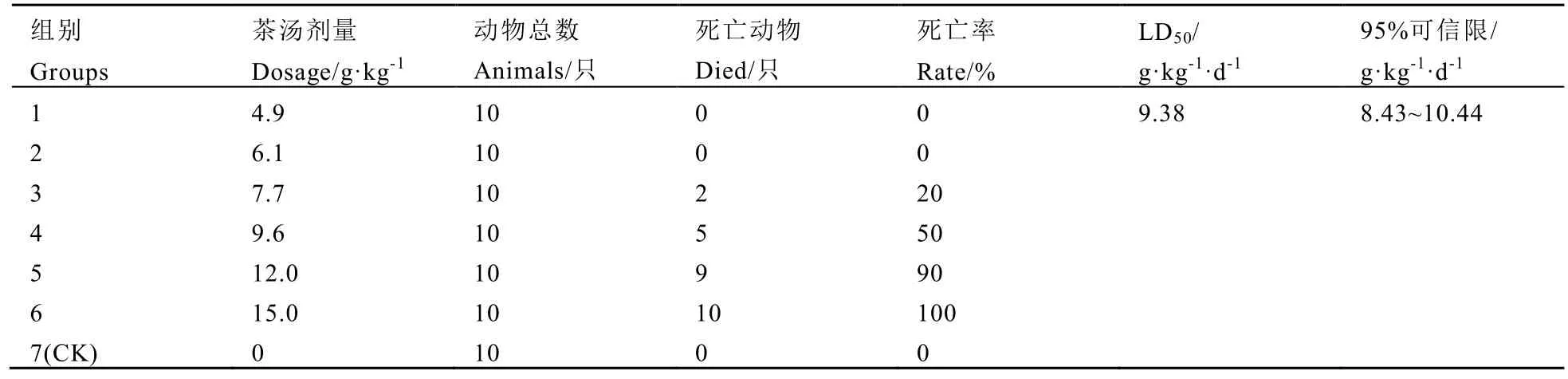
表3 急性毒性实验统计分析结果Table 3 Statistical analysis of acute toxicity experiments
2.2.3 对各组小鼠体质量的影响
在急性毒性实验灌胃后对存活的小鼠进行称重观察,计算其平均体质量和偏差值。结果如表4所示,六堡茶灌胃处理后,各剂量组存活小鼠在1~3 d内体质量增加缓慢。与对照组相比,基本上呈显著性差异(P<0.05)。灌胃5 d和7 d以后,小鼠体质量增速有所加快,呈现剂量依赖关系;与对照组比较,低剂量组(4.9 g·kg-1和6.1 g·kg-1)小鼠体质量无显著性差异,高剂量组(7.7~12 g·kg-1)基本呈现了显著差异(P<0.05或P<0.01)。这些结果表明低剂量六堡茶汤灌胃对小鼠体质量影响较小,接近于半致死剂量的六堡茶汤灌胃对小鼠体质量影响较大,可能由于六堡茶浓度过高引起中毒而造成机体损伤。
2.2.4 半致死剂量与内含成分含量的关系
为了探讨六堡茶可能的致死原因,我们初步分析了六堡茶半致死剂量与主要内含成分茶多酚和咖啡碱含量的关系。陆益等[13]的研究表明,茶多酚的 LD50为 2 640 mg·kg-1;根据我国食品添加剂手册记载:咖啡碱对小鼠的LD50为 127~248 mg·kg-1[14]。本研究结果如表5所示,六堡茶 LD50灌胃剂量时茶多酚和咖啡碱含量分别为1082 mg·kg-1和301 mg·kg-1,已大于咖啡碱的 LD50,同时也接近茶多酚的LD50的一半。由此可以推断,小鼠死亡的原因可能与过高浓度的咖啡碱甚至茶多酚中毒有关。
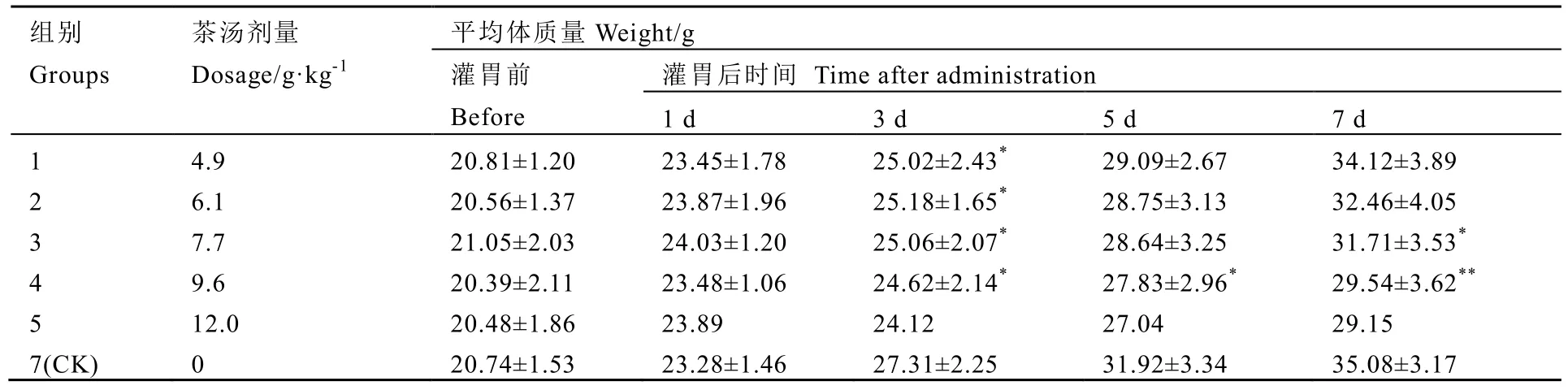
表4 各组动物平均体质量情况Table 4 Weight of animals in each group
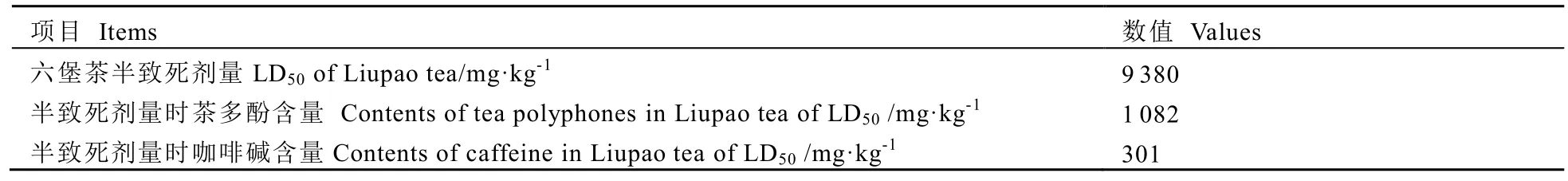
表5 六堡茶半致死剂量时的茶多酚和咖啡碱含量Table 5 Contents of tea polyphones and caffeine in Liupao tea of LD50
表6 六堡茶水提物对大鼠体质量的影响Table 6 Effect of Liupao tea extract on the body weight of rats g

表6 六堡茶水提物对大鼠体质量的影响Table 6 Effect of Liupao tea extract on the body weight of rats g
注:试验总天数为30 d,第4周的天数为9 d。Note: The total number of days for the test is 30 days. The number of days for fourth week was set to 9 days.
性别Sex组别Groups初重Initial weight第1周First week第2周Second week第3周Third week第4周Fourth week♂空白对照组 69.5±6.6 113.5±12.3 161.3±10.9 198.5±16.3 239.2±15.4六堡茶低组 69.8±8.3 110.8±10.2 158.5±18.4 194.5±21.4 235.7±18.0六堡茶中组 70.1±5.4 114.3±14.6 160.2±20.3 196.5±15.8 232.5±15.9六堡茶高组 68.7±7.5 111.6±9.1 156.2±15.7 189.7±22.1 228.9±17.3♀空白对照组 67.9±7.2 104.7±10.8 143.6±16.5 168.9±15.9 197.1±13.8六堡茶低组 66.1±6.7 103.9±8.5 145.2±14.8 170.3±17.6 196.5±12.7六堡茶中组 65.3±5.8 104.4±15.1 141.9±13.4 164.6±14.7 190.8±16.4六堡茶高组 67.5±6.2 101.8±14.6 143.0±17.6 165.5±20.5 191.0±18.8
2.3 亚急性毒性试验结果
2.3.1 动物一般表现
在连续30 d的灌胃过程中,与对照组比,各给药组动物只在初灌六堡茶水提物后活动略减少,未见饮食、睡眠、毛色、粪便、自主活动等方面的明显异常,表明连续 30 d给大鼠灌服六堡茶水提物,对大鼠一般状况无明显影响。
2.3.2 六堡茶对大鼠体质量的影响
试验结果见表 6。以 470、940和 1 880 mg·kg-1·d-13个剂量的六堡茶样给大鼠灌胃30 d,实验期间,各剂量组雌雄大鼠每周的体质量与对照组比较,体质量有减轻的趋势,但差异均无统计学意义(P>0.05),表明长期灌胃六堡茶水提物对大鼠的体质量增长无明显影响。
2.3.3 对大鼠血液常规指标的影响
以不同剂量的六堡茶水提物给大鼠灌胃30 d后,将每组大鼠活体取血进行血象检查。表7显示,与对照组相比,各剂量组雌雄大鼠的红细胞总数(RBC)、红细胞压积(HCT)、平均红细胞体积(MCV)、红细胞分布宽度变异系数(RDW)、平均红细胞血红蛋白浓度(MCHC)、平均血小板体积(MPV)均无显著差异(P>0.05),且都在正常范围之内。表8也指出,灌胃六堡茶水提物对雌雄大鼠的白细胞总数(WBC)及其分类(淋巴细胞、单核细胞和中性粒细胞)影响不显著(P>0.05)。这些结果说明长期饮用六堡茶对大鼠血液常规指标无明显不良影响。
2.3.4 对大鼠主要脏器指数的影响
以3个剂量的六堡茶给大鼠灌胃30 d后,将大鼠处死解剖,取肝、肾、脾、肺、睾丸、卵巢,称重并计算脏器指数(表 9)。与空白对照组比较,六堡茶各剂量组大鼠的脏器指数差异性均无统计学意义(P>0.05)。说明长期饮用六堡茶对大鼠脏器指数无影响。
2.3.5 对大鼠血液生化指标及肝功能的影响
如表10所示,以3个剂量的六堡茶给大鼠灌胃 30 d后,将所有老鼠活体取血进行血液生化指标及肝功能检查。与正常组相比,六堡茶各剂量组大鼠的谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白(HDL-C)、血糖(GLU)水平基本没有明显的差异(P>0.05),但 TG和TC的水平有降低的趋势。这些结果说明六堡茶对大鼠代谢和肝肾功能无明显不良影响,且能促进脂质的代谢。
3 讨论
目前六堡茶安全性研究还不够细致深入,尤其是急性和亚急性毒性试验涉及较少,但它是安全性毒理学评价中最重要的一个环节,最能直观体现出六堡茶的毒性大小。
表7 六堡茶水提物对大鼠血液常规指标的影响Table 7 Effect of Liupao tea extract on the haematological index of rats

表7 六堡茶水提物对大鼠血液常规指标的影响Table 7 Effect of Liupao tea extract on the haematological index of rats
性别Sex组别Groups红细胞总数RBC/×1012·L-1红细胞压积HCT/%平均红细胞体积MCV/f L红细胞分布宽度变异系RDW/%平均红细胞血红蛋白浓度MCHC/g·L-1平均血小板体积MPV/f L♂空白对照组 6.9±0.5 41.3±1.7 62.9±3.5 12.2±1.4 338.2±8.6 6.5±1.1六堡茶低组 6.6±0.7 42.4±2.8 63.3±4.1 10.9±1.5 337.4±6.3 6.2±0.9六堡茶中组 6.8±0.5 39.8±2.5 61.8±2.9 11.6±0.8 343.6±7.0 5.8±0.4六堡茶高组 6.4±0.8 38.5±6.9 62.1±3.8 11.4±1.0 339.1±7.2 5.9±0.5♀空白对照组 7.1±0.2 40.7±4.2 64.1±2.5 12.8±0.8 330.2±7.5 6.2±0.7六堡茶低组 7.2±0.5 39.6±2.7 62.4±4.2 12.3±0.6 327.7±8.1 6.3±1.0六堡茶中组 7.0±0.4 41.1±3.8 61.8±1.8 11.9±1.2 326.8±4.6 5.9±0.8六堡茶高组 6.9±0.2 39.2±3.6 61.4±3.1 11.8±1.4 333.2±9.0 5.6±1.2
表8 六堡茶水提物对大鼠白细胞的影响Table 8 Effect of Liupao tea extract on the white blood cell of rats

表8 六堡茶水提物对大鼠白细胞的影响Table 8 Effect of Liupao tea extract on the white blood cell of rats
性别Sex组别Groups白细胞数目WBC/×109·L-1白细胞分类Classification of white blood cell/%淋巴细胞 Lymph 单核细胞 Mon 中性粒细胞 Gran♂空白对照组 10.4±3.2 73.8±3.4 5.1±0.9 21.1±2.9六堡茶低组 10.1±4.7 74.1±5.2 4.6±0.7 21.3±5.2六堡茶中组 11.6±3.8 73.6±1.3 4.4±0.8 22.0±4.3六堡茶高组 12.7±3.5 73.3±2.6 4.5±0.5 22.2±3.2♀空白对照组 9.8±4.1 73.5±4.1 5.5±0.5 21.0±4.5六堡茶低组 10.4±3.6 72.3±6.3 5.6±0.6 22.1±3.7六堡茶中组 9.6±3.2 73.0±3.8 5.1±0.4 21.9±3.8六堡茶高组 11.3±2.9 72.7±4.0 4.9±0.9 22.4±5.0
表9 六堡茶对大鼠主要脏器指数的影响Table 9 Effect of liupao tea on the main organ index of rats %

表9 六堡茶对大鼠主要脏器指数的影响Table 9 Effect of liupao tea on the main organ index of rats %
性别Sex组别Groups肝Liver肾Kidney脾Spleen睾丸或卵巢Testis or ovary心Heart肺Lung♂空白对照组 3.04±0.15 0.80±0.08 0.22±0.05 0.92±0.09 0.35±0.05 0.47±0.04六堡茶低组 3.17±0.24 0.84±0.07 0.23±0.03 0.94±0.10 0.35±0.08 0.48±0.05六堡茶中组 3.03±0.29 0.84±0.10 0.21±0.03 1.02±0.14 0.38±0.06 0.50±0.08六堡茶高组 3.15±0.31 0.87±0.12 0.25±0.02 0.98±0.07 0.37±0.03 0.51±0.06♀空白对照组 3.16±0.30 0.85±0.06 0.23±0.04 0.07±0.01 0.36±0.08 0.50±0.07六堡茶低组 3.21±0.26 0.88±0.10 0.25±0.07 0.07±0.02 0.37±0.05 0.49±0.10六堡茶中组 3.13±0.32 0.86±0.07 0.28±0.11 0.08±0.01 0.40±0.11 0.52±0.08六堡茶高组 3.28±0.21 0.90±0.05 0.26±0.06 0.08±0.03 0.39±0.07 0.53±0.12
表10 六堡茶对大鼠血液生化指标及肝功能的影响Table 10 Effect of Liupao tea on blood biochemical parameters and liver functions of rats

表10 六堡茶对大鼠血液生化指标及肝功能的影响Table 10 Effect of Liupao tea on blood biochemical parameters and liver functions of rats
性别 Sex 组别 Groups ALT/U·L-1 AST/U·L-1 TC/mmol·L-1 TG/mmol·L-1 HDL-C/mmol·L-1 GLU/mmol·L-1♂空白对照组 51.3±3.4 194.5±31.8 2.34±0.43 1.04±0.16 1.05±0.12 6.98±1.31六堡茶低组 52.6±9.0 200.7±30.5 2.26±0.25 0.93±0.13 0.98±0.21 6.85±0.90六堡茶中组 58.1±10.8 212.4±38.1 2.18±0.41 1.01±0.22 1.01±0.19 7.04±0.58六堡茶高组 55.9±6.5 199.6±45.2 2.25±0.35 0.97±0.31 0.94±0.17 7.09±0.82♀空白对照组 49.7±6.2 191.3±36.9 2.30±0.57 1.08±0.19 1.16±0.20 7.07±0.36六堡茶低组 49.3±10.5 196.9±22.8 2.07±0.44 1.01±0.28 0.98±0.22 7.12±0.55六堡茶中组 53.6±7.1 201.8±31.4 2.23±0.40 0.99±0.32 1.07±0.16 7.03±1.09六堡茶高组 54.1±5.8 206.5±29.6 2.15±0.62 0.95±0.24 1.02±0.24 7.08±0.67
本研究在急性毒性试验中测得六堡茶半致死剂量为 9.38 g·kg-1,大于 5 g·kg-1的经口急性毒性标准,可以判定为实际无毒。从小鼠中毒及死亡症状如强直震颤、摇头、呆滞、闭眼、竖尾惊厥、临死前仅几秒钟的挣扎,可以初步推测六堡茶致小鼠中毒及死亡为中枢神经毒性引起;六堡茶内含成分分析表明,半死剂量的六堡茶含有较高浓度的茶多酚和咖啡碱(1 082 mg·kg-1和 301 mg·kg-1),已大于咖啡碱的 LD50,同时也较为接近茶多酚LD50的一半。已有研究认为,过高浓度的咖啡碱能对中枢神经系统机能造成损伤[15]。由此可以进一步推断小鼠死亡的原因可能与过高浓度的咖啡碱甚至茶多酚引起的中枢神经系统损伤有关。六堡茶亚急性毒性实验期间各组动物饮食、排泄、活动均正常,未观察到中毒表现。六堡茶各剂量组动物体质量、血液学、血液生化指标以及脏器指数较对照组均无统计学差异(P>0.05),主要脏器在外观形态上未发现有明显病理变化。这些结果表明,六堡茶对大鼠的生长发育无不良影响,对动物的造血功能、肝肾功能、器官组织均无明显毒性。但是六堡茶的灌胃能一定程度地降低大鼠体质量以及血清TG和TC含量,也一定程度地验证了它可能具有降脂减肥的功效[16-17],但仍然需要后续进一步的研究确认。
因此,从急性和亚急性毒理学角度看,广西六堡茶的饮用安全性是非常高的,正常饮用六堡茶对人类身体并无有害影响,但任何东西的使用都应该在一个合理的范围,超出了这个范围就不可能发挥好的作用甚至引起副作用。本研究为六堡茶的安全性评价提供了科学依据,为其进一步开发应用奠定了基础。
[1]龙志荣, 马士成, 梅宇, 等. 六堡茶产业市场形势分析报告[J]. 广东茶业, 2013(3): 23-27.
[2]刘勤晋, 陈文品, 白文祥, 等. 普洱茶急性毒性安全性评价研究报告[J]. 茶叶科学, 2003, 23(2): 141-145.
[3]马伟光, 黄之镨, 游文龙, 等. 配方普洱茶的急性毒性研究[J]. 茶叶科学, 2010, 30(1): 9-12.
[4]龚加顺, 陈文品, 周红杰, 等. 云南普洱茶特征成分的功能与毒理学评价[J]. 茶叶科学, 2007, 27(3): 201-210.
[5]肖文军, 傅冬和, 任国谱, 等. 茯茶毒理学试验报告[J].茶叶科学, 2007, 27(4): 307-310.
[6]刘子音, 王远亮, 许爱清. “金花” 菌食品安全性毒理学评价[J]. 农产品加工学刊, 2011(7): 29-32.
[7]覃良, 黄宇声, 刘冠萍. 六堡茶毒性研究[J]. 中国民族民间医药杂志, 2013(3): 39-40.
[8]中华人民共和国卫生部. 保健食品检验与评价技术规范[Z]. 卫法监发 [2003]42号. 2003.
[9]陈仁惇. 营养保健食品[M]. 北京:中国轻工业出版社, 2006.
[10]徐叔云, 卞如濂, 陈修. 药理实验方法学[M]. 2版. 北京:人民卫生出版社, 1991.
[11]纪云晶. 实用毒理学手册[M]. 北京: 中国环境科学出版社, 1991.
[12]袁伯俊, 王治乔. 新药临床前安全性评价与实践[M]. 北京: 军事医学科学出版社, 1997.
[13]陆益, 杨帆, 梁宁生, 等. 茶多酚毒理学实验研究[J]. 广西医科大学学报, 2005, 22(6): 831-834.
[14]陈亮延, 吴永方. 茶色素毒理学研究[J]. 武汉职工医学院学报, 1996, 24(4): 25-27.
[15]黄旭, 李晨曦, 汪越, 等. 咖啡因对大鼠海马神经元形态学的影响[J]. 解剖科学进展, 2014(1): 5-8.
[16]张栩颜, 黄宇声, 刘冠萍, 等. 六堡茶对高脂血症小鼠血脂及脂质过氧化的影响[J]. 医学理论与实践, 2013, 26(5): 563-564.
[17]黄宇声, 张栩颜, 刘冠萍, 等. 六堡茶降脂作用试验研究[J]. 中国保健营养: 下半月, 2013(3): 875-876.
Research on Acute and Subacute Toxicity Evaluation of Liupao Tea
WU Wenliang1,2,3,6, LIN Yong1,2,3*, LIU Zhonghua1,2,3, HUANG Jian'an1,2,3, LONG Zhirong4,5, TENG Cuiqing4,5, MA Shicheng4,5, QIU Ruijin4,5, CAO Zhonghuan4,5
1. Key Lab of Tea Science of Education Ministry, Hunan Agricultural University, Changsha 410128, China; 2. National Research Center of Engineering Technology for Utilization of Botanical Functional Ingredients, Changsha 410128, China; 3. Collaborative Innovation Center of Utilization of Functional Ingredients from Botanicals, Changsha 410128, China; 4. Wuzhou Academy of Liupao Tea, Wuzhou 543003, China; 5. Wuzhou Institute of Agricultural Sciences, Wuzhou 543003, China; 6. Tea of Institute, Hunan Academy of Agricultural Sciences , Changsha 410125, China
Liupao tea has a long history and is characterized as famous agricultural products of Guangxi, but the study of its safety is not enough. In order to verify the safety, the main physicochemical components of Liupao tea from Wuzhou were measured by conventional test method of national standard, then, the acute and subacute toxicities of Liupao tea were systemically studied in accordance with the procedures for toxicological assessment on food safety. The experimental results showed that, the physicochemical indexes of Liupao tea were repeatable, whichwere followed with Guangxi local standards in the acute toxicity test. Using bliss method, the calculated median lethal dose (LD50) of Liupao tea was 9.38 g·kg-1with 95% confidence interval (8.43~10.44 g·kg-1), which was higher than acute toxicity criteria (5 g·kg-1). In the subacute study, compared with the control group, no death or clinical signs, or abnormally hematological, biochemical and histopathological changes were found in either groups of rats receiving daily oral gavage of Liupao tea. The three dose treatments were 0.47, 0.94 and 1.88 g·kg-1·d-1for 30 days (P>0.05). Thus, Liupao tea products belong to the actual non-toxic grade and fulfill the requirements of food safety according to the food toxicology standards.
Liupao tea, acute toxicity, subacute toxicity, median lethal dosage
TS272.5+4;R285.5
A
1000-369X(2017)02-173-09
2017-01-11
2017-02-26
湖南农业大学青年科学基金项目(15QN22)、梧州市科学研究与技术开发计划项目(201402214、201501028)、2015年梧州市六堡茶产业化项目、国家自然科学基金项目(31100502)
吴文亮,男,在读博士研究生,主要从事茶叶加工及茶叶功能成分化学研究。*通讯作者:ly2005306@163.com
