益气活血中药黄芪-丹参对脂多糖致急性肺损伤大鼠防治作用的机制研究
2017-03-29秦丽窦永起李敏王毓国
秦丽 窦永起 李敏 王毓国
·论著·
益气活血中药黄芪-丹参对脂多糖致急性肺损伤大鼠防治作用的机制研究
秦丽 窦永起 李敏 王毓国
目的 观察益气活血中药黄芪-丹参对脂多糖(lipopolysaccharide, LPS)致急性肺损伤(acute lung injury, ALI)大鼠TLR-4/NF-κB信号通路的影响。方法 SD雄性大鼠40只,随机分成正常对照组、模型对照组、地塞米松组、益气活血中药组,各组10只;除正常对照组气管内滴注生理盐水,其余各组滴注LPS(5 mg/kg)制备ALI模型;造模前后各3天干预组予以2 mL相应药物(益气活血中药0.59 g/mL或地塞米松5 mg/kg),其余组予以等量的生理盐水灌胃;于末次灌胃给药2小时后处死大鼠,免疫组织化学法检测大鼠肺组织中Toll样受体4(Toll-like receptor 4,TLR-4)、白介素1受体相关激酶1(interleukin-1 receptor-associated kinase-1,IRAK-1)、核转录因子κB(Nuclear factor kappa B,NF-κB)蛋白表达的含量,qPCR测定肺组织中TLR-4、IRAK-1、NF-κB mRNA表达量。结果 LPS造模组大鼠肺组织中TLR-4、IRAK-1、NF-κB mRNA表达和蛋白表达均高于正常对照组(P<0.01),且模型对照组高于地塞米松组和中药组(P<0.01);中药组TLR-4、IRAK-1 mRNA表达和蛋白表达量与地塞米松组无明显差异(P>0.05),而NF-κB mRNA表达和蛋白表达量高于地塞米松组(P<0.05)。结论 益气活血中药黄芪-丹参对LPS致ALI大鼠的防治作用可能与其下调TLR-4/NF-κB信号通路有关。
益气活血中药; 脂多糖; 急性肺损伤; Toll样受体4; 白介素1受体相关激酶; 核转录因子κB
急性肺损伤(acute lung injury, ALI)以肺泡-毛细血管膜损伤和渗透性增加、中性粒细胞浸润、肺组织水肿以及失控的氧化应激和炎症过程为特征[1-3]。急性呼吸窘迫综合征是ALI的严重阶段,临床表现为急性肺水肿、顽固性低氧血症和进行性呼吸窘迫,为常见的急危重症[4-5]。Toll样受体4(Toll-like receptors 4, TLR-4)是一种横跨膜蛋白和信号转录分子,脂多糖(lipopolysaccharide,LPS)进入肺内激活TLR-4后,募集MyD88(molecule myeloid differentiation primary response gene 88) 蛋白分子,随之导致白介素1受体相关激酶 (interleukin-1 receptor-sociated kinase,IRAK-1)活化,最终通过信号转导通路激活核转录调节因子(nuclear factor-kappa B,NF-κB)[6-7]。活化的NF-κB引发多种炎症因子合成并释放,包括肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α),白介素1β(interleukin-1β, IL-1β)及白介素6(interleukin-6,IL-6)等,进而导致肺组织的弥漫性炎症损伤[8-9]。临床研究发现[10]益气活血中药能改善ALI患者肺循环高凝状态,降低血液黏度,显著减轻炎性反应,对肺有较好的保护作用,疗效确切;且前期动物实验研究表明[11]益气活血中药黄芪-丹参能够减少LPS致ALI大鼠支气管肺泡灌洗液中蛋白浓度及肺组织中炎症因子的含量,并减轻肺水肿和肺组织的病理损伤,起到防治急性肺损伤的作用。基于文献调研和以上结果,本实验进一步研究黄芪-丹参防治ALI作用机制是否通过调节TLR-4/NF-κB信号通路实现。通过气管内滴注LPS溶液制备大鼠ALI模型,观察益气活血中药黄芪-丹参对大鼠肺组织中TLR-4、IRAK-1、NF-κB mRNA表达及蛋白表达的影响,探讨益气活血法防治ALI的分子机制。
1 材料与方法
1.1 实验动物
选用两月龄健康清洁级SD雄性大鼠40只,体质量为(200±20)g,由中国人民解放军军事医学科学院实验动物中心提供,许可证号:SCXK(军):2012-0004。大鼠在清洁动物房适应性饲养1周后进行试验,期间自由摄食、饮水,室温18~24℃,相对湿度40%~70%,每天12小时光照维持,昼夜循环。
1.2 主要试剂
LPS,Sigma公司,批号L2880;戊巴比妥钠,Germany公司,批号K2208;Rabbit Anti-TLR-4(批号:bs-1021R)、Rabbit Anti-IRAK-1(批号:bs-3194R)、Rabbit Anti-NF-κB/p65(批号:bs-20160R)、免疫组化试剂盒(批号:sp-0023)均购自北京博奥森生物技术有限公司,DAB显色试剂盒(中杉金桥,ZLI-9017);RNApure超纯总RNA提取试剂盒(批号:70621562)、M-MLV Ⅲ First-Strand cDNA Synthesis Kit(批号:656666BB)、Green qPCR Master Mix(批号:706084XX)均购自博迈德生物有限公司。大鼠TLR-4、IRAK-1、NF-κB 及内参GAPDH引物由 Primer Express 设计合成,序列见表1。
1.3 主要仪器
旋转蒸发器(RE53CS,上海亚荣生化仪器厂);切片机(莱卡2016, 上海莱卡仪器有限公司); 包埋机(湖北孝感亚鹏仪器厂);台式冷冻离心机(1-15K,SIGMA);电热恒温箱(DHG-9240A,北京陆希科技有限公司);OLYMPUS BX60显微镜成像系统,Image-Pro Plus 5.1图像分析系统;实时荧光定量PCR仪器(SteponeTM 272006169型,美国Applied Biosystem公司)。
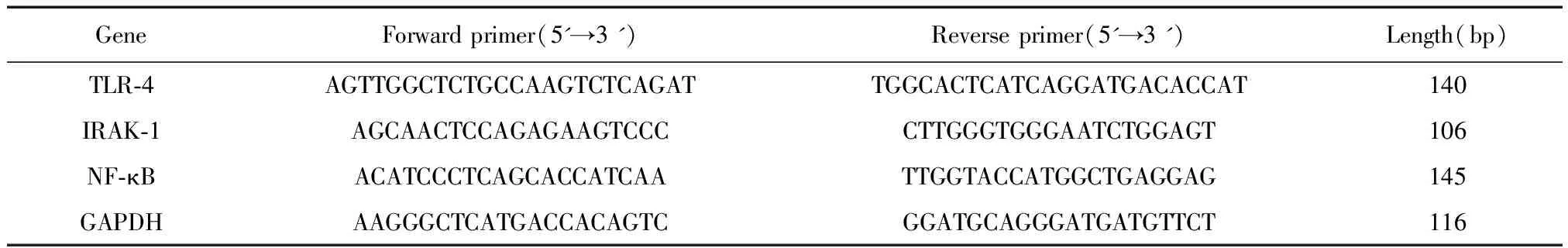
表1 引物序列
1.4 药物及制备
益气活血中药由生黄芪和丹参组成,两者用量比例为2∶1,生药材由解放军总医院中药房采购及鉴定,经过浸泡、煎煮和过滤后,在恒温水浴锅(60℃)中浓缩成含生药0.59 g/mL的药液,按大鼠与人体体表面积换算公式计算[12]。
1.5 动物分组及处理方式
SD雄性大鼠40只,随机分成正常对照组、模型对照组、地塞米松组、益气活血中药组,各组10只。中药组大鼠在造模前3天每天予以益气活血中药2 mL灌胃(1次/天,含生药量0.59 g/mL),其余组大鼠每天予以同体积的生理盐水。造模成功后,中药组每天予以益气活血中药2 mL(0.59 g/mL)灌胃,地塞米松组大鼠每天予以2 mL地塞米松(5 mg/kg)溶液灌胃,正常对照组和模型对照组大鼠每天予以生理盐水2 mL灌胃,1次/天,连续给药3天。
1.6 大鼠ALI模型制备
采用LPS暴露式气管滴注方法制备ALI模型[13]。除正常对照组外,其余各组均给予气管内滴注LPS(5 mg/kg)溶液。大鼠用3%戊巴比妥钠(30 mg/kg)腹腔注射进行麻醉,固定大鼠仰卧位,无菌操作正中切开颈部组织,使气管暴露,用1 mL注射器由气管向肺方向滴注LPS溶液,而后将大鼠直立、旋转并左右摇晃,使LPS溶液在肺内均匀分布,从而建立内毒素性急性肺损伤大鼠模型。正常对照组大鼠按上述方法向气管滴入同等量的生理盐水。
1.7 标本取材
所有大鼠在造模灌胃后第3天麻醉称重,腹主动脉放血处死后剪开胸部皮肤,暴露胸腔;取大鼠左叶组织装入冻存管后迅速放入盛有液氮的器皿中,缓冲10分钟后放入-80℃保存备用;取大鼠右肺下叶组织,放入装有4%多聚甲醛溶液的西林瓶中固定48小时。
1.8 检测指标
1.8.1 大鼠肺组织中TLR-4、IRAK-1、NF-κB蛋白表达的检测 按说明书用SABC免疫组织化学法检测肺组织中TLR-4、IRAK-1、NF-κB蛋白的表达。400倍光镜下每张切片随机选取5个视野,光亮度设定一致,用OLYMPUS BX60显微镜采集图像,Image-Pro Plus 5.1图像分析系统对结果进行半定量分析,测定每个肺组织的阳性颗粒的积分光密度(IOD),以均值作为该样本TLR-4、IRAK-1、NF-κB蛋白的相对表达量,IOD值越高,说明其蛋白表达越多。
1.8.2 大鼠肺组织中TLR-4、IRAK-1、NF-κB mRNA表达量的测定 称取-80℃冻存的左肺100 mg组织放到均浆器中,加入1 mL裂解液后在冰上充分碾磨,按试剂盒说明书步骤提取总RNA,测定样品260 nm、280 nm吸光度值(A),A260/A280在1.8~2.0,表明所提取的总RNA可用。取1 μg RNA,加入Oligo(dT)20(0.5 μL-1)1 μL、5×RTMix 5 μL、M-MLⅧ 1 μL组成逆转录体系,合成cDNA第一链。然后使用实时荧光定量PCR仪进行扩增,Green qPCR Master Mix 25 μL、Forward Primer 1 μL、Reverse Primer 1 μL、cDNA 2 μL和RNase-Free H2O组成50 μL反应体系,每个样品平行设置3个复孔。采用Comparative Delta-delta CT法,以GAPDH基因为内参,对各样本TLR-4、IRAK-1、NF-κB mRNA进行相对定量分析,计算RQ值(2-△△Ct)。
1.9 统计学处理

2 结果
2.1 大鼠肺组织中TLR-4、IRAK-1、NF-κB蛋白表达
TLR-4蛋白主要分布于肺组织的细胞膜和细胞浆中,阳性着色为棕黄色,见图1。IRAK-1蛋白主要表达于肺组织的细胞质内,阳性着色为棕褐色颗粒,见图2。NF-κB蛋白主要分布于肺组织的细胞质和细胞核上,阳性着色为棕黄色颗粒状,见图3。与正常对照组比较,LPS造模各组阳性信号(棕色或棕褐色)明显增多,TLR-4、IRAK-1、NF-κB蛋白表达IOD值均升高(P<0.01);与模型对照组比较,地塞米松组和中药组阳性信号减少,TLR-4、IRAK-1、NF-κB蛋白表达均降低(P<0.01);中药组NF-κB蛋白表达IOD值高于地塞米松组(P<0.05),TLR-4、IRAK-1表达无明显差异(P>0.05)。详见表2。

表2 各组大鼠肺组织中TLR-4、IRAK-1、NF-κB蛋白表达(IOD)
注: 与正常对照组比较,aP<0.01;与模型对照组比较,bP<0.01;与地塞米松组比较,cP<0.05。

注:A:正常对照组;B:模型对照组;C:地塞米松组;D:益气活血中药组

注:A:正常对照组;B:模型对照组;C:地塞米松组;D:益气活血中药组
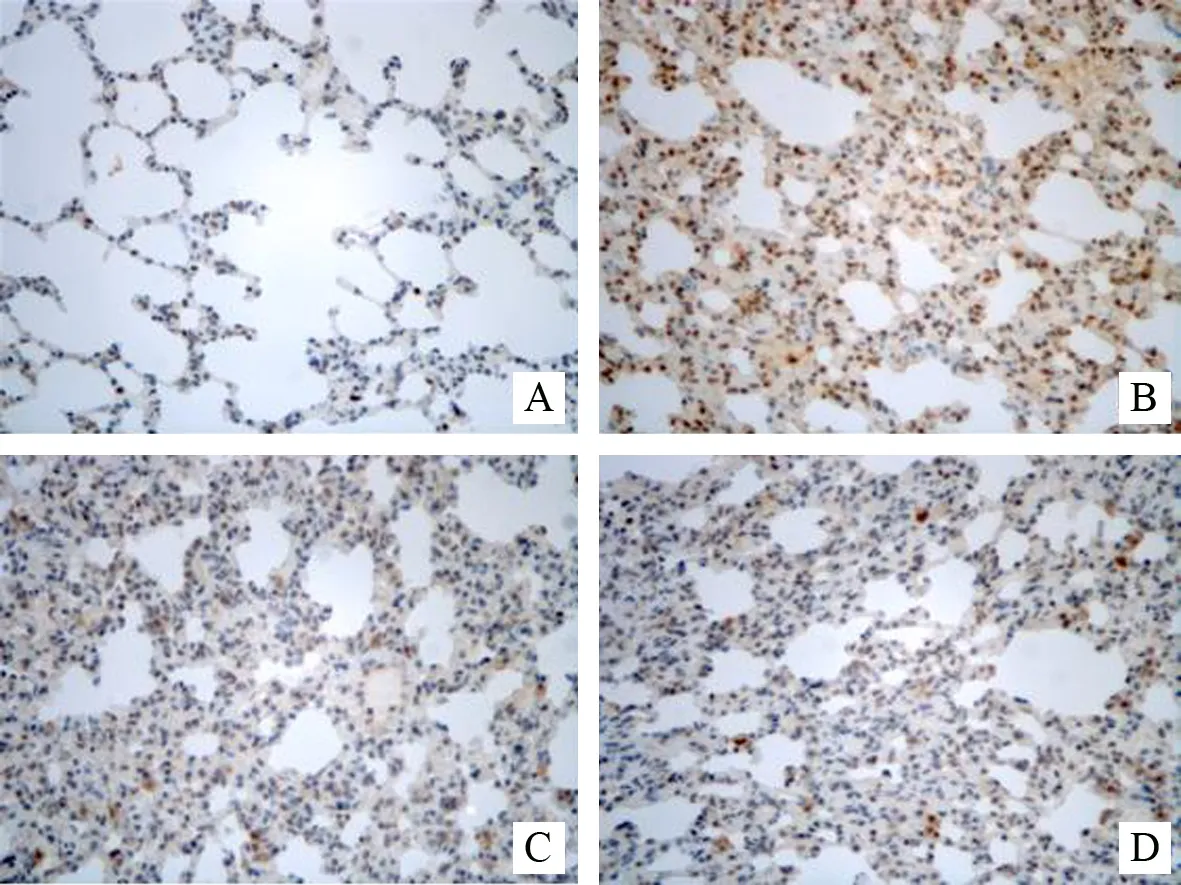
注:A:正常对照组;B:模型对照组;C:地塞米松组;D:益气活血中药组
2.2 大鼠肺组织TLR-4、IRAK-1、NF-κB的mRNA表达量
与正常对照组比较,LPS造模各组TLR-4、IRAK-1、NF-κB mRNA相对表达量均升高(P<0.01);与模型对照组比较,地塞米松组和中药组TLR-4、IRAK-1、NF-κB mRNA相对表达均减少(P<0.01);中药组TLR-4、IRAK-1 mRNA表达与地塞米松组无明显差异(P>0.05), 而NF-κB mRNA高于地塞米松组(P<0.05)。见表3。

表3 各组大鼠肺组织中TLR-4 、IRAK-1、NF-κB mRNA相对表达量RQ值
注:与正常对照组比较,aP<0.01;与模型对照组比较,bP<0.01;与地塞米松组比较,cP<0.05。
3 讨论
Toll样受体家族是高度保守的模式识别受体之一,被视为先天性免疫与获得性免疫应答的“桥梁”,能够识别各种病原相关分子模式,如TLR-4能够识别特异性识别革兰氏阴性菌细胞壁的主要成分LPS[14-15]。LPS属于细菌内毒素的一种,能够引起肺部的急性炎症反应和免疫应答[16]。气管内滴入LPS诱导内毒素型ALI动物模型方法已经广泛运用于ALI发病机理和药物防治的研究[17]。
许多研究表明ALI的发生发展与TLR-4/NF-κB信号通路的活化密切相关,药物干预下调此信号通路能够起到防治ALI的作用[9,18]。TLR-4是一种跨膜受体蛋白,位于细胞膜外的结构域能够识别各种病原体,位于细胞内的结构则参与信号通路的转导[19]。NF-κB是信号通路中重要的下游分子,具有强大的核转录调节功能,能够启动多个炎症性基因的表达,导致多种炎症因子如TNF-α、IL-1、IL-10的合成和释放,从而导致失控的炎症反应过程[20]。IRAK-1作为信号通路过程中的重要转接点,属于白介素1受体相关激酶IRAK家族中的一员,具有激酶活性并可发生自身磷酸化,导致信号通路的向下传递。
本实验从细胞膜受体TLR-4、胞内分子IRAK-1及细胞核受体NF-κB上研究益气活血中药对LPS诱导ALI大鼠的影响。研究结果显示,气管内滴入LPS造模后,肺组织中TLR-4、IRAK-1、NF-κB mRNA表达量均增加,相应的蛋白合成亦增多,表明LPS刺激了肺组织TLR-4/NF-κB信号通路的活化。而在益气活血中药组中,TLR-4、IRAK-1、NF-κB mRNA表达和蛋白表达均下调,说明了前期动物实验中益气活血中药防治LPS诱导ALI大鼠的分子机制,黄芪丹参合用可抑制TLR-4/NF-κB信号通路,从而减少炎症因子的合成,缓解肺部的炎症反应和病理损伤。但ALI的发生是有多种机制参与,中药的作用也涉及多个方面,故关于益气活血中药防治ALI的其他作用机制可进一步研究。
[1] Matthay MA, Zemans RL. The acute respiratory distress syndrome: pathogenesis and treatment[J]. Annu Rev Pathol, 2011, (1): 147-163.
[2] Rubenfeld GD, Caldwell E, Peabody E, et al. Incidence and outcomes of acute lung injury[J]. N Engl J Med, 2005, 353(16): 1685-1693.
[3] Piper A, Song Y, Eves ND, et al. Year in review 2013: Acute lung injury, interstitial lung diseases, sleep and physiology[J]. Respirology, 2014, 19(3): 428-437.
[4] Matthay MA, Ware LB, Zimmerman GA. The acute respiratory distress syndrome[J]. J Clin Invest, 2012, 122(8): 2731-2740.
[5] Wheeler AP, Bernard GR. Acute lung injury and the acute respiratory distress syndrome: a clinical review[J]. Lancet, 2007,369(9572): 1553-1564.
[6] Imai Y, Kuba K, Neely GG, et al. Identification of oxidative stress and Toll-like receptor 4 signaling as a key pathway of acute lung injury[J]. Cell, 2008, 133(2): 235-49.
[7] Ringwood L, Li L. The involvement of the interleukin-1 receptor-associated kinases (IRAKs) in cellular signaling networks controlling inflammation[J]. Cytokine, 2008, 42(1): 1-7.
[8] Yang R, Yang L, Shen X, et al. Suppression of NF-kappaB pathway by crocetin contributes to attenuation of lipopolysaccharide-induced acute lung injury in mice[J]. Eur J Pharmacol, 2012,674(2-3):391-6.
[9] Feng G, Jiang ZY, Sun B, et al. Fisetin Alleviates Lipopolysaccharide-Induced Acute Lung Injury via TLR4-Mediated NF-kappaB Signaling Pathway in Rats[J]. Inflammation, 2016, 39(1): 148-57.
[10] Li M, Yang MH, Dou YQ, et al. Clinical research on supplementing Qi and activating blood circulation herbs on lung protection in acute lung injury ventilation patients[J]. Zhong Yao Cai, 2014,37(11): 2113-2116.
[11] 秦丽,王毓国,李敏,等.益气活血中药对脂多糖致急性肺损伤大鼠的防治作用[J].环球中医药,2016,9(5):548-552.
[12] 徐叔云,卞如濂,陈修.药理实验方法学[M].3版.北京:人民卫生出版社,2002:200-204.
[13] Feng G, Sun B, Li TZ. Daidzein attenuates lipopolysaccharide-induced acute lung injury via toll-like receptor 4/NF-kappa B pathway[J]. Int Immunopharmacol, 2015,26(2):392-400.
[14] Akira S, Takeda K, Kaisho T. Toll-like receptors: critical proteins linking innate and acquired immunity[J]. Nat Immunol, 2001,2(8): 675-680.
[15] Kaisho T, Akira S. Toll-like receptor function and signaling[J]. J Allergy Clin Immunol, 2006, 117(5): 979-987.
[16] Rathinam VA, Fitzgerald KA. Immunology: Lipopolysaccharide sensing on the inside[J]. Nature, 2013, 501(7466): 173-175.
[17] Matute-Bello G, Frevert CW, Martin TR. Animal models of acute lung injury[J]. Am J Physiol Lung Cell Mol Physiol, 2008,295(3): 379-399.
[18] Zhang X, Sun CY, Zhang YB, et al. Kegan Liyan oral liquid ameliorates lipopolysaccharide-induced acute lung injury through inhibition of TLR4-mediated NF-kappa B signaling pathway and MMP-9 expression[J]. J Ethnopharmacol, 2016, 186: 91-102.
[19] Drexler SK, Foxwell BM. The role of Toll-like receptors in chronic inflammation[J]. Int J Biochem Cell Biol,2010,42(4):506-518.
[20] Hoesel B, Schmid JA. The complexity of NF-kappa B signaling in inflammation and cancer[J]. Mol Cancer, 2013, 12: 86.
(本文编辑: 禹佳)
Study the mechanism of supplementingqiand activating blood herbs on Lipopolysaccharide-induced acute lung injury in rats
QINLi,DOUYongqi,LIMin,etal.DepartmentofTraditionalChineseMedicine,ChinesePLAGeneralHospital,Beijing100853,China
Correspondingauthor:LIMin,E-mail:kittenlee1115@126.com
Objective To investigate the effects of supplementingqiand activating blood herbs astragalus membranaceus and salvia miltiorrhiza on TLR-4/NF-kappa B signaling pathway in rats with acute lung injury induced by lipopolysaccharide. Methods Forty healthy male SD rats were randomly divided into normal control group, model control group, dexamethasone group, herb group, ten in each group. ALI models were established by intratracheal instillation of LPS (5 mg/kg),while normal control group was instilled normal saline. 3 days before and after making the model,the drug(0.59 g/mL herbs or dexamethasone for 5 mg/kg)or same amount of normal saline was given in each group by gavage. Rats were sacrificed after 2h of the last administration. Then the protein and mRNA expressions of TLR-4, Interleukin-1 receptor-associated kinase-1 and NF-kappa B were measured by reverse transcriptase polymerase chain reaction and immunohistochemistry respectively.Results Compared with normal control group, the protein and mRNA expressions of LPS groups was higher (P<0.01); compared with model control group, dexamethasone group and herbs group was decreased(P<0.01); the expression levels of TLR-4, IRAK-1 in herb group were close to dexamethasone group (P>0.05),but the level of NF-κB was higher in herb group (P<0.05) . Conclusion The protective and therapeutic effects of astragalus membranaceus and salvia miltiorrhiza on LPS-induced ALI in rats maybe due to its ability to modulate TLR-4/ NF-κB signaling pathways.
Supplementingqiand activating blood herbs; Lipopolysaccharide; Acute lung injury; TLR-4; IRAK-1; NF-κB
国家自然科学基金(81303131)
100853 北京,中国人民解放军总医院中医科[秦丽(硕士研究生)、窦永起、李敏、王毓国]
秦丽(1990- ),女,2014级在读硕士研究生。研究方向:中西医结合临床。E-mail:qinlizi301@163.com
李敏(1980- ),博士,主治医师。研究方向:中西医结合临床。E-mail:kittenlee1115@126.com
R285.5
A
10.3969/j.issn.1674-1749.2017.01.001
2016-06-11)
