培美曲塞单药或联合吉非替尼治疗EGFR-TKI耐药后晚期非小细胞肺癌临床观察
2017-03-27刘红柳杨家梅
刘红柳,杨家梅
郑州大学第二附属医院肿瘤科,河南 郑州 450000
培美曲塞单药或联合吉非替尼治疗EGFR-TKI耐药后晚期非小细胞肺癌临床观察
刘红柳,杨家梅
郑州大学第二附属医院肿瘤科,河南 郑州 450000
背景与目的:生长因子受体-酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)治疗晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)获得性耐药后尚无标准的治疗方案,亟待探寻有效的后续治疗方法。为临床应用提供指导,该研究旨在比较后续治疗采用培美曲塞单药或联合吉非替尼治疗EGFR-TKI获得性耐药的晚期NSCLC的临床疗效及安全性。方法:入组既往接受过EGFR-TKI治疗后进展的晚期NSCLC患者62例。其中32接受培美曲塞联合吉非替尼治疗,设为联合组;30例单用培美曲塞治疗,设为化疗组。评价临床疗效及不良反应。结果:联合组客观有效率(objective response rate,ORR)为46.9%,高于化疗组的20%,差异有统计学意义(χ2=4.933,P<0.05);两组疾病控制率(disease control rate,DCR)差异无统计学意义(P>0.05);联合组的中位无病生存期(progression-free survival,PFS)为8.0个月,化疗组中位PFS为6.3个月,差异有统计学意义(χ2=8.063,P<0.05),两组总生存期(overall survival,OS)差异无统计学意义(P>0.05)。联合组中性粒细胞减少、皮疹的发生率高于化疗组,差异有统计学意义(P<0.05),Ⅲ~Ⅳ不良反应两组差异无统计学意义(P>0.05)。结论:晚期NSCLC患者EGFR-TKI获得性耐药后,采用培美曲塞联合吉非替尼较单用培美曲塞显示出更优势临床有效率和中位PFS,不良反应可耐受,值得临床推广运用。
培美曲塞;吉非替尼;非小细胞肺癌;表皮生长因子受体-酪氨酸激酶抑制剂
非小细胞肺癌(non-small cell lung cancer,NSCLC)占肺癌总发病率的80%~85%,早期症状不典型,70%患者初诊时即发现转移[1],失去手术机会,预后差,以铂类为基础的双药联合是标准的一线治疗方案。规范的全身化疗虽然能延缓进展,延长生存期,但有效率仅为25%~35%,中位生存时间为8~10个月,无法获得进一步的突破[2]。近年来广泛应用表皮生长因子受体-酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFRTKI)对EGFR突变的晚期NSCLC疗效显著,成为主要的治疗方案。但EGFR-TKI治疗10~14个月后不可避免的出现耐药,病情再次进展[3]。目前EGFR-TKI获得性耐药后的晚期NSCLC尚无标准的治疗方案。本研究观察郑州大学第二附属医院62例晚期NSCLC患者EGFR-TKI获得性耐药后采用培美曲塞单药或联合吉非替尼治疗的临床疗效及安全性。
1 资料和方法
1.1 一般资料
入组郑州大学第二附属医院2012年3月—2014年10月期间收治的晚期NSCLC患者62例,均经病理学诊断为腺癌;初始EGFR突变阳性,接受EGFR-TKI治疗有效后出现耐药进展,进展后未进行基因检测;ECOG评分0~2分,均有影像学检查可评价的病灶,预计生存期3个月以上,无严重基础疾病,治疗前无化疗禁忌证。其中,男性40例,女性22例;年龄39~70岁,中位年龄56岁;既往EGFR-TKI治疗进展时间4~23个月,中位进展时间12个月。32例患者接受培美曲塞联合吉非替尼治疗,设为联合组;30例单用培美曲塞案治疗,设为化疗组。两组一般资料对比差异无统计学意义(P>0.05,表1)。

表1 两组一般资料的对比Tab. 1 Patient demographics and clinical characteristics of two groups
1.2 治疗方法
1.2.1 联合组
培美曲塞500 mg/m2,静脉滴注,第1天,吉非替尼250 mg/d,口服。每21天为1个周期,直至肿瘤进展或不良反应无法耐受。治疗疗程波动2~9个周期,中位疗程为5个周期。进展后采用细胞毒性药物姑息性化疗、局部姑息性放疗。
1.2.2 化疗组
培美曲塞500 mg/m2,静脉滴注,第1天。每21天为1个周期,直至肿瘤进展或不良反应无法耐受。治疗疗程波动2~8个周期,中位疗程为4个周期。进展后采用细胞毒性药物姑息性化疗、局部姑息性放疗,未给予EGFR-TKI治疗。
1.3 评价指标
1.3.1 近期疗效
化疗前通过影像学测量记录病灶大小,化疗每2个周期重复同种影像学检查,比较病灶大小。参照实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)[4],分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),以(CR+PR)/N为客观有效率(objective response rate,ORR),(CR+PR+SD)/N为疾病控制率(disease control rate,DCR),其中N为每组病例数。
1.3.2 远期疗效
随访病情变化,随访时间截止至2015年7月,联合组中位随访时间为12.7个月,化疗组中位随访时间为10.0个月。无进展生存期(progress-free survival,PFS)为从开始治疗到全身任何部位肿瘤进展的时间;总生存期(overall survival,OS)为患者开始化疗至任何原因死亡的时间。
1.3.3 不良反应
不良反应按NCI评价标准分为0~Ⅳ级。
1.4 统计学处理
采用SPSS 17.0进行统计学分析,计数资料比较采用χ2检验,PFS和OS采用Kaplan-Meier和log-rank进行检验分析,P<0.05为差异有统计学意义。
2 结 果
2.1 近期临床缓解情况
全部入组62例病例均完成2个周期化疗,可评价疗效。联合组ORR为46.9%,高于化疗组的20%,差异有统计学意义(χ2=4.933,P<0.05),两组DCR差异无统计学意义(P>0.05,表2)。
2.2 远期生存情况
联合组的中位PFS为8.0个月,化疗组中位PFS为6.3个月,差异有统计学意义(χ2=8.063,P<0.05),两组OS差异无统计学意义(P>0.05,图1、2)。

图1 两组的PFS比较Fig. 1 The comparison of PFS of two groups
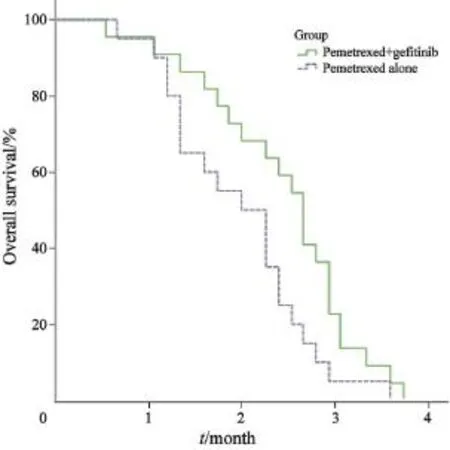
图2 两组的OS比较Fig. 2 The comparison of OS of two groups
2.3 不良反应
两组不良反应主要表现在血液系统毒性和胃肠道反应,Ⅰ~Ⅱ级多见,Ⅲ~Ⅳ级发生率低。联合组中性粒细胞减少、皮疹的发生率较化疗组偏高,差异有统计学意义(P<0.05),经对症处理缓解,未影响后续化疗。Ⅲ~Ⅳ不良反应差异无统计学意义(P>0.05,表3)。
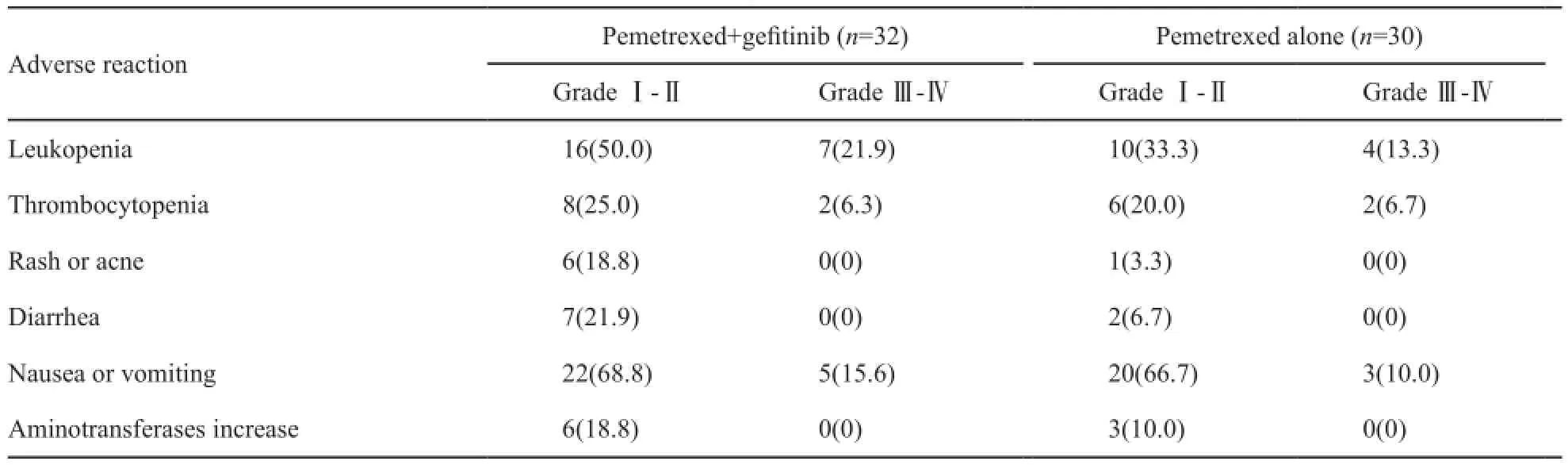
表3 两组不良反应比较Tab. 3 The comparison of the adverse reaction of two groups[n(%)]
3 讨 论
EGFR是原癌基因c-erbB1的表达产物,高表达于多种类型的肿瘤,包括NSCLC。EGFRTKI通过竞争性的抢占酪氨酸激酶区域的ATP结合位点,抑制磷酸化过程和细胞内信号传导,诱导细胞周期滞留、凋亡和抑制血管形成[5]。以吉非替尼为代表的EGFR-TKI药物能明显改善EGFR基因突变阳性晚期NSCLC患者有效缓解率,提高生活质量,延长生存期,目前被多部指南推荐用于EGFR基因突变阳性晚期NSCLC的一线治疗和EGFR基因突变状态不明的二、三线治疗[6]。然而,EGFR-TKI药物治疗一段时间后不可避免地会出现获得性耐药。目前对EGFR-TKI获得性耐药后的治疗缺乏高级别的临床研究证据,多为经验性用药。
有研究表明,EGFR-TKI获得性耐药的患者可从全身化疗中获益[7],也有研究指出继续使用EGFR-TKI药物联合化疗也表现出明显的临床缓解和生存获益[8]。对比两者的优势,有研究发现相比单纯化疗组,联合EGFR-TKI化疗组获得更高的DCR和中位PFS[9]。Goldberg等[10]回顾性研究了78例EGFR-TKI治疗失败的晚期NSCLC,化疗联合EGFR-TKI组ORR为 41%,单用化疗组ORR为18%,联合组中位PFS为4.4个月,单用化疗组中位期PFS为4.2个月,两组OS差异无统计学意义。EGFR-TKI联合化疗是能够有效治疗EGFR-TKI获得性耐药NSCLC的策略之一。刘明月等[11]采用培美曲塞单药,寻琛等[12]采用培美曲塞联合EGFR-TKI治疗EGFR-TKI获得性耐药的晚期NSCLC,均观察到临床缓解和生存获益。有研究通过体外实验发现,吉非替尼和培美曲塞联合作用于NSCLC的吉非替尼耐药细胞表现出明显的协同效应,在抑制肿瘤细胞增殖和促进凋亡都较单用培美曲塞或吉非替尼组有优势[13]。本研究观察培美曲塞单药或联合吉非替尼治疗EGFR-TKI获得性耐药的晚期NSCLC患者,对比观察两者临床疗效的优势,以其为临床用药提供指导。
本研究化疗组30例用培美曲塞单药治疗,联合组32例采用培美曲塞联合吉非替尼治疗,结果显示联合组ORR为46.9%,化疗组为20%,差异有统计学意义(χ2=4.933,P>0.05)。联合组显示出更具优势的临床有效率,两组DCR分别为84.4%和80.0%,差异无统计学意义(P>0.05)。联合组的中位PFS为8.0个月,化疗组中位PFS为6.3个月,差异有统计学意义(χ2=8.063,P<0.05),两组OS差异无统计学意义(P>0.05)。此外,在不良反应方面,联合组中性粒细胞减少、皮疹的发生率较化疗组偏高,差异有统计学意义(P<0.05)。不良反应多表现为轻度,经对症处理后缓解。
综上所述,对于EGFR-TKI获得性耐药的晚期NSCLC患者,培美曲塞联合吉非替尼相比单用培美曲塞,显示出更好的临床有效率和中位PFS,不良反应可以耐受,有一定的临床推广和运用价值。本研究样本量较少,结果尚需大样本研究进行验证。
[1] JEMAL A, SIEGEL R, XU J, et al. Cancer statistics, 2010[J]. CA Cancer J Clin, 2010, 60(5): 277-300.
[2] 张 斌, 张 霞, 高亚杰, 等. 培美曲塞单药与联合用药治疗复发晚期非小细胞肺癌的临床观察[J]. 临床肿瘤学杂志, 2011, 16(10): 41-46.
[3] JACKMAN D, PAO W, RIELY G J, et al. Clinical definition of acquired resistance to epidermal growth factor receptor tyrosine kinase inhibitors in non-small cell lung cancer[J]. J Clin Oncol, 2010, 28(2): 357-360.
[4] THERASSE P, ARBUCK S G, EISENHAUER E A, et al. New guidelines to evaluate the response to treatment in solid tumors. European Organization for Research and Treatment of Cancer, National Cancer Institute of the United States, National Cancer Institute of Canada[J]. J Natl Cancer Inst, 2000, 92(3): 205-216.
[5] GRUNWALD V, HIDALGO M. Developing inhibitors of the epidermal growth factor receptor for cancer treatment[J]. J Natl Cancer Inst, 2003, 95(12): 851-867.
[6] DAHABREH I J, LINARDOU H, SIANNIS F, et al. Somatic EGFR mutation and gene copy gain as predictive biomarkers for response to tyrosine kinase inhibitors in non-small cell lung cancer[J]. Clin Cancer Res, 2010, 16(1): 291-303.
[7] WU J Y, SHIH J Y, YANG C H, et al. Second-line treatments after first-line gefitinib therapy in advanced non-small cell lung cancer[J]. Int J Caner, 2010, 126(1): 247-255.
[8] LI S, ZHOU F, REN S, et al. Response to pemetrexed rechallenge after acquired resistance of EGFR-TKI in a patient with advanced NSCLC[J]. Lung Cancer, 2014, 84(2): 203-205.
[9] 李剑英, 吴晓敏, 何灵慧. EGFR-TKI联合化疗治疗EGFRTKI获得性耐药的晚期非小细胞肺癌疗效分析[J]. 中国癌症杂志, 2013, 23(6): 462-466.
[10] GOLDBERG S B, OXNARD G R, DIGUMARTHY S, et al. Chemotherapy with Erlotinib or chemotherapy alone in advanced non-small cell lung cancer with acquired resistance to EGFR tyrosine kinase inhibitors[J]. Oncologist, 2013, 18(11): 1214-1220.
[11] 刘明月, 侯桂琴, 高天慧, 等. 培美曲塞治疗EGFR-TKI获得性耐药的晚期非小细胞肺癌疗效观察[J]. 肿瘤防治研究, 2012, 39(6): 713-715.
[12] 寻 琛, 王 琳, 廖 峰, 等. 培美曲塞联合EGFR-TKI用于EGFR-TKI治疗失败后晚期NSCLC 的临床观察[J].实用癌症杂志, 2014, 29(8): 915-917.
[13] WU M, YUAN Y, PAN Y Y, et al. Combined gefitinib and pemetrexed overcome the acquired resistance to epidermal growth factor receptor tyrosine kinase inhibitors in non-small cell lung cancer[J]. Mol Med Rep, 2014, 10(2): 931-938.
Pemetrexed with gef i tinib or pemetrexed alone in advanced non-small cell lung cancer with acquired resistance to EGFR tyrosine kinase inhibitors
LIU Hongliu, YANG Jiamei (Department of Oncology,
the Second Affiliated Hospital of Zhengzhou University, Zhengzhou 450000, Henan Province, China)
Background and purpose: New treatment methods should be explored for non-small cell lung cancer (NSCLC) patients with acquired resistance to epidermal growth factor receptor-tyrosine kinase inhibitor (EGFR-TKI). This study compared the curative ef f ect of pemetrexed with gef i tinib or pemetrexed alone in advanced NSCLC with acquired resistance to EGFR-TKI. Methods: This study included 62 NSCLC patients with advanced EGFR gene mutation and acquired resistance to EGFR-TKI. Among those, 32 patients were treated with pemetrexed and gef i tinib, and 30 patients treated with gef i tinib alone. The dif f erences in outcomes between the two strategies were assessed. Results: Objective response rate (ORR) was 46.9% for those treated with pemetrexed and gef i tinib and 20% for those treated with pemetrexed alone(χ2=4.933, P<0.05). There was no signif i cant dif f erences between the two groups on disease control rate (DCR) (P>0.05). The median progression-free survival (PFS) was 8.0 months on pemetrexed and gefitinib group and 6.3 months on pemetrexed alone (χ2=8.063, P<0.05). There was no significant differences between the two groups on overall survival (OS) (P>0.05). Higher occurrence of leukocytopenia and rash was observed in the pemetrexed and gef i tinib group than in the pemetrexed group (P<0.05). There was no signif i cant dif f erences between the two groups on grade 3-4 toxicities (P>0.05). Conclusion: This study was to demonstrate that continuation of EGFR-TKI with pemetrexed in patients with acquired resistance improves outcomes compared with pemetrexed alone.An improved response rate and PFS were observed in this study. A larger prospective clinical trial is needed to further evaluate this promising strategy.
Pemetrexed; Gef i tinib; Advanced non-small cell lung cancer; Epidermal growth factor receptor-ty-rosine kinase inhibitor
YANG Jiamei E-mail: yxxlvip@sina.com
10.19401/j.cnki.1007-3639.2017.02.009
R734.2
A
1007-3639(2017)02-0135-05
2016-08-30
2016-12-10)
杨家梅 E-mail:yxxlvip@sina.com
