使用Jam及Sandwich球囊技术处理冠状动脉穿孔2例
2017-03-27罗建方刘媛黄文晖董豪坚何鹏程陈纪言
罗建方 刘媛 黄文晖 董豪坚 何鹏程 陈纪言
·病例报告·
使用Jam及Sandwich球囊技术处理冠状动脉穿孔2例
罗建方 刘媛 黄文晖 董豪坚 何鹏程 陈纪言
经皮冠状动脉介入治疗; 冠状动脉穿孔; 明胶海绵
1 临床资料
病例1 患者 男,55岁。因“反复胸闷3年余”入住广东省人民医院。既往高血压病史10年,血压控制良好,无糖尿病史。吸烟20年,每天10支左右;饮酒史10年,每周半斤左右。入院查体:体温36.5℃,脉搏64次/min,呼吸18次/min,血压106/74 mmHg(1 mmHg=0.133 kPa),中等体型,自动体位,颈静脉无充盈,双肺呼吸音正常,未闻及干、湿性啰音,心界不大,心率64次/min,心律齐,各瓣膜听诊区未闻及杂音,腹部平软,肝脾未触及,双下肢无水肿。血常规示:白细胞计数11.30×109/L,中性粒细胞比值80.10%,其余均正常。后复查血常规正常。尿、大便常规检查正常。心电图示:Ⅱ、Ⅲ、aVF导联ST段压低0.1~0.3 mV,V1、V2导联ST段压低0.1 mV,入院后观察心电图无急性心肌梗死的动态演变。超声心动图示:心脏各房室不大,心脏、形态、结构大致正常,心脏收缩功能正常,左心室射血分数(LVEF)60%。X线胸片未见异常。肌钙蛋白及心肌酶较正常轻度增高。B型脑利钠肽(BNP)93.6 pg/ml(正常范围)。生化检查示:血糖、血脂、肝功能、肾功能正常。冠状动脉造影示:冠状动脉右优势型,左主干未见狭窄;前降支近中段60%狭窄;左回旋支细小,未见狭窄;右冠状动脉近段完全闭塞,伴弥漫性钙化病变,后三叉可见经间隔支形成左向右侧支循环,拟行经皮冠状动脉介入治疗(PCI)。
PCI过程及Jam球囊技术:经右股动脉入径,以6 F AL1指引导管进入右冠状动脉开口;在Finecross微导管支持下,使Pilot150导丝通过右冠状动脉闭塞病变到达后降支(PDA),将微导管沿导丝跨过病变,在微导管内抽出Pilot150导丝,交换为旋磨导丝,以1.5 mm旋磨头对右冠状动脉进行旋磨处理,复查造影显示PDA近端穿孔(Ellis Ⅲ型,图1)。在破口处使用2.0 mm×20.0 mm球囊以2~3 atm(1 atm=101.325 kPa)扩张封堵约60 min仍无法闭合破口,转而采用Jam球囊技术处理破口。在球囊继续低压扩张封堵破口情况下,重新以导丝引入Finecross微导管至PDA近端,撤出微导管导引导丝,保留微导管尖端于PDA破口近端。负压回抽封堵球囊,轻轻前送封堵球囊,暴露冠状动脉破口并确保球囊近端越过破口,使破口刚好位于微导管尖端与球囊近端之间。重新低压扩张球囊封闭PDA,并经微导管缓慢注入制备好的明胶海绵颗粒0.5 ml(图2和图3A),并观察5~10min,复查造影未见对比剂外渗。负压回抽封堵球囊,缓慢拉出至体外(图3B)。重新造影示:PDA破口成功封闭,未见对比剂外渗,PDA远端TIMI血流0~Ⅰ级。手术过程中患者无胸闷不适,床边超声检测心包积液约1~2 mm,无急性心脏压塞表现。术后复查心电图、肌钙蛋白轻度升高。继续予以阿司匹林等药物治疗出院,1个月后返院复查造影,右冠状动脉主干及PDA通畅,血流TIMI Ⅲ级,无明显残余狭窄,无对比剂外渗(图4)。
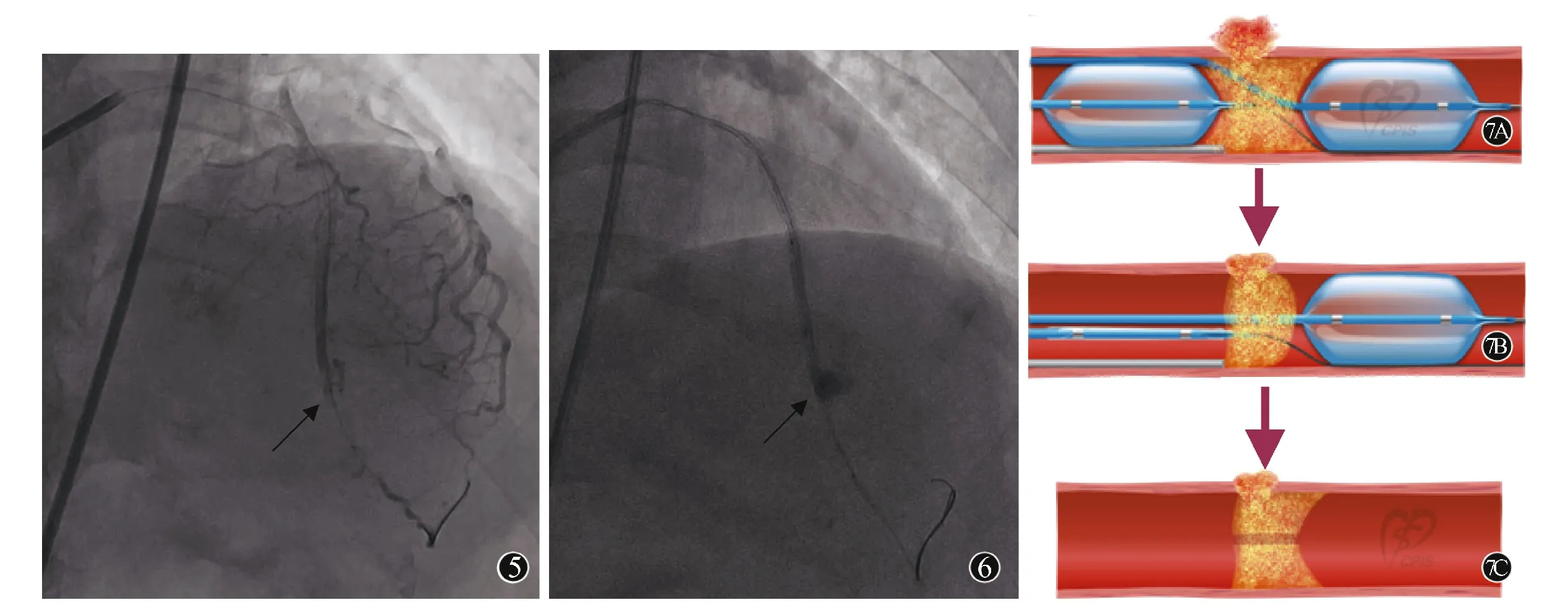
图5 对比剂外渗(箭头示) 图6 缓慢注入制备好的明胶海绵颗粒(箭头示) 图7 Sandwich球囊技术示意图 7A:于破口两端低压扩张球囊,注射明胶海绵0.3 ml封堵破口;7B:复查造影未见对比剂渗出,先回抽并退出近端球囊;7C:再次复查造影未见对比剂渗出,回抽并退出远端球囊

图4 复查造影未见残余狭窄,无对比剂渗出
病例2 患者 男,62岁。因“反复胸闷2年”入院。既往有2型糖尿病史、高血压病史,长期大量吸烟史。入院查体:生命体征平稳,双肺呼吸音正常,未闻及干、湿性啰音,心界不大,心率64次/min,心律齐,各瓣膜听诊区未闻及杂音,腹部平软,全腹无压痛及反跳痛,双下肢无水肿。辅助检查示:血常规正常;尿、大便常规检查正常;肌钙蛋白及心肌酶检查正常,BNP在正常范围。生化检查示:血糖、血脂、肝功能、肾功能均正常。心电图示:窦性心律,V1、V2、V3导联ST段压低0.1~0.3 mV。超声心动图示:心脏各房室不大,心脏形态、结构大致正常,心脏收缩功能正常,LVEF 63%。X线胸片示:心、肺、膈未见异常。冠状动脉造影示:前降支中段慢性完全闭塞病变(CTO),拟行PCI。
PCI过程及Sandwich球囊技术:以7 F EBU 3.75指引导管进入左冠状动脉开口,以顺应性球囊2.0 mm×20.0 mm扩张前降支病变并置入1枚2.25 mm×33.00 mm药物洗脱支架,释放后复查造影显示支架远段冠状动脉穿孔(Ellis Ⅲ型, 图5)。常规球囊封堵无法封闭破口,转而使用Sandwich球囊技术处理破口。以导丝引入球囊1.3 mm×15.0 mm置于破口远端,第2根导丝引入球囊2.0 mm×20.0 mm置于破口近端,使冠状动脉破口刚好位于两个球囊之间,以第3根导丝引入Finecross微导管使导管尖端至两球囊之间的冠状动脉破口处,低压扩张两个球囊,使冠状动脉破裂段位于两球囊之间,经微导管缓慢注入制备好的明胶海绵颗粒0.3 ml于冠状动脉破裂段(图6、图7),并观察5~10 min,负压回抽两个球囊,回抽后缓慢拉出指引导管。重新造影示前降支破口成功封闭,未见对比剂外渗,前降支远端TIMI血流Ⅰ级。患者无胸闷不适,无心脏压塞等表现。术后超声心动图未见明显心包积液,继续予以双联抗血小板等冠心病二级预防药物治疗,临床随访一般情况良好。
2 讨论
冠状动脉破裂、冠状动脉穿孔为PCI最严重的并发症之一,可导致急性心肌梗死、急性心脏压塞或需紧急冠状动脉旁路移植术甚至导致死亡等。有报道显示,冠状动脉破裂、穿孔发生率为0.1%~3%[1-2]。Ellis等[3]根据影像学形态特征将冠状动脉穿孔分为三型:Ⅰ型,X线下可见对比剂局部呈蘑菇或溃疡状向血管外突出,局限于冠状动脉外膜下,无外漏,多由导丝、支架或旋磨、旋切装置引起,较为常见;Ⅱ型,X线下可见对比剂渗漏至心肌或心包内,但无喷射状漏出;Ⅲ型,X线下可见对比剂通过>1 mm的冠状动脉破口,呈喷射状漏入心包、心腔或冠状静脉。Ⅲ型又可分两个亚型:ⅢA型,对比剂漏入心包;ⅢB型,对比剂漏入心室腔或其他部位。
冠状动脉穿孔的处理包括非外科手术处理与外科手术处理。处理总的原则为封闭穿孔和保持血流动力学稳定,应首先考虑解除心脏压塞,必要时急诊外科手术治疗。对于部分Ellis Ⅱ型、Ⅲ型冠状动脉穿孔,球囊压迫往往难以奏效,应在行球囊压迫止血的同时采取进一步的补救措施。而经典的微导管法通过微导管将自体脂肪、血栓、弹簧圈、明胶海绵甚至是缝线等送至破口堵塞止血,但只适用于较少存活心肌或直径较小的血管远段末梢的穿孔。对于血管体部的穿孔常常需要各种类型的覆膜支架进行处理,而最终会残留异物于冠状动脉腔内。
作者结合明胶海绵特性及球囊封堵特点,针对冠状动脉体部的穿孔进行封堵方法的改良。病例1中以6 F指引导管完成Jam球囊技术,旋磨后血管体部破裂穿孔,破口较大且位于血管主支体部,性质明显与导丝通过或球囊扩张所致穿孔有异,大大提高了封堵难度。以球囊封闭破口远端血管,在破口段注射明胶海绵,因远端球囊封堵原因,明胶像“果酱”一样挤向周边的冠状动脉破口并机械性闭塞,最后回撤球囊(必要时低压扩张)时会把同时被明胶闭塞的冠状动脉主干拖出一条通道以保持血管通畅。该法因明胶可能会往破口近段血管蔓延而导致主干闭塞段较长,因而仅适用于供血面积较小的血管,以防主干被闭塞导致严重缺血。同理,在病例2中,前降支行支架术后,于支架中远端冠状动脉破裂穿孔,患者靶血管直径小,且已置入支架,单纯球囊封堵无效情况下进行覆膜支架置入,从技术及预后来说都不是最理想的处理方式。术者希望在封堵有效的情况下保持支架通畅且少残留异物,单纯使用Jam球囊技术可能会因明胶挤进破口的同时往血管近段挤压,过多地残留于支架管腔而导致支架急性血栓形成,因此使用Sandwich球囊技术予以处理。Sandwich球囊技术进一步改良了Jam球囊技术的局限,把明胶海绵的注射空间进一步局限在破口的局部(两个球囊之间),让更多的明胶留在破口处,最大程度地降低其在主支血管的残留量,减少对主支血流的影响。
明胶海绵的主要成分是从猪的皮肤中提取的,其在水中不能溶解,但在人体内约4~8周完全降解吸收。颗粒明胶海绵通过放射消毒,细菌内毒素含量<0.5 EU/ml,无过敏反应,无急慢性毒性作用,其本身没有药理作用,是通过栓塞机械性地阻断血流而达到封堵效果。在用于冠状动脉穿孔栓塞时制备方法如下:备好10 ml干洁注射器并拔除活塞,把一瓶明胶海绵颗粒栓塞剂(颗粒直径350 μm,杭州艾力康医药科技有限公司)约100 mg倒入注射器中(手指封闭注射器出口以防明胶漏出);以3 ml对比剂+3 ml生理盐水(1:1)混合倒入注射器中,与明胶海绵充分混和;通过三通连接管把制备好的明胶海绵混合液灌入5 ml注射器中;最后使用该注射器经微导管在X线透视下缓慢轻柔推注约0.5 ml明胶海绵混合液至靶目标,必要时增加注射剂量直到破口封闭。本文所介绍的两种封堵方法各有特点:Jam球囊技术主要用于主支血管体部的穿孔封堵,以1根6 F指引导管、1根微导管及1枚冠状动脉球囊即可完成;而Sandwich球囊技术同样适用于主支体部的穿孔,特别是破口较大,封堵过程中需要持续以球囊辅助封堵者,需要1根7 F指引导管(或2根6 F指引导管)、1根微导管及2枚冠状动脉球囊方可完成。
本文资料初步表明,使用Jam及Sandwich球囊技术是有效救治冠状动脉血管体部穿孔的新方法,特别是对于血管主支体部大破口的处理,残留异物少并可在短期内被吸收,在临床实际操作中运用灵活,有望进一步提高冠状动脉穿孔的救治成功率。
[1] Gruberg L, Pinnow E, Flood R, et al. Incidence, management, and outcome of coronary artery perforation during percutaneous coronary intervention.Am J Cardiol,2000,86(6):680-682.
[2] 李国庆,穆叶赛·尼加提,雷建新,等.心包腔内注入凝血酶治疗经皮冠状动脉介入治疗围术期急性心脏压塞的疗效和体会(附13例).中国介入心脏病学杂志,2016,24(6):326-329.
[3] Ellis SG, Ajluni S, Arnold AZ, et al. Increased coronary perforation in the new device era: incidence, classification, management, and outcome. Circulation, 1994,90(6):2725-2730.
10.3969/j.issn.1004-8812.2017.02.013
广东省科技计划项目(2013B031800024);广东省科技计划项目(2015A020210064)
510080 广东广州, 广东省心血管病研究所,广东省冠心病防治研究重点实验室,广东省人民医院心内科
陈纪言,Email: sychenjiyan@sina.com
R541.4
2016-09-23)
