八角枫根中1个新的生物碱及其细胞毒活性研究
2017-03-25邢欢欢周堃杨艳周玲董伟王月德
邢欢欢+周堃+杨艳+周玲+董伟+王月德+马航赢+周敏+叶艳青+胡秋芬
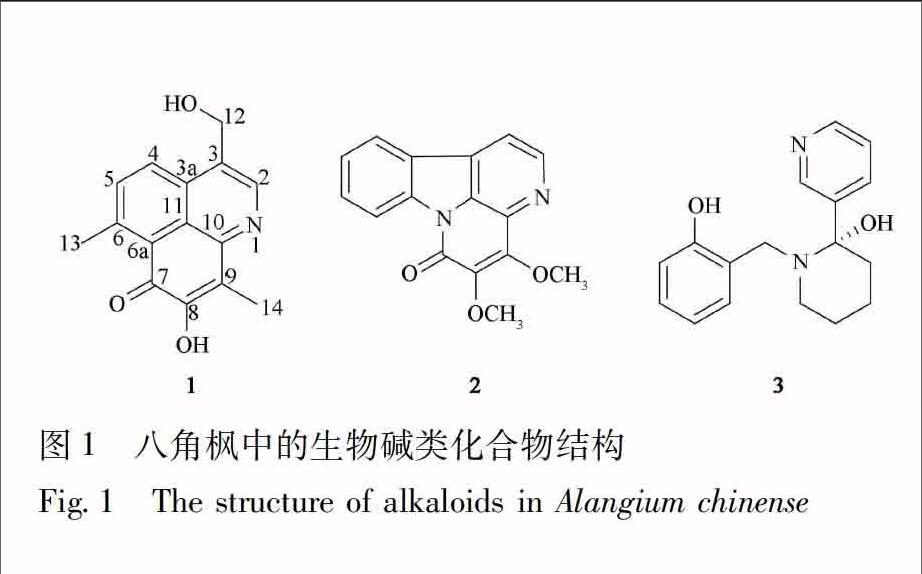
[摘要]对八角枫Alangium chinense 根的化学成分进行研究,运用硅胶、凝胶、MCIgel 树脂及 RPHPLC 等多种色谱技术分离纯化,并根据理化性质和波谱数据鉴定化合物的结构,同时用 MTT 法测定化合物的细胞毒活性。从八角枫根的 90%乙醇提取物中分离鉴定了 3 个生物碱类化合物 (1~3),其中化合物1为新化合物,命名为 8羟基3羟甲基6,9二甲基7H苯并[de]异喹啉7酮,其对 NB4, A549, SHSY5Y, PC3, MCF7 的 IC50分別为 42, 35, 57, 28, 39 μmol·L-1,该化合物具一定的细胞毒活性。
[关键词]八角枫; 生物碱; 细胞毒活性
A new cytotoxic alkaloid from roots of Alangium chinense
XING Huanhuan, ZHOU Kun, YANG Yan, ZHOU Ling, DONG Wei, WANG Yuede, MA Hangying,
ZHOU Min, YE Yanqing, HU Qiufen*
(Key Laboratory of Chemistry in Ethnic Medicinal Resources, State Ethnic Affairs Commission & Ministry
of Education, Yunnan Minzu University, Kunming 650500, China)
[Abstract]We have carried out the chemical investigation on the roots of Alangium chinense The chemical constituents from the roots of Achinense were isolated and purified by various chromatographic techniques, such as silica gel, MCIGel resin, Sephadex LH20 and high performance liquid chromatography As a result, three alkaloids (13) were isolated from 90% EtOH extracts of the roots of this plant Their structures were elucidated by physicalchemical properties and spectral data Among them, compound 1 is a new compound, determined as 8hydroxy3hydroxymethyl6,9dimethyl7Hbenzo[de]isoquinolin7one Cytotoxicity of the compounds was evaluated by the MTT method Compound 1 displayed cytotoxicity against NB4, A549, SHSY5Y, PC3 and MCF7 cell lines with IC50 values of 42, 35, 57, 28 and 39 μmol·L-1, respectively
[Key words]Alangium chinense; alkaloid; cytotoxicity
八角枫又名白龙须、八角梧桐、五角枫等,为八角枫科八角枫属植物Alangium chinense (Lour) Harms。八角枫(华木瓜)是一种落叶灌木或乔木,常生于溪边、旷野及山坡阴湿杂林中,为密源植物,在我国主要分布于陕西、甘肃、江苏、安徽、浙江、江西、福建、河南、湖北、湖南、广东、四川、贵州、云南等地[12]。其性温,味辛、苦,具有祛风除湿,舒筋活络,散淤止痛之功效[3],根和皮药效最好。其叶用于跌打骨折,外刀伤出血;花用于头风痛及胸腹胀满。在云南民间常用于风湿痹痛,肢体麻木,跌打损伤。
目前国内外学者对八角枫进行过一些化学成分研究,主要报道的化合物有:倍半萜、三萜、生物碱、甾体等[45]。Zhang Yang 等[4]报道了八角枫中的生物碱及倍半萜具有抗病毒活性和抗氧化活性,为充分利用我国丰富的民族药资源,进一步从天然植物宝库中发掘活性化合物,本文对八角枫根的化学成分进行了研究,并从中分离到 3 个生物碱类化合物,其中化合物1为新化合物,且该化合物具有一定的细胞毒活性。
1材料
UV2401A 紫外光谱仪 (日本岛津公司);BioRad FTS185 傅里根变换红外光谱仪 (美国伯乐BIORAD 公司);DRX500 型核磁共振仪 (瑞士布鲁克公司);API QSTAR 飞行时间质谱 (美国应用生物公司),VG Autospec3000 高分辨质谱 (英国质谱仪器公司),半制备 HPLC 分析仪器为岛津 LC8A 型高效液相色谱仪,色谱柱为安捷伦公司 Zorbax PrepHT GF (212 mm ×250 mm,7 μm) 和安捷伦 Zorbax C18 (94 mm ×250 mm,5 μm)。柱色谱硅胶 (80~100,150~200 目)、GF254 (100 mm×100 mm) 硅胶板,均为青岛海洋化工厂生产;MCI 填充材料为 MCIgel CHP20P (75~150 μm);凝胶为 Sephadex LH20;薄层色谱法显色,显色剂为5%H2SO4乙醇溶液,喷洒后加热显色;工业用三氯甲烷、甲醇、乙酸乙酯。
八角枫于 2014 年 10 月采于云南大理,标本经云南民族大学民族药资源化学重点实验室杨青松副教授鉴定为八角枫科植物八角枫,标本 (编号2014060) 保存于云南民族大学民族药资源化学重点实验室标本馆。
2提取与分离
取八角枫根 25 kg 晒干,粉碎,过 30 目筛,然后用 90%乙醇水溶液超声提取 4 次(每次用 35 L 的 90%乙醇水溶液室温浸泡 7 d后超声 30 min 提取),滤过,合并提取液,用 3%酒石酸溶液10 L稀释后用乙酸乙酯萃取3次。水相用氢氧化钠调节 pH 为 90~100 后再用乙酸乙酯萃取 3 次,将乙酸乙酯相减压浓缩得浸膏 186 g。浸膏用 20 g 粗硅胶 (80~100 目) 拌样,烘干,用 120 g硅胶 (150~200 目) 经柱色谱分离,三氯甲烷丙酮 (20∶1,9∶1,8∶2,7∶3,6∶4,5∶5) 梯度洗脱,分成 6 个部分。将三氯甲烷丙酮 8∶2 洗脱部分用甲醇溶解,采用 Agilent 公司的 Zorbax PrepHT GF (212 mm ×250 mm,7 μm) 反相柱,以 52% 甲醇水溶液为流动相,体积流量为 15 mL·min-1,收集 315 min 的色谱峰,得化合物2粗品,收集 286 min 的色谱峰,得化合物 1 粗品,收集 262 min 的色谱峰,得化合物 3 粗品。粗品再以甲醇为流动相,用葡聚糖凝胶柱 Sephadex LH20 纯化得化合物 1 (115 mg),2 (128 mg),3 (146 mg),见图1。
3结构鉴定
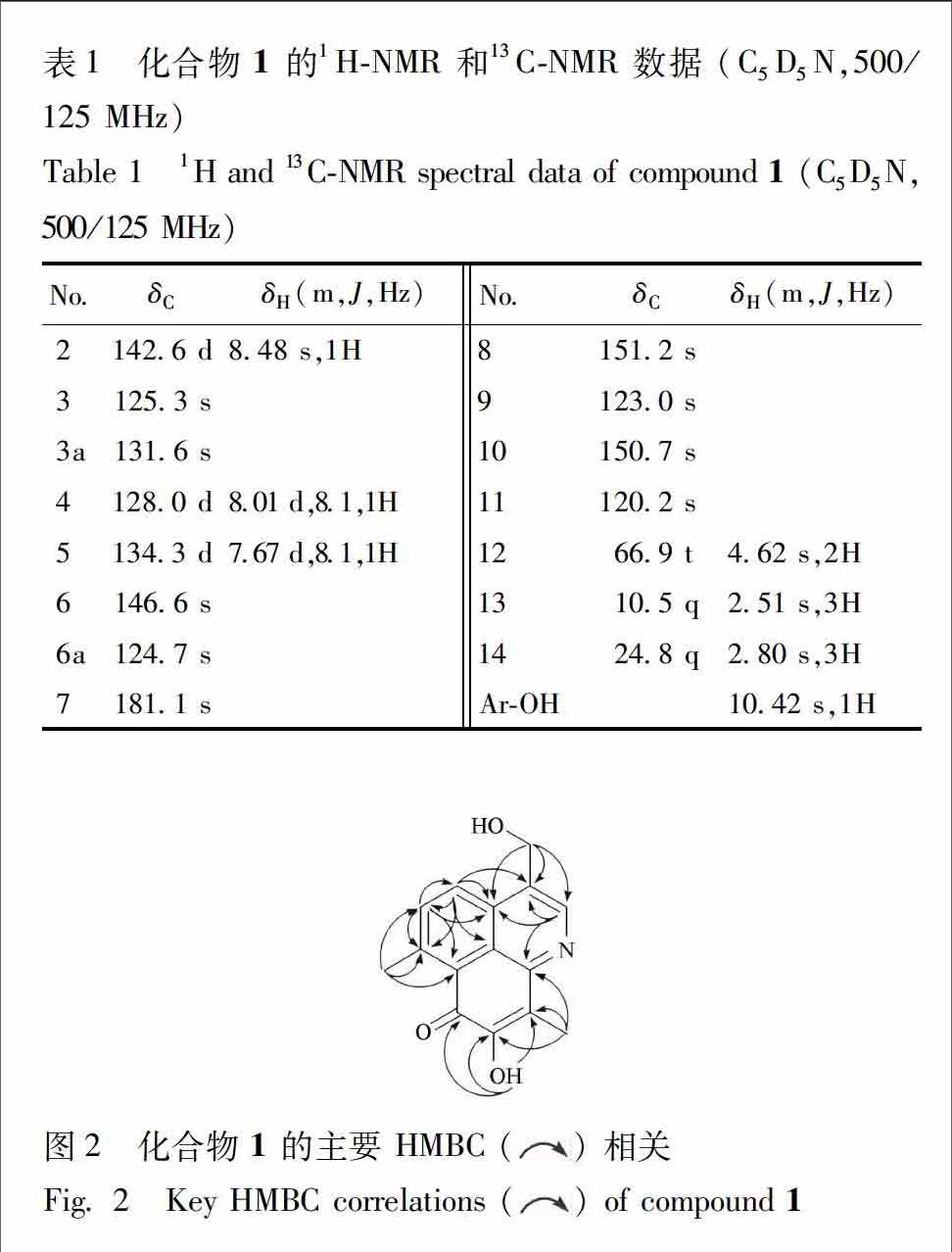
化合物1为橙红色胶状物,UV λ(nm): 210 (428),246 (376),342 (382); IRν(cm-1): 3 412,3 185,2 963,1 650,1 610,1 567,1 462,1 385,1 310,1 267,1 135,1 032,861,728; ESIMS m/z 278 [M+Na]+,HRESIMS m/z 278079 8 [M+Na]+ (計算值 278079 3,C15H13NNaO3)。结合1H 和13CNMR 谱确定分子式为 C15H13NO3,不饱和度为 10。其红外光谱显示化合物中有羟基 (3 412 cm-1)、羰基 (1 650 cm-1) 和芳环 (1 610,1 567,1 462 cm-1) 信号,紫外光谱在 246,342 nm 有最大吸收也证实化合物中存在芳环结构。从1HNMR 谱 (数据归属见表1) 信号可以看出化合物中有 3 个芳香族氢信号 [δH 848 (1H,s),801 (1H,d,J=81 Hz),767 (1H,d,J=81 Hz)];2 个甲基信号 [δH 251 (3H,s) 和 280 (3H,s)];1 个氧化亚甲基信号 [δH 462 (2H,s)];以及 1 个酚羟基信号 (δH 1042,br s)。化合物的13CNMR 和 DEPT 谱显示该化合物含有 8 个芳香季碳 (δC 1253 s,1316 s,1466 s,1247 s,1512 s,1230 s,1507 s,1202 s);3 个芳香次甲基 (δC 1426 d,1280 d,1343 d);1 个 α,β不饱和羰基 (δC 1811 s);2 个甲基 (δC 105 q 和 248 q);以及 1 个氧化的亚甲基 (δC 669 t)。通过 HSQC 谱对化合物的碳氢信号进行了一一对应归属。在 HMBC 谱中,见图2,观测到了 H13 和 C5、C6、C6a,H5 和 C3a、C6a、C4,H4 和 C3、C3a、C11,H212 和 C2、C3、C3a,以及 H2 和 C3、C3a、C12、C10 的相关,可证实化合物中存在 3羟甲基6甲基异喹啉的结构片断。进一步通过 H14 和 C8、C9、C10 的 HMBC 相关,可推测 α,β不饱和羰基中的 β碳 (C9) 与 C14 甲基及异喹啉环的 C10 位相连。酚羟基取代在 C8 位可根据 C8 的化学位移值 (δC 1512 s) 在低场,以及酚羟基信号 (δH 1042) 和 C7、C8、C9 的 HMBC 相关确定。此外,C6a 的化学位移 (δC 1247) 偏高场,推测 C6a 可能连接在羰基中的 α碳 (C7),同时结合该化合物还有1个不饱和度,从而确定 C6a 和羰基 (C7) 直接连接形成 1 个六元环。另外,化合物 1 和文献[4]报道的化合物 8hydroxy3,6,9trimethyl7Hbenzo[de]quinolin7one 非常相似,和文献报道化合物相比,化合物 1 中多了 1 个羟甲基信号,而少了 1 个甲基信号,而且上述 HMBC 相关证明羟甲基取代在母核的 C3 位,证明化合物 1 为文献化合物甲基 (C12) 被氧化为羟甲基的产物,这进一步证实了化合物 1 的结构。至此该化合物的结构得以确定,并命名为8羟基3羟甲基6,9二甲基7H苯并[de]异喹啉7酮。
邢欢欢等:八角枫根中一个新的生物碱及其细胞毒活性研究
化合物2分子式为C16H12N2O3,1HNMR (C5D5N,500 MHz) δ: 866 (1H,d,J=56 Hz,H2), 783 (1H,d,J=56 Hz,H3),768 (1H,m,H8),731 (1H,m,H9),742 (1H,m,H10),752 (1H,m,H11),389 (3H,s,OMe13),382 (3H,s,OMe14); 13CNMR (C5D5N,125 MHz) δ: 1465 (C2),1183 (C3),1085 (C4),1316 (C5),1368 (C6),1332 (C7),1187 (C8),1245 (C9),1202 (C10),1126 (C11),1348 (s),1484 (C13), 1457 (C14),1669 (C15),546 (OMe13),608 (OMe14)。通过其波谱数据与文献对比,鉴定为4,5dimethoxycanthin6one[6]。
化合物3分子式为C17H20N2O2,1HNMR (C5D5N,500 MHz) δ: 182 (2H,m,H3),211 (1H,d,J=140 Hz,H4),166 (1H,m,H4),184 (1H,m,H5),168 (1H,m,H5),287 (1H,m,H6),278 (1H,d,J=11 Hz,H6),864 (1H,s,H2′),776 (1H,d,J=75 Hz,H4′),722 (1H,dd,J=50,80 Hz,H5′),848 (1H,dd,J=15,50 Hz,H6′),678 (1H,d,J=80 Hz,H3″),682 (1H,m,H4″), 715 (1H,m,H5″),696 (1H,d,J=80 Hz,H6″),394 (1H,d,J=170 Hz,H7″); 336(1H,d,J=170 Hz,H7″); 13CNMR (C5D5N,125 MHz) δ: 911 (C2),256 (C3),412 (C4),214 (C5),493 (C6),1468 (C2′),1399 (C3′),1348 (C4′),1238 (C5′),1480 (C6′),1516 (C1″),1194 (C2″),1283 (C3″),1210 (C4″),1293 (C5″),1169 (C6″),486 (C7″)。通过其波谱数据与文献对比,鉴定为2hydroxyNhydroxybenzylanabasine[4]。
4化合物的细胞毒活性
由于多数文献报道生物碱类化合物具有明显的细胞毒活性,因此对化合物 1 进行了细胞毒活性筛选。细胞毒活性检测采用改良的 MTT 测定法[7],以紫杉醇为阳性对照药,采用 5 种人源癌细胞株 (NB4,A549,SHSY5Y,PC3,MCF7),紫杉醇的 IC50分别为003,002,005,005,003 μmol·L-1,化合物 1 的 IC50分别为42,35,57,28,39 μmol·L-1,结果表明化合物 1 对所测试的人源肿瘤细胞增殖具有一定的细胞毒活性。
[参考文献]
[1]刘毅,徐莛婷,趙波,等苗药八角枫的药学研究进展[J]微量元素与健康研究,2012, 29 (1): 57
[2]徐佳佳,翟科峰,董璇,等 八角枫的研究进展[J] 黑龙江农业科学,2016 (2): 143
[3]熊难茜,查俊苗药八角枫的研究进展[J]科协论坛,2013 (8): 108
[4]Zhang Y, Liu Y B, Li Y, et al Sesquiterpenes and alkaloids from the roots of Alangium chinense[J] J Nat Prod, 2013, 76 (6): 1058
[5]翟科峰,王青遥,叶竹青,等 八角枫化学成分的系统定性研究[J]时珍国医国药,2012,23 (2): 295
[6]Kondo Y, Takemoto T The structure of a new βcarboline alkaloid from Picrasma ailanthoides Planchon[J] Chem Pharm Bull,1973, 214: 837
[7]Hu Q F, Zhou B, Ye Y Q, et al Cytotoxic deoxybenzoins and diphenylethylenes from Arundina graminifolia[J] J Nat Prod, 2013, 76 (10): 1854[责任编辑丁广治]
[收稿日期]20160909
[基金项目]国家自然科学基金项目 (21362044,21032085);云南省高校科技创新团队项目(IRTSTYN 201411);2016年云南民族大学研究生创新基金科研项目(2016YJCXS13)
[通信作者]*胡秋芬,教授,硕士生导师, Tel: (0871)68329045, Email: huqiufena@aliyuncom
