基于凝血活性和星点设计—效应面法的黄槐复方提取工艺研究
2017-03-25李鹏程刘涛伍月张倩付春梅刘翠
李鹏程+刘涛+伍月+张倩+付春梅+刘翠
[摘要]運用纤维蛋白原平板法,以凝血酶为参照,建立体外凝血活性测定的方法,以体外凝血活性为指标,筛选黄槐复方提取路线,并在单因素试验基础上,以黄芩苷、芦丁提取转移率和浸膏得率的综合评分值为因变量,乙醇浓度、溶剂用量、提取时间为影响因素,利用星点设计3因素5水平试验,进行二次多项式拟合,通过效应面法优选黄槐复方提取工艺,并测定其凝血活性。结果表明凝血酶浓度在04~16 U·mL-1与沉淀圈面积呈良好线性关系,r=0997 5;平均加样回收率为1038%,RSD 47%;黄槐合提浸膏的沉淀圈面积3881 mm2,比分提浸膏沉淀圈面积大;黄槐浸膏的日用量的活性8428 U。黄槐复方的最佳提取工艺为加6倍量40%乙醇,提取3次,每次2 h,综合评分值预测值为9426,验证值为8834,与预测值偏差为628%,最佳提取工艺制得的中间体凝血活性较好。所建立的方法可以简便、快速、准确地测定黄槐复方的凝血活性,可用于后续工艺的筛选以及质量控制。
[关键词]黄槐复方; 凝血活性; 纤维蛋白原平板法; 星点设计效应面法
Optimization of extraction technology from compound Huanghuai
based on coagulation activity and central composite design
response surface methodology
LI Pengcheng1, LIU Tao2*, WU Yue2, ZHANG Qian2, FU Chunmei2, LIU Cui2
(1 Sichuan Industrial Institute of Antibiotics, Chengdu University, Chengdu 610052, China;
2 College of Pharmacy and Biological Engineerin, Chengdu University, Chengdu 610106, China)
[Abstract]To establish a method for the determination of coagulation activity in vitro by using fibrinogen plate method The extraction route of compound Huanghuai was optimized by selecting thrombin as the reference substance The comprehensive score of extract yield and the extraction transfer rate of baicalin and rutin was set as the dependent variable, with alcohol concentration, solvent volume and extraction time as the influence factors in central composite design for quadratic fitting, and the extraction process of compound Huanghuai was optimized by using response surface methodology The results of thrombin concentration and precipitation zone area showed a good linear relationship in 0416 U·mL-1, r=0997 5 The average recovery rate was 1038% and the RSD was 47 %. The circle of precipitation area of compound Huanghuai combined extract was 3881 mm2, which was bigger than that of fractionated extract The activity on the daily amount of compound Huanghuai extract was 8428 U; and the optimum extraction technology was as follows: alcohol concentration 40%, extracted 3 times, the liquidsolid ratio 6∶1, and extraction time 2 h The predicted value of comprehensive score was 9426 and the measured value was 8834, respectively, with a relative deviation of 628% The coagulation activity of the intermediate obtained by optimal extraction process was better So the method established in this paper was simple, fast and accurate for determination of coagulation activity of compound Huanhuai, which can be also used for the screening of followup process and quality control
[Key words]compound Huanghuai; coagulation activity; fibrinogen plate method; central composite designresponse surface methodology
崩漏是妇科常见病,当前临床应用的化学药物有缩宫素(oxytocin)和前列腺素(prostaglandins)等制剂[1],这些药物都有程度不同的副作用。中医药治疗包括产后出血在内的妇科出血症,有着悠久的历史,无明显副作用。黄槐酒为《济阴纲目》中提的传统经典方[2]。由黄芩及槐米组成,以黄酒为溶剂,以烧红的称砣为热源进行提取。方中黄芩性苦,寒。具有清热燥湿,泻火解毒,止血的功效[3]。槐米性苦,微寒,凉血止血,具有清肝泻火之功[3]。两者合用达到泻火解毒,凉血止血之功,中药复方的提取工艺路线(分提或合提)对复方药效有着重要的影响,目前研究多以指标成分确定复方提取工艺路线,本研究采用纤维蛋白原平板法[4]对复方提取工艺路线所得的提取物的药效进行评价,可解决指标成分不能直接反应疗效的问题。鉴于文献中黄槐酒的提取溶剂为酒,而古代所用的酒含醇量为20%左右,因此,本文采用20%乙醇作为提取溶剂,另外本实验在单因素试验基础上,采用星点设计效应面法优选黄槐复方的提取工艺。
1材料
SQP Satorious电子天平[赛多利斯科学仪器(北京)有限公司];XFS280MB手提式压力蒸汽灭菌器(浙江新丰医疗器械有限公司);DH系列电热恒温箱(西安禾普生物科技有限公司);医用型洁净工作台(苏州市金净净化设备科技有限公司);HS3120超声波清洗器(天津市恒奥科技发展有限公司);702N Hamilton微量进样器(瑞士哈美顿博纳图斯股份公司);P230Ⅱ型高效液相色谱仪(大连依利特分析仪器有限公司);DZF6050A 型真空干燥箱(北京中兴伟业仪器有限公司);BS6KH 型电子天平(上海友声衡器有限公司);FA2004 型电子分析天平(上海良平仪器仪表有限公司生产)。
黄芩、槐米药材均购自四川省荷花池中药材市场,经成都大学刘涛研究员鉴定为唇形科黄芩植物的干燥根和豆科植物槐的干燥花蕾。黄芩苷对照品(批号150725,纯度>98%,四川省维克奇生物科技有限公司);芦丁对照品(批号150622,纯度>98%,四川省维克奇生物科技有限公司);牛凝血酶试剂(上海经科化学科技有限公司,批号T201503);牛血纤维蛋白原试剂(上海经科化学科技有限公司,批号F20150901);生理盐水(四川科伦药业有限公司,批号B15042001);黄槐合提、分提浸膏(由实验室制得,批号分别为20160302,20160303);甲醇为色谱纯,水为娃哈哈纯净水,其余试剂均为分析纯。
2方法与结果
21凝血活性的测定方法
211纤维蛋白原平板的制备取经灭菌的直径为10 cm的培养皿,分别加入1%琼脂溶液25 mL、03%纤维蛋白原溶液20 mL,摇匀,静置30 min使其凝固后,用打孔器打出直径为3 mm的小孔,备用[5]。
212黄槐分提与合提的浸膏制备精密称取黄芩100 g,槐米25 g,加入8倍量20%乙醇,提取3次,每次1 h,滤过,合并提取液,减压浓缩干燥(60 ℃,-008 MPa),即得黄槐合提浸膏;精密称取黄芩100 g,槐米25 g,分别加入8倍量20%乙醇,提取3次,每次1 h,滤过,分别合并提取液,减压浓缩干燥(60 ℃,-008 MPa),即得黄槐分提浸膏。
213供试品溶液的制备精密称取黄槐浸膏2份,每份1 g,置2个具塞锥形瓶中,分别加入生理盐水、纯净水各10 mL,称定质量,超声5 min,放冷,再称定质量,用相应的试剂补足失重,摇匀,滤过,取续滤液,即得。
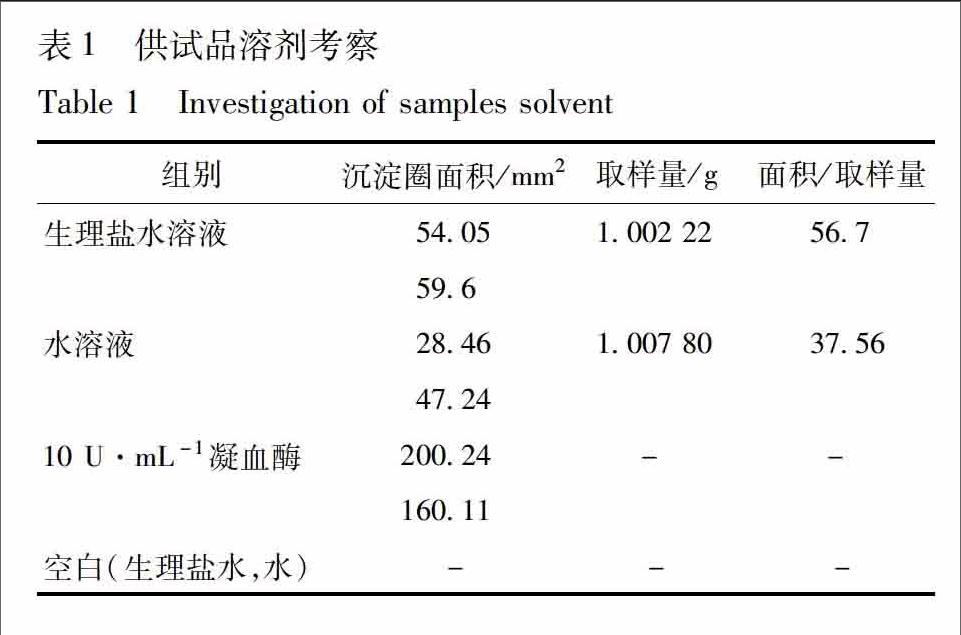
214溶剂的考察分别精密移取2种供试品溶液、生理鹽水、纯净水各25 μL,进行同板点样,同一板内点样2次,平行实验2次。37 ℃恒温培养17 h后测定沉淀圈的面积,见表1。实验结果得到生理盐水制备的供试品沉淀圈清晰可见且面积较大,空白样品无干扰。故选用生理盐水作为供试品制备的溶剂。
22标准曲线的绘制
分别精密移取04,4,8,12,16 U·mL-1凝血酶溶液25 μL,进行同板点样(点入上述纤维平
板的小孔中),共点5次, 37 ℃恒温培养17 h后测定沉淀圈的面积,以凝血酶浓度为横坐标,沉淀圈面积为纵坐标,得线性方程为Y=1764X+4739,r=0997 5,结果表明,凝血酶在浓度为04~16 U·mL-1与沉淀圈面积呈良好的线性关系。
23精密度试验
231同板精密度试验分别精密吸取冷藏于4 ℃的10 U·mL-1凝血酶溶液25 μL,进行同板点样(点入上述纤维平板的小孔中),共点6次,37 ℃恒温培养17 h后测定沉淀圈的面积,计算RSD。结果RSD 49%,同板精密度良好。
232异板精密度试验分别精密吸取冷藏于4 ℃的10 U·mL-1凝血酶溶液25 μL,进行异板点样(点入上述纤维平板的小孔中),共点6次,37 ℃恒温培养17 h后测定沉淀圈的面积,计算RSD。结果RSD 40%,异板精密度良好。
24重复性试验
取同一批号的黄槐合提浸膏(批号20160302)1 g,精密称定,按212项下方法,用生理盐水作为溶剂,平行制备6份供试品溶液,分别精密吸取供试品溶液25 μL,进行同板点样(点入上述纤维平板的小孔中),37 ℃恒温培养,17 h后测定沉淀圈的面积,计算面积与取样量的比值,并计算RSD。结果RSD 38%,重复性良好。
25稳定性试验
取同一批号的黄槐合提浸膏(批号20160302)1 g,精密称定,按212项下方法,用生理盐水作为溶剂,制备供试品溶液,分别于0,05,1,15,2,25 h进行同板点样(点入上述纤维平板的小孔中),每次点样量为25 μL,37 ℃恒温培养,17 h后测定沉淀圈的面积,计算RSD。结果RSD 24%,稳定性良好。
26加样回收试验
取同一批号的黄槐合提浸膏(批号20160302,活性292 U·g-1)6份,每份05 g,精密称定,分别精密吸取2 U·mL-1凝血酶溶液1 mL,按212项下方法,用生理盐水作为溶剂制备供试品溶液,分别精密吸取供试品溶液25 μL,进行同板点样(点入上述纤维平板的小孔中),37 ℃恒温培养,17 h后测定沉淀圈的面积,计算加样回收率。结果平均回收率为1038%,RSD 47%。表明本方法回收率良好。
27黄槐复方的提取路线的筛选
按照相同的生药量分别精密称取黄槐合提浸膏1 g,黄槐分提浸膏(黄芩浸膏078 g,槐米浸膏019 g)于2个具塞锥形瓶中,精密移取生理盐水10 mL于2个锥形瓶中,称定质量,超声5 min,放冷,再称定质量,用相应的试剂补足失重,摇匀,滤过,取续滤液,分别精密移取2种供试品溶液、生理盐水、10 U·mL-1凝血酶各25 μL,进行同板点样,同一板内点样2次,平行试验2次。37 ℃恒温培养17 h后测定沉淀圈的面积。结果黄槐合提浸膏的沉淀圈面积为3881 mm2,分提浸膏的沉淀圈面积为3453 mm2,表明黄槐合提浸膏的凝血作用强于分提浸膏的凝血作用,因此选用合提的方式。
28混合对照品的活性标准曲线的制备及其活性测定
分别精密移取质量浓度为2016,4032,6048,8064,1008 g·L-1的混合对照品溶液及空白溶剂各25 μL,进行同板点样(点入上述纤维平板的小孔中),共点6次,37 ℃恒温培养17 h后测定沉淀圈的面积,以對照品浓度为横坐标,沉淀圈面积为纵坐标,得线性方程为Y=0799X+8694,r=0995 5,结果表明,黄芩苷、芦丁在总浓度为2016~10080 g·L-1与沉淀圈面积呈良好的线性关系,空白无干扰。表明后续的提取工艺可以以黄芩苷、芦丁的提取转移率指标进行研究。利用黄芩苷、芦丁的含量来反映其凝血活性的大小,测得其活性为1921 U·g-1。
29黄芩苷、芦丁的测定
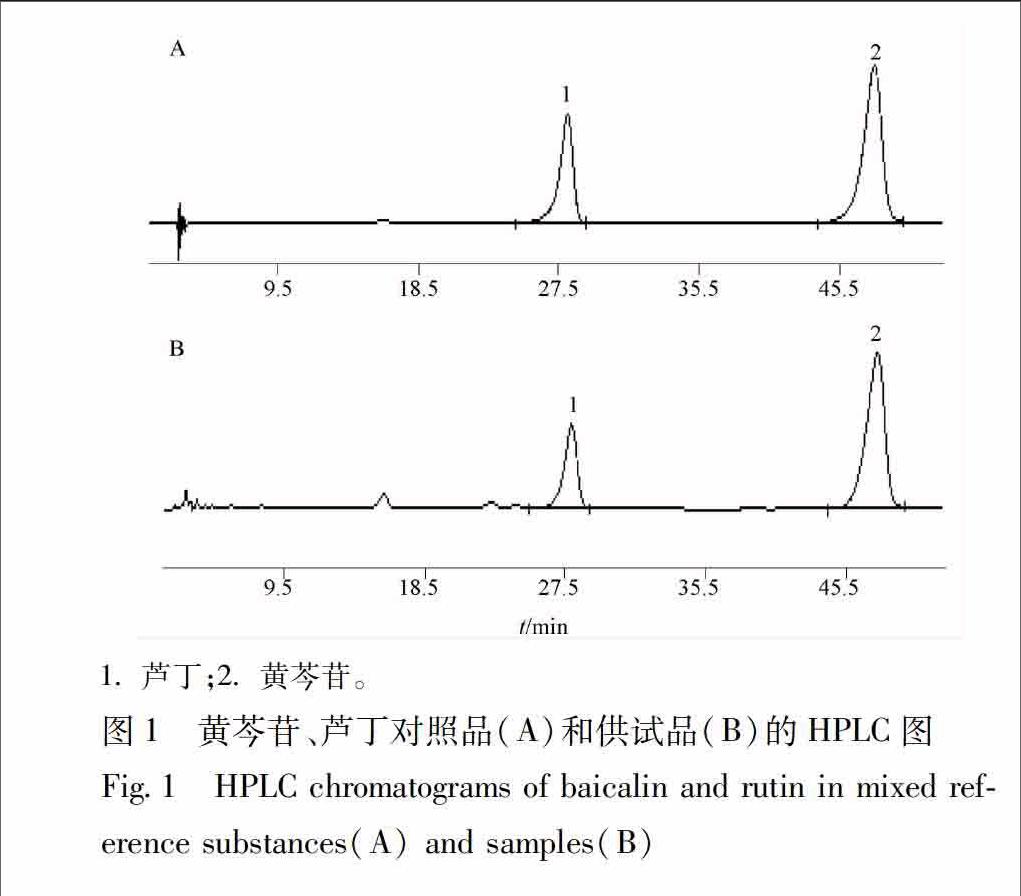
291色谱条件Hypersil ODS2色谱柱(46 mm×250 mm,5 μm),流动相甲醇1%冰醋酸溶液(31∶69),检测波长257 nm,进样量10 μL,见图1。
292对照品溶液的制备取黄芩苷对照品、芦丁对照品适量,精密称定,加甲醇制成每1 mL含0165 mg黄芩苷、0088 6 mg芦丁的混合对照品溶液,即得。
293黄槐复方提取液供试品溶液的制备精密量取黄槐复方提取液1 mL至25 mL量瓶中,加流动相稀释至刻度,摇匀,即得。
294线性关系考察分别配制黄芩苷、芦丁混合对照品溶液,其中芦丁质量浓度为0008 86,0044 3,0088 6,0177 2,0265 8,0310 1 g·L-1,黄芩苷质量浓度为0016 5,0082 5,0165,033,0495,0577 5 g·L-1,按照291项下色谱条件进样,测定峰面积。以峰面积为纵坐标(Y),黄芩苷、芦丁进样浓度为横坐标(X),绘制标准曲线,得芦丁的回归方程为Y=18 211X-7928,r=0999 0,表明芦丁在 0008 86~0310 1 g·L-1进样浓度与峰面积呈良好的线性关系;黄芩苷的回归方程为Y=12 548X+3468,r=0999 0,表明黄芩苷在0016 5~0577 5 g·L-1进样浓度与峰面积呈良好的线性关系。
210浸膏得率的测定
精密量取黄槐复方提取液 100 mL,置已干燥至恒重的蒸发皿中蒸干,于105 ℃干燥 3 h,置干燥器中冷却30 min,迅速精密称重,计算浸膏得率。浸膏得率=浸膏质量/药材总质量×100%。
211单因素试验
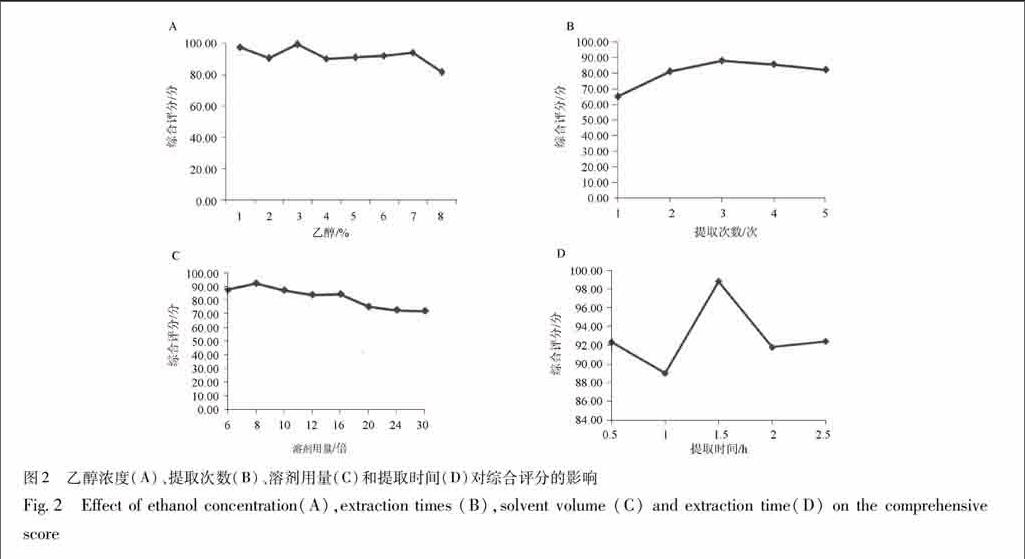
2111乙醇浓度考察鉴于文献中黄槐酒的提取溶剂为酒[2],因此,本文采用乙醇作为提取溶剂。称取黄芩50 g,槐米125 g,平行8份,分别加入8倍10%,20%,30%,40%,50%,60%,70%,80%乙醇,分别提取3 次,每次提取1 h,合并提取液,滤过,测定其黄芩苷、芦丁提取转移率[6]以及浸膏得率,结果按黄芩苷提取转移率芦丁提取转移率浸膏得率=5∶3∶2进行综合评分计算[78],结果见图2。结果表明,随着乙醇浓度增加,综合评分随之下降,30%乙醇时,综合评分最高为9925。因此将乙醇浓度定为30%。
2112提取次数考察称取黄芩50 g,槐米125 g,平行5份,分别加入8倍30%乙醇,分别提取1,2,3,4,5次,每次提取时间为1 h,合并提取液,滤过,测定其黄芩苷、芦丁提取转移率以及浸膏得率,按综合评分计算,结果见图2。结果表明,随着提取次数的增加,综合评分随之先是上升后下降,当提取次数为3次时,分数最高为8831。结合工业生产的实际,同时由于提取次数为非连续变量,回归处理较困难,因此将提取次数定为3次。
2113乙醇用量考察称取黄芩50 g,槐米125 g,平行8份,分别加入6,8,10,12,16,20,24,30倍30%乙醇,提取3次,每次1 h,合并提取液,滤过,取滤液测定其黄芩苷、芦丁提取转移率以及浸膏得率,按综合评分计算,结果见图2。结果表明,随着溶剂用量的增加,综合评分分数先是随之增加,后随之下降。当溶剂用量达到8时,分数最高为9231。因此选择8倍的溶剂用量。
2114提取时间考察称取黄芩50 g,槐米125 g,平行5份,分别加入8倍30%乙醇,提取3次,每次提取时间分别为05,1,15,2,25 h,合并提取液,滤过,测定其黄芩苷、芦丁提取转移率以及浸膏得率,按综合评分计算,结果见图2。结果表明,随着提取时间的延长,综合分数随之上升后又下降,当提取时间为15 h时,综合评分分数最高为9883,因此选择提取时间为15 h。
212星点设计效应面优化提取工艺
2121因素与水平的确定根据单因素试验结果,选取乙醇用量(6~10倍)、提取时间(05~25 h)、乙醇浓度(10%~50%),提取次数为3次。根据星点设计的原理,每因素设5水平,用代码值-α,-1,0,1,α来表示(2因素设计的α=1732)。代码值所表示的实际操作物理量表见表
2。将黄芩苷的提取转移率、芦丁的提取转移率及浸膏得率数值进行综合评分[911],而本试验要求黄芩苷和芦丁的提取转移率及浸膏得率越高越好,结果见表3。
2122模型拟合采用DesignExpertV806(1)软件,以各综合评分值对自变量进行多元线性回归和二项式拟合。得多元线性方程:Y=64902 58+8908 56X2+0230 95X3 (r=0532 6, P<005),二项式方程:Y=221939 55-40926 90X1+17469 11X2-0170 48X3-0952 02X1X2+ 0016 187X1X3-0132 86X2X3+ 2661 15X12+1013 77X22 +0007 853 66X32(r=0780 9,P<0000 1),根据
统计软件对各项系数进行的t检验结果,删除P>05的项后,再进行二项式方程拟合,达到简化模型目的。所得方程为Y=219721 14-40002 52X1 +8908 56X2+0230 95X3 +2544 47X12(r=0749 4,P<005)。从拟合方程的相关系数可见,多元线性回归方程的相关系数较低,而多元二项式拟合方程相关系数较高,拟合效果较好。
2123效应面优化及预测性评价根据优化后的二项式方程,运用DesignExpertV806(1)软件绘制评价指标随因素变化的三维效应面图和等高线图,见图3~5。
从效应面和等高线图可知,最优区域综合评分值>85,当X1的取值在6~8倍,X2的取值在2~25 h,X3的取值在38%~50%时,综合评分值落在最高效应值区间。进一步通过DesignEXpertV806(1)软件预测分析,获得一组综合评分响应值最大的优化条件:X1为6倍,X2为2 h,X3为40%,选择最佳提取工艺为加6倍量40%乙醇,提取3次,每次2 h。
213驗证试验
称取黄芩50 g,槐米125 g,平行3组,按优选的提取工艺进行验证试验,并将预测值与实测值进行偏差计算,结果见表4。可知,预测值与实测值间的偏差为628%,表明采用星点设计效应面法选择的黄槐复方提取工艺重复性好,建立的数学模型具有较好的预测性,拟合结果合理、可靠。
214验证工艺浸膏凝血活性测定
按照相同的生药量分别精密称取3批黄槐浸膏09 g,于3个具塞锥形瓶中,精密移取生理盐水10 mL于3个锥形瓶中,称定质量,超声5 min,放冷,再称定质量,用相应的试剂补足失重,摇匀,滤过,取续滤液,分别精密移取3种供试品溶液、生理盐水、10 U·mL-1凝血酶各25 μL,进行同板点样,37 ℃恒温培养17 h后测定沉淀圈的面积。平行试验3次。结果RSD为59%,表明星点设计效应面选出的工艺浸膏凝血活性较好,可以用于黄槐复方的提取,见表5。
3讨论
目前中药复方的提取工艺优选的主要指标为指标性成分含量及其转移率,但指标性成分含量不能直接反映中药复方的药效,纤维蛋白原平板法测定凝血活性的重复性好,准确性高,操作简单,直观,稳定,测定结果能有效反映中药复方的药效。
黄槐复方来源于明朝武之望的经典名著《济阴纲目》,临床主要用于泻火止血,妇女崩漏所致大出血。在预实验中,本研究将其与宫血宁胶囊等7 个上市品种的凝血功能进行了对比研究,研究结果表明黄槐浸膏的日用量的活性为8428 U,而已上市品种中最大的活性药品为断血流胶囊,其活性为7898 U,与本品活性8428 U相比,本方的活血功能较强,提示有较好的开发价值。由于本文研究对象为复方整体凝血活性,对于复方中具凝血活性的成分有待进一步研究。
在预实验中,黄芩苷、芦丁混合对照品显示出较好的凝血活性,呈现出较好的量效关系,表明可以以芦丁、黄芩苷的提取转移率为指标进行后续提取精制工艺研究。
本实验在单因素实验基础上,采用星点设计效应面法得出乙醇浓度、提取时间、溶剂用量3个因素对黄槐复方中黄酮类成分提取百分含量的效应趋势,优化了黄槐复方的提取工艺条件。从对本次实验数据所绘制的曲面图可以看出,提取时间对考察指标影响较大,而溶剂用量和乙醇浓度对考察指标的影响较小。对于此最优工艺实测评分值约为88,不及单因素考察中最优处方评分值高,可能存在着因素间的互相作用,另一方面,本文是在考虑了实际大生产过程中节约溶剂、时间、成本等因素,选择了此工艺。
在进行供试品溶剂考察研究中发现,分别用水和生理盐水溶解浸膏,得到的2种溶液性状均未见不溶物,而空白试验表明,2种溶剂均未有沉淀圈,其面积相差较大的原因,有待进一步研究,另外,需要考虑影响实验结果的因素,包括避免高温使酶失活等相关降低酶活性的因素,兼顾各种溶液混合顺序、试液的配制操作、点样浓度等。经过预试验确定本文中纤维蛋白原测定的各种参数,结果表明该方法稳定,重复性较强,提示体外活性评价法可作为黄槐复方提取工艺参数优选的指标。
经查阅大量文献,发现对黄槐复方止血功效的研究报道较少,本研究基于纤维蛋白原平板法,建立了测定中药复方中间体的凝血活性的方法,弥补了中药复方提取工艺优选中筛选指标的不足,是一种易于推广的实验方法,能为以后筛选中药生产工艺路线提供参考。
[参考文献]
[1]Enakpene C, Morhasonbello I, Enakpene E, et al Oral misoprostol for the prevention of primary postpartum hemorrhage during third stage of labor[J] J Obstet Gynaecol Res, 2007,33(6): 810
[2]武之望济阴纲目 [M] 北京:人民卫生出版社, 2006
[3]中国药典 一部[S] 2015: 302
[4]廖共山, 班建东 一种外检测凝血酶、类凝血酶的新方法——纤维蛋白原平板法[J] 广西医科大学学报, 2008, 25(6): 967
[5]董培智, 朴晋华, 党爱华, 等 量反应平行线法在溶栓胶囊蚓激酶效价测定方法学研究中的应用[J] 中国中药杂志, 2010, 35(11): 1410
[6]刘涛, 苟小军, 万德光, 等 基于“中药成分临床利用率”的中药材药用品质评价模式的商建[J] 中草药, 2015, 46(13): 1863
[7]严冬慧,邓仙梅,孟江,等星点设计效应面法优化炒茺蔚子炮制工艺[J].中国实验方剂学杂志,2016,22(21):10
[8]王倩倩, 王锦玉, 马振山, 等 星点设计效应面法优化解毒通络颗粒的提取工艺[J] 中国实验方剂学杂志, 2014, 20(9): 15
[9]黄元红, 卫天喜, 张发生, 等 星点设计效应面法优选丹参提取工艺[J] 中国实验方剂学杂志, 2010, 16(17): 28
[10]周洪伟,郝丽静,杨勇,等星点设计效应面法优化玄参提取工艺[J]世界中医药,2012,7(5):455
[11]李媛, 张龙, 崔荣辉, 等 星点设计效应面法优选小儿健脾膏的提取工艺[J] 中国实验方剂学杂志, 2014, 20(7): 37
[责任编辑孔晶晶]
[收稿日期]20160907
[基金项目]四川省千人计划项目(2013332)
[通信作者]*刘涛,研究员级高级工程师,研究方向为中成药质量再评价研究,Email:liutao0578@sinacom
[作者简介]李鹏程,硕士研究生, Email:sigualpc@sinacom
