银杏达莫注射液中总银杏酸HPLC检测法的建立及其含量分析
2017-03-19马海霞杨广安谭琪明何珺
马海霞,杨广安,谭琪明,何珺
银杏达莫注射液中总银杏酸HPLC检测法的建立及其含量分析
马海霞1,杨广安1,谭琪明1,何珺2
(1. 铜仁职业技术学院,贵州 铜仁 554300 ; 2. 贵州省生化工程中心,贵州 贵阳 550025)
采用高效液相色谱仪检测银杏达莫注射液中总银杏酸,建立了检查方法并对含量进行了分析。通过对白果新酸(C13∶0)在11.0~88.0 μg·mL-1呈良好线性关系,回归方程为:= 8558.8+ 8.5854(2=0.999 8),平均添加回收率为103.02%(RSD=0.72%),精密度的RSD为0.89%,稳定性的RSD为1.09%,银杏达莫注射液中银杏酸的最低检出量为2.2 ng·mL-1,银杏达莫注射液中未检测到总银杏酸,表明样品符合银杏达莫注射液质量标准。所建立的以白果新酸为标准品测定总银杏酸的HPLC法具有较好的精密度和重现性,可用于银杏达莫注射液的质量控制,为银杏达莫注射液现行质量标准的提高提供可靠的理论依据。
HPLC;银杏达莫注射液;总银杏酸;白果新酸
银杏达莫注射液由银杏叶提取物和双嘧达莫制备而成的中药复方剂,因含有较高的总黄酮醇苷、萜类内酯等,具有降血糖、软化血管及抗氧化、增强免疫等功效[1],临床上主要用于抗血小板聚集、预防和治疗动脉硬化及高血压引起的冠状动脉供血不足、心绞痛、心肌梗塞等疾病,是心脑血管及外周循环障碍的有效治疗药[2]。但相关研究证实了该类制剂具有致敏性、免疫毒性、细胞毒性等不良反应[3-5],孙锴[6]等研究表明银杏酸可呈剂量依赖性地抑制肝细胞线粒体活力,造成肝损伤。其原因主要与EGb中残留的银杏酸有关,因此在制剂中必须限定其含量。
银杏达莫注射液中黄酮类和萜类内酯含量测定报道居多[7-8],然而对银杏酸的分析方法报道很少。如李兰崇[9]等使用HPLC法检测考察银杏叶片、银杏茶及银杏胶囊中银杏酸的含量;杜小伟[10]等使用HPLC对舒血宁注射液中总银杏酸做了限量检查。目前,笔者未见对银杏达莫注射液中银杏酸含量测定的文献报道。本文以白果新酸(C13∶0)作为标准品对银杏达莫注射液中银杏酸含量测定,为银杏达莫注射液质量标准的提高提供可靠的依据。
1 实验部分
1.1 实验试剂和仪器
银杏达莫注射液,山西普德药业股份有限公司提供。标准品:白果新酸(C13∶0)(批号: 111690-200702,中国药品生物制品检定所)。银杏总酸试剂: (批号: 111594-200603 ,中国药品生物制品检定所);甲醇(色谱纯,天津市科密欧化学试剂有限公司);磷酸(分析纯,贵阳高新技术开发区华通化学试剂厂);其他试剂均为分析纯。分析型HPLC:(1100 series) Agilent Technology,U.S; C18高效液相色谱柱(大连依利特分析仪器有限公司);BSA124S电子天平(赛多利斯科学仪器(北京)有限公司);RE-52A旋转蒸发仪(上海亚荣生化仪器厂);SHB-Ⅲ循环水式多用真空泵(郑州长城科工贸有限公司);SG2200HE超声波清洗器(上海冠特超声仪器公司);其他为一般常规仪器。
1.2 实验方法
1.2.1 色谱条件
色谱柱:Hypersil ODS-2 C18(4.6×150 mm);流动相:甲醇-0.4%磷酸溶液(85∶15);流速:1.0 mL·min-1;检测波长:310 nm;柱温:(45±0.1)℃。
1.2.2 溶液的制备
标准品溶液制备:精密称取标准品白果新酸适量,加甲醇制成每1 mL含88 μg的溶液,作为标准品储备液。另取总银杏酸标准品适量,加甲醇制成每1 mL含20 μg的溶液,作定位用定位标准品溶液。
样品溶液制备:取50 mL银杏达莫注射液,混匀,浓缩至4 mL左右,加甲醇定容至5 mL,作为样品溶液。
阴性样品样液制备:按处方称取双嘧达莫和丙二醇,按样品溶液制备,作阴性样液。
1.2.3 系统适用性试验
精密量取标准品溶液2.5 mL置5 mL量瓶中,用甲醇定容至刻度,摇匀,作为标准品溶液。分别取标准品溶液、样品溶液和阴性样品样液进行HPLC分析,记录色谱图。
1.2.4 线性关系考察
精密量取白果新酸标准品溶液1.25,2.5,5.0,6.6 mL分别置于10 mL量瓶中,用甲醇定容至刻度,摇匀,配制成标准品溶液,在HPLC上进样分析并记录色谱图。
1.2.5 检测限
以白果新酸测定检测限,采用测量基线噪声的色谱条件、测量基线噪声。
1.2.6 精密度试验
直接取标准品溶液20 μL重复进样分析5次,记录色谱图。
1.2.7 稳定性试验
直接取标准品溶液20 μL分别在0,2,4,8,12,24 h,记录峰面积。
1.2.8 重复性试验
取08140920、08140921、081409样品22批样品,按1.2.2项制备3份样液,分别平行6份, 每次进样20 μL,记录峰面积。
1.2.9 添加回收试验
取5瓶10 mL装银杏达莫注射液,混匀,分别加入标准品,按溶液制备项下方法操作,制成样品溶液。将上述溶液在液相色谱仪上测定2次,计算加样回收率,重复试验3次。
1.2.10 样品含量测定
取3批银杏达莫注射液样品,按1.2.2项下制备样品溶液进样20 μL测定,采用外标法,以白果新酸为标准品,计算总银杏酸的含量。
2 结果与分析
2.1 系统适用性试验
分别取标准品溶液、样品溶液和阴性样品样液进行HPLC分析,记录色谱图如图1所示。样液、阴性样品谱图(如图3、图4所示)中在上述组分的峰位处均无干扰峰出现。
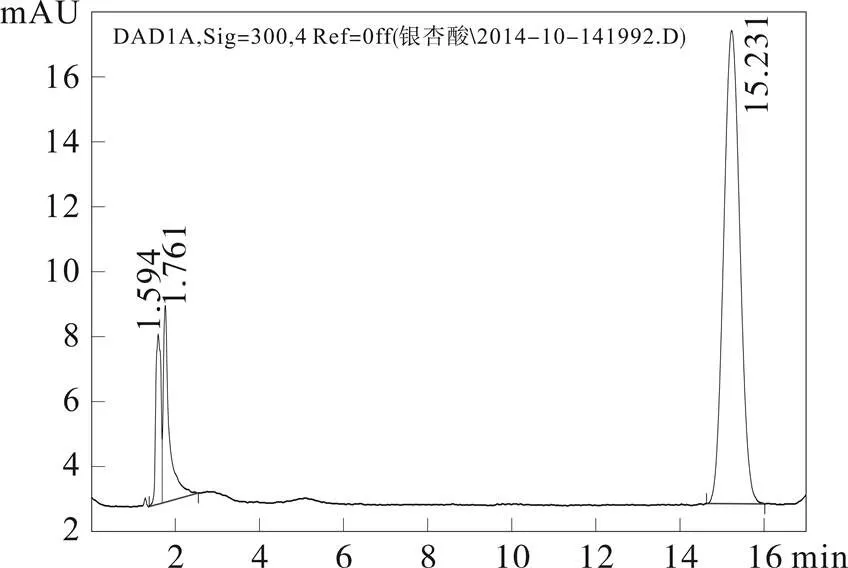
图1 白果新酸标准品HPLC图谱

图2 总银杏酸标准品HPLC图谱
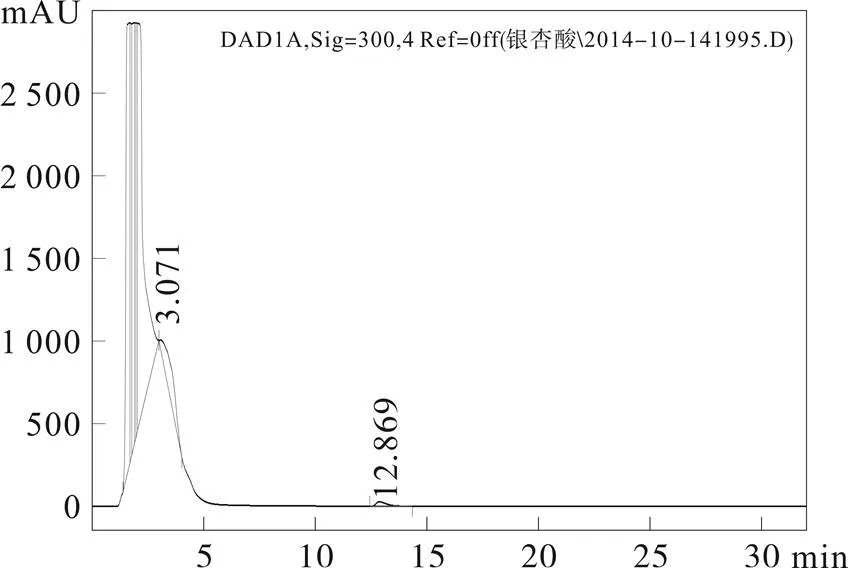
图3 银杏达莫样品HPLC图谱
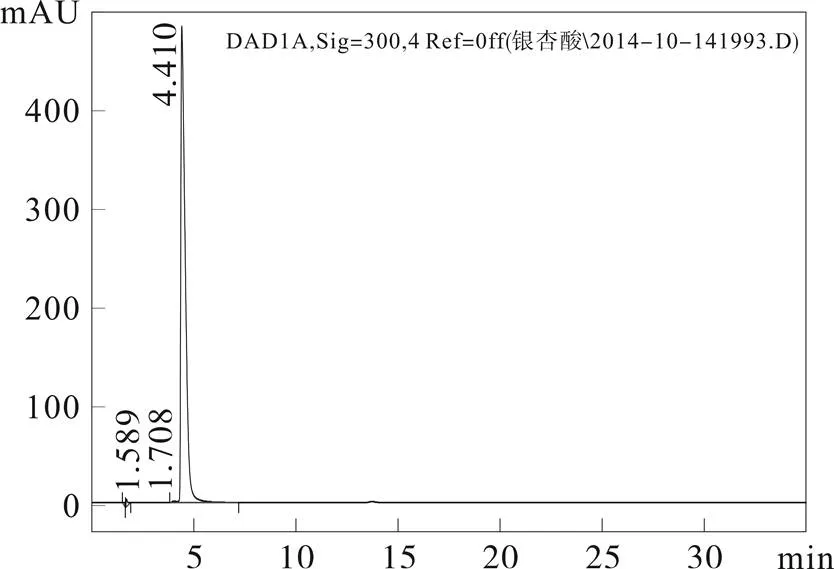
图4 银杏达莫阴性对照(双嘧达莫)HPLC图谱
2.2 检测限
以白果新酸测定检测限。结果检测限(信噪比S/N=3):检出浓度为1.1×10-2mg·mL-1,折算成银杏达莫注射液的最低检出量为2.2 ng·mL-1。
2.3 线性关系考察
以白果新酸标准品的质量的对数值为横坐标,以峰面积的对数值为纵坐标,进行回归分析。回归方程分别为:= 8 558.8+ 8.585 4(2=0.999 8)。线性范围11.0~88.0 μg·mL-1,见表1。
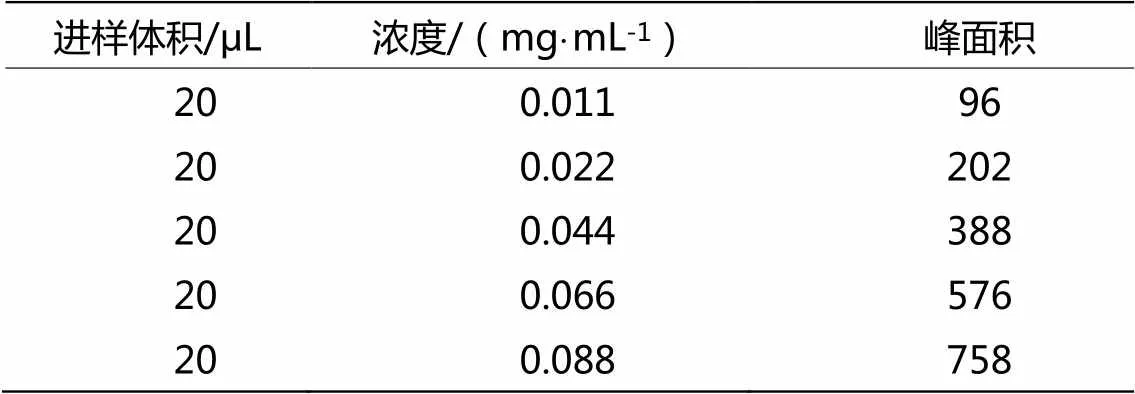
表1 线性关系考察
2.4 精密度试验
直接取标准品溶液重复进样分析5次,记录色谱图。测得白果新酸的峰面积的RSD为0.89%,表明进样精密度很好,结果见表2。

表2 精密度实验(n=5)
2.5 稳定性试验
直接取标准品溶液分别在0、2、4、8、12、24 h记录峰面积。表明溶液在24 h内稳定,测得白果新酸的峰面积的RSD为1.09%,实验结果见表3。

表3 稳定性实验
2.6 重复性试验
取08140920批样品,按1.2.2项制备样液,分别平行6份,进样20 μL,结果均未检出银杏酸。
2.7 添加回收试验
取5瓶10 mL装银杏达莫注射液,混匀,按表1所示量分别加入标准品,照样品溶液制备项下方法操作,制成样品溶液。将上述溶液在液相色谱仪上测定2次,计算加样回收率,重复试验3次。结果白果新酸回收率为103.02%(RSD=0.72%)见表4。

表4 回收实验结果(n=3)
2.8 样品含量测定
取3批银杏达莫注射液样品,按1.2.2项下制备样品溶液进样20 μL测定,采用内标法,以白果新酸为标准品,计算总银杏酸的含量。结果均未检测出银杏酸,见图3。结果表明,该批次银杏达莫注射液为检测出总银杏酸,符合其产品要求质量标准。
3 讨 论
本实验中采用样液浓缩直接进样方法,减少了有机试剂的使用,操作更加方便、有效,安全性更高。但由于样品易起泡,因此在真空浓缩时要加入少量的无水乙醇,能有效地去泡。
银杏达莫注射液的质量标准规定每1 mL含总银杏酸不得超过10 ng。以白果新酸测定检测限,结果检测限(信噪比S/N=3):检出浓度为1.1×10-2mg·mL-1,折算成银杏达莫注射液的最低检出量为2.2 ng·mL-1,因此采用所建立HPLC法检测银杏达莫注射液均未检测出银杏酸,表明样品中银杏酸符合质量要求,该方法具有一定的可行性。
4 结 论
所建立的以白果新酸为标准品测定总银杏酸的HPLC法具有较好的精密度和重现性,可用于银杏达莫注射液中有害杂质银杏酸的质量控制,为银杏达莫注射液现行质量标准的提高提供可靠的理论依据。
[1] 赵艳平.银杏叶提取物的药理研究状态综述[J].中国医药指南,2010, 8(3):44.
[2] 宾驰.银杏达莫注射液的药理作用及临床应用研究进展[J].中国药业杂志,2010,19(14):81.
[3] 韦丽华,李懿.银杏叶制剂的药理作用及不良反应[J].海峡药学,2007 (7):101-103
[4] Baron-Ruppert G, Luepke N P. Evidence for toxic effects of alkylphenols from Ginkgo biloba inthehen seggtest [J]. Phytomedicine, 2001, 8 (2):133.
[5] 杨小明,陈钧.烷基酚酸的生物活性研究进展[J].中草药,2003, 34(5):5.
[6] 孙锴,潘小海,黄诗颖,等.银杏酸对大鼠肝脏线粒体的损伤作用[J].中国药理通讯,2009,26(2):56.
[7] 杨青波,靳凤云,陈伟,等. 银杏达莫注射液中黄酮类和萜类内酯7种成分的含量测定[J]. 中草药,2014, 45(22):3279.
[8] 毕雨萌,孙国祥,于秀明. HPLC-ELSD法测定银杏达莫注射液中萜类内酯的含量[J]. 中南药学,2007 (2):124-127 .
[9] 李兰崇,尹志芳,杨宇强,等.几种银杏类制剂中银杏酸的高效液相色谱法测定[J].中国实用医药,2015,10(1):233.
[10] 杜小伟,王京辉,王萌萌,等.舒血宁注射液中总银杏酸的HPLC法限量检查[J].药物分析杂志,2009,29(1):170.
Establishment of HPLC Method for Determination of Total Ginkgolic Acid in Ginkgo Biloba Injection and Its Content Analysis
1,1,1,2
(1. Tongren Polytechnic College, Guizhou Tongren 554300, China;2. Research Center of Biochemistry Engineering of Guizhou Province, Guizhou Guiyang 550025, China)
The total ginkgolic acid in ginkgo biloba injection was detected by high performance liquid chromatography (HPLC), and the determination method and ginkgolic acid content were analyzed. The regression equation was Y = 8558.8X + 8.5854 (R2= 0.9998), and the average recovery was 103.02% (RSD = 0.9998), and the precision RSD was 0.89%, the stability RSD was 1.09%, and the lowest detection rate of ginkgolic acid was 2.2 ng·mL-1in Ginkgo biloba.No total ginkgolic acid was detected, indicating that the sample meets the quality standards of Ginkgo biloba injection. The HPLC method for the determination of total ginkgolic acid by using ginkgo acid as the standard has good precision and reproducibility, so it can be used for the quality control of ginkgo dipyridamole injection.
total ginkgolic acid; ginkgolic acid(C13∶0); ginkgo leaf extract and dipyidamole injection; HPLC
2017-09-20
马海霞(1989-),女,讲师,硕士研究生,山东省菏泽市人,2016年毕业于贵州大学学校药物化学专业,研究方向:天然药物分析。
O 657
A
1004-0935(2017)12-1229-04
