4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的合成与表征
2017-03-14周贤陈川靳佐雄叶辉沈杰
周贤,陈川,靳佐雄,叶辉,沈杰
(1.黄冈师范学院化工学院,催化材料制备及应用湖北省重点实验室,湖北 黄冈 438000;2.南开大学药学院,天津 300071)
4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的合成与表征
周贤1,陈川1,靳佐雄1,叶辉1,沈杰2
(1.黄冈师范学院化工学院,催化材料制备及应用湖北省重点实验室,湖北 黄冈 438000;
2.南开大学药学院,天津 300071)
糖苷酶抑制剂因其独特的体内作用机制而广受关注.以1,2,3,4,6-五-O-乙酰基-α-D-半乳糖为原料,通过溴代、叠氮化,与3-丁烯-1-醇发生Click反应得到化合物4,再经叠氮化反应、水解反应、催化氢化反应,得到目标化合物4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑.采用核磁共振谱(1H NMR、13C NMR、DEPT 135)、高分辨质谱等对目标化合物进行了结构表征,确证了结构,为后续合成更多的新型糖苷酶抑制剂提供了重要前体.
半乳糖;三唑;糖苷酶抑制剂;合成;表征
0 引言
糖苷酶抑制剂是一类含氮的拟糖物,从结构上分为两大类.第一类氮原子在糖环上,也叫作氮杂糖类衍生物,如野尻霉素、半乳糖苷酶抑素、寡糖酶抑素等.第二类氮原子在糖环外,如α-葡萄糖苷酶抑制剂、半乳糖苷酶抑制剂、唾液酸抑制剂、淀粉酶抑制剂等.α-葡萄糖苷酶抑制剂是一类较成熟的治疗糖尿病的口服药物,主要包括阿卡波糖、伏格列波糖等[1-2].β-半乳糖苷酶抑制剂主要用于抑制β-半乳糖苷酶和其他糖苷酶.
目前高选择性的β-半乳糖苷酶抑制剂的研究相对较少,主要集中在含有单个氮原子的半乳糖的合成,而以三唑环代替单个氮原子的分子设计仅出现在氮杂糖类衍生物中[3-4].三唑环具有良好的理化特性,通过氢键、偶极-偶极作用、π-π堆叠作用,从而提高与酶的结合力.本文中通过Click反应引入三唑环,设计合成了一种新型的4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑抑制剂,并对其结构进行了表征,希望通过进一步的酶学实验,可得到更多的新型糖苷酶抑制剂.具体的合成路线[5-9]见图1,总共6步反应,总产率为20%.

图1 4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的合成路线
1 实验部分
1.1 试剂与仪器 仪器:Bruker 400 MHz型核磁共振仪;Varian 7.0 T FTMS高分辨质谱仪;Bruker Tensor 27 型红外光谱仪;SHZ-Ⅲ型循环水式真空泵(上海荣生化学仪器厂;恒温加热磁力搅拌器;AL-206型电子天平(上海,梅特勒-拖利多公司)、DZF-602 型真空干燥箱(上海精宏实验设备有限公司)、磁力搅拌器、旋转蒸发仪、氮气保护装置.
试剂:所有试剂均为市售,试剂纯度均为分析纯.THF经钠珠预干燥,加热回流至指示剂二苯甲酮呈蓝色后蒸出;DCM、DMF、CH3OH经4A分子筛干燥备用.
1.2 化合物2的合成 将1,2,3,4,6-五-O-乙酰基-α-D-半乳糖(13.5 g, 34.69 mmol)溶于无水二氯甲烷(200 mL),氮气置换,冷却至0 ℃,加入溴化氢的乙酸溶液(25.0 mL, 142.75 mmol),反应1 h后,升至室温反应1 h.TLC监测原料反应完全,依次用冰水、饱和碳酸氢钠溶液、饱和食盐水洗涤,无水硫酸钠干燥,减压浓缩,得到无色油状液体13.1 g,产率91.8%.




1.7 化合物7的合成 化合物6(190 mg, 0.61 mmol) 溶于甲醇,加入Pd/C(10%, 19 mg),氢气置换后并插上氢气球,室温搅拌3 h.TLC监测反应完全后,硅藻土过滤,滤液减压浓缩,得到无色糖浆120 mg,产率73.8%.1H NMR(400 MHz, CD3OD-d4):δ为8.06 (s, 1 H),5.55(d,1 H,J=9.2 Hz),4.15 (t, 1 H,J=9.2 Hz), 3.99 (d, 1 H,J=3.2 Hz), 3.85 (t, 1 H,J=6.0 Hz), 3.77-3.30 (m, 3 H), 3.01 (t, 1 H,J=6.8 Hz), 2.91 (t, 1 H,J=6.8 Hz);13C NMR (100 MHz, CD3OD-d4):δ为146.3, 122.6, 90.1, 79.8, 75.1, 71.4, 70.3,62.3,48.9,41.7,28.5;HRMS(ESI):calcd for[C10H18N4O5+H]+m/z275.135 5, foundm/z275.134 8.
2 结果与讨论


图2 4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的1H NMR图谱


图3 4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的13C NMR图谱
2.3 DEPT 135谱图 图4为目标产物在 CD3OD-d4中的DEPT 135图谱.其中,62.4、42.1、29.6等3处共振信号的出峰方向与其他位移刚好相反,表明这3个共振信号代表结构式中亚甲基的共振信号.
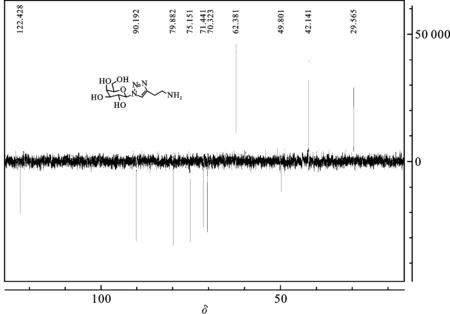
图4 4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的DEPT 135图谱
2.4 高分辨质谱图 图5为目标产物的高分辨质谱图,在m/z=275.134 8处为目标化合物的分子离子峰,且强度最高,与计算值275.135 5相符,进一步证实了目标化合物的结构.

图5 4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的高分辨质谱图
通过核磁共振谱(1H NMR、13C NMR、DEPT 135)、高分辨质谱等对4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑的结构进行了表征,图谱分析结果表明,能够确证该化合物的结构与结构式相符.
3 结论
本文中以2-乙酰氨基-2-脱氧-D-葡萄糖为原料,通过溴代、叠氮化,与3-丁烯-1-醇发生Click反应得到化合物4,再经叠氮化反应、水解反应、催化氢化反应,得到目标化合物4-氨基乙基-1-(β-D-半乳糖基)-1,2,3-三唑.采用核磁共振谱(1H NMR、13C NMR、DEPT 135)、高分辨质谱等对目标化合物进行了结构表征,确证了结构,为后续合成糖苷酶抑制剂提供了基础.三唑环具有良好的理化特性,通过氢键、偶极-偶极作用、π-π堆叠作用增强结合能力,而糖基部分竞争性的结合酶的活性部位,氨基可与多种基团结合,预计将获得多种新型糖苷酶抑制剂,可应用于药物研发及糖类化合物的分离材料等,具有广阔的应用前景.
[1] 李铁海,郭利娜,李中华,等.O-GlcNAcase抑制剂[J].化学进展, 2011, 23(8): 1657-1664.
[2] 于彩云,高兆兰,陈天姿,等.天然产物中α-葡萄糖苷酶抑制剂的研究进展[J].食品工业科技, 2015, 22: 394-399.
[3] Heightman T D, Vasella A T. Recent insights into inhibition, structure, and mechanism of configuration-retaining glycosidases[J].Angew Chem Int Ed, 1999, 38, 750-770.
[4] Gloster T M, Davies G J. Glycosidase inhibition: assessing mimicry of the transition state[J].Organic & Biomolecular Chemistry, 2010, 8: 305-320.
[5] Heidlas J E, Lees W J, Pale P, et al. Gram-scale synthesis of uridine 5′-diphospho-N-acetylglucosamine: comparison of enzymic and chemical routes[J].The Journal of Organic Chemistry, 1992, 57: 146-151.
[6] Branderhorst H M, Liskamp R M, Visser G M, et al. Strong inhibition of cholera toxin binding by galactose dendrimers[J].Chemical Communications, 2007: 5043-5045.
[7] Cagnoni A J, Varela O, Gouin S G, et al. Synthesis of multivalent glycoclusters from 1-thio-β-D-galactose and their inhibitory activity against theβ-galactosidase from E.coli[J].The Journal of Organic Chemistry, 2011, 76: 3064-3077.
[8] Li T, Guo L, Zhang Y, et al. Design and synthesis of O-GlcNAcase inhibitors via ‘click chemistry’and biological evaluations[J].Carbohydrate Research, 2011, 346: 1083-1092.
[9] Mitchell S A, Pratt M R, Hruby V J, et al. Solid-phase synthesis of O-linked glycopeptide analogues of enkephalin[J].The Journal of Organic Chemistry, 2001, 66: 2327-2342.
(责任编辑 胡小洋)
Synthesis and characterization of 4-aminoethyl-1-(β-D-galactopyranosyl)-1,2,3-triazole
ZHOU Xian1,CHEN Chuan1,JIN Zuoxiong1,YE Hui1,SHEN Jie2
(1.Hubei Key Laboratory for Processing and Application of Catalytic Materials,
College of Chemical Engineering, Huanggang Normal University, Huanggang 438000, China;
2.College of Pharmacy, Nankai University, Tianjin 300071, China)
Glycosidase inhibitors have been attracted growing interests owing to their unique mechanism of action in vivo. By bromination, azido reaction with 1,2,3,4,6-penta-O-acetyl-α-D-galactopyranose and click reaction, compound 4 was obtained and furthered reacted with azide, hydrolysis reaction, and catalytic hydrogenation, the title compound 4-aminoethyl-1-(β-D-galactopyranosyl)-1,2,3-triazole was synthesized. The structure of the title compound was characterized and confirmed by (1H,13C)NMR, DEPT 135, HRMS. It provided a new precursor for synthesis of more neo-glycosidase inhibitors in the further step.
galactose; triazole; glycosidase inhibitors; synthesis; characterization
2016-05-10
湖北省科技支撑计划项目(2015CFC818)和大学生创新创业训练计划项目(201510514030)资助
周贤(1995-),女,本科生;叶辉,通信作者,讲师,E-mail:huiye_81@163.com
1000-2375(2017)02-0161-05
O629.1;O621.3
A
10.3969/j.issn.1000-2375.2017.02.011
