飞燕草素联合3-MA增敏抗HER-2阳性乳腺癌细胞效应
2017-03-08陈静瑶朱彦锋余小平
陈静瑶,周 杰,韩 彬,李 飞,朱彦锋,余小平
(成都医学院公共卫生系,四川成都 610500)
飞燕草素联合3-MA增敏抗HER-2阳性乳腺癌细胞效应
陈静瑶,周 杰,韩 彬,李 飞,朱彦锋,余小平*
(成都医学院公共卫生系,四川成都 610500)
目的:研究飞燕草素(delphinidin,Dp)联合自噬抑制剂3-甲基腺嘌呤(3-Methyladnine,3-MA)对HER-2+乳腺癌细胞MDA-MB-453的抑制效应。方法:用不同浓度飞燕草素处理MDA-MB-453细胞,CCK-8检测细胞增殖情况;荧光斑点实验和Weston Blot实验检测飞燕草素对细胞自噬的诱导情况;Weston Blot实验检测3-MA对自噬的抑制状况,CCK-8检测飞燕草素联合3-MA对细胞增殖状况的影响。结果:飞燕草素能有效抑制MDA-MB-453细胞增殖,诱导MDA-MB-453细胞自噬并呈剂量依赖效应;3-MA有效抑制MDA-MB-453细胞自噬,同时增强自噬飞燕草素抗HER-2+乳腺癌细胞MDA-MB-453增殖效应。结论:飞燕草素联合自噬抑制剂3-MA,能促进飞燕草素抗HER-2+乳腺癌细胞MDA-MB-453增殖。
飞燕草素,乳腺癌,自噬,增敏
乳腺癌是全球第二大最常见肿瘤,其发病率位于女性肿瘤之首,直至2012年,全球每年有167万女性新增病例,占所有肿瘤的25%[1]。HER-2受体阳性型乳腺癌占乳腺肿瘤的25%~30%[2],预后不佳。因此,积极开发HER-2受体靶向治疗药物对HER-2+乳腺癌的治疗至关重要。目前乳腺癌的常规治疗方案表现出明显的毒副作用,严重影响患者生存质量[3-4]。膳食类植物含有的化学物质在膳食中广泛存在,易获得,毒副作用低,对乳腺癌的预防和辅助治疗能发挥积极作用[5]。
近年来黄酮类化合物花青素的抗癌作用受到关注,发现其能发挥除抗氧化作用外的抗增殖和转移效应[6]。然而,花青素抗HER-2+乳腺癌的机制仍有不明确的部分,飞燕草素作为花青素六种主要单体化合物之一,在花青素中丰度较高,活性较强[7],被认为抗癌疗效优于其他花青素单体而成为本次研究的对象。
自噬是一种进化保留过程,在抗癌作用中表现出双刃剑作用,其中,当细胞处于恶性微环境如饥饿或代谢应激压力时,能介导细胞内长寿蛋白转化,消除损伤或多余的细胞器,维持细胞代谢平衡,发挥保护癌细胞效应[8-9]。近年来研究多显示,抑制自噬的保护效应对增敏化疗抗癌作用至关重要[10-11],因此,本文将探讨飞燕草素在抑制HER-2+乳腺癌细胞MDA-MB-453增殖的同时是否诱导保护性自噬,以及抑制自噬能否增敏飞燕草素抗HER-2+乳腺癌效应。
1 材料与方法
1.1 材料与仪器
人乳腺癌细胞MDA-MB-453 HER-2+中国科学院上海细胞库;飞燕草素(纯度≥95%)、3-Methyladnine(M9281) 美国Sigma公司;L-15培养基、转染液OPTI-MEM 美国Gibco公司;胎牛血清 美国Millipore公司;质粒提取试剂盒 德国QIAGEN公司;CCK-8 日本Dojindo公司;pEX-GFP-hLC3WT荧光质粒 上海交通大学;Lipofectamine2000 美国Invitrogen公司;BCA蛋白定量试剂盒 美国Thermo公司;LC3-I/II(2775) 美国Cell Signaling Technology公司;ATG5(ab78073) 英国Abcam公司。
IX71型倒置荧光相差显微镜 日本OLYMPUS公司;台式高速冷冻离心机、ND-2000型微量紫外可见光分光光度计 美国Thermo公司;化学发光凝胶成像仪、Weston blot及转膜设备 美国Bio-Rad公司;酶标仪 美国BioTek公司。
1.2 实验方法
1.2.1 细胞培养 MDA-MB-453细胞用含有10%胎牛血清的L-15培养基于细胞培养箱37 ℃,5%CO2条件培养,每48 h换液,选对数生长期细胞实验。
1.2.2 CCK-8检测细胞增殖抑制 将对数期细胞用胰酶消化后制成细胞悬液。将细胞稀释至8×104个/mL,接种于96孔板,24 h后,加入飞燕草素。设计0、1.25、2.5、5、10、20、40、80、160、200 μmol/L十个浓度,每个浓度3个复孔。DMSO作为溶剂对照。飞燕草素作用48 h后,吸弃原培养基,加入含10% CCK-8的新培养基100 μL/孔,37 ℃孵育2 h,于酶标仪450 nm波长下检测吸光度即OD值。计算药物细胞存活率及IC50值。存活率=(实验组OD值-空白组OD值)/(对照组OD值-空白组OD值)。用SPSS21.0软件回归法中的probit程序计算IC50值。
1.2.3 实验设计与分组 根据CCK-8实验结果,荧光斑点实验和自噬诱导鉴定实验分为,对照组:含DMSO的L-15培养基,实验组:以IC50值为基准,再左右各取一个浓度的飞燕草素处理细胞;自噬抑制实验,选择对细胞增殖抑制最强和自噬诱导能力最强的飞燕草素浓度作为实验剂量,分为对照组、飞燕草素处理组、自噬抑制组,鉴定使用3-MA后自噬是否被抑制,为下一步检测抑制自噬后细胞生长增殖能力做准备;使用抑制剂后的细胞生长增殖能力检测实验,分为对照组、3-MA处理组、飞燕草素处理组、3-MA和飞燕草素联合处理组。联合处理组先以5 mmol/L的3-MA预处理2.5 h后,再加入飞燕草素处理48 h,检测细胞增殖抑制情况。
1.2.4 荧光斑点实验检测细胞自噬水平 将细胞以2.5×104个/mL的密度接种于六孔板,24 h后,去除培养基后将配置好的转染试剂滴加到六孔板中,轻摇混匀,孵育24 h,观察细胞与脂质体融合状态,当细胞与脂质体融合度达70%~80%,吸出脂质体混合物,用培养基清洗细胞后分别以含DMSO的培养基为对照组,根据IC50值(40 μmol/L)选择浓度为20、40、80 μmol/L的飞燕草素为实验组处理细胞,48 h后观察细胞内荧光斑点数目。
1.2.5 蛋白分离和定量 将细胞用PBS清洗后加入200 μL细胞裂解液和蛋白酶抑制剂混合物,于冰上裂解30 min,收集细胞于EP管,低温高速离心(4 ℃ 1.6×104r/min,15 min),回收上清液,用BCA蛋白定量试剂盒测定蛋白浓度,在酶标仪450 nm波长下得出OD值,绘制标准曲线,回归系数>0.99方可定量检测蛋白浓度,根据标准品曲线计算待测样品蛋白浓度,根据蛋白浓度,按每孔50 μg总蛋白制备上样样品。
1.2.6 Weston Blot检测蛋白表达水平 将定量后的蛋白与4×样品缓冲液按比例混合,煮沸5 min后,将蛋白定量加于SDS-PAGE胶体孔中,加以80 V 30 min,120 V 1 h电压进行蛋白分离;再将蛋白转移致PVDF膜(200 mA,2 h),之后用5% BSA溶液于37 ℃封闭1 h后直接加入相应蛋白抗体,4 ℃孵育过夜。TBST清洗(3×10 min)后加入HRP-共轭二次抗体,37 ℃孵育2 h,再以TBST 清洗(3×10 min),最后用ECL化学发光底物显色。
1.2.7 数据处理 实验数据用均数±标准差(±s)表示,采用SPSS 21.0软件进行单因素方差分析(one-way ANOVA),组间比较采用Dunnett-t检验,p值设为0.05。
2 结果与分析
2.1 飞燕草素有效抑制MDA-MB-453细胞增殖
飞燕草素是具有抗肿瘤特性的黄酮类植物化合物,能通过多种机制抑制不同的肿瘤细胞增殖。如飞燕草素通过抑制AKT/ERK1/2/AMPK信号通路抑制卵巢透明细胞癌,通过转染小RNA促进恶性胶质瘤死亡,通过调节凋亡相关的肿瘤坏死因子诱导配体抑制前列腺癌细胞等[12-14],并且还能通过抑制肿瘤细胞血管内皮生长因子,普遍抑制受该因子调节的肿瘤细胞的生长[15]。为探讨飞燕草素对HER-2+乳腺癌细胞增殖的影响机制,将检测飞燕草素是否影响HER-2+乳腺癌细胞增殖,以及影响程度与实验计量的关系。
以不同浓度的飞燕草素处理MDA-MB-453细胞,通过CCK-8实验检测飞燕草素对细胞生长抑制状况的影响。实验结果显示,飞燕草素能有效抑制MDA-MB-453乳腺癌细胞增殖,拟合绘制细胞存活率曲线(图1),计算得出IC50值约为40 μmol/L。以此为依据,选择20、40、80 μmol/L浓度的飞燕草素作为实验剂量,进行进一步实验。
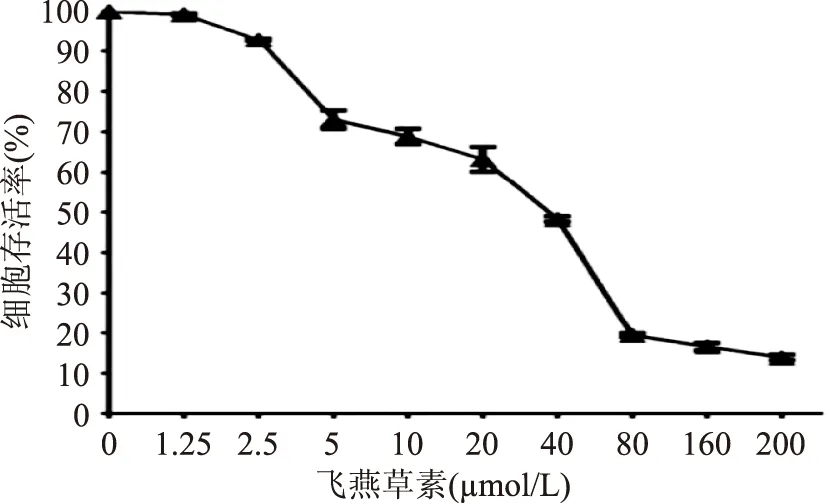
图1 飞燕草素对MDA-MB-453细胞存活率的影响Fig.1 The effect of delphinidinto MDA-MB-453 cell on viability
2.2 飞燕草素能诱导MDA-MB-453细胞自噬
为检测飞燕草素是否诱导MDA-MB-453细胞自噬,将GFP-LC3质粒转染入细胞分别用20、40、80 μmol/L浓度的飞燕草素刺激该细胞,检测细胞内自噬体的数量。实验结果显示,飞燕草素处理乳腺癌细胞后,细胞内荧光斑点数量增加,并存在剂量依赖效应(图2A)。20 μmol/L飞燕草素处理(图2b)后造成个别细胞呈现全亮绿色现象,这可能是由于荧光斑点过密且相互重叠造成。为进一步确认飞燕草素诱导乳腺癌细胞自噬,通过Weston Blot检测LC3蛋白在细胞内转化情况,实验结果发现,飞燕草素处理乳腺癌细胞MDA-MB-453导致细胞内LC3-I型蛋白转化为LC3-II型蛋白,并且,LC3-II型蛋白表达水平随飞燕草素浓度的增加而增加,LC3-I型蛋白表达逐渐减弱(图2B),呈现剂量依赖效应。同时,检测了调控自噬表达的关键蛋白ATG5。自噬的形成是通过一系列自噬相关基因协同作用产生,特别是当调节自噬体膜形成的关键基因Atg7被激活后,Atg7将激活自噬相关基因Atg12,Atg12又进一步激活Atg10,并最终与Atg5结合,形成自噬体前体细胞,为最终形成自噬体做准备。因此,ATG5蛋白作为Atg5基因的活性形式,是调节自噬体形成的关键蛋白的终末环节,若自噬相关基因Atg系列被激活将最终表现为ATG5蛋白表达增强。通过检测ATG5蛋白的表达情况说明飞燕草素诱导的自噬是受ATG5蛋白调控的结果,同时也验证自噬体的形成。实验结果发现,与对照组相比,ATG5蛋白随飞燕草素浓度的增加表达增强(图2C),说明飞燕草素通过ATG5调控自噬体的形成。
近年研究已表明自噬与肿瘤细胞的生长密切相关,诱发保护性自噬能促进肿瘤细胞的存活,诱发致死性自噬则加速细胞死亡,称自噬性细胞死亡。飞燕草素抑制乳腺癌细胞增殖同时诱发自噬,推测乳腺癌细胞的增殖抑制可能与自噬密切相关,因此,进一步研究了自噬与乳腺癌细胞生长增殖的关系。
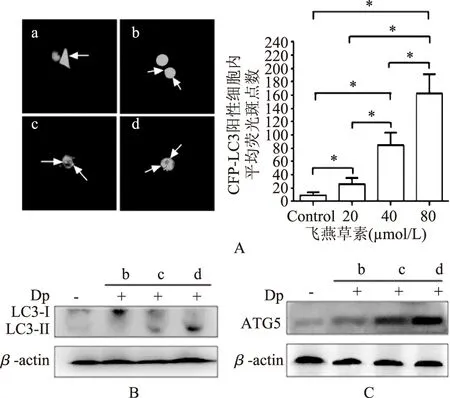
图2 飞燕草素能诱导MDA-MB-453乳腺癌细胞自噬Fig.2 Delphinidin induced autophagy in MDA-MB-453 cells注:A:MDA-MB-453细胞瞬时转染GFP-LC3荧光质粒后分别以DMSO(对照组)以及20、40、80 μmol/L(实验组)飞燕草素处理48 h;荧光斑点数的平均值来源于50次随机视野计数平均值,放大倍数为400×;B:免疫印迹发检测分别以DMSO(对照组)以及不同浓度的飞燕草素处理48 h后LC3-II/LC3-I蛋白的表达情况;C:免疫印迹发检测分别以DMSO(对照组)以及不同浓度的飞燕草素处理48 h后ATG5蛋白的表达情况;“-”:对照组;“+”:处理组;*p<0.05;a:DMSO;b:20 μmol/L;c:40 μmol/L;d:80 μmol/L。
2.3 3-MA抑制自噬促进HER-2+乳腺癌细胞死亡
保护性自噬的诱发与化疗耐药的产生息息相关,严重影响化疗药物疗效,如一型干扰素诱导抗乳腺癌细胞效应被自噬效应中和,当自噬被化学或基因沉默的方法抑制后方表现一型干扰素增敏效应[20];自噬抑制增加乳腺癌对激素药物他莫昔芬的敏感性[21];3-MA能增加HER-2单克隆抗体曲妥珠对HER-2 阳性乳腺癌的治疗作用[22]。由此可见,自噬抑制的增敏作用已成为乳腺癌治疗的有效措施。
实验发现,飞燕草素有效抑制癌细胞增殖的同时诱导了自噬,基于自噬的双刃剑作用,使用化学抑制剂3-MA抑制自噬,检测自噬对乳腺癌细胞增殖的影响。3-MA是自噬早期抑制剂,能通过抑制自噬体的成熟从而抑制自噬进程,导致LC3-II蛋白表达减少[16-17],根据前述的实验结果可知,80 μmol/L浓度的飞燕草素抑制细胞增殖和诱导细胞的自噬能力最强,因此选作实验剂量,并通过CCK-8实验检测自噬对细胞生长增殖的影响。
为确定3-MA对乳腺癌细胞的自噬抑制作用,通过荧光斑点实验和检测自噬标记蛋白LC3-II/LC3-I检测自噬抑制情况。实验结果表明,与飞燕草素单独处理组相比,3-MA与飞燕草素共处理组细胞内荧光斑点数目明显减少(图3A),LC3-II蛋白表达明显减弱,LC3-I蛋白表达明显增强(图3B)。说明3-MA有效抑制了飞燕草素诱导的MDA-MB-453细胞自噬。
为进一步检测抑制自噬后的细胞增殖状况,通CCK-8实验检测细胞存活率。结果显示,与对照组相比,3-MA处理组的细胞增殖情况未受到明显影响,与之相反,3-MA与飞燕草素联合处理组与飞燕草素单独处理组相比,细胞明显产生增殖抑制现象(图3C)。这说明抑制自噬能有效促MDA-MB-453细胞死亡,而自噬在飞燕草素抑制乳腺癌细胞增殖过程中可能产生了保护效应。目前已有研究显示,多种植物化学物质,如槲皮素、白花丹素、紫檀芪等均能诱导癌细胞产生保护性自噬,即抑制自噬能有效增敏化疗效应,促进肿瘤细胞死亡[18-19]。这对于开发飞燕草素等一系列低毒副作用的植物化学物质作为临床辅助用药治疗乳腺癌,减小耐药作用,提高患者生存质量具有积极意义。
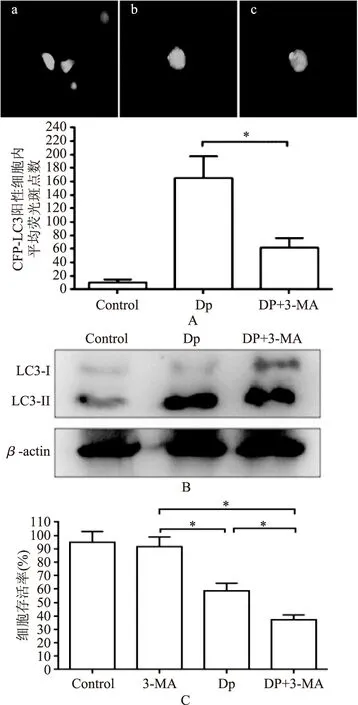
图3 3-MA抑制自噬促进MDA-MB-453细胞死亡Fig.3 3-MA promotes MDA-MB-453 cellsdeath by suppressing autophagy注:A:荧光斑点数的平均值来源于50次随机视野计数平均值,放大倍数为400×,a:DMSO;b:80 μmol/L飞燕草素;c:80 μmol/L飞燕草素+3-MA;B:免疫印迹发检测分别以DMSO(对照组)、80 μmol/L飞燕草素、80 μmol/L飞燕草素+3-MA处理48 h后LC3-II/LC3-I蛋白的表达情况;*p<0.05。
3 结论
综上所述,飞燕草素有效抑制HER-2+乳腺癌细胞增殖并诱导保护性自噬,抑制自噬,增敏飞燕草素抗HER-2+乳腺癌细胞效应。
[1]Ferlay J,Soerjomataram I,Ervik M,et al. GLOBOCAN 2012 v1.0,Cancer Incidence and Mortality Worldwide:IARC CancerBase No. 11. Lyon,France:International Agency for Research on Cancer;2013. Available from:http://globocan. iarc.fr. Accessed on 28 May 2014.
[2]Slamon DJ,Leyland-Jones B,Shak S,et al. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2[J]. N Engl J Med,2001,344:783-792.
[3]Guo S,Wong S. Cardiovascular toxicities from systemic breast cancer therapy[J].Front Oncol,2014(4):346.
[4]Duchnowska R,Biernat W,Szostakiewicz B,et al. Correlation between Quantitative HER-2 protein expression and risk for brain metastases in HER-2+advanced breast cancer patients receiving Trastuzumab-containing therapy[J]. Oncologist,2012,17:26-35.
[5]Pratheeshkumar P,Son YO,Korangath P,et al. Phytochemicals in cancer prevention and therapy[J]. Biomed Res Int,2015:324021.
[6]Chen XY,Zhou J,Luo LP,et al. Black rice anthocyanins suppress metasis of breast cancer cells by targeting RAS/RAF/MAPK pathway[J]. Biomed Res Int,2015:414250.
[7]罗丽萍,余小平,韩彬,等. 花青素主要成分与HER-2激酶区的分子对接[J].生物工程学报,2014,30(3):504-513.
[8]Lu J,Sun DP,Gao S,et al. Cyclovirobuxine D induces autophagy-associated cell death via the Akt/mTOR Pathway in MCF-7 human breast cancer cells[J]. J Pharmacol Sci,2014,125(1):74-82.
[9]Shi YM,Yang L,Geng YD,et al. Polyphyllin I induced-apoptosis is enhanced by inhibition of autophagy in human hepatocellular carcinoma cells[J]. Phytomedicine,2015,22(13):1139-1149.
[10]Rodríguez CE,Reidel SI,Bal de Kier Joffé ED,et al. Autophagy protects from trastuzumab-induced cytotoxicity in HER2 overexpressing breast tumor spheroids[J]. PLoS One,2015,10(9):e0137920.
[11]Brigger D,Schläfli AM,Garattini E,et al. Activation of RARαinduces autophagy in SKBR3 breast cancer cells and depletion of key autophagy genes enhances ATRA toxicity[J]. Cell Death Dis,2015(6):e1861.
[12]Ko H,Jeong MH,Jeon H,et al. Delphinidin sensitizes prostate cancer cells to TRAIL-induced apoptosis,by inducing DR5 and causing caspase-mediated HDAC3 cleavage[J]. Oncotarget,2015,6(12):9970-9984.
[13]Lim W,Jeong W,Song G.Delphinidin suppresses proliferation and migration of human ovarian clear cell carcinoma cells through blocking AKT and ERK1/2 MAPK signaling pathways[J]. Mol Cell Endocrinol,2016,15(422):172-181.
[14]Chakrabarti M,Ray SK. Direct transfection of miR-137 mimics is more effective than DNA demethylation of miR-137promoter to augment anti-tumor mechanisms of delphinidin in human glioblastoma U87MG and LN18 cells[J]. Gene,2015,573(1):141-152.
[15]Keravis T,Favot L,Abusnina AA,et al. Delphinidin Inhibits Tumor Growth by Acting on VEGF Signalling in Endothelial Cells[J]. PLoS One,2015,10(12):e0145291.
[16]Wu YT,Tan HL,Shui G,et al. Dual role of 3-methyladenine in modulation of autophagy via different temporal patterns of inhibition on class I and III phosphoinositide 3-kinase[J]. J Biol Chem,2010,285(14):10850-10861.
[17]Levine B,Kroemer G. Autophagy in the pathogenesis of disease[J]. Cell,2008,132(1):27-42.
[18]Chen WC,Hsu KY,Hung CM,et al. The anti-tumor efficiency of pterostilbene is promoted with a combined treatment of Fas signaling or autophagy inhibitors in triple negative breast cancer cells[J]. Food Funct,2014,5(8):1856-1865.
[19]Yan-Cong Li,Shu-Ming He,Zhi-Xu He,et al. Plumbagin induces apoptotic and autophagic cell death through inhibition of the PI3K/Akt/mTOR pathway in human non-small cell lung cancer cells[J]. Cancer Lett,2014,344(2):239-259.
[20]Ambjørn M,Ejlerskov P,Liu Y,et al. IFNB1/interferon-β-induced autophagy in MCF-7 breast cancer cells counteracts its proapoptotic function[J]. Autophagy,2013,9(3):287-302.
[21]Amaral C,Varela C,Azevedo M,et al. Effects of steroidal aromatase inhibitors on sensitive and resistant breast cancer cells:aromataseinhibition and autophagy[J]. J Steroid Biochem Mol Biol,2013,135:51-59.
[22]Lozy F,Cai-McRae X,Teplova I,et al. ERBB2 overexpression suppresses stress-induced autophagy and renders ERBB2-induced mammary tumorigenesis independent of monoallelicloss[J]. Autophagy,2014,30,10(4):662-676.
Delphinidin sensitizes anti-tumor effect to HER-2+breast cancer cells by combining with 3-MA
CHEN Jing-yao,ZHOU Jie,HAN Bin,LI Fei,ZHU Yan-feng,YU Xiao-ping*
(Department of Public Health,Chengdu Medical College,Chengdu 610500,China)
Objective:To research the effect of delphinidin(Dp)combines with 3-Methyladnine(3-MA),inhibitor of autophagy,to HER(human epidermal growth factor receptor-2,HER-2)positive breast cancer cell MDA-MB-453. Methods:HER-2+breast cancer cells MDA-MB-453 were treated by Dp. Proliferation of MDA-MB-453 cells was detected by CCK-8. Fluorescence dot assay and Weston Blot were used to identify autophagy in breast cancer cells. Weston blot was used to assay condition of autophagy inhibition of 3-MA to MDA-MB-453 cell and CCK-8 tests combination effect of Dp and 3-MA to MDA-MB-453 cell. Results:Dp suppressed proliferation effectively and induced autophagy in dose-dependent manner in MDA-MB-453 cells. However,3-MA could restrain the autophagy,which sensitized anti-proliferation of Dp to MDA-MB-453 cell. Conclusion:Combination of Dp and 3-MA which suppresses autophagy can sensitize anti-proliferation effect of HER-2+breast cancer cell MDA-MB-453.
delphinidin;breast cancer;autophagy;sensibilization
2016-07-18
陈静瑶(1988-),女,在读硕士研究生,研究方向:植物化学物抗肿瘤分子机制,E-mail:cdyxucjy@sina.com。
*通讯作者:余小平(1970-),男,博士,教授,研究方向:植物化学物抗肿瘤分子机制,E-mail:cyggwsyxp@sina.com。
国家自然科学基金(81573154);国家自然科学基金(81273074);四川省省属高校科研创新团队项目(14TD0023);四川省青年科技创新研究团队项目(2014TD0021)。
TS201.4
A
1002-0306(2017)02-0354-05
10.13386/j.issn1002-0306.2017.02.060
