Fe3+掺杂对硝酸羟胺热稳定性的影响及其机理
2017-02-28刘建国安振涛李天鹏卞立新
刘建国,安振涛,2,张 倩,2,李天鹏,卞立新,李 赫
(1.军械工程学院弹药工程系,河北 石家庄 050003;2.军械工程学院弹药保障与安全性评估军队重点实验室,河北 石家庄050003;3.沈阳铁路局通化军事代表办事处,吉林 通化 134000)
Fe3+掺杂对硝酸羟胺热稳定性的影响及其机理
刘建国1,安振涛1,2,张 倩1,2,李天鹏1,卞立新1,李 赫3
(1.军械工程学院弹药工程系,河北 石家庄 050003;2.军械工程学院弹药保障与安全性评估军队重点实验室,河北 石家庄050003;3.沈阳铁路局通化军事代表办事处,吉林 通化 134000)

物理化学;硝酸羟胺; HAN; Fe3+; 热稳定性; 机理
引 言
硝酸羟胺(HAN)是羟胺的硝酸盐,由还原组分NH3OH和氧化组分NO3组成[1]。硝酸羟胺基推进剂密度大、比冲高、安全、无毒,其优越的性能引起了人们的强烈兴趣[2]。然而在推进剂的制备和生产过程中,往往涉及到HAN的贮存问题,贮存不当会酿成严重事故。如,从20世纪70年代到20世纪90年代,萨凡那河厂和汉福特厂发生了多起存放中的HAN发生爆炸的事故[3],其原因主要是钢铁容器被腐蚀导致HAN被Fe3+污染,HAN热分解而引起爆炸。因此,研究Fe3+对HAN热稳定性的影响具有重要意义。
目前,关于HAN热分解的研究主要集中于研制新型催化剂加速HAN的燃烧。Rachid Amrousse等[4]研究了铱(Ir)催化剂对HAN的催化分解,通过测量HAN单组元推进剂的点火延迟时间、点火温度以及燃烧室压力,对Ir催化剂的催化能力进行了表征。Dan Amariei等[5]研究了铂(Pt)催化剂对80%HAN水溶液的催化分解,通过拉曼光谱测试HAN水溶液分解产物的种类和浓度,对不同温度下Pt催化剂的催化能力进行评估。然而,关于生产和贮存过程中金属离子掺杂对HAN热稳定性的影响研究较少,尤其是Fe3+对HAN热稳定性的影响及其机理还未见详细报道。本实验通过热分析方法研究了Fe3+掺杂对HAN热分解动力学参数的影响,并对Fe3+的影响机理进行了研究,以期为HAN的安全使用和贮存提供科学依据。
1 实 验
1.1 材料和仪器
硫酸羟胺、硝酸钡、FeCl3,均为分析纯,国药试剂有限公司。
DSC Q2000差示扫描量热仪,美国TA公司。
1.2 样品制备
HAN采用复分解法于实验室条件下制备[6],按摩尔比1∶1称取硫酸羟胺和硝酸钡,将硝酸钡加入50℃去离子水中搅拌至完全溶解,加入硫酸羟胺反应20min后过滤硫酸钡沉淀,将所得滤液蒸馏,得到HAN质量分数为90%以上的溶液。为了研究Fe3+掺杂对HAN热稳定性的影响,用FeCl3
配制质量分数为0.2%的HAN溶液以供测试分析。
1.3 性能测试
采用差示扫描量热仪进行热分析,样品质量为(0.480 0±0.020 0)mg,升温区间25~250℃,气氛为流动N2,流速为50mL/min。坩埚为标准液体铝坩埚,采用压片机密封,升温速率分别为3、4、5K/min。
2 结果与讨论
2.1 Fe3+掺杂对HAN热分解特性的影响
采用DSC测定无Fe3+以及Fe3+掺杂时HAN在不同升温速率下的热分解特性,结果如图1和表1所示。

图1 不同升温速率下HAN和HAN/Fe3+的DSC曲线Fig.1 DSC curves of HAN and HAN/ Fe3+ at different heating rates

β/(K·min-1)T0/KTe/KTp/KΔHd/(kJ·g-1)HANHAN/Fe3+HANHAN/Fe3+HANHAN/Fe3+HANHAN/Fe3+3401.85391.73410.55396.98413.11398.534.53502.19404408.58395.66417.47399.08419.27401.383.36504.68505409.41396.44421.10404.19422.90406.443.69803.6600
注:Te为放热分解DSC曲线前缘上斜率最大点的切线与外延基线交点所对应的温度(oneset温度),为试样的分解温度;T0为DSC曲线离开基线的温度;Tp为DSC曲线的峰顶温度;ΔHd为分解焓变。
从图1可知,随着升温速率的增加,HAN热分解DSC曲线的放热峰向高温方向移动,放热峰起始阶段的曲线切线斜率很大,表明一旦发生分解反应,将在短时间内达到最大分解速率,对于事故的预防和控制不利。另外,分解过程很快,整个反应过程能够在较短的时间内完成。而且峰形曲线比较尖锐,表明热分解非常剧烈。热分解焓变的平均值分别为3.8660kJ/g和3.5130kJ/g,均大于800J/g,根据文献[9]中的失控反应严重程度评估标准,反应失控的严重度是“灾难性的”。
起始分解温度反映热分解反应的难易程度,通常用于评估样品的热稳定性[8]。从图1可以看出,加入Fe3+后,HAN热分解的DSC曲线放热峰向着低温方向移动,起始分解温度降低。从表1可以看出,Fe3+掺杂HAN在不同升温速率下的起始分解温度平均降低约16℃,表明HAN中混入Fe3+,其热稳定性将会降低。
图2为无Fe3+以及Fe3+掺杂时HAN在不同升温速率下的转化率(α)与温度的关系曲线。分解反应的转化率与反应时间之间是相互对应的关系,反应温度与时间之间存在着线性关系,所以转化率与温度之间存在着相互对应的关系,图2中3条曲线的形状与变化趋势相似,表明DSC测试中各自的反应历程基本相同[9]。

图2 HAN和HAN/Fe3+热分解的α-T关系曲线Fig.2 Relation curves between conversion (α) and temperature for thermal decomosition of HAN and HAN/ Fe3+
2.2 热分解反应动力学参数计算
2.2.1 Kissinger法
采用Kissinger方法,结合不同升温速率下的DSC曲线峰温,通过线性回归求解热分解动力学参数,计算方程如式(1)所示[10]:
(1)


表2 HAN和HAN/Fe3+热分解的动力学参数
根据文献[11],在已知活化能和指前因子的基础上,由Arrhenius公式对热分解反应速率常数进行计算。其中,HAN热分解的反应速率常数对应于5K/min升温速率下的分解峰温,计算得到无Fe3+时HAN热分解的反应速率常数k1=0.2249,Fe3+掺杂时HAN热分解的反应速率常数k2=0.2886,受反应温度、活化能和指前因子的影响,Fe3+掺杂使得HAN热分解的反应速率常数增加了28.32%。
2.2.2 Ozawa法
常用的Ozawa公式[12]为:
(2)
式中:β为升温速率,K/min;A为指前因子,s-1;α为反应深度;R为理想气体常数,8.314J/(mol·K-1);T为温度,K;Ea为表观活化能;F(α)为机理函数的积分形式。
将不同升温速率下的βi、Ti和αi,(i=1,2,3,…)代入Ozawa方程,无Fe3+以及Fe3+掺杂时HAN热分解反应活化能的计算结果如表3所示。
从表3可以看出,α在0.20~0.90时表观活化能的变化较小,与其他方法得到的结果相近,不同方法得到的表观活化能得到相互验证。另外,由Ozawa法计算的表观活化能的稳定性可知,HAN的热分解机理在α为0.20~0.90时具有一致性,即HAN的热分解遵循同一机理函数。
由表观活化能、指前因子以及反应速率常数的计算结果可知,Fe3+掺杂的HAN热分解表观活化能略有升高,指前因子大幅增加。在反应温度、活化能和指前因子的共同影响下,硝酸羟胺热分解的反应速率常数增大。Fe3+掺杂加快了HAN的热分解,对HAN的热稳定性具有显著影响。
3 机理研究
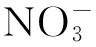

图3 NH2OH和的分子构型Fig.3 Molecular configurations of NH2OH

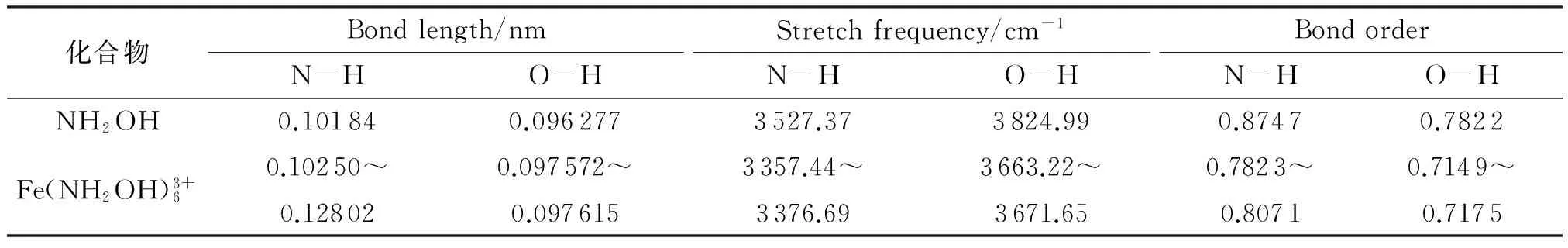
化合物Bondlength/nmStretchfrequency/cm-1BondorderN-HO-HN-HO-HN-HO-HNH2OH0.101840.0962773527.373824.990.87470.7822Fe(NH2OH)3+60.10250~0.128020.097572~0.0976153357.44~3376.693663.22~3671.650.7823~0.80710.7149~0.7175


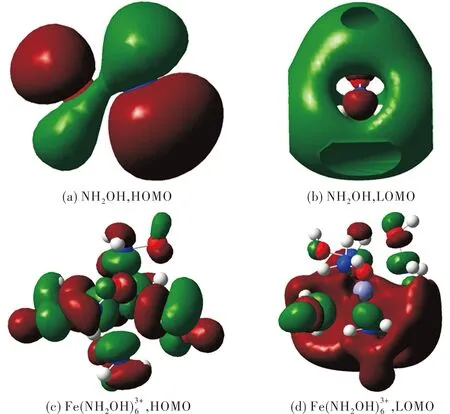
图4 NH2OH及其与Fe3+形成复合物的前线分子轨道Fig.4 Frontier molecular orbital of HAN and complex of HAN combined with Fe3+
从图4可以看出,NH2OH与Fe3+形成配位化合物后,N-H和O-H键周围的电子云密度逐渐减小,键的强度减弱,从前线分子轨道的角度也可以对机理进行解释。

4 结 论
(1)Fe3+掺杂使得HAN热分解DSC曲线放热峰向低温方向移动,起始分解温度平均降低了约16℃,HAN的热稳定性明显降低。热分解表观活化能略有升高,指前因子大幅增加,受到反应温度、活化能和指前因子的影响,Fe3+的掺杂加快了HAN的热分解,对HAN的热稳定性具有明显的影响。

(3)在HAN的贮存和使用过程中,严禁使用铁制容器贮存HAN,并严格控制HAN中Fe3+的含量。可以在HAN中加入花色素、吡咯烷或者硫醇烷等配体,其含有的O、N和S原子具有更大的电负性,Fe3+更倾向于与其形成配合物,阻止HAN与Fe3+直接接触,有效抑制Fe3+对HAN热分解的影响。
[1] WEI Chun-yang,Rogers W J,Mannan M S.Thermal decomposition hazard evaluation of hydroxylamine nitrate[J].Journal of Hazardous Materials,2006,130: 163-168.
[2] 贺芳,方涛,李亚裕,等.新型绿色液体推进剂研究进展[J].火炸药学报,2006,29(4): 54-57.HE Fang,FANG Tao,LI Ya-yu,et al.Development of green liquid propellants [J].Chinese Journal of Explosives & Propellants(Huozhayao Xuebao),2006,29(4): 54-57.
[3] Liu L J,Wei C Y,Guo Y Y,et al.Hydroxylamine nitrate self-catalytic kinetics study with adiabatic calorimetry [J].Journal of Hazardous Materials,2009,162: 1217-1222.
[4] Amrousse R,Katsumi T,Niboshi Y,et al.Performance and deactivation of Ir-based catalyst during hydroxylamine nitrate catalytic decomposition [J].Applied Catalysis A: General,2013,452: 64-68.
[5] Amariei D,Courthéoux L,Rossignol S,et al.Catalytic and thermal decomposition of ionic liquid monopropellants using a dynamic reactor [J].Chemical Engineering and Processing,2007,46: 165-174.
[6] 汪洪涛,周集义.硝酸羟胺NH2OH·HNO3制备及其稳定剂综述[J].化学推进剂与高分子材料,2007,5(2): 18-23.WANG Hong-tao,ZHOU Ji-yi.Preparation of hydroxylamine nitrate (NH2OH·HNO3) and its stabilizer [J].Chemical Propellants & Polymeric Materials,2007,5(2): 18-23.
[7] Francis Stoessel.化工工艺的热安全-风险评估与工艺设计[M].陈网桦,彭金华,陈利平,译.北京:科学出版社,2009: 73.
[8] 孙峰,谢传欣,黄飞,等.Fe3+掺杂对双氧水热稳定性的影响[J].安全与环境学报,2010,10(4): 176-180.SUN Feng,XIE Chuan-xin,HUANG Fei,et al.Effects of Fe3+content on the thermal stability of hydrogen peroxide [J].Journal of Safety and Environment,2010,10(4): 176-180.
[9] 鲍士龙,陈网桦,陈利平,等.2,4-二硝基甲苯热解自催化特性鉴别及其热解动力学[J].物理化学学报,2013,29(3): 479-485.BAO Shi-long,CHEN Wang-hua,CHEN Li-ping,et al.Identification and thermokinetics of autocatalytic exothermic decomposition of 2,4-dinitrotoluene [J].Acta Phyisico-Chimica Sinica,2013,29(3),479-785.
[10] 刘环环,姜炜,郝嘎子.CuCr2O4/石墨烯复合粒子的制备及其对AP的催化作用[J].推进技术,2015,36(8): 1257-1261.LIU Huan-huan,JIANG Wei,HAO Ga-zi.Synthesis of copper chromite/graphene nanocomposites and its characterization as catalyst for AP[J].Journal of Propulsion Technology,2015,36(8): 1257-1261.
[11] 李是良,张炜.镁基水反应金属燃料的热分解性能[J].推进技术,2009,30(6): 740-744.LI Shi-liang,ZHANG Wei.Thermal decomposition characteristics of magnesium-based hydroreactive metal fuel[J].Journal of Propulsion Technology,2009,30(6): 740-744.
[12] QI Zhen-li,ZHANG Duan-feng,CHEN Fei-xiong,et al.Thermal decomposition and non-isothermal decomposition kinetics of carbamazepine[J].Russian Journal of Physical Chemistry,2014,88(13): 2308-2313.
[13] Lee H S,Litzinger T A.Chemical kinetic study of HAN decomposition[J].Combustion and Flame,2003,135: 151.
[14] Barney G S,Duval P B.Model for predicting hydroxylamine nitrate stability in plutonium process solutions[J].Journal of Loss Prevention in the Process Industries,2011,24: 76.
[15] Rachid A,Toshiyuki K,Noboru I,et al.New HAN-based mixtures for reaction control system and low toxic spacecraft propulsion subsystem: thermal decomposition and possible thruster applications[J].Combustion and Flame,2015,162: 2686.
[16] 余宗学.过渡金属氧化物对高氯酸铵催化热分解反应的研究[D].南京:南京理工大学,2009.Yu Zong-xue.Study on the catalytic effect of transition metal oxides on the thermal decomposition of ammonium perchlorate [D].Nanjing: Nanjing University of Science & Technology,2009.
[17] RONG Chun-ying,LIAN Shi-xun,YIN Du-lin,et al.Towards understanding performance differences between approximate density functionals for spin states of iron complexes [J].Journal of Chemical Physics,2006,125(17): 174102-174109.
[18] 王一,王永,韩克利.非血红素配合物[FeIV(O)(TMC)(NCMe)]2+与[FeIV(O)(TMCS)]+的几何结构、电子结构、成键性和反应活性比较[J].高等学校化学学报,2008,29(12): 2469-2473.WANG Yi,WANG Yong,HAN Ke-li.Comparison between [FeIV(O)(TMC)(NCMe)]2+and [FeIV(O)(TMCS)]+non-heme complexes of geometric,electronic structures,bonding and reactivities [J].Chemical Journal of Chinese Universities,2008,29(12): 2469-2473.
Effects of Doping of Fe3+on the Thermal Stability of Hydroxylamine Nitrate and Its Mechanism
LIU Jian-guo1,AN Zhen-tao1,2,ZHANG Qian1,2,LI Tian-peng1,BIAN Li-xin1,LI He3
(1.Department of Ammunition Engineering,Ordnance Engineering College,Shijiazhuang 050003,China; 2.Military Key Laboratory for Ammunition Support and Safety Evaluation,Ordnance Engineering College,Shijiazhuang 050003,China; 3.Military Representative Office,Shenyang Railway Administration,Tonghua Jilin 134000,China)

physical chemistry;hydroxylamine nitrate; HAN; Fe3+; thermal safety; mechanism
10.14077/j.issn.1007-7812.2017.01.011
2016-08-15;
2016-09-11
刘建国(1988-),男,博士研究生,从事含能材料制备及分子模拟研究。E-mail: liujiangnan5676@163.com
张倩(1974-),女,副教授,从事含能材料制备及分子模拟研究。E-mail: zhangqian-zlf@163.com
TJ55;TQ123.6
A
1007-7812(2017)01-0053-06
