CNVplex联合STR技术在复发性流产遗传学查因中的应用*
2017-02-21杨月芬王俏霞许逸琴杨灿锋肖建平
杨 岚,杨月芬,王俏霞,许逸琴,杨灿锋,肖建平△
(南京医科大学附属无锡妇幼保健院:1.产前诊断中心;2.计划生育中心,江苏无锡 214002)
论著·临床研究 doi:10.3969/j.issn.1671-8348.2017.04.005
CNVplex联合STR技术在复发性流产遗传学查因中的应用*
杨 岚1,杨月芬2,王俏霞2,许逸琴2,杨灿锋1,肖建平1△
(南京医科大学附属无锡妇幼保健院:1.产前诊断中心;2.计划生育中心,江苏无锡 214002)
[摘要] 目的 运用快速检测绒毛染色体拷贝数变化的方法探讨复发性流产查因途径。方法 对60例反复自然流产病例的绒毛样本(孕13周前)分别进行多重DNA拷贝数(CNVplex)和荧光原位杂交(FISH)技术检测,所有样本同时行绒毛培养核型分析验证。结果 48例培养成功的复发性流产病例,染色体异常率为60.42%。其中48例CNVplex检测结果与核型分析相一致:包括20例染色体正常者、23例常染色体三体,3例三倍体和2例45,XO(Turner综合征);而FISH检测结果中与核型分析结果相符的只有38例。对于非嵌合体和非结构异常样本,两种方法与细胞遗传学核型分析结果符合率分别为100%(CNVplex)和79.17%(FISH)。结论 应用CNVplex 联合短串联重复序列(STR)技术可检测绒毛染色体拷贝数及检测5 Mbp以上的重复和缺失异常,利于分析流产病因。
绒毛膜绒毛;流产,习惯性;染色体;非整倍体;核型分析;拷贝数变化
[Abstract] Objective The study is to present a novel assay for rapid detection of fetal aneuploidies in chorionic villus for spontaneous abortion.Methods Fetal chorionic villus samples were collected from 60 cases of women diagnosed with recurrent spontaneous abortion (RSA) before 13 weeks gestation.All samples were analyzed using CNVplex (copy number variations multiplex) assay and fluorescence in situ hybridization (FISH) in addition to chromosome analysis.All villi specimens were cell cultured and karyotyped to confirm the fetal chromosomal status.Results Among 48 successfully cultured and karyotyped samples,the chromosomal abnormality rate was 60.42%.The results of karyotyping and the CNVplex assay were identical,both yielding 20 cases of euploidies,23 autosomal aneuploidies,3 triplodies and 2×monosomies(Tumer Syndrome).However,FISH obtained only 38 results identical to karyotyping.Two cases of deletion and duplication of chromosome were also identified by CNVplex but not always by karyotyping.As for non-mosaic and non-structural abnormity samples,the concordance between cytogenetics and genotyping was 100% in CNVplex and 79.17% in FISH.Conclusion With CNVplex combined with STR(short tandem repeat) assay,we can detect the aneuploidy abnormalities as effectively as routine karyotyping without the need for cell culture,while also analyzing deletions and duplications(larger than 5 Mbp) that are not always detected by karyotype analysis.Our study demonstrates that CNVplex assay is an efficient,convenient,and accurate method to explore the etiology of miscarriage.
自然流产是妇产科的常见病、多发病之一,发生率达全部妊娠的15%,近年有上升趋势。其原因众多,涉及遗传、解剖、免疫、内分泌、感染、环境及其他未知因素等[1]。遗传因素尤其是染色体异常通常被认为是最常见的自然流产病因,研究证实,孕早期自然流产染色体异常发生率达50%~60%[1-2],其中多数为染色体数目异常[3-6]。因此对早期停育胚胎进行染色体分析十分重要。核型分析虽被认为是判断染色体结果的金标准,但从培养的绒毛细胞获取核型结果需时较长,且有一定的失败率。现今多种方法如PCR或FISH可用于检测染色体非整倍体异常[7],其他诸如QF-PCR、NGS、CMA等虽都有不需细胞培养和快速诊断的优势[2,8-9],但尚缺乏兼具低成本、高效、应用范围广的分子检测技术。本研究选用多重DNA拷贝数(CNVplex)联合短串联重复序列(STR)技术针对复发性流产组织进行24种染色体的拷贝数检测,通过两种方法的阳性符合率比较,旨在探讨CNVplex联合STR技术在流产组织染色体快速诊断中的应用价值。
1 资料与方法
1.1 一般资料 选择2014-2015年经超声诊断胚胎停止发育在本院行清宫手术的孕妇60例,患者平均年龄30.5岁,排除全身性感染、外力、负重等因素。孕龄为48~91 d。清宫手术时无菌采集绒毛组织约10 g,显微镜下挑选绒毛50 mg左右,经处理分别按CNVplex技术及荧光原位杂交(FISH)法检测,所有样本同时进行绒毛细胞核型分析。
1.2 方法
1.2.1 绒毛细胞培养法 无菌采取清宫术标本放入无菌杯中,按标准方法[10]用无菌生理盐水洗涤后,于显微镜下挑取优质绒毛组织,切成碎片,接种于羊水培养基的培养瓶中,置37 ℃,5% CO2培养箱培养。静置6~7 d后,在倒置显微镜下观察,见到梭形细胞克隆后给予换液;继续培养2~3 d,当出现较多圆形细胞时给予收获。
1.2.2 染色体制备与核型分析 将秋水仙素(10 g/mL)加入培养瓶中继续培养4 h后弃培养液,加入低渗液进行低渗处理20 min,再进行预固定、固定、制片,80 ℃老化2 h。常规G显带、姬姆萨染色。镜下计数20个核型。分析5个显带良好分裂相,嵌合体则增加中期相计数。
1.2.3 FISH检测 FISH根据13、16、21、22号染色体的单一序列探针,18,X,Y着丝粒探针来分析分裂中期的绒毛染色体。根据说明书进行杂交、洗涤、复染、荧光显微镜分析。7种不同的染色体荧光信号被用来分析每个样本的100个细胞,按操作规范进行结果分析。
1.2.4 CNVplex和STR检测 (1)样本DNA提取:按常规提取方式对绒毛样本进行DNA提取(浓度不能低于20 ng/μL);(2)连接反应:各反应管加入总量150 ng的相应体积的DNA样本,灭菌蒸馏水补至8 μL,阴性对照加8 μL洗脱液。按说明书配制预混合液体系:混匀后每管分装12 μL到反应孔中,置PCR仪上(ABI 2720 PCR仪)进行如下反应:98 ℃ 2 min;95 ℃ 30 s,60 ℃ 3 h 5个循环;60 ℃保存。连接反应共15 h,反应结束后加入10 μL“终止液”终止反应并混匀;(3)连接产物多重荧光PCR扩增:对连接探针产物,进行多重PCR扩增。按说明书配制预混合液体系:混匀后每管分装19 μL,加入1 μL连接产物,置PCR仪上进行扩增: 95 ℃ 5 min ;5×(94 ℃ 20 s,62 ℃-1 ℃/cycle 40 s,72 ℃ 1.5 min);94 ℃ 20 s,57 ℃ 30 s,72 ℃ 1.5 min,27个循环;68 ℃ 1 h;保存于4 ℃;(4)扩增产物荧光毛细管电泳分离:取1 μL扩增产物稀释液与0.1 μL LIZ500,8.9 μL Hi-Di混匀,95 ℃变性5 min后置ABI测序仪(PRISM 3130XL)检测。数据由Gene Mapper ID 4.0 (Applied Biosystems),CNVplex Converter (GeneSky)及CNV Reader 1.0 (GeneSky)软件自动分析;(5)拷贝数计算;(6)结果判断:如果连续5个以上目标区的拷贝数值为0.8~1.2,代表1个CNV拷贝;1.75~2.25代表2个CNV拷贝;2.7~3.3代表3个CNV拷贝;3.6~4.4代表4个CNV拷贝。如果连续3个以上目标区的拷贝数值偏离正常拷贝数,并且至少2个检测值的拷贝数为1,则这些探针决定区域判定为缺失(0~0.1或0.8~1.2)或重复(2.7~3.3)。如果一染色体上至少连续3个探针的拷贝数值在2.25~2.7,则提示可能为嵌合体或母血污染样本。(8) STR检测:选取染色体2、4、5、7、8、10、11、12、13、15、16、18、X,Y上高杂合度的17个位点设计引物,对母血及绒毛组织样本分别进行17个STR位点的检测,同时对17个多重荧光PCR产物进行毛细管电泳分析,通过比较检测到的两者位点来源判断绒毛组织有无母血污染。
1.3 统计学处理 采用SPSS13.0软件进行统计处理,计数资料以率表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 核型分析结果 在60例绒毛培养病例中,培养成功率80%(48/60),其中阳性率为60.42% (29/48),异常结果中,最常见的是16 (20.69%),21 (13.79%),22 (10.34%)号三体,三倍体 (10.34%);其次为X单体,15,13三体(均为6.9%);最少见的是3,7,10,11,12,和20号三体。同时笔者发现2例常染色体三体同时伴有9号臂间倒位;1例12三体伴有8号染色体短臂末端缺失,见表1。
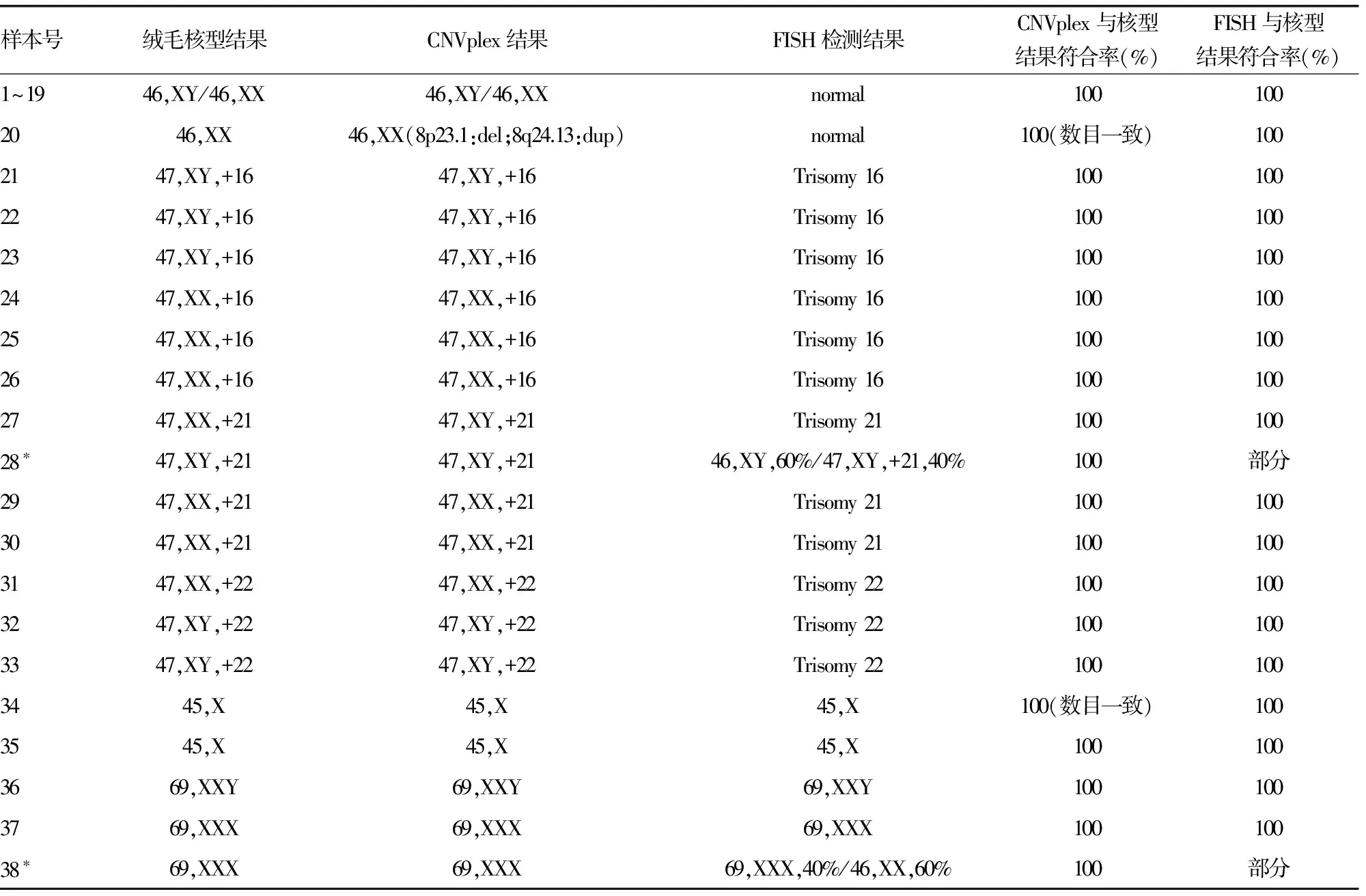
表1 应用CNVplex,FISH和核型分析检测的胎儿染色体结果
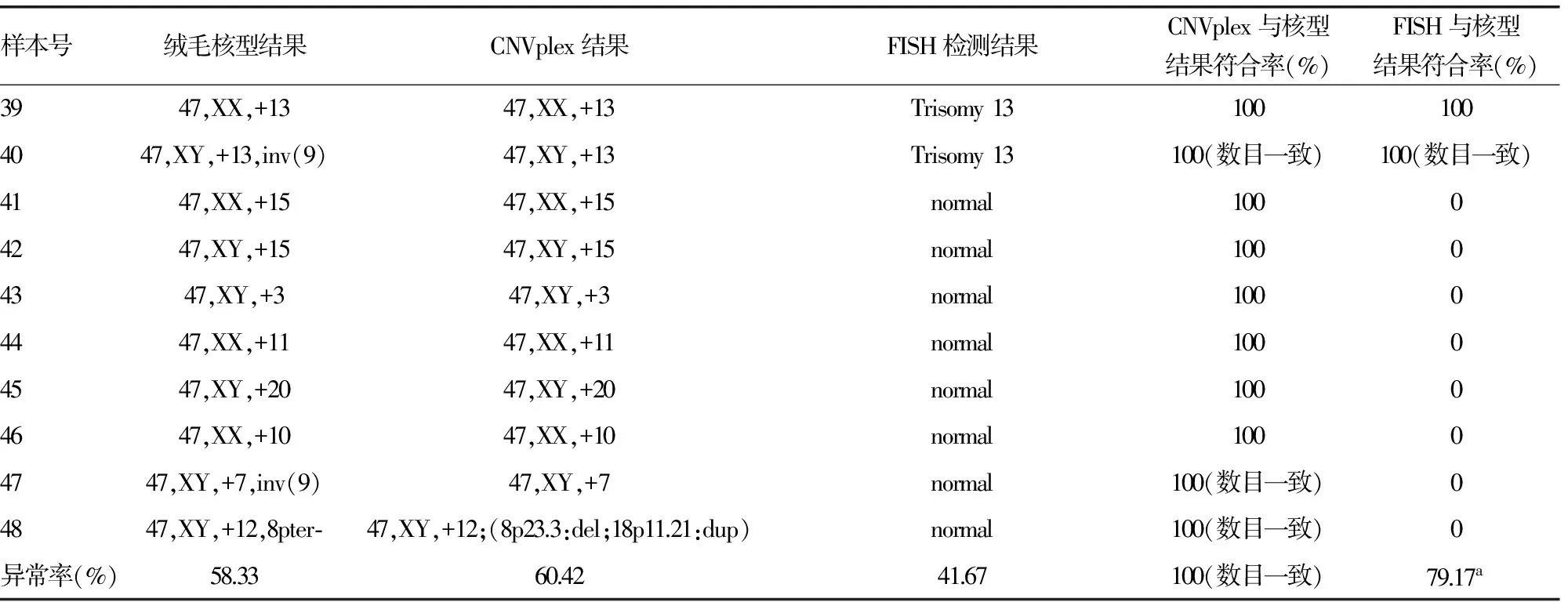
续表1 应用CNVplex,FISH和核型分析检测的胎儿染色体结果
*:由mini-STR assay检测到的母血污染样本;a:χ2=11.16,P<0.01,与CNVplex比较。
2.2 FISH检测结果 在48例培养成功的绒毛样本中,FISH检测成功率(100%)。其中包括6例16三体,4例21三体,3例22三体,3例三倍体,13三体和X染色单体各2例,以及28例整倍体。与核型分析结果比较,FISH检测的异常率为41.67%(20/48),另外8例三体征样本由于FISH探针的限制未能检出。FISH检出两例嵌合体(46,XY,60%/47,XY,+21,40%;69,XXX,40%/46,XX,60%),但最后被核型分析排除。与核型分析结果相比,FISH检测总的符合率为79.17% (38/48)。
2.3 CNVplex检测结果 CNVplex检测和核型分析获得了47个样本的一致结果,包括19例正常整倍体,23例常染色体三体,3例三倍体,2例X染色单体。此外,CNVplex还检出了1例12三体伴8p23.1:del(34 Mbp);18p11.21:dup(6 Mbp),见图1。1例46,XX伴8p23.1:del(5 Mbp);8q24.13:dup(7 Mbp),但这2例重复和缺失没有全部被核型分析所检出。在CNVplex方法中,在染色体数目异常的结果符合率为100%。同时,联合STR检测两例绒毛样本被证实有母血污染,见表1,图2,3。综上,CNVplex对绒毛样本的检测成功率为100%,结果异常率为60.42% (29/48)。
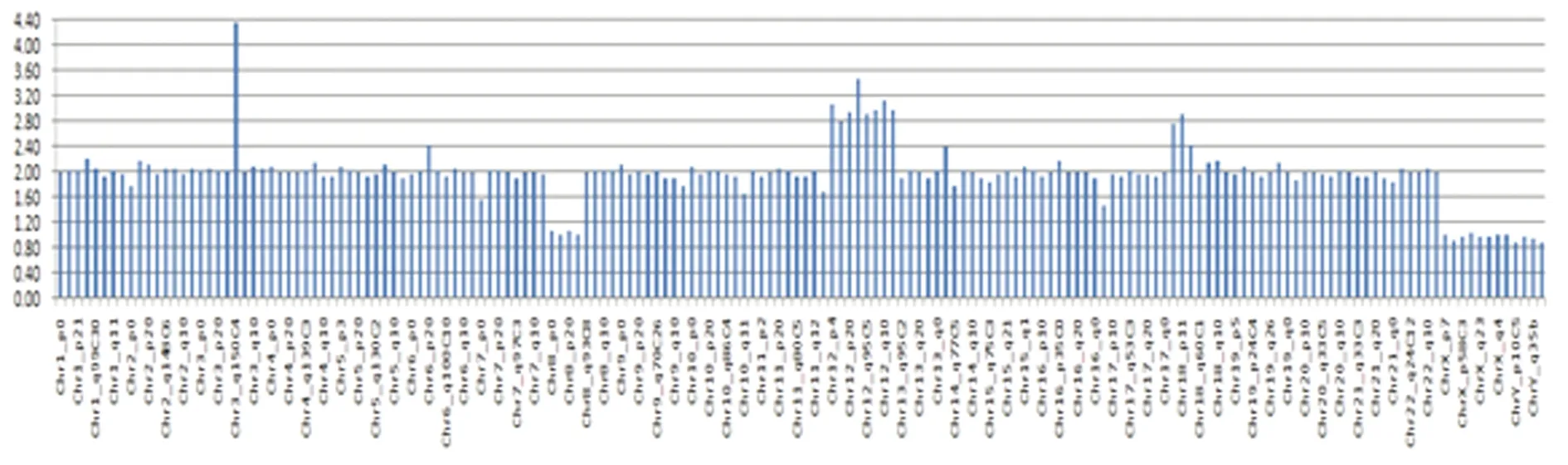
图1 病例 47,XY,+12;(8p del;18p dup) 的CNVplex拷贝数检测结果示意图

STR对D7S820位点的分型检测提示该绒毛样本的双等位基因A11,A9分别遗传其父母。

STR对D13S317位点的分型检测示该绒毛样本一等位基因A11系遗传其父亲,而另外与其母相同的A8,A12等位基因均在绒毛中检测到,含母血污染。
3 讨 论
CNVplex高通量基因拷贝数检测技术(以下简称CNV plex技术)是在多重连接探针扩增技术(MLPA)基础上改进的一个新技术,它与MLPA比较,优势在于探针分布广,CNVplex每条染色体设计5~8个探针,24种染色体共计170个探针,保证了染色体覆盖的广度和深度,同时配以质控探针,使检测结果更精准,其操作更简便,快捷,通量高。该技术除可检测24种染色体数目异常,还可检测5 Mbp以上的缺失或重复,同时对可疑母血污染的绒毛及母血样本的DNA采用STR技术可检测个体识别位点而明确样本是否受母血干扰,也可检出比较基因组杂交(CGH)技术不能检出的多倍体异常。准确的遗传学检测可减少异常流产患者不必要的额外检查,减轻其心理压力[11-12]。比较本研究两种方法与核型分析结果的符合率[(79.17%(FISH)vs.100% (CNVplex)],对于非嵌合体和非结构异常样本,本研究结果显示CNVplex技术可快速、准确地检测所有染色体数目异常,与FISH技术相比显得更有效(P<0.01)。虽然FISH技术可通过分析更多细胞对嵌合体提供较传统核型分析更精确的估计[13],但本研究采用的FISH探针仅能检出7种染色体异常,且无法排除母血污染。经FISH检测出的两例嵌合体46,XY,60%/47,XY,+21,40%和69,XXX40%/46,XX,60%,最终由核型分析分别验证为47,XY,+21和69,XXX,该结果由STR检测发现为母血污染所致。对于FISH技术,尽管对于13,16,18,21,22三体,X单体,三倍体等数目异常的检测灵敏度是100%,但如不加以核型分析,会有28.6%的数目异常病例漏检。如需检测所有染色体,将极大增加FISH探针的试验成本,也不适于临床的广泛应用。
虽然细胞遗传学核型检查是诊断的金标准,能在较低分辨率下分析所有染色体的数目和结构异常,但由于流产绒毛的性状问题等有较高的培养失败率[8,14],易出现漏诊。核型分析可检测平衡重排如易位、倒位等结构异常,本研究虽发现2例常染色三体伴9号染色体臂间倒位,但臂间倒位并非异常流产的主要原因,因而不影响CNVplex技术在产前检测绒毛染色体异常的临床应用。此外,CNVplex发现两例缺失、重复异常(片段大小5~7 Mbp),其中1例为46,XX:8p23.1:del(5 Mbp);8q24.13:dup(7 Mbp),查询OMIM和Decipher基因数据库,8p23.1区域包含GATA4基因,文献报道该基因的拷贝数异常可能影响胎儿心脏发育和导致胚胎停育[15]。对该病例,虽没有染色体数目异常,但该区域缺失很可能是引起胚胎停育的主要因素。该异常在核型分析由于分辨率低而未能检出。因而,CNVplex技术除了无需细胞培养、可快速检测所有染色体数目异常,还能检测核型分析无法检出的5 Mb左右的结构异常,可潜在地作为替代侵入性核型分析的一种产前诊断胚胎染色体异常的检测技术。
近年来,产前检测胎儿非整倍体疾病的分子诊断技术陆续涌现,如Illumina测序平台、ACGH、染色体微阵列分析技术(CMA)[16-18]。虽然这些方法有较高的分辨率和准确度,但其检测成本远高于CNVplex,此外,这些方法对生物信息学分析有着较高要求,且ACGH无法检测三倍体。而QF-PCR也可检测主要的三体征[8,19],并能对产前样本的母血污染检测作出初步评估,但它无法检测染色体结构异常。CNVplex的结果就非整倍体而言与核型分析结果都相一致,显示了在流产绒毛遗传检测中的良好诊断价值。但其不足之处是无法判断绒毛组织嵌合体样本的比例,这可通过核型分析进一步明确。
本研究显示复发性流产胚胎的非整倍体比例为60.42%,其中三体征最常见,占比79.3%(23/29),与之前的报道相符[6,20],其次为三倍体10.3%(3/29),单体征6.9% (2/29)。对于染色体异常的咨询意见:对绒毛染色体数目异常,多数研究已报道为受精卵形成过程中染色体不分离所致,如双亲染色体正常,在排除内分泌、免疫、感染、解剖因素后,可在优生指导下自然受孕,如反复出现流产,可采取胚胎植入前诊断来筛选正常胚胎;对于胚胎染色体结构异常者,可进一步检查双亲,从而明确胚胎染色体结构异常的遗传来源,再根据双亲染色体结果对下次受孕进行咨询指导。而对于染色体正常样本,其病因可能与接触有害物质等环境因素有关[21,22],或由某些特定基因的多态性或基因的插入/缺失导致[23-25]。这些亚显微结构的遗传学病因,需应用PCR-RFLP或基于单核苷酸多态性(SNP)的微阵列分析技术进一步加以明确[25-26],这有待于我们进一步探讨。
综上,本研究表明CNVplex技术是一种快速、准确、低成本的可检测流产组织染色体异常的新方法。准确提供遗传学检查结果不仅可有效减少异常流产患者的心理压力,同时有助于临床医师进行有效的遗传咨询,在优生遗传学领域有着重要的应用价值。
[1]Alonso López AG,Bermejo Huerta S,Hernández Galván R,et al.Cytogenetic diagnosis of first trimester spontaneous abortion[J].Ginecol Obstet Mex,2011,79(12):779-784.
[2]Wang BT,Chong TP,Boyar FZ,et al.Abnormalities in spontaneous abortions detected by G-banding and chromosomal microarray analysis (CMA) at a National reference laboratory[J].Mol Cytogenet,2014,7(7):33-38.
[3]Rolnik DL,Carvalho MH,Catelani AL,et al.Cytogenetic analysis of material from spontaneous abortion[J].Rev Assoc Med Bras,2011,56(6):681-683.
[4]熊丽,刘杰,邓康,等.早期自然流产绒毛细胞培养及染色体核型分析[J].南方医科大学学报,2009,29(1):64-67.
[5]Andrews WW.What is new in stillbirth:Important recent articles[J].Obstet Gynecol,2015,125(1):160-161.
[6]Suciu N,Plaiasu V.A time stamp comparative analysis of frequent chromosomal abnormalities in Romanian patients[J].J Matern Fetal Neonatal Med,2014,27(1):1-6.
[7]Grimshaw GM,Szczepura A,Hultén M,et al.Evaluation of molecular tests for prenatal diagnosis of chromosome abnormalities[J].Health Technol Assess,2003,7(10):1-146.
[8]Donaghue C,Mann K,Docherty Z,et al.Combined QF-PCR and MLPA molecular analysis of miscarriage products:an efficient and robust alternative to karyotype analysis[J].Prenat Diagn,2010,30(2):133-137.
[9]Deng YH,Yin AH,He Q,et al.Non-invasive prenatal diagnosis of trisomy 21 by reverse transcriptase multiplex ligation-dependent probe amplification[J].Clin Chem Lab Med,2011,49(4):641-646.
[10]Smidt-Jensen S,Christensen B,Lind AM.Chorionic villus culture for prenatal diagnosis of chromosome defects:reduction of the long-term cultivation time[J].Prenat Diagn,1989,9(5):309-319.
[11]Nikcevic AV,Tunkel SA,Kuczmierczyk AR,et al.Investigation of the cause of miscarriage and its influence on women′s psychological distress[J].Br J Obstet Gynaecol,1999,106(8):808-813.
[12]Diego-Alvarez D,Garcia-Hoyos M,Trujillo MJ,et al.Application of quantitative fluorescent PCR with short tandem repeat markers to the study of aneuploidies in spontaneous miscarriages[J].Hum Reprod,2005,20(5):1235-1243.
[13]Haoud K,Mellali S,Gouas L,et al.Prevalence of aneuploidies in products of spontaneous abortion:interest of FISH and MLPA[J].Morphologie,2014,98(320):40-46.
[14]Mcclelland LS,Allen SK,Larkins SA,et al.Implementation and experience of an alternative QF-PCR and MLPA diagnostic strategy to detect chromosomal abnormalities in fetal and neonatal pathology samples[J].Pediatr Dev Pathol,2012,14(6):460-468.
[15]Yu S,Zhzou XG,Fiedler SD,et al.Cardiac defects are infrequent findings in individuals with 8p23.1 genomic duplications containing GATA4[J].Circ Cardiovasc Genet,2011,4(6):620-625.
[16]Xie W,Tan Y,Li X,et al.Rapid detection of aneuploidies on a benchtop sequencing platform[J].Prenat Diagn,2013,33(3):232-237.
[17]Viaggi CD,Cavani S,Malacarne M,et al.First-trimester euploid miscarriages analysed by array-CGH[J].J Appl Genet,2013,54(3):353-359.
[18]Dhillon RK,Hillman SC,Morris RK,et al.Additional information from chromosomal microarray analysis (CMA) over conventional karyotyping when diagnosing chromosomal abnormalities in miscarriage:a systematic review and meta-analysis[J].BJOG,2014,121(1):11-21.
[19]胡婷,刘洪倩,朱红梅,等.多重定量荧光PCR在胎儿常见染色体非整倍体快速诊断中的应用[J].中华医学遗传学杂志,2014,31(2):214-218.
[20]Jenderny J.Chromosome aberrations in a large series of spontaneous miscarriages in the German population and review of the literature[J].Mol Cytogenet,2014,7:38-46.
[21]Zhang BY,Wei YS,Niu JM,et al.Risk factors for unexplained recurrent spontaneous abortion in a population from southern China[J].Int J Gynaecol Obstet,2010,108(2):135-138.
[22]Pan X,Liu X,Li X,et al.Association between environmental dioxin-related toxicants exposure and adverse pregnancy outcome:systematic review and meta-analysis[J].Int J Fertil Steril,2015,8(4):351-366.
[23]何淼,康冰,廖世秀,等.河南地区汉族人群原因不明复发性流产与HLA-DRB1等位基因多态性的相关性[J].中华医学遗传学杂志,2014,31(4):504-507.
[24]Zong C,Sha Y,Xiang H,et al.Glutathione S-transferase A1 polymorphism and the risk of recurrent spontaneous abortion in Chinese Han population[J].J Assist Reprod Genet,2014,31(3):379-382.
[25]Levy B,Sigurjonsson S,Pettersen B,et al.Genomic imbalance in products of conception:single-nucleotide polymorphism chromosomal microarray analysis[J].Obstet Gynecol,2014,124(2 Pt 1):202-209.
[26]Naderi-Mahabadi F,Zarei S,Fatemi R,et al.Association study of forkhead box P3 gene polymorphisms with unexplained recurrent spontaneous abortion[J].J Reprod Immunol,2015,110:48-53.
Application of CNVplex combined with STR assay for genetic etiology exploration in chorionic villus of recurrent spontaneous abortion*
YangLan1,YangYuefeng2,WangQiaoxia2,XuYiqin2,YangCanfeng1,XiaoJianping1△
(1.PrenatalDiagnosisCenter;2.DepartmentofFamilyPlanning,WuxiMaternalandChildHealthHospitalAffiliatedNanjingMedicalUniversity,Wuxi,Jiangsu214002,China)
chorionic villus;abortion,habitual;chromosome,aneuploidy;karyotyping;copy number variation
R715.5;R711.6
A
1671-8348(2017)04-0446-04
2016-09-24
2016-10-22)
